DIABETE MELLITO
•
•
•
1.
2.
3.
Malattia multifattoriale o complessa (azione
combinata di più geni e fattori ambientali)
Il termine diabete, deriva dal greco, indica una
eccessiva produzione di urina
comprende alcune malattie con eziologia
differente ma aventi in comune:
Aumento concentrazione ematica di glucosio
(iperglicemia persistente a digiuno)
Poliuria
glicosuria
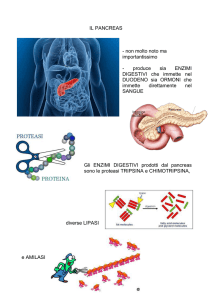
PANCREAS
• Il pancreas è una ghiandola del peso
di circa 100g.
• Consta di parte esocrina (secreto
all'esterno del sistema vascolare) ed
endocrina
(secreto
nel
sistema
vascolare)
parte esocrina
• è costituita da un tessuto ghiandolare acinare di tipo
sieroso
• Il secreto (di tipo acquoso, pH 7,5-8) si versa nel duodeno
insieme alla bile.
• Contiene composti organici ed inorganici ed enzimi sotto
forma di Zimogeni (inattivi), necessari per la digestione
proteica e sono:
• Tripsinogeno,
Chimotripsinogeno,
Proelastasi
e
Procarbossipeptidasi A e B. Dopo attivazione essi
vengono
trasformati
rispettivamente
in:
Tripsina,
Chimotripsina, Elastasi e Carbossipeptidasi A e B.
• E' secreta anche una Alfa-Amilasi per la digestione
dell'amido e degli zuccheri complessi e per la digestione
dei grassi è secreta una Colipasi, che lega i Trigliceridi e li
rende disponibili all'azione della lipasi.
PANCREAS
• La parte endocrina è costituita da un
gruppo di cellule fino a 5.000 che
costituiscono le isole di Langerhans o insulae
che producono differenti ormoni.
pancreas endocrino
• I due principali ormoni che intervengono nella
regolazione della glicemia sono insulina e
glucagone (cellule alfa). Si tratta di due ormoni
polipeptidici che svolgono un'azione antagonista
sul metabolismo glucidico in particolare, ma anche
su quello lipidico e proteico.
• Lo stimolo principale per l'immissione in circolo di
insulina è il livello della glicemia: se per qualsiasi
ragione
questo
aumenta,
l'insulina,
viene
immediatamente liberata in circolo affinché
diminuisca la concentrazione ematica del glucosio.
L' OMEOSTASI GLUCIDICA
L’ipeglicemia post-prandriale stimola le cellule beta delle isole di
Langherans a secernere insulina e contemporaneamente le cellule
alfa a ridurre la secrezione di glucagone.
Questi due ormoni sono tra i principali regolatori dell’omeostasi
glucidica in quanto contribuiscono significativamente al
mantenimento della glicemia al valore di 70-100 mg/dl.
L'insulina abbassa la concentrazione ematica del glucosio, mentre il
glucagone l’innalza: la prima favorisce la captazione e l'utilizzazione
di glucosio da parte delle cellule, mentre il secondo ne favorisce il
passaggio da alcuni tessuti nel sangue
Nel digiuno di breve durata (fino a circa 24h), la glicemia mantiene il
suo valore basale perché il rifornimento di glucosio al sangue è
assicurato dal processo di glicogenolisi,
nel digiuno prolungato lo stesso compito è assicurato dal processo di
neoglicogenesi.
Attraverso tali meccanismi vengono combattute le conseguenze,
dell'ipoglicemia che si rifletterebbero soprattutto a livello cerebrale
in quanto i neuroni necessitano di un continuo apporto di glucosio,
che in essi, penetra con meccanismo insulino-indipendente.
Nel digiuno prolungato l'organismo è anche in grado di ricavare dai
grassi molecole, che sono utilizzate dalle cellule dell' organismo in
alternativa al glucosio, ovvero i corpi chetonici.
• Dopo un pasto, il glucosio assorbito dal tratto intestinale
provoca un aumento della glicemia. I
carboidrati
nell’intestino, vengono ridotti a monosaccaridi (glucosio,
fruttosio e galattosio, assorbiti dalle cellule della mucosa
intestinale e, da qui, sono trasportati al sangue e poi al fegato,
il quale trasforma in glucosio anche il fruttosio e il galattosio.
FEGATO
Tessuti
Cellule
(diffusione
facilitata)
GLUCOSIO
GLICOGENOSINTESI
SANGUE
(iperglicemia postprandiale)
GLICOLISI
gluconeogenesi
• Attività di glicogenosintesi è esplicata anche
dal muscolo, in tal modo il glicogeno funge a
livello epatico e muscolare da riserva di
glucosio
• Il fegato è inoltre in grado di effettuare anche
la gluconeogenesi (“nuovo zucchero”), ovvero
formare glucosio da precursori non saccaridici
(alcuni aa, lattato, glicerolo),
quando
diminuiscono
le
riserve
di
carboidrati
nell’ipoglicemia,
oppure
quando
i
glucocorticoidi, specialmente cortisolo, sono
liberati dalla corteccia surrenale: il cortisolo in
particolare mobilita le proteine da quasi tutte le
cellule dell'organismo, rendendole disponibili
sottoforma di aa.
Secrezione di insulina
•L’assunzione di cibo stimola la secrezione di insulina, il
principale ormone regolatore della glicemia e una diminuzione
dei livelli di glucagone.
•L’insulina determina:
• una diminuzione della liberazione epatica di glucosio perché
inibisce la scissione di glicogeno in glucosio (glicogenolisi) e
della
sintesi
di
nuovo
glucosio
dagli
amminoacidi
(gluconeogenesi).
•Il
fegato,
che
è
liberamente
permeabile al glucosio, sequestra circa il 50% di glucosio
per convertirlo a glicogeno (azione controllata dall’insulina). Il
glucosio non sequestrato dal fegato viene distribuito nel
muscolo e nel tessuto adiposo. Le cellule adipose utilizzano
glucosio per formare ac. grassi a lunga catena che esterificati
con il glicerolo vengono riversati nel sangue.
•Quando la glicemia tende a scendere, si
verifica un
graduale
aumento della produzione epatica di glucosio,
contemporaneamente alla diminuzione dei livelli plasmatici di
insulina e ad un aumento di glucagone.
INSULINA
• Quindi l'azione principale dell'insulina consiste nel far
diminuire la concentrazione ematica del glucosio. Ciò
avviene principalmente a tre livelli: fegato, tessuto
muscolare e adiposo.
• Fegato: inibisce la produzione epatica di
glucosio,riducendo
la
glicogenolisi
e
la
gluconeogenesi. Stimola la captazione epatica di
glucosio
• Muscolo: stimola la captazione di glucosio, e
inibisce il flusso dei precursori gluconeogenici verso
il fegato (es;alanina, lattato, piruvato)
• Tessuto adiposo Stimola la captazione di glucosio,
inibisce il flusso dei precursori gluconeogenici verso
il fegato (glicerolo) e riduce il substrato energetico
per la gluconeogenesi epatica (ac.grassi non
esterificati)
INSULINA
• Viene prodotta dalle cellule ß degli isolotti
pancreatici a partenza da un precursore di
110 aminoacidi detto preproinsulina, che
viene trasformata prima in proinsulina e poi
in insulina
• L’insulina appartiene a un famiglia di peptidi
tra loro correlati detti insulin like growth
factors, IGF. Questi peptidi in particolare
l’IGF1 sono i mediatori dell’azione esercitata
dall’ormone della crescita e sono dette
somatomedine.
INSULINA
• La secrezione di insuline è un processo finemente
regolato al fine di mantenere concentrazioni
plasmatiche costanti di glucosio sia a digiuno che
dopo i pasti.
• Il glucosio stimola la produzione di insulina dopo
penetrazione all’interno della cellula ß, e induce
una secrezione bifasica con un primo picco dopo
1-2 minuti e di breve durata, e una seconda fase
tardiva ma di maggiore durata.
• Altre sostanze stimolano il rilascio di insulina, come
gli ac.grassi, i corpi chetonici, gli aa, diversi ormoni
gastrointestianli
come
la
gastrina,
la
colecistochinina, la secretina, il VIP.
INSULINA
• In condizioni di digiuno il pancreas ne secerne circa
40 µg (1 unità U) nell’arco di 1 ora
• Dopo ingestione di cibo si verifica un rapido
aumento dei livelli di insulina nel sangue portale.
• L’insulina stimola il trasporto del glucosio all’interno
del tessuto muscolare e adiposo
• Il glucosio penetra nelle cellule attraverso diffusione
facilitata mediata da una famiglia di trasportatori
detta GLUT
• L’insulina è in grado di regolare la sintesi di tali
trasportatori e di promuovere la traslocazione
energia-dipendente delle vescicole intracellulari
che contengono tali trasportatori verso la
membrana plasmatica; questo effetto è reversibile,
infatti i trasportatori ritornano a livello intracellulare
dopo la rimozione dell’insulina.
INSULINA
• La diffusione facilitata del glucosio
all’interno della cellula avviene lungo
un gradiente decrescente assicurato
dalla fosforilazione del glucosio in G6P
ad opera di alcune esochinasi.
• La sintesi di diverse esochinasi in
differenti tessuti è regolata a livello
trascrizionale dall’insulina
INSULINA
• L’insulina blocca la trascrizione della
fosfoenolpiruvato
carbossichinasi
enzima deputato alla gluconeogenesi
• Ciò spiega come l’insulina inibisca la
gluconeogenesi e perché il fegato
produca un eccesso di glucosio in
situazioni
di
insulino
resistenza
caratteristiche del diabete non insulino
dipendente
recettore
• Presente in tutte le cellule comprese quelle che
normalmente non sono bersaglio dell’insulina
• E’ costituito da 2 subunità a extracellulari che contengono
il sito di legame per l’insulina, e da 2 subunità ß
intracellulari ad attività tirosino-chinasica.
• L'interazione dell'insulina con la porzione extracellulare del
recettore è seguita dalla trasduzione di un segnale che
comporta la fosforilazione dei residui tirosinici presenti nella
porzione citoplasmatica, alla quale fa seguito a livello
citoplasmatico la fosforilazione a cascata di numerose
proteinchinasi, culminante nell' attivazione di un fattore di
trascrizione che nel DNA modula la trascrizione di numerosi
geni che codificano per i prodotti responsabili dei
numerosi effetti esercitati da questo ormone.
glucagone
• prodotto dalle cellule alfa pancreatiche, il suo
compito principale consiste nel far aumentare il
livello di glucosio nel sangue. Questo avviene
perché ha un ruolo opposto a quello dell'insulina,
quindi:
• stimola la scissione del glicogeno in glucosio
• stimola la lipolisi (scissione dei grassi) all'interno degli
adipociti con simultanea inibizione dell'ingresso del
glucosio in questo tessuto.
• il glucagone non solo favorisce l'immissione in
circolo
del
glucosio,
ma
ne
blocca
l'immagazzinamento rendendolo pronto per l'utilizzo
da parte dell'organismo.
Principali effetti esercitati da altri
ormoni
• Agli effetti iperglicemizzanti indotti dal glucagone si
associano a quelli innescati da altri ormoni.
• L'adrenalina incrementa la concentrazione ematica del
glucosio attraverso:
• attivazione della fosforilasi epatica con conseguente
incremento della glicogenolisi e immissione di glucosio
nel sangue
• attivazione della fosforilasi muscolare e conseguente
incremento della glicolisi con produzione di lattato, che
passa nel sangue e raggiunge il fegato dove viene
trasformato in glicogeno.
• In tale maniera l'adrenalina provvede al continuo
rimpiazzamento del glicogeno epatico, di cui essa
stessa ha favorito il consumo.
Principali effetti esercitati da altri
ormoni
•I
glicocorticoidi,
pur
stimolando
la
glicogenosintesi epatica e muscolare,
inducono
contemporaneamente
iperglicemia con un triplice meccanismo:
• a) inibizione nelle cellule B delle isole
pancreatiche della sintesi di insulina,
• b) riduzione della penetrazione del glucosio
nelle cellule,
• c) stimolazione della neoglicogenesi, che
comporta una eccessiva proteolisi.
• Inoltre essi stimolano la lipolisi e la formazione
di corpi chetonici.
Principali effetti esercitati da altri
ormoni
• L'ormone della crescita (GH), determina molti
effetti, il principale è quello di stimolare
l'accrescimento
staturale
nell'infanzia
e
nell'adolescenza con l'intermediazione delle
somatomedine o IGF, che vengono sintetizzati e
rilasciati dagli epatociti, stimolati dal GH per il
quale esprimono specifici recettori.
• Esse sono definite anche fattori similinsulinici
(Insulin like Growth Factors = IGF) in quanto
espletano un' azione simile a quella dell'insulina
• Essi infatti stimolano nelle cellule la penetrazione
del glucosio, mediata dai suoi trasportatori, e la
sua
trasformazione
metabolica
(azione
similinsulinica).
Principali effetti esercitati da altri ormoni
• quando il GH è secreto in eccesso si ha
invece un'azione opposta, per cui il GH
si definisce ormone diabetogeno.
L'eccesso di GH:
• contrasta
sia
la
captazione
intracellulare del glucosio che la sua
fosforilazione in sede intracellulare;
• stimola la glicogenolisi epatica, che
causa rilascio di glucosio nel sangue;
• incrementa la lipolisi, con conseguente
formazione di corpi chetonici.
IL DIABETE MELLITO INSULINODIPENDENTE
(DI I TIPO O IDDM)
• è provocato dalla progressiva riduzione delle
cellule B delle isole pancreatiche di Langherans,
• La riduzione delle cellule B è causata dalla loro
progressiva distruzione ad opera del sistema
immunitario, su predisposizione genetica, per cui
questa forma di diabete mellito è da considerarsi
una vera e propria malattia autoimmune
• nel sangue si riduce progressivamente la
concentrazione dell'insulina (insulinemia)
• La precisa natura della predisposizione genetica
non è stata ancora definita con certezza. Si tratta
di malattia ereditaria poligenica o multifattoriale,
causata dall’azione di più geni, le cui conseguenze
si manifestano quando nel corso della vita
intervengono anche determinati fattori ambientali.
IL DIABETE MELLITO INSULINODIPENDENTE (DI I
TIPO O IDDM)
Si
ritiene che mutazioni a carico dei geni, definiti
diabetogeni,
predispongano
al
diabete
mellito,
modificando la struttura antigenica delle cellule beta delle
isole di Langherans in modo che alcune molecole espresse
sulla loro superficie presentino modificazioni strutturali che
le fanno riconoscere come estranee dal sistema
immunitario, il quale scatena contro di esse una risposta
anticorpale e cellulomedíata.
In alternativa, si ritiene che i suddetti geni inducano una
particolare
suscettibilità
alle
infezioni
virali,che
rappresenterebbero il movente eziologico scatenante
della reazione autoimmunitaria.
Il ruolo dei fattori ambientali è dimostrato dal fatto che nei
gemelli
monocoriali
la
malattia
colpisce
contemporaneamente i due fratelli solo nel 50% dei casi.
IL DIABETE MELLITO INSULINODIPENDENTE (DI I
TIPO O IDDM)
• Sotto l'aspetto istopatologico, il coinvolgimento
autoimmune delle cellule beta si manifesta con la
presenza di un processo infiammatorio in corrispondenza
delle isole pancreatiche con infiltrazione di linfociti
prevalentemente citotossici (CD8+).
• Inoltre nel sangue sono presenti anticorpi diretti verso i
vari costituenti delle isole pancreatice.
• La deficienza di insulina fa sì che la terapia selettiva del
diabete di tipo I sia essenzialmente di tipo sostitutivo. Per
lungo tempo i pazienti affetti da IDDM sono stati curati
con iniezioni di insulina di origine animale, ma da diversi
anni è entrata nella pratica terapeutica l'insulina
umana, ottenuta con tecniche di ingegneria genetica.
• Si tratta di un progresso di grande rilievo perché
impedisce l’instaurarsi di fenomeni di sensibilizzazione
immunitaria con formazione di anticorpi neutralizzanti
l'insulina di origine animale, discretamente frequente nei
pazienti trattati con insulina animale.
DIABETE MELLITO INSULINOINDIPENDENTE
(DI II TIPO O NIDDM)
rappresenta circa 1'85% di tutte le forme di diabete, ha
non solo una maggiore incidenza dello IDDM, ma si
differenzia da esso per una serie di motivi:
1) ha un esordio tardivo, tanto da essere stato definito in
passato come diabete dell'adulto.
2) colpisce preferenzialmente soggetti obesi,
3) non è provocato da deficiente produzione di insulina,
4) non è una malattia autoimmune.
5) presenta una notevole familiarità,
6) non è caratterizzato dalla riduzione delle cellule B delle
isole pancreatiche, le quali al contrario si presentano
frequentemente iperplastiche e producono insulina in
eccesso, che si riflette in una elevata insulinemia.
DIABETE MELLITO INSULINOINDIPENDENTE
(DI II TIPO 0 NIDDM)
• colpisce preferenzialmente soggetti obesi, con lunga
abitudine all'iperalimentazione e abbondante e ripetuta
assunzione di carboidrati che induce la comparsa di una
iperglicemia postprandiale di livello più elevato del
normale.
• Questa determina il rilascio nel sangue di una maggiore
quantità di insulina (iperinsulinemia) da parte delle cellule B
che vanno incontro ad una progressiva iperplasia. Questa
condizione si riflette in una minore espressione da parte
delle cellule insulinodipendenti dei recettori per l'insulina ed
in una riduzione della loro capacità di legare questo
ormone per il fenomeno della "down regulation".
DIABETE MELLITO INSULINOINDIPENDENTE
(DI II TIPO 0 NIDDM)
CONSEGUENZE:
Si riduce la possibilità di rifornimento cellulare di glucosio,
verosimilmente aggravata in alcuni casi anche da difetti
collegati
al
meccanismo
d'azione
intracellulare
dell'insulina e da altri difetti concernenti il trasporto del
glucosio attraverso la membrana plasmatica, operata
dai GLUT, che sono le molecole preposte all'ingresso del
glucosio all'interno delle cellule, che avviene con un
meccanismo di diffusione facilitata.
Certamente la familiarità ha un substrato genetico, che non
è stato ancora definito, ma che deve verosimilmente
coinvolgere i meccanismi preposti all'espressione dei
recettori per l’insulina.
DIABETE SECONDARIO
si manifesta in conseguenza degli effetti indotti da altre patologie che
inducono scomparsa o esaurimento funzionale delle cellule B.
La scomparsa può essere provocata dall'asportazione chirurgica del
pancreas (neoplasie o gravi traumi) o dalla loro distruzione, indotta
da pancreatiti (virali o da alcuni farmaci).
L’esaurimento funzionale delle cellule B può intervenire in pazienti che
per lungo tempo sono stati affetti da iperglicemia di grado elevato.
Le più comuni patologie responsabili sono:
gigantismo (nel giovane) e l'acromegalia (nell'adulto), causati da un
adenoma
delle
cellule
somatotrope
dell'adenoipofisi
(somatotropinoma) secernente un eccesso di GH.
sindrome di Cushing, dovuta ad un adenoma funzionante delle cellule
corticotrope dell'adenoipofisi (corticotropinoma) producente un
eccesso di ACTH che stimola il corticosurrene a secernere un
eccesso di ormoni glicocorticoidi, oppure ad un tumore funzionante
del corticosurrene, direttamente responsabile della ipersecrezione di
glicocorticoidi
feocromocitoma, che è un tumore derivante dalle cellule cromaffini
della midollare del surrene che sintetizza e secerne catecolamine in
eccesso
Il diabete secondario può anche avere una un substrato genetico per
mutazioni responsabili della sintesi di una insulina abnorme, priva di
funzione o per mutazioni che bloccano la sintesi dei recettori per
l'insulina.
FISIOPATOLOGIA DELLA SINDROME
DIABETICA
Sia il diabete di tipo I che II sono responsabili di:
1.
Riduzione della penetrazione intracellulare e della
utilizzazione del glucosio, che si accumula nel sangue
(iperglicemia), raggiungendo anche valori di 1000-1200
mg/dl (10-12 volte superiori al normale:100 mg/dl).
CONSEGUENZE:
Le cellule dell'organismo, si trovano circondate da liquido ad
elevata concentrazione di glucosio, che non possono
utilizzare.
Si realizza uno spreco di glucosio, che si aggrava ulteriormente
quando la concentrazione ematica è >180 mg /dl, poiché il
glucosio in eccesso non viene riassorbito a livello tubulare
renale ma viene eliminato con l'urina.
La presenza di un eccesso di glucosio nel filtrato glomerulare
incrementa la diuresi osmotica, con perdita di acqua e di
elettroliti (sodio, potassio, calcio, magnesio, fosfati, cloruri).
FISIOPATOLOGIA DELLA SINDROME
DIABETICA
2)Riduzione del contenuto proteico per stimolazione della
neoglicogenesi (cioè della trasformazione degli aminoacidi
glicogenetici delle proteine in glucosio con conseguente
ulteriore incremento della glicemia).
CONSEGUENZE:
Riduzione delle masse muscolari per depauperamento di
proteine, che insieme alla ridotta o mancata utilizzazione del
glucosio è responsabile della sensazione di fame, che spinge
all’iperalimentazione.
Le proteine sono danneggiate dall'eccessiva presenza di
glucosio nel sangue (glicosilazione), che altera il
funzionamento di tutte le proteine (strutturali ed enzimatiche)
con comparsa di complicanze. La prima proteina glicosilata
scoperta nei diabetici fu l'emoglobina, una piccola quantità
di emoglobina glicosilata è presente anche nel sangue dei
soggetti normali, ma la sua concentrazione aumenta
considerevolmente nei diabetici, per questo motivo il suo
dosaggio viene eseguito per determinare la gravità della
malattia.
FISIOPATOLOGIA DELLA SINDROME
DIABETICA
3. Incremento della lipolisi, che comporta mobilizzazione di
lipidi dai depositi ed alterazioni del metabolismo lipidico.
CONSEGUENZE:
La scarsa penetrazione di glucosio all’interno delle cellule è
responsabile dell’iperglicemia e del fatto che le cellule
ricavano per lo più energia dai lipidi che vengono
metabolizzati con formazione in eccesso di ac. grassi.
Da questi si forma in grande quantità acetil coenzima A
che induce un sovraccarico del ciclo degli acidi
tricarbossilici con la conseguenza che l'eccesso viene
trasformato nel fegato in corpi chetonici (acido
acetacetico, acido beta-idrossibutirrico, ed acetone).
Siccome la sintesi di questi si verifica con rapidità > alla
loro metabolizzazione, si accumulano nel sangue.
corpi chetonici
Nel sangue i corpi chetonici esercitano una duplice
azione:
1. per la loro attività osmotica aggravano la
disidratazione cellulare indotta dall' aumentata
concentrazione ematica di glucosio
2. In quando acidi forti, cedono idrogenioni
determinando uno stato di acidosi metabolica.
I corpi chetonici vengono eliminati con l'urina
(chetonuria). La presenza di questi acidi nei tubuli
renali richiama dal sangue sodioioni che passano
nell'urina, con la conseguenza che si riduce la
concentrazione di sodioioni nel sangue, dove
vengono sostituiti da idrogenioni
(H +), con
aggravamento dell'acidosi metabolica. Se questa
non viene compensata si può avere coma
diabetico, con possibile esito mortale.
COMPLICANZE DEL DIABETE MELLITO
• La complicanza più frequente è l'aterosclerosi, favorita dalle
alterazioni del metabolismo lipidico (iperlipidemia ed in particolare
ipertrigliceridemia con aumento della concentrazione ematica di
VLDL-colesterolo e riduzione delle HDLcolesterolo) e dalla
glicosilazione delle proteine presenti nella membrana basale della
tonaca intima della parete arteriosa.
• L'aterosclerosi, che interessa le arterie coronarie, quelle cerebrali,
quelle delle estremità è definita macroangiopatia diabetica. Essa è
responsabile della comparsa di accidenti cardiovascolari, che
rappresentano il 60% della cause di morte nei diabetici.
• Per microangiopatia diabetica si intende, invece, il coinvolgimento
delle arteriole del microcircolo, caratterizzato da un notevole
ispessimento della membrana basale dell'endotelio e responsabile
della comparsa di ulcere a carico delle estremità, soprattutto di
quelle inferiori. La presenza di ateromi si associa alla formazione di
trombi, che aggravano, a causa del restringimento del lume
vascolare, l'apporto di sangue con conseguente deficiente fornitura
di 02 e di nutrienti alle cellule dei distretti interessati (occhio, rene,
cervello, cuore, estremità).
COMPLICANZE DEL DIABETE MELLITO
• apparato oculare: cataratta, riportabile secondo molti autori,
alla glicosilazione delle proteine del cristallino. Retinopatia
diabetica, che può determinare cecità in conseguenza di
stravasi emorragici nei vasi retinici e la maculopatia
diabetica, che subentra in conseguenza dell'imbibizione
edematosa della macula.
• nefropatia diabetica, che inizia con alterazioni della funzione
filtrante del rene che determina la comparsa di microalbinuria
che gradualmente si trasforma in proteinuria, sempre più
grave per culminare spesso in grave insufficienza renale.
• sistema nervoso periferico: neuropatia diabetica, che induce
una molteplicità di sintomi a carico di numerosi organi.
• Infezioni: sia batteriche che virali, per alterazione delle cellule
immunitarie.