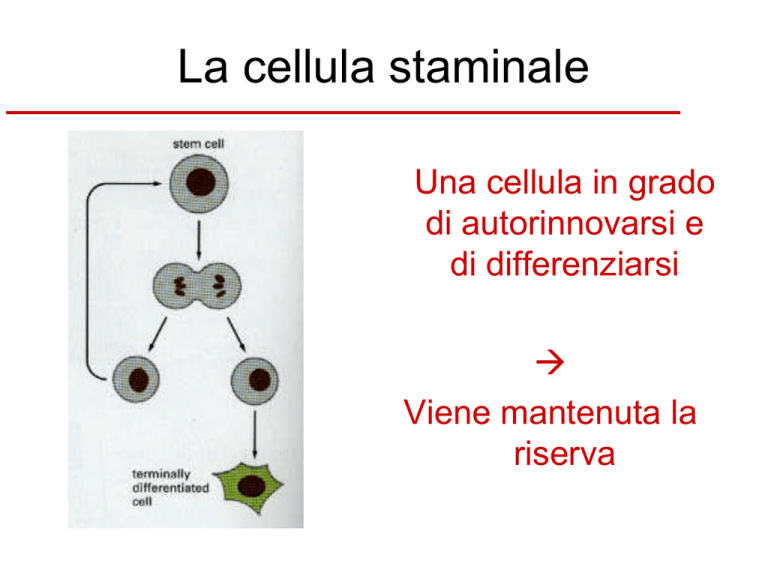
La cellula staminale
Una cellula in grado
di autorinnovarsi e
di differenziarsi
Viene mantenuta la
riserva
Cellule staminali
• Malattie fino ad oggi incurabili, per le quali
si può prospettare un terapia con cellule
staminali:
• Sclerosi laterale amiotrofica (ALS), morbo
di Parkinson, morbo di Altzheimer
• Infarto miocardico
• Cirrosi epatica
• Diabete
• …sla .
Cellule staminali
• In base all’origine vengono classificate in
• Embrionali (ESC)
• Somatiche Adulte (ASC)
Cellule staminali dell’adulto
• Presenti soprattutto nei tessuti a ricambio
fisiologico: epiteli e sangue
• Trovate anche in altri tessuti a ricambio
limitato: muscolo scheletrico (cellule
satelliti)
• Recentemente evidenziate, anche se
molto limitatamente, in tessuti una volta
considerati “perenni”: nervoso e miocardio
Cellule staminali dell’adulto
• Tessuti diversi ne contengono livelli diversi
• Queste cellule staminali hanno
generalmente una potenzialità limitata al
tipo cellulare maturo che compone il
tessuto/organo
il microambiente (nicchia) dà
indicazioni sul destino della cellula
staminale
• L’utilizzo delle cellule staminali derivate dai
tessuti negli individui adulti ha due limiti:
1. la difficoltà di isolamento, seguente espansione
e mantenimento in laboratorio nello stato
indifferenziato
2. una volta isolate, la difficoltà di indurne la
differenziazione in molti tessuti diversi da quello
dal quale sono state estratte.
• Invece per quanto riguarda il trapianto di cellule
dal cordone ombelicale, si riduce così il rischio di
rigetto di trapianto, rispetto a quello compiuto
con cellule staminali prelevate da midollo.
Cellule mesenchimali staminali (MSC)
riparano il cuore infartuato
Sussman, Nature 5 aprile 2001
Fecondazione dell’Ovocita
Cellule staminali embrionali
Differenziamento delle cellule staminali
Cellule staminali embrionali
vantaggi
• Ottenibili più facilmente
• Più attive e veloci rispetto le adulte
• Totipotenti (possono creare qualsiasi
tessuto)
Cellule staminali embrionali
problematiche
• Poco controllabili; potrebbero diventare
tumorali
• Qualora dovessero essere trapiantate,
potrebbero essere rigettate, perché non
compatibili con il ricevente
Da dove provengono gli embrioni umani?
Questi embrioni vengono creati durante la fase di routine
delle cure contro la sterilità (FIVET).
Un solo ciclo di trattamento di FIVET comprende la
fecondazione simultanea di più ovuli. In seguito, vari ovuli
fecondati vengono reimpiantati nella madre, mentre i
rimanenti vengono congelati nell'eventualità in cui il primo
tentativo di fecondazione non andasse a buon fine.
In tutta l'Unione Europea ci sono, attualmente, almeno
100.000 embrioni "di riserva" conservati in specifici
congelatori.
Se la FIVET ha invece successo, la coppia può decidere se
donare gli embrioni inutilizzati a fini di ricerca oppure
eliminarli.
Clonazione riproduttiva
Cumulina con al madre nutrice, la pecora Dolly, gatto, cane, ..
Nature, 23 luglio 1998
Cos'é la clonazione ?
• La parola "clone" deriva dal greco κλων,
che significa germoglio o ramoscello
• In biologia indica la possibilità di duplicare
il patrimonio biologico (genetico) di
qualsiasi essere vitale con produzione di
individui biologicamente uguali
• si tratta di una forma di riproduzione
a-sessuata e a-gamica
Questioni aperte
• Di ordine tecnico:
– La bassa efficienza (vedi Dolly: 1 nascita su 29
embrioni trasferiti in utero su 277 fusioni)
– Le patologie riscontrate negli organismi clonati
– Di ordine etico: in riferimento all’uomo e ad altre
specie viventi
Clonazione terapeutica
• procedimento che prevede la generazione
di cellule staminali pluripotenti derivate dal
paziente, la loro espansione in coltura,
differenziazione nell’istotipo necessario e
trapianto.
• prevede il trasferimento del nucleo di una
cellula somatica matura in un oocita
Terapia con cellule staminali umane
CLONAZIONE PER TRAPIANTO NUCLEARE
il materiale di partenza sono degli ovociti, dai quali vengono aspirati con
un ago il globulo polare ed i cromosomi (gli ovociti vengono enucleati), così
che vi rimanga solo il citoplasma. Dopo di che avviene la sostituzione
(trapianto nucleare) con il nucleo di una cellula somatica di un
paziente; Questa tecnica è stata studiata ed utilizzata per la clonazione
della pecora Dolly.
La produzione di cellule staminali mediante questa tecnica rende necessaria la
formazione di un embrione il cui sviluppo viene arrestato allo stadio di
blastocisti; non si tratta quindi dello sviluppo completo di un embrione dal
quale poi si preleverebbero tessuti o organi di ricambio. La tecnica del
trasferimento nucleare potrebbe essere impiegata in un programma
terapeutico al fine di costituire una fonte adeguata di rifornimento cellulare al
paziente. L’impiego di questa tecnica delinea la possibilità di avere a
disposizione linee cellulari pluripotenti direttamente dalle cellule trapiantate
dai pazienti, evitando il passaggio della formazione di un embrione mediante
una sorta di “autotrapianto”; al momento però lo stato delle conoscenze non
permette l’attuazione di quest’ultima opzione. Il trapianto nucleare somatico
appena spiegato viene detto “clonazione terapeutica”, che si differenzia da
quella riproduttiva che dà invece origine ad un intero organismo.
“Trasferimento nucleare”
secondo il Rapporto Dulbecco
1
2
rimozione
del nucleo aploide
oocita umano NON fecondato
o altre forme di citoplasto artificiale
3
4
isolamento del nucleo diploide
da cellule somatiche del paziente
5
sviluppo in vitro
trasferimento nucleare
6
derivazione di cellule
embrionali staminali umane
Non richiede la formazione dell’embrione umano,
ma prevede il passaggio diretto
di cellule staminali o tessuto specifiche
Risoluzione maggioritaria della Commissione Dulbecco
•
Diciotto membri della Commissione hanno fissato l’attenzione sul fatto che
anche in Italia esiste un elevato numero di embrioni soprannumerari
• La scelta di destinare una parte di questi embrioni a ricerche dalle quali
possono derivare notevoli benefici per l'umanità non comporta una
concezione strumentale dell’embrione, né costituisce un atto di mancanza
di rispetto nei confronti della vita umana
• A fronte dell'inevitabile destino riservato a una parte degli embrioni
crioconservati e non più impiantabili, la Commissione ritiene che la
bilancia penda a favore della destinazione di tali embrioni agli scopi di una
ricerca suscettibile di salvare la vita di milioni di esseri umani
• Sul piano dei principi, tale soluzione trova sostegno nel principio di
beneficialità. In forza di ciò, tale soluzione dà corpo alla nostra
responsabilità verso le prossime generazioni, alle quali indubbiamente
ridonderanno i benefici degli sforzi che oggi facciamo nella lotta contro le
malattie e la sofferenza.
Risoluzione minoritaria della Commissione
(Card. Ersilio Tonini, Adriano Bompiani, Bruno Dallapiccola, Domenico Di Virgilio, Enrico
Garaci, Luigi Lorenzetti, Girolamo Sirchia)
• L'embrione è un essere umano con potenzialità di
sviluppo (e non un essere umano potenziale)
• l'embrione, come ogni essere umano, ha diritto alla vita
• L'embrione va rispettato come persona
• Le argomentazioni che proibiscono moralmente di creare
embrioni per la sperimentazione, valgono anche per la
proibizione dell'utilizzo di quelli già esistenti. Nell'un
caso come nell'altro, infatti, compare il mancato
riconoscimento dell'embrione come soggetto umano e,
quindi, la sua possibile strumentalizzazione, almeno
nella prima fase della sua esistenza.
Prospettive future: terapia genica
• Le cellule staminali sono in grado di accettare e
tollerare, molto meglio di cellule mature, geni
introdotti dall’esterno con tecniche d'ingegneria
genetica, mirate a correggere l’effetto patologico di
geni difettosi o mutati
• Un singolo trasferimento di gene in una cellula
staminale renderebbe infatti disponibili cellule del
sangue, della pelle, del fegato, e perfino del cervello
“corrette”
TERAPIA
GENICA
Definizione di terapia genica
Insieme di procedimenti atti a curare o alleviare una malattia modificando
geneticamente le cellule dei pazienti.
IN VIVO
EX VIVO
Il materiale è trasferito
nelle cellule direttamente
nel paziente
Le cellule sono prelevate
per inserirvi “in vitro” il
materiale genetico e poi
reintrodotto nel paziente
Le principali classi di malattie che possono essere trattate con la terapia genica
comprendono:
le malattie infettive;
i tumori (attivazione di un oncogene o inattivazione di un gene oncosoppressore o di
un gene preposto all’apoptosi);
le malattie ereditarie;
le malattie del S.I. (allergie, infiammazioni e malattie autoimmuni).
A seconda del tipo di patogenesi si possono prendere in considerazione strategie
differenti di terapia genica.
TRASFERIMENTO GENICO IN VIVO
I geni clonati sono trasferiti direttamente nei tessuti del paziente.
Rappresenta l’unica alternativa per tessuti in cui le cellule non possono essere
coltivate “in vitro” in numero sufficiente (cellule cerebrali) e/o non possono
essere reimpiantate nel paziente.
Uso di liposomi e vettori virali. Impianto di cellule produttrici del vettore (VPC),
infettate “in vitro” con un retrovirus ricombinante, in modo che le cellule VPC
trasferiscano il gene alle cellule circostanti.
Si richiede il trasferimento di un gene clonato in cellule patologiche, spesso si
tratta di un minigene prodotto artificialmente con una sequenza di cDNA unita
ad una sequenza di regolazione che induce elevati livelli di espressione
Efficiente sistema di trasferimento con cellule staminali (piccola popolazione
di precursori indifferenziati da cui derivano le cellule mature differenziate di
ciascun tessuto).
Le cellule staminali non solo producono cellule del tessuto maturo, ma hanno
la capacità di rinnovarsi a dare una popolazione immortale di cellule.
Terapia genica in vivo ed ex vivo
20
40
60
80
100
TS 32*
TS 35
TS 39
TS 33*
TS 34
TS 44*
Lactobacillus curvatus ATCC 25601
TS 43
TS 36*
TS 47*
TS 53*
TS 49*
Lactobacillus parac. paracasei LMG 12586
Lactobacillus parac. tolerans LMG 9191
S 22*
Lactobacillus plantarum ATCC 14917
TS 48*
TS 31*
TS 38*
S 19
TS 50
S 24*
S 25
TS 52*
TS 45
CR 12
CR 17
TS 46*
S 28
S 21
S 20
CR 3
CR 4
TS 37*
TS 40*
TS 41
S 30
CR 11
CR 14
CR 1*
CR 5
Lactobacillus sakei ATCC 15521
S 18*
S 27
S 26
CR 16
CR 9*
CR 10
CR 6
CR 7
CR 8
CR 2
S 23
S 29
TS 51*
CR 15
CR 13*
TS 42*