Azione anti-fibrotica
per offrire più vita
Azione
anti-fibrotica1
dello spironolattone
dimostrata nel cane
Immagine: I. Raymond-Letron ENVT
SPIRONOLATTONE
SVILUPPATO
DALLA
RICERCA
CEVA
SANTE
ANIMALE
CEVA VETEM
FIBROSI E INSUFFICIENZA
CARDIACA
>
ORGANIZZAZIONE STRUTTURALE DEL CUORE
Il cuore è costituito da 3 strati: endocardio, miocardio ed epicardio
• Miocardio = muscolo cardiaco2
• Miociti: 25%
• Cellule non miociti : 75% principalmente fibroblasti
• In condizioni fisiologiche:
• Equilibrio tra entrambi i tipi di cellule
In corso di insufficienza cardiaca:
- alterazione del rapporto tra miociti e fibroblasti
- perdita dei miociti e sostituzione con fibrolasti
- eccesso di deposito di collagene2,3
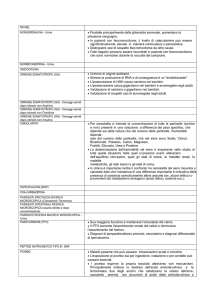
Figura 1: Fibrosi interstiziale sub endocardiale miocardica:
area fibrotica (collagene) colorata in blu (Masson Trichrome,
x40; Photo I. Raymond-Letron ENVT)
CONSEGUENZA: FIBROSI PATOLOGICA MIOCARDICA
RIMODELLAMENTO CARDIACO E FIBROSI
• Definizione di rimodellamento
“
Il rimodellamento cardiaco è un processo complesso che coinvolge modificazioni genetiche,
molecolari e cellulari nei miocardiociti e dello spazio interstiziale (cellule non miociti), che portano
ad alterazioni strutturali e funzionali progressive come dilatazione cardiaca, fibrosi interstiziale e
(Remme WJ, 2003, Cardiovascular Drugs
una riduzione della contrattilità e rilassamento.
4
Ther. 17: 349-60)
“
>
> Principale caratteristica del rimodellamento:
- Fibrosi e dilatazione cardiaca5
> Identificazione del rimodellamento come dilatazione cardiaca:
- Radiografia ed ecocardiografia6
• In cani con Malattia Mixomatosica della Valvola Mitralica si
riscontra una significativa fibrosi miocardica e vascolare 7
• Principali fattori responsabili di questi cambiamenti 3,8
• Carico emodinamico
• Attivazione Sistema Renina - Angiotensina - Aldosterone
> Aldosterone: ruolo chiave dimostrato nel rimodellamento
cardiaco e nel processo fibrotico 9
RUOLO DELL’ALDOSTERONE
NELLA FIBROSI CARDIOVASCOLARE
>
EFFETTO DIRETTO SUL SISTEMA CARDIOVASCOLARE
L’aldosterone si lega ai recettori mineralcorticoidi (MR) del cuore e dei vasi10
• Effetti sul cuore:9,11
Aldosterone
MR
• Fibrosi miocardica
• Effetto sui vasi:9,12
• Fibrosi vascolare
• Ipertrofia della parete vasale
• Conseguenze cliniche:1,13,14
Figura 2: Aldosterone legato ai MR
• Ridotta contrattilità cardiaca, aumento del rigurgito mitralico, aritmia, vasocostrizione e
perdita dell’elasticità vasale
> Affaticamento cardiaco, minore ossigeno ai tessuti
> Peggioramento dell’insufficienza cardiaca
> Aumento della mortalita’
SPIRONOLATTONE:
INTERESSE TERAPEUTICO
>
PROTEZIONE CONTRO GLI EFFETTI DANNOSI
DELL’ALDOSTERONE
Lo spironolattone si lega ai recettori al posto dell’aldosterone: inibizione diretta
• ACE inibitori:
• Non inibiscono la produzione locale di aldosterone
• Parziale e temporanea inibizione dell’aldosterone
(aldosterone escape) 8,15,16
MR
Spironolattone
Aldosterone
• Spironolattone blocca completamente
gli effetti dell’aldosterone 9,10,17
> Spironolattone riduce la fibrosi
cardiovascolare1,9,17
Figura 3: Lo spironolattone si sostituisce all’aldosterone e si
fissa ai suoi recettori. L’azione dell’aldosterone è bloccata.
SPIRONOLATTONE
IL PRIMO ANTAGONISTA DELL ‘ALDOSTERONE
CON EFFETTO ANTIFIBROTICO IN VETERINARIA
> Migliora la sintomatologia clinica dell’insufficienza cardiaca18
> Riduce il rischio di mortalità del 69% 19
• In combinazione con la terapia standarda
• Efficace dai primi segni clinici (Stadio II ISACHCb)
a
b
Terapia standard: ACE inibitore e/o furosemide e/o digossina
International Small Animal Cardiac Health Council
I.C.
• In cani con rigurgito mitralico causato da
mixomatosi della valvola mitralica
Dosaggio: 2 mg/kg/giorno
Compresse divisibili e appetibili
INDICAZIONE(I): Le compresse di PRILACTONE sono usate in combinazione con una terapia standard (incluso un supporto diuretico, quando necessario) per il trattamento dell’insufficienza cardiaca congestizia
causata da rigurgito valvolare nel cane. SPECIE DI DESTINAZIONE: Cani. POSOLOGIA PER CIASCUNA SPECIE, VIA(E) E MODALITÀ DI SOMMINISTRAZIONE: Via orale. 2 mg di spironolattone per kg di
peso vivo una volta al giorno. Il prodotto deve essere somministrato con il cibo. La compressa può essere mischiata con una piccola quantità di cibo offerta prima del pasto principale o somministrata direttamente in
bocca dopo il pasto. PRESENTAZIONI: Le compresse di PRILACTONE vengono fornite in scatole da 30 compresse in blister. PROPRIETÀ FARMACODINAMICHE: Lo spironolattone ed i suoi metaboliti attivi (incluso
7 -tiometil-spironolattone e canrenone) fungono da specifici antagonisti dell’aldosterone e svolgono la loro azione mediante blocco competitivo del recettore dei mineralcorticoidi localizzato a livello renale, cardiaco
e vasale. Lo spironolattone è un farmaco natriuretico (descritto in passato come blando diuretico). Nel rene, lo spironolattone inibisce la ritenzione del sodio indotta dall’aldosterone portando ad un rapido aumento
dell’escrezione del sodio, con conseguente escrezione d’acqua e ritenzione di potassio. L’effetto renale dello spironolattone e dei suoi metaboliti diminuisce il volume del liquido extracellulare e, conseguentemente, il
precarico cardiaco e la pressione atriale sinistra. Il risultato è un miglioramento della funzionalità cardiaca. A livello del sistema cardiovascolare lo spironolattone previene gli effetti dannosi dell’aldosterone. Nonostante
il meccanismo d’azione preciso non è stato ancora chiaramente determinato, l’aldosterone induce fibrosi del miocardio, rimodellamento miocardico e vascolare e disfunzioni endoteliali. In studi sperimentali nel cane,
è stato visto che il trattamento prolungato con antagonisti dell’aldosterone previene la disfunzione progressiva del ventricolo sinistro ed attenua il rimodellamento ventricolare sinistro in cani affetti da insufficienza
cardiaca cronica. In uno studio clinico che ha valutato l’aspettativa di vita di cani affetti da insufficienza cardiaca congestizia, dopo 15 mesi di terapia si è riscontrata una riduzione del 65% del rischio
di mortalità nei cani trattati con lo spironolattone in aggiunta alla terapia standard, rispetto ai cani trattati con la sola terapia standard. (La mortalità è stata classificata come decesso o eutanasia
causata da insufficienza cardiaca). Quando utilizzato in combinazione agli ACE-inibitori, lo spironolattone potrebbe contrastare gli effetti dell’aldosterone “escape”. Un leggero aumento dei livelli di aldosterone nel
sangue può essere osservato negli animali in trattamento. Si ritiene che ciò dipenda dall’attivazione dei meccanismi di feedback senza conseguenze cliniche avverse. Per ulteriori informazioni vedere foglietto illustrativo.
CEVA VETEM
CEVA VETEM S.p.A. - Via Colleoni 15 - 20041 Agrate Brianza (MI) - Tel. 0396559.442 - Fax 0396559.244 - e-mail:[email protected]
www.cevavetem.it
02/10
1 Yang SS, Han W, Zhou HY, et al. Effects of spironolactone on electrical and structural remodeling of atrium in congestive heart failure dogs. Chin Med J (Engl) 2008; 121 (1): 38-42.
2 Jugdutt BI. Remodeling of the myocardium and potential targets in the collagen degradation and synthesis pathways. Curr Drug Targets Cardiovasc Haematol Disord
2003; 3 (1): 1-30.
3 Hill JA, Olson EN. Cardiac plasticit
4 Remme WJ. Pharmacological modulation of cardiovascular remodeling: a guide to heart failure therapy. Cardiovasc Drugs Ther 2003; 17 (4): 349-360. y. NEngl J
Med 2008; 358 (13): 1370-1380.
5 Kalidindi SR, Tang WH, Francis GS. Drug insight: aldosterone-receptor antagonists in heart failure - the journey continues. Nat Clin Pract CardiovascMed 2007; 4 (7): 368-378.
6 Borgarelli M, Savarino P, Crosara S, et al. Survival characteristics and prognostic variables of dogs with Mitral Regurgitation attributable to Myxomatous Valve Disease.
J Vet Intern Med 2008; 22 (1): 120-128.
7 Falk T, Jonsson L, Olsen LH, et al. Arteriosclerotic changes in the myocardium, lung, and kidney in dogs with chronic congestive heart failure and myxomatous mitralvalve
disease. Cardiovasc Pathol 2006;15 (4): 185-193.
8 Oyama MA. Neurohormonal activation in canine degenerative mitral valve disease: implications on pathophysiology and treatment. J Small Anim Pract 2009;50 Suppl 1: 3-11.
9 Ovaert P, Elliott J, Bernay F, et al. Aldosterone receptor antagonists – how cardiovascular actions may explain their beneficial effects in heart failure. Jvet Pharmacol
Therap 2010. Ahead of print.
10 Lombes M, Farman N, Bonvalet JP, et al. Identification and role of aldosterone receptors in the cardiovascular system. Ann Endocrinol(Paris) 2000; 61(1): 41-46.
11 Lijnen PJ, Petrov VV, Fagard RH. Myocardial renin-angiotensin-aldosterone system and extracellular matrix remodeling. Current Topics in Pharmacology 2003; 7: 33-67.
12 Virdis A, Neves MF,Amiri F,et al. Spironolactone improves angiotensin-induced vascular changes and oxidative stress. Hypertension2002;40(4):504-510.
13 Falk T, Jönsson L, Olsen LH, et al. Correlation of cardiac pathology and clinical findings in dogs with naturally occuring congestive heart failure. Abstract. Proceedings of
the 17th annual ACVIM congress. Budapest Hungary. September 13th -15th. Abstract 233. 2007: 636.
14 Falk T. Canine arteriosclerosis occurrence and importance in different heart diseases. 2. Arteriosclerosis- an overview. PhD Thesis 2008; 11-15.
15 MacDonald KA, Kittleson MD, Larson RF, et al. The effect of ramipril on left ventricular mass, myocardial fibrosis, diastolic function, and plasma neurohormones in Maine
Coon cats with familial hypertrophic cardiomyopathy without heart failure. JVet Intern Med 2006; 20(5): 1093-1105.
16 Häggström J, Höglund K, Borgarelli M. An update on treatment and prognostic indicators in canine myxomatous mitral valve disease. JSmall Anim Pract 2009; 50
(Suppl 1): 25-33.
17 Tan LB, Schlosshan D, Barker D. Fiftieth anniversary of aldosterone: from discovery to cardiovascular therapy. Int J Cardiol 2004; 96 (3): 321-333.
18 EMEA. Veterinary Medicines. Prilactone®. European Public Assessment Report Scientific discussion. 2007.
19 Bernay F,Bland JM, Häggström J, et al. Efficacy of spironolactone on survival in dogs with naturally occurring Mitral Regurgitation caused by Myxomatous Mitral Valve Disease.
J Vet Intern Med 2010. Jan 2010.
RISERVATO AI SIGG. MEDICI VETERINARI E FARMACISTI
Bibliografia: