Ipotalamo ed ipofisi posteriore
Regolazione neuroendocrina della omeostasi
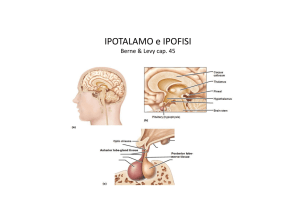
L’Ipotalamo fa parte del diencefalo, è localizzato al di sotto del talamo tra lamina terminalis e corpi mammillari
formando la parete ed il pavimento del terzo ventricolo.
ventricolo Il rilascio degli ormoni ipotalamici è regoalto da differenti
segnali da altre regioni cerebrali, da afferenze viscerali e da livelli circolanti di substrati ed ormoni.
Correlazioni anatomiche tra ipotalamo ed ipofisi
L’Ipotalamo è funzionalmente ed anatomicamente legato alla ipofisi anteriore e posteriore grazie al supporto ematico
fornito dal sistema portale locale. Le arterie ipofisarie anteriori (SHA), le arterie ipofisarie medie, e le arterie ipofisarie
inferiori (IHA), forniscono il supporto di sangue arterioso alla eminenza mediana ed all’ipofisi. I neuroni
magnocellulari dei nuclei sopraottico (SON) e paraventricolare (PVN) hanno lunghi assoni che terminano nella ipofisi
posteriore. Gli assoni dei neuroni parvicellulari terminano nella eminenza mediana, dove rilasciano neuropeptidi. Le
vene portali lunghe drenano la eminenza mediana trasportando i peptidi dai capillari del plesso primario al plesso
secondario che irrora l’ipofisi anteriore.
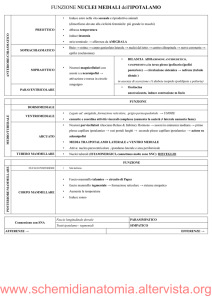
I sei principali ormoni ipofisiotrofici e le localizzazioni
predominanti delle loro cellule di origine
Ormone
Nucleo
ipotalamico
Cellula
Ormone
TRH
Nucleo
paraventricolare
Tireotropa
TSH
LHRH
Ipotalamo ant. e
mediale; area
pre
ottica settale
Gonadotropa
FSH/LH
CRH
Porzione
mediale
parvocellulare
d l nucleo
del
l
paraventricolare
Corticotropa
ACTH
GHRH
Nucleo arcuato
Somatotropa
GH
Somatostatina
i
Area
paraventricolare
anteriore
Somatotropa
GH
Dopamina
Nucleo Arcuato
Lattotropa
PRL
target
target
Sintesi e processing di ossitocina ed argininvasopressina
(AVP)
Effetti fisiologici e regolazione del rilascio di ossitocina
Il rilascio di ossitocina è stimolato dalla distensione della cervix a termine della gravidanza e dalla contrazione dell’utero
durante il parto. I segnali sono trasmessi dai nuclei paraventricolare (PVN) e sopraottico (SON) dell’ipotalamo, ove
inducono un feedback positivo di regolazione del rilascio di ossitocina. L’aumento del numero di recettori per l’ossitocina,
l’incrementato numero di gap junctions tra le cellule muscolari lisce e la incrementata sintesi di prostaglandine innalza la
responsività del muscolo uterino. Il rilascio di ossitocina determina un incremento nella contrattilità uterina, stimolando la
fase espulsiva e la involuzione dell’utero dopo il parto. Anche la suzione stimola il rilascio di ossitocina che induce
contrazione delle cellule mioepiteliali che sono presenti nel dotto galattoforo, inducendo la escrezione di latte.
Meccanismi cellulari di azione della AVP
La principale funzione della AVP è di incrementare il riassorbimento dell’acqua. La AVP si lega ad un
recettore legato ad una proteina G, denominato V2R, presente a livello delle principali cellule del tubulo
distale. Il legame attiva la formazione di AMPc e la formazione di protein chinasi A (PKA). La PKA fosforila
la acquaporina2 (AQP2) nella membrana delle cellule luminali consentendo la permeabilità all’acqua che
lascia la cellula grazie all’azione della acquaporina3 (AQP3) e della acquaporina4 (AQP4) che sono
espresse costitutivamente nella membrana basolaterale delle principali cellule.
I t
Integrazione
i
dei
d i segnalili che
h stimolano
ti l
il rilascio
il
i di AVP
Riduzione PA
Cervello
Centri midollari
Cervello
Osmorecettori
+
_
SO
PV
Peduncolo
Ipovolemia
Aumento osmolalità
plasmatica
Adenoipofisi
Neuroipofisi
+
Vasopressina (AVP)
V2R – AQPs
Cuore
Tubulo renale
+
Ritenzione di acqua
Vasocostrizione
+
Normovolemia





![MATEMATICA DI PRIMAVERA [6] A. Utilizzando la formula diretta e](http://s1.studylibit.com/store/data/000877889_1-bb89aa9dad05c1f6555758a9b74714eb-300x300.png)