(B)InAn
(C)
imaginary
real
cells signals
cell feed
in which
signals
a complex
are linked
to and
of
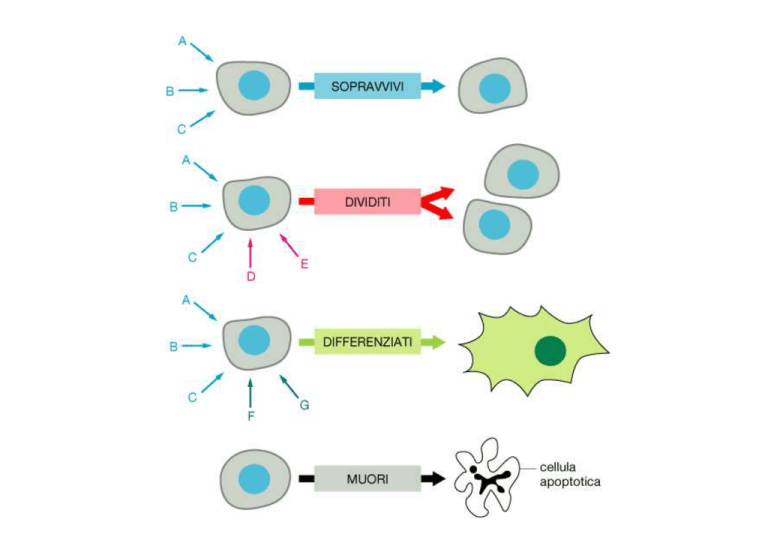
(A)into
In
response
to network
internal
responses
partially
redundant
by linear
external
signals,
a cell
unbranched
interactions,
pathways
the
outcome
chooses
between
stasis, of
stimulation
of
which apoptosis
is notoreasy
inhibition.
to
mitosis,
and
Humananalytically.
predict
cells
do not
sometimes
differentiation.
function like this.
Controllo del Ciclo Cellulare
-Rispondere in modo adeguato ai segnali esterni
-Attivazione di enzimi e proteine responsabili della
conduzione dei vari processi al momento giusto
- Disattivazione alla fine del processo
Punti di controllo
G1 – Start
La cellula cresce, aumenta la propria massa
• Corretta quantità di nutrienti
• Adeguati segnali extra-cellulari
Punti di controllo
G2/M
La cellula completa l’accrescimento
• Controllo massa
• Replicazione del DNA completata
Punti di controllo
Transizione Metafase - Anafase
La cellula si preparara alla citodieresi
• Controllo integrità del fuso mitotico
• Corretta disposizione dei cromosomi
Negli organismi multicellulari la capacità di procedere
oltre i diversi punti di restrizione del Ciclo Cellulare è
regolata da ormoni e fattori di crescita,
che possono stimolare od inibire la divisione cellulare
attivando una
cascata di reazioni mediate da protein-chinasi
citoplasmatiche.
Possiamo considerare il controllo del ciclo come la
risultante di un delicato equilibrio tra l’attività di
proteine diverse.
Tra di esse sembrano rivestire particolari importanza:
• Le protein chinasi ciclina dipendenti CDK
• Le cicline
Le protein chinasi ciclina dipendenti CDK
Sono enzimi capaci di trasferire un gruppo fosfato da
una molecola di ATP ad una specifica proteina
bersaglio modificandone la funzionalità.
Questi enzimi sono sempre presenti nelle cellule ma
non sono sempre attivi:
lo diventano grazie alla loro associazione con
particolari proteine attivatrici, le cicline
Le cicline
Sono proteine la cui concentrazione intracellulare varia
periodicamente in maniera ciclica ed in modo netto
oscillando da zero a valori relativamente elevati
che vengono raggiunti in momenti critici del ciclo
cellulare.
Esse non posseggono attività enzimatica propria,
ma la capacità di interagire con proteine-chinasi
specifiche predisponendone l’attività funzionale
Le protein-chinasi dipendenti da cicline sono eterodimeri:
le subunità catalitiche sono chiamate chinasi dipendenti
da cicline (CDK), poiché la loro attività chinasica dipende
dall’associazione con una ciclina;
Le cicline costituiscono le subunità regolatrici.
L’associazione di una subunità catalitica (dotata
di attività chinasica) con una delle differenti
cicline disponibili determina
la fosforilazione di proteine target diverse e
l’attivazione di pathways chimiche specifiche.
Cdk4 – Ciclina D e Cdk6 – Ciclina D
Cdk2 – Ciclina E
Cdk2 – Ciclina A
Cdk1 – Ciclina A e Cdk1 – Ciclina B
a metà ed alla fine della fase G1
alla fine della fase G1
durante la fase S
durante la fase G2 e la Mitosi
Cell-cycle dependent phosphorylation of Rb
Phosphorylation of Rb
allows cells to transit
the restriction point
and enter S phase
Hyperphosphorylated Rb
p
p
Rb
p
p
p
p
Restriction point
Rb
p
S
p
Rb
p
phase
p
G1
phase
G2
G0
M
Quiescent cells
p
Hypophosphorylated Rb
p
Rb
phase
phase
p
p
p
Rb
p
p
p
p
Rb
p
Il passaggio attraverso il punto di restrizione G0 richiede l’attività
del fattore E2F, il quale promuove la trascrizione di geni codificanti
le proteine necessarie per la duplicazione del DNA cellulare.
Questo fattore è attivato da Cdk2, Ciclina E e Ciclina A.
L’attività di E2F è inibita dal legame con la proteina Rb
ipofosforilata, presente durante la fase M. Le Cdk 4/6, la Ciclina D, e
successivamente la Cdk2 e la ciclina E, fosforilano Rb provocando
il rilascio e la conseguente attivazione di E2F
I danni subiti dal DNA nucleare sono identificati da un
sistema di controllo, attivo durante G1 e G2, che si basa
sulla attivazione di p53, un fattore di trascrizione che
stimola l’espressione di p21CIP.
Questo cyclin-kinase inhibitor (CKI) si lega ai complessi
Cdk-Ciclina e li inibisce, causando l’arresto del ciclo in
G1 oppure in G2 finchè il danno non sia stato riparato
The role of p53 in the cell cycle
apoptosis (cell death)
DNA synthesis
UV irradiation leads
p53
S
to cell cycle arrest
G0
Quiescent cells
phase
G1
phase
G2
M
phase
Mitosis
phase
Growth and
preparation for
cell division
In alternativa, se i danni subìti dal DNA sono di
notevole entità, la proteina p53 attiva il macchinario
apoptotico e determina così il suicidio della cellula.
LIFE
The
term
“life”
describes
a
combination of phenotypes such as
metabolic activity, its restriction to
complex structures, growth, and the
potential to identically self-reproduce.
& DEATH
“Death”, of course, does not occur in
this description. In prokaryotes, death
only seems to be a consequence of
environmental conditions that are not
compatible with the biochemistry and
metabolism that accompanies “life”. In
eukaryotes this accidental cell death
constitutes the phenotype called
necrosis.
Okada et al. 2004 Nature Reviews Cancer 4: 592592-603
Perdita della normale morfologia con diminuzione del volume cellulare,
specifica degradazione del DNA e delle proteine, comparsa dei corpi apoptotici
ed attivazione della fagocitosi tissutale.
Le pathways coinvolte nella morte cellulare per suicidio sono
oggetto di numerosissimi studi e
non sono ancora del tutto caratterizzate
La morte cellulare programmata è determinata geneticamente
(circa 300 geni del nostro genoma)
Proteine proapoptotiche (Bax-alfa)
Proteine antiapoptotiche (Bcl2)
(A) Oocytes with a high level of pro-apoptotic
gene expression, possessing an imbalance
towards programmed cell death.
(B) Oocytes with almost equal distribution
of pro- and anti-apoptotic factors suggestive of
a balance between survival and death molecule
contributions.
(C) Oocytes with an excess of anti-apoptotic
factors indicative of a strong survival pathway.
Distribution of five pro- and anti-apoptotic
genes in 15 individual MII stage human
unfertilized oocytes obtained from several
patients. The expression of Bag-1 (yellow),
Bax (orange), Bcl-x (pale blue), Hrk (red) and
Mcl-1 (dark blue) was determined using
quantitative dot–blot RT-PCR. The total
amount of gene expression was calculated
for these pro-apoptotic (orange and red) and
anti-apoptotic (yellow, pale blue and dark blue)
genes, each pie piece representing the
contribution for that particular gene. The
oocytes were then grouped on the basis of their
expression profiles.
Negli Eucarioti multicellulari il controllo dinamico
della morte cellulare per suicidio,
suicidio,
in stretta correlazione con quello della proliferazione,
oltre ad essere un meccanismo fondamentale durante lo sviluppo
embrionale (Rimodellamento dell’
dell’embrione)
consente l’l’eliminazione delle cellule senescenti, danneggiate
oppure mutate senza che venga alterato l’l’assetto fisiologico
dell’
dell’organismo.
APOPTOSI
I meccanismi genetici e molecolari dell’apoptosi furono identificati per la
prima volta nel nematode Caenorhabditis elegans . Basandosi sugli studi
eseguiti su questo animale, si è stabilito di suddividere il processo apoptotico in
3 fasi.
1) induzione
2) esecuzione
3) riconoscimento e fagocitosi
del corpo apoptotico
FASE DI INDUZIONE
Le vie indotte possono essere due
Via dei recettori della morte
Via mitocondriale
Via dei recettori della morte
Nella via dei recettori della morte intervengono i legami di
specifiche molecole-segnale ai propri recettori posti sulla
membrana plasmatica: ad esempio, il legame del recettore Fas col
suo ligando Fas-L determinerebbe un avvio del processo
apoptotico
Via mitocondriale
Nella via mitocondriale intervengono i mitocondri, con la liberazione di
attivatori delle caspasi come il citocromo C, con cambiamenti nel
trasporto elettronico, con l'alterata ossido-riduzione cellulare con la
partecipazione della famiglia delle proteine pro- e anti-apoptiche Bcl-2
FASE DI ESECUZIONE
La fase di esecuzione è comune a quasi tutte le vie
d’innesco ed è costituita da una serie di reazioni
enzimatiche a cascata. Una volta innescata, la reazione
non è più arrestabile e procede automaticamente,
portando a morte la cellula.
RICONOSCIMENTO E FAGOCITOSI
Nei tessuti i corpi apoptotici vengono riconosciuti e fagocitati dalle
cellule circostanti e dai macrofagi e degradati all’interno dei lisosomi.
il risultato finale è sempre quello di eliminazione “pulita”
Con la comparsa degli organismi multicellulari,
la morte cellulare per suicidio
acquista un significato biologico
Omologhi di geni coinvolti
nella morte cellulare per
suicidio sono stati trovati nei
protisti,
protisti, anche se con
funzione apparentemente
differente.
Inoltre forme primitive di morte
cellulare “non necrotica” sono
state osservate in alcuni
protozoi ed in eubatteri.
eubatteri.
Caratterizzazione del Macchinario Apoptotico
Kroemer et al. (2005) Nature Medicine 11 (7): 725
In alcuni casi l’avvenire dell’apoptosi è programmato, cioè è parte
integrante del programma di sviluppo e differenziamento degli
organismi (morte cellulare programmata);
in altri casi l’avvio del processo apoptotico è determinato da eventi
accidentali quali:
danni subiti dalle strutture e molecole della cellula (e.g., le
membrane, il DNA genomico oppure quello mitocondriale,
l’RNA e le proteine), che non siano di entità tale da causare la
morte per necrosi
mancanza di fattori trofici, tra i quali i più caratterizzati sono le
neurotrofine (e.g., NGF, BDNF e NT-3) che sono essenziali per il
corretto sviluppo del sistema nervoso
Alterazioni dell’attività di proteine pro o anti apoptotiche
possono causare:
•
Malattie neurodegenerative
•
Neoplasie












