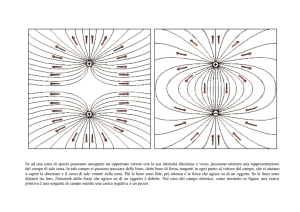
“Sulle metodiche impedenziometriche”
Ing. Tony Talluri, Akern R&D-Firenze
1. Analisi d’impedenza bioelettrica (BIA) a corpo intero.
Attualmente l'unico metodo in grado di valutare specificamente l'idratazione in qualsiasi condizione
clinica e indipendentemente dal peso corporeo è l'analisi d’impedenza bioelettrica (BIA), a corpo intero
(whole-body BIA). Bioimpedenza e impedenza bioelettrica sono usati come sinonimi. Utilizzata e
interpretata correttamente, la BIA è in grado di cogliere variazioni d’idratazione tissutale d’interesse clinico,
per misura diretta e specifica di grandezze elettriche dipendenti solo dall'idratazione tissutale. E' una tecnica
relativamente recente, che ha potuto trovare impiego clinico solo a partire dagli anni '80, in seguito alla
realizzazione d’analizzatori portatili (RJL Systems negli USA, /Akern Srl in Italia) che operassero in
analogia all'elettrocardiografo.
La tecnica attuale, infatti, sfrutta gli elettrodi cutanei utilizzati per l'ECG, posizionati in due coppie
(tecnica tetrapolare mano-piede) consentendo l'esecuzione delle misure in modo rapido (meno di cinque
minuti, inclusa l'applicazione degli elettrodi), non invasivo, innocuo, ripetibile, a basso costo, con i vantaggi
della portabilità (dall'ambulatorio, alla corsia, alla sala dialisi, alla terapia intensiva) e senza interferenze con
altra strumentazione elettrica sanitaria.
La tecnica di misura tetrapolare è semplice: sono applicati quattro elettrodi cutanei, una coppia sul
dorso della mano (preferita la destra), uno sull'articolazione metacarpo-falangea del III dito (elettrodo
iniettore), e l'altro sull'articolazione radio-ulnare (elettrodo sensore), e una coppia sul dorso del piede
omolaterale, uno sull'articolazione metatarso-falangea del III dito (iniettore), e l'altro sull'articolazione tibiotarsica (sensore). Il paziente, supino, non a contatto con elementi metallici, può tenere scoperti solo mano e
piede ipsilaterali, con arti inferiori divaricati di 45° e arti superiori abdotti di 30° per evitare contatti cutanei
con il tronco. I cavetti dell'analizzatore sono collegati con pinzette agli elettrodi.
Figura 1
Nella BIA standard, viene iniettato un impulso di corrente alternata a 50 kHz d’intensità innocua per i
tessuti (400 µA).
Alcuni analizzatori restituiscono un valore d’impedenza (modulo del vettore, in Ohm), altri riescono a
misurare le due componenti del vettore impedenza, Resistenza (R) e Reattanza (Xc) in Ohm. Non viene
utilizzata corrente continua (frequenza zero kHz), che non potrebbe attraversare le membrane cellulari.
La BIA è basata sul principio che i tessuti biologici si comportano come conduttori, semiconduttori o
dielettrici (isolanti). Le soluzioni elettrolitiche intra ed extracellulari dei tessuti magri sono ottimi conduttori,
mentre osso e grasso sono sostanze dielettriche, e non vengono attraversati dalle correnti utilizzate nei
pletismografi d’impiego clinico [1-4].
I metodi d’analisi della composizione corporea sono stati classificati esaustivamente in sei categorie,
essendo basati su tre quantità misurabili (proprietà, componenti, o la combinazione delle due) e su 2 tipi di
funzioni matematiche (tipo I, ottenute da analisi statistica di misure quantitative, e tipo II, contenenti rapporti
o proporzioni costanti) [1]. La BIA come metodo di analisi della composizione corporea, pur nascendo
come metodo basato su una proprietà misurabile (impedenza), può essere classificata come metodo tipo I
basato su proprietà e su funzioni statistiche (intervalli di confidenza, di tolleranza, regressioni semplici o
multivariate), come tipo I combinato, ma anche tipo II combinato, secondo la complessità delle assunzioni
[1]. Infatti, la misura dell'impedenza fornita dall'analizzatore BIA può venire sfruttata seguendo due vie: la
BIA convenzionale e la BIA vettoriale. Nella BIA convenzionale, numerosi software, sfruttando equazioni
di regressione (Tabella 1) che generalmente includono statura, peso, età, e sesso, trasforma la misura di
impedenza in volumi (intracellulare, extracellulare), masse (grassa, magra, cellulare), metabolismo basale, e
altre grandezze dell'analisi di composizione corporea. Nella BIA vettoriale, come nella lettura dell'ECG,
viene interpretata la misura diretta di impedenza per via grafica fornendo una valutazione semiquantitativa
dell'idratazione tissutale.
2.BIA convenzionale.
La BIA si è sviluppata nell'ambiente dei nutrizionisti che hanno ottenuto risultati molto interessanti
nell'analisi della composizione corporea dell'adulto sano o, comunque con idratazione normale e costante.
Tutti questi risultati, senza eccezione, non sono applicabili al paziente uremico, che semplicemente non ha
mai un'idratazione normale e costante. Molti nefrologi, peraltro, nella pratica clinica e in letteratura, hanno
utilizzato la BIA convenzionale anche nell'uremico in dialisi, ottenendo risultati contrastanti, la cui
accuratezza dipendeva dall'idratazione dei gruppi di pazienti studiati.
Tutti i metodi di analisi della composizione corporea, inclusa la BIA convenzionale, mirano a
quantificare i compartimenti in condizioni fisiologiche e patologiche. La quantificazione dei compartimenti in
unità di massa (Kg) o di volume (L) quando sia vincolata ad assunzioni di struttura o di funzioni dei
compartimenti stessi, può risultare accurata soltanto in condizioni fisiologiche di stato stazionario, e pertanto
poco utile al clinico, in particolare al nefrologo. Esclusi i metodi multicompartimentali basati sull'attivazione
neutronica [1], improponibili nella pratica clinica, tutti i metodi attuali di analisi, inclusi i comuni metodi di
riferimento degli studi di composizione corporea, come la diluizione isotopica, l'idrodensitometria e la
densitometria (dual energy X-ray absorptiometry, DXA) sono accurati solo se l'idratazione è normale,
uniforme e costante [1-5].
I fluidi del corpo umano vengono ripartiti in acqua corporea totale (total body water, TBW),
distribuita nei compartimenti intracellulare (LIC) ed extracellulare (LEC), questo a sua volta suddiviso in
intravascolare ed interstiziale. Ad eccezione dello spazio intravascolare e di eventuali raccolte patologiche, i
fluidi non sono liberi ma legati e distribuiti nella struttura della massa corporea. La massa corporea può
essere pensata in termini di un modello bicompartimentale, come massa grassa (fat mass, FM) e massa
senza grasso (fat-free mass, FFM). Gran parte delle applicazioni della BIA convenzionale sono basate sul
modello bicompartimentale. La massa senza grasso può essere ulteriormente ripartita in massa magra (lean
body mass) e contenuto minerale osseo, ottenendo un modello tricompartimentale della massa corporea
[1], impiegato nelle analisi DXA a corpo intero.
La BIA convenzionale consente di ottenere stime accurate di TBW, FFM e FM nell'adulto sano, con
coefficienti di correlazione sempre prossimi a 1 (r > 0.95) e un errore di stima dell'ordine di 3-4 Kg [3,614]. La quantificazione della TBW in L o Kg viene ottenuta a partire dal rapporto fra statura (H) al
quadrato e R (indice di impedenza, H2/Z o di resistenza H2/R) al quale vengono aggiunte altre variabili per
aumentare l'accuratezza della regressione. Nella Tabella 1 sono riportate equazioni di regressione
raccomandate in letteratura [6] per stimare nell'adulto la TBW, la FFM, e la FM per differenza della FFM
2
dal peso corporeo. Molti stimano la TBW e da questa calcolano la FFM= TBW/0.73. Spesso non si
conoscono le formule utilizzate nei software del commercio.
Purtroppo, qualsiasi condizione associata ad idratazione della FFM differente dal 73% (TBW= 0.73 x
FFM) introduce una distorsione nelle stime di questi compartimenti, con imprevedibile propagazione
dell'errore anche nei metodi di riferimento [1]. Esempi: la DXA evidenziava una riduzione post-HD non
solo della massa magra anche della densità ossea (0.6%). La BIA convenzionale forniva stime "peggiori"
della DXA e le pliche cutanee venivano ridotte del 5% [15]. Con la DXA in HD (6 mesi) si determinava un
aumento di FM di 2.1 Kg, un calo di massa magra di 1.2 Kg, a fronte di un aumento di peso del paziente
di 0.96 Kg (e ipotensione) [16].
Pertanto, a parità di accuratezza della misura della proprietà bioelettrica impedenza (errore dello
strumento analizzatore), le stime dei compartimenti di un soggetto che non sia adulto sano, saranno tanto
meno accurate quanto più la realtà clinica si discosterà dalle assunzioni standard (es. edema, disidratazione,
cachessia, e obesità a qualsiasi età, ma anche crescita normale del neonato e del lattante). Quest’errore
delle stime dei compartimenti non è quantificabile, perché anche i metodi di riferimento della composizione
corporea assumono l'idratazione costante, né prevedibile.
L'inutilità clinica delle stime dei compartimenti fornite dalla BIA convenzionale con formule della è
dimostrata [20].
La distorsione (bias) fra formule differenti aumenta sia per TBW che per FFM, e quindi per FM, negli
obesi e negli edematosi. Ma anche nei soggetti sani la variabilità è eccessiva per sostenere un ragionevole
uso clinico.
Questo fenomeno è dovuto alla differente posizione del vettore sul piano R-Xc [20,28].
L'errore dell'utente può essere evitato facendo buon uso delle misure dirette di impedenza fornite dal
pletismografo analizzatore.
3.IMPEDENZIOMETRIA A MULTIFREQUENZA
Teoricamente una corrente alternata a bassa frequenza (< 5 kHz) dovrebbe circolare solo nei fluidi
extracellulari, mentre una corrente a frequenza elevata (> 500 kHz) dovrebbe attraversare anche tutte le
cellule contenenti soluzioni elettrolitiche. Tuttavia la frequenza standard a 50 kHz presenta delle proprietà
ottimali, attraversando la maggior parte delle cellule e generando un vettore di impedenza con angolo di
fase massimo nello spettro di frequenze da 5 a 1000 kHz (rapporto massimale segnale/rumore).
Va subito chiarito che la tecnica a multifrequenza deve essere discriminata fra spettroscopica (Hanai, ColeCole, Fricke) e non ossia misurazione del modulo (Z) a varie frequenze, in quanto quest’ultima e’ una
tecnica datata [Thommaset 1963], che limitandosi a misurare il modulo (Z) a frequenze che in genere
vanno da 5Khz a 500 Khz, cerca di discriminare la ECW con il rapporto alta/bassa frequenza (in genere
100khz/5Khz)
a. SPETTROSCOPIA A IMPEDENZA
In teoria, e in cellule sospese in soluzione, la stima dei volumi del LEC si otterrebbe dalla R a
frequenza 0 e la stima della TBW dalla R a frequenza infinita, e la stima del LIC dalla differenza.
Con la spettroscopia a impedenza e quindi con strumenti sensibili alla fase a tutte le frequenze,
applicando la trasformata di Cole-Cole si ottiene i valori di R teorici a frequenza 0 e i valori di R teorici a
frequenza infinita, usando come modello bioelettrico il modello Fricke o Hanai che sono modelli in vitro. In
realtà nei tessuti, il percorso della corrente è più complesso. Contrariamente al modello in vitro, una
corrente a bassa frequenza attraversa fibre muscolari sulle quali l'impatto sia avvenuto con direzione
3
parallela [4,26]. Peraltro, studi clinici comparati hanno sempre dimostrato una correlazione elevata fra le
misure sia di R sia di Xc ottenute a 50 kHz con quelle ottenute alle frequenze elevate [37-39].
b. Multifrequenza non spettroscopica
Per discriminare fra totale ed extracellulare usa il rapporto”Zl/Zh” ossia il risultato della divisione dei
valori di Z ottenuti a frequenza “bassa” (tipicamente 5Khz) e frequenza “alta” (tipicamente 100Khz).
Quest’approccio non ha dato risultati clinicamente utili [41]
Infine, la misura dell'impedenza alle frequenze elevate rappresenta un problema tecnico, che in qualche
analizzatore si traduce in instabilità delle misure. Questo comporta una propagazione dell'errore nelle
formule di regressione, annullando eventuali vantaggi dell'analisi dei compartimenti LEC e LIC.
La multifrequenza ha avuto un momento di “successo” commerciale legato alla novità, e alle robuste
campagne pubblicitarie, ma una volta messa alla prova clinica, ha dimostrato la sua inadeguatezza [41, 37]
Se si considera che la valutazione dell’assetto nutrizionale con impedenziometria e’ basato sopratutto
sulla stima della Massa Cellulare (BCM) [ 42, 43 ], non si riscontra ad oggi l’esistenza letteratura
specifica di validazione per la tecnica multifrequenza per la BCM, per la quale sono usate equazioni che
sono specifiche della BIA Akern/RJL Systems, ossia BIA tradizionale del tipo sensibile alla fase, a 50Khz.
Le nostre proposte.
L’analisi della composizione corporea se è usata per diagnosticare lo stato nutrizionale, lo stato di
idratazione e le relative loro variazione (follow-up) per essere clinicamente utile, necessita al pari di tutti gli
strumenti di diagnosi, di due requisiti essenziali: sensibilità e specificità.
L’uso di due parametri fondamentali, quale l’altezza ed il peso per ottenere i volumi di TBW, FFM,
FM, BCM, ECW, etc rendono tutti i metodi di analisi della composizione corporea o poco specifici, in
quanto le variazioni di peso sono aspecifiche (può variare uno solo dei compartimenti elencati, mentre il
peso è distribuito a pioggia su tutti) e poco sensibili soprattutto sugli adulti in quanto l’altezza e’ una
costante e quindi inserire una costante per scoprire una variabile fa perdere di sensibilità.
Tuttavia entrando nel merito delle equazioni, e’ opportuno che l’Utente abbia ben presente che non
esistono equazioni validata ma strumenti validati attraverso equazioni ricavate usando le misure degli
stessi.Ossia prima è effettuata la misurazione bioelettriche, dopo l’analisi di regressione verso metodiche di
riferimento. Le equazioni diventano cosi specifiche per popolazione e per strumento ( rif. Marta Van Loan,
Chumlea, Cameron )
Di conseguenza
1- La letteratura di validazione allegata è SPECIFICA per strumenti. Tale specificità è rilevabile nei
capitoli "Materiali e Metodi" ed é stata chiarita in più riprese da pubblicazioni guida.
2- Gli studi di validazione per la stima attraverso il BIA 101 RJL Systems della Massa Cellulare e del
rapporto Na/K di Harry Shizgal, così come quelli di Kotler, Certow sulla massa cellulare etc. sono
specifici per strumento, e a nostra conoscenza non esistono pubblicazioni di validazione di stima della
Massa Cellulare con impedenziometri, anche se funzionanti in multifrequenza..
La soluzione proposta, che fa uso diretto delle misure ottenute dalla BIA tradizionale a 50 Khz sono
le seguenti:
A:BIA VETTORIALE
Basi razionali della BIA vettoriale.
4
L'impedenza bioelettrica è una proprietà misurabile dovuta alla conduzione ionica dei tessuti, in altre
parole dell'idratazione dei tessuti. La corrente alternata a intensità e frequenza (50 kHz) costanti iniettata
sulla cute da elettrodi-cerotto attraversa le soluzioni elettrolitiche del LEC e del LIC di tutti i tessuti, esclusi
grasso e osso, generando un Vettore impedenza Z, espresso in Ohm. Le membrane cellulari e le interfacce
dei tessuti sfasano la conduzione di corrente (angolo di fase fra tensione e corrente del vettore Z)
generando la componente capacitiva di Z, ovvero Xc [1-4].
Il Vettore Z può essere rappresentato in coordinate polari con modulo e angolo di fase, oppure nelle
usuali coordinate rettangolari Z= (R, Xc), ovvero Z= R + j Xc, con le due componenti Resistenza (R,
dipendente dalle soluzioni LIC+LEC attraversate) e Reattanza (Xc, dipendente da membrane e interfacce
attraversate). La rappresentazione rettangolare (R, Xc) con R in ascisse e Xc in ordinate fornisce oltre al
modulo |Z|=√(R2 + Xc2) anche l'angolo di fase come arcotangente di Xc/R.
La BIA quindi può riconoscere e misurare specificamente solo il compartimento conduttore dei tessuti,
compartimento espresso come valore di R dalle soluzioni elettrolitiche intra ed extracellulari, e come valore
di Xc dall'insieme delle membrane cellulari del compartimento stesso. L'estensione ad altri compartimenti è
stata una forzatura, con ottima tenuta statistica di correlazione nell'adulto normale, ma catastrofica nel
patologico.
Analisi vettoriale con il Grafo Resistenza-Reattanza.
Le limitazioni insite nelle assunzioni della BIA convenzionale possono essere superate seguendo un
approccio fenomenologico basato sull'analisi vettoriale delle misure dirette R e Xc fornite dal pletismografo,
in assenza di vincoli a modelli compartimentali o assunzioni sull'idratazione.
Il metodo denominato Grafo Resistenza-Reattanza (Grafo RXc) confronta il vettore misurato in un
individuo con l'intervallo di riferimento della popolazione normale, di forma ellissoidale, espresso in
percentili della distribuzione normale (gaussiana) bivariata (Fig. 1) [17,18]. Un grafo è una
rappresentazione grafica quantitativa di relazioni complesse fra variabili, non riducibili a rappresentazioni
grafiche semplici, come una distribuzione di frequenza (istogramma), una correlazione fra due variabili
(diagramma di dispersione), o un sistema dinamico di regolazione (diagramma a blocchi). Il metodo del
Grafo RXc può essere classificato come metodo di analisi di composizione corporea basato su una
proprietà elettrica (conduzione ionica dei tessuti) descritta dalla più semplice funzione statistica di tipo I,
ovvero la deviazione standard bivariata delle proprietà elettriche misurate (property-based method, type I
function) [1].
Nell'adulto le due componenti R e Xc del vettore impedenza Z sono correlate significativamente sia nel
soggetto normale che nel patologico [17-22], perfino nelle misure segmentarie di impedenza [23], con
coefficiente di correlazione simile nei maschi e nelle femmine. Pertanto ogni variazione, fisiologica o
patologica, di R o di Xc è tendenzialmente associata ad una variazione proporzionale dell'altra
componente. La correlazione fra R e Xc, la stessa fra R/H e Xc/H, determina la forma ellissoidale delle
distribuzioni di probabilità bivariate (intervalli di confidenza e tolleranza). Se la correlazione fra le
componenti non fosse nulla, le ellissi di probabilità diventerebbero cerchi [14,24]. Lo stesso livello di
correlazione è stato osservato anche nei bambini sani in età prescolare (1-6 anni) [25]. Questa correlazione
invalida molti risultati delle comuni analisi statistiche univariate della letteratura, condotte separatamente su
R o su Xc.
Siccome l'opposizione al passaggio della corrente [2-4,26] dipende anche dalla lunghezza del
conduttore (Z= Impedività x Lunghezza / Area di sezione del conduttore), si può ottenere una
standardizzazione fra individui (conduttori) di lunghezza diversa dividendo il vettore Z per la statura,
ovvero, in coordinate rettangolari Z/H= (R/H, Xc/H) o Z/H= R/H + j Xc/H. Si ottiene così un'espressione
per l'impedenza in Ohm/m con le dimensioni di Impedività/Area di sezione, grandezza indipendente dalla
5
lunghezza del conduttore e che rappresenta sul Grafo RXc l'opposizione alla conduzione ionica di un
individuo rispetto alla variabilità della popolazione di riferimento. Questa trasformazione di vettore bivariato
è valida anche per le variabili casuali complesse (com'è Z, di cui R è rappresenta la parte reale e Xc la
parte immaginaria), ed è invariante per la forma delle ellissi, le probabilità associate e l'angolo di fase.
L'elevata variabilità (biologica) della composizione corporea, fra sessi, fra individui dello stesso
genere, e nello stesso individuo in tempi diversi, può essere rappresentata statisticamente sfruttando la
distribuzione gaussiana (normale) bivariata del vettore impedenza. Il vettore Z misurato nel soggetto
"medio" di riferimento può pertanto essere rappresentato al centro di ellissi di probabilità (ellissi di
isodensità di probabilità, sezioni parallele al piano RXc della classica campana gaussiana), dette ellissi di
tolleranza, la cui area (percentile) fornisce la probabilità di contenere un punto (vettore) del piano RXc
[17,18].
La distribuzione normale bivariata del vettore impedenza nella popolazione sana, con tre percentili di
riferimento (ellissi di tolleranza al 50%, 75% e 95%) e specifica per genere, è nota per la popolazione
adulta italiana (726 soggetti, 15-85 anni, BMI 17-31) [18].
Il metodo del Grafo RXc consente la rappresentazione del vettore sia di gruppi che di individui. Sono
calcolati intervalli di confidenza al 95% per i vettori medi e intervalli di tolleranza per singoli vettori. Le
formule per il calcolo dei parametri delle ellissi di confidenza e tolleranza sono riportate altrove [17,24]
Un vettore medio di un gruppo di soggetti (RXc mean graph, Grafo RXc media) viene rappresentato
come freccia al centro dell'ellisse di confidenza al 95% (Fig. 1). Se due ellissi di confidenza al 95% non
s’intersecano, i due vettori medi differiscono significativamente (P < 0.05) per lunghezza, per angolo di fase
o per entrambi. Il test T2 di Hotelling è il test statistico inferenziale equivalente [17,24,27].
Un vettore individuale, unica determinazione su un soggetto (RXc point graph, Grafo RXc punto)
viene rappresentata da un punto sulle ellissi di tolleranza della popolazione di riferimento. Le misure ripetute
sullo stesso soggetto, con una spezzata che congiunge i punti successivi (RXc path graph, Grafo RXc
percorso) in un follow-up di bioimpedenza. In pratica il Grafo RXc percorso porta al confronto statistico
diretto, per via grafica, della variabilità individuale con quella collettiva [17].
Una proprietà importante del metodo è di operare indipendentemente dalla conoscenza del peso
corporeo, misura che in situazioni cliniche particolari (es. paziente a postura obbligata o in unità di terapia
intensiva) per le comuni valutazioni antropometriche o di bilancio metabolico.
Il metodo ovviamente richiede le misure esplicite delle due componenti R e Xc, che gli analizzatori di
impedenza RJL-Akern (RJL Systems, Clinton Twp, MI, USA, riescono a fornire con grande stabilità di
misura anche fra strumenti di diversa generazione.
Altri analizzatori in commercio in Italia non rilevano direttamente e separatamente R e Xc, e pertanto
non consentono l'applicazione del metodo del Grafo RXc.
Il metodo del Grafo RXc potrebbe anche garantire un'applicazione corretta delle formule di
regressione della BIA convenzionale, formule utilizzate nei software degli apparecchi per BIA. Più il vettore
di un soggetto cade vicino al centro della distribuzione (dentro all'ellisse di tolleranza al 50%), più dovrebbe
esser elevata l'accuratezza delle formule di regressione convenzionali (validate su soggetti normali) per la
stima dei volumi (TBW, in L) e delle masse (FFM e FM, in Kg). E' verosimile che l'accuratezza si
mantenga soddisfacente entro l'ellisse di tolleranza al 75% [28].
La validazione clinica non è stata ancora completata. Finora sono state identificate sul Grafo RXc le
regioni occupate dai vettori Z di pazienti con differenti gradi d’idratazione e d’obesità-magrezza. Altre
variazioni della composizione corporea potrebbero trovare una rappresentazione tipica sul Grafo RXc,
allargando l'orizzonte delle applicazioni cliniche [29].
Interpretazione del Grafo Resistenza-Reattanza.
6
Le variazioni di composizione corporea rilevabili sul Grafo RXc sono associate a variazioni
d’idratazione tissutale (variazioni d’impedenza). Dalla validazione clinica condotta finora si può formulare
una regola di lettura del Grafo RXc molto semplice (vedi figura):
a) Variazioni dell'idratazione senza alterazioni della struttura tissutale (tipicamente variazioni in acuto) sono
associate ad un accorciamento (iperidratazione) o un allungamento (disidratazione) del vettore
impedenza lungo l'asse maggiore delle ellissi di tolleranza [17,23,31,28,19,20,21,22].
b) A fronte di una stessa variazione d’idratazione, i vettori corti migrano poco, i vettori lunghi migrano
molto. Il Grafo RXc è quindi più sensibile nella regione di disidratazione rispetto alla regione
dell'edema. Questa proprietà è dovuta alla relazione non lineare (iperbolica) fra impedenza e acqua
corporea [28]. Un vettore è considerato corto se fluttua di sotto al polo inferiore dell'ellisse di
tolleranza al 50% (limite inferiore della mediana normale). E’ considerato lungo se fluttua oltre il polo
superiore dell'ellisse di tolleranza al 50% (limite superiore della mediana normale).
c) Variazioni dello "stato di nutrizione" dei tessuti (cellule e proteine strutturali interstiziali idrofile) [13],
senza alterazioni dell'idratazione tissutale, sono associate ad una migrazione del vettore nella direzione
dell'asse minore delle ellissi, con aumento progressivo dell'angolo di fase (obesità per i vettori corti,
massa muscolare per i vettori lunghi), o con riduzione progressiva dell'angolo di fase (cachessia per i
vettori corti, anoressia per i vettori lunghi).
d) Variazioni combinate d’idratazione e struttura dei tessuti sono associate a migrazioni del vettore lungo la
combinazione delle due direzioni principali.
e) Variazioni ortogonali (solo R, o solo Xc), ad analizzatore tarato (tester a R e Xc fisse), sono errori di
misura (cortocircuiti da contatto fra arti e tronco, elettrodi scaduti o poco adesivi, cute ricoperta di
creme, circuiti instabili sulle connessioni dei cavetti).
1. Idratazione tissutale.
Un vettore più corto (R minore) indica contenuto tissutale di fluidi maggiori e un vettore più lungo (R
maggiore) indica contenuto di fluidi minore. La correlazione fra Xc e R associa variazioni d’idratazione dei
tessuti a migrazioni del vettore lungo l'asse maggiore delle ellissi (polo inferiore-polo superiore). Un'alterata
distribuzione di membrane cellulari e interfacce interstiziali rispetto alle soluzioni elettrolitiche (intra ed
extracellulari) si associa a migrazioni del vettore con direzione differente dall'asse maggiore (es. anoressia,
cachessia, obesità grave). Questa relazione fondamentale può essere osservata anche nei vegetali [4]. Dati
preliminari nel bambino in età prescolare sono risultati consistenti con quelli ottenuti nell'adulto [25]. Valori
di R più elevati ricorrevano in neonati (3 gg) sottopeso e in lattanti (2-6 mesi) disidratati rispetto a controlli,
anche a fronte di differenti posizionamenti degli elettrodi [30].
Il Grafo RXc, operando solo su grandezze elettriche non richiede il peso corporeo e quindi può
spiegare le variazioni di peso attraverso la trasformazione di un vettore bivariato continuo in una valutazione
semiquantitativa dell'idratazione su scala ordinale a 7 punti (basata sulle tre ellissi di isodensità di probabilità
e sui due versi dell'asse maggiore: entro il 50%, fra 50% e 75% polo inferiore o superiore, fra 75% e 95%
polo inferiore o superiore, fuori del 95%, polo inferiore o superiore) in qualsiasi condizione clinica.
Data l'inclinazione dell'asse maggiore delle ellissi di tolleranza, dovuta alla correlazione fra R e Xc,
l'accumulo di fluidi è associato a vettori più corti con angolo di fase minore. Finora è stato identificato il
polo inferiore dell'ellisse di tolleranza al 75% come soglia per l'edema apparente nell'adulto, con 100% di
Sensibilità, 92% di Specificità, e 99% di Valore Predittivo Negativo per prevalenze di edema inferiori al
25%. In altri termini, un soggetto con vettore interno al polo inferiore dell'ellisse al 75%, ha una probabilità
inferiore a 1% di avere edema apparente [17,20,31]. Pertanto l'analisi vettoriale può identificare
l'iperidratazione subclinica nel paziente che sta accumulando fluidi prima della comparsa dell'edema, segno
7
clinico inequivocabile di espansione dei fluidi, ma che diventa apparente dopo un aumento di peso di 4-5
Kg, corrispondente ad un'espansione del LEC del 30% [32].
In Fig. 1 è indicata la traiettoria (media) seguita dal vettore medio di gruppi di pazienti con progressiva
espansione dei volumi fluidi, dai pazienti con insufficienza renale cronica (IRC) in terapia conservativa, ai
pazienti con proteinuria nefrosica (SN), a quelli con edema apparente (Edema).
Per la disidratazione, più difficile da identificare clinicamente, non è stata ancora identificata una soglia
di utilità clinica sulle ellissi di tolleranza. E' probabile che il polo superiore dell'ellisse al 75% rappresenti un
confine importante [17,19,22,28], consistente anche con la distribuzione dei vettori nel colera [33] e al
termine di una seduta di emodialisi [21].
Le indicazioni dell'analisi vettoriale BIA sono risultate complementari a quelle fornite dalla Pressione
Venosa Centrale (PVC). Nonostante la correlazione negativa significativa fra PVC e la coppia R/H e
Xc/H, il 93% dei pazienti con PVC elevata (> 13 mmHg) presentavano vettori corti, fuori del polo
inferiore dell'ellisse di tolleranza al 75%, ma solo il 10% di pazienti con PVC bassa (0-3 mmHg)
presentava vettori di impedenza lunghi, oltre il polo superiore dell'ellisse di tolleranza al 75% [22]. Pertanto
le infusioni in questi pazienti con PVC bassa potrebbero venire modulate sulle indicazioni dell'analisi
vettoriale BIA.
2. Discriminazione fra grasso e fluidi.
Nonostante la debole corrente iniettata non attraversi il tessuto grasso, l'analisi vettoriale col Grafo
RXc consente di differenziare l'accumulo di grasso dall'accumulo di fluidi nell'adulto, verosimilmente grazie
alla differente struttura dei tessuti molli conduttori nelle due situazioni.
I vettori degli obesi (BMI > 31 Kg/m2) sono mediamente più corti del normale, ma con angolo di fase
conservato o maggiore (Tabella 2, Fig. 1). In altri termini il vettore di un obeso con BMI= 40 Kg/m2 può
cadere dentro o fuori dell’ellisse di tolleranza al 75%. Se è corto e cade fuori dell’ellisse al 75%, conserva
un angolo di fase normale. E' stata individuata una funzione discriminante (barriera lineare) capace di
identificare correttamente (91%) i vettori corti appartenenti ad obesi senza edema (sopra la barriera) e
quelli dei pazienti con edema (sotto la barriera) [20].
Una verifica della sensibilità specifica del metodo per l'idratazione si è ottenuta dimostrando un
allungamento del vettore in obesi uremici dopo rimozione di circa 3 Kg di fluidi con seduta di HD, a fronte
di nessuna migrazione del vettore dopo un mese di dieta ipocalorica con perdita di 7-11 Kg di peso
(Tabelle 4 e 5) [20].
Da casi aneddotici, il vettore di grandi obesi che sviluppano insufficienza cardiorespiratoria con edema
apparente, migra nella direzione dei vettori dei pazienti con edema, accorciandosi e riducendo
progressivamente l'angolo di fase. Migrazioni in direzione opposta si possono osservare dopo rimozione di
fluidi con emodialisi. Pertanto anche le variazioni di idratazione nell'obeso, ove le formule BIA
convenzionali producono stime distorte dei volumi e delle masse, sul Grafo RXc causano le stesse
migrazioni del vettore di impedenza dei soggetti non obesi.
3. Analisi vettoriale BIA in HD.
Il peso raggiunto dal paziente alla fine di una seduta di emodialisi (HD) che abbia rimosso il massimo
di fluidi senza indurre ipotensione viene definito convenzionalmente peso secco.
Un gruppo di studio nazionale (HD-BIA study group, 38 Centri, riportati in Appendice) ha
recentemente potuto determinare su 1116 pazienti (età 16-89 a) che raggiungevano il peso secco senza
sintomi (stabili), la distribuzione del vettore impedenza all'inizio e alla fine della seduta HD (Tabella 6) [21].
Il vettore medio migrava dal polo inferiore (pre-HD) al polo superiore (post-HD) dell'ellisse mediana della
popolazione sana.
8
La distribuzione dei singoli vettori intorno ai vettori medi migrava ciclicamente entro l'ellisse di
tolleranza al 75%, dal polo inferiore (inizio seduta) al polo superiore (fine seduta), indicando che la terapia
sostitutiva riusciva a mantenere le caratteristiche bioelettriche normali dei tessuti degli uremici in HD.
Queste migrazioni cicliche del vettore di impedenza sul Grafo RXc (accorciamento-allungamento),
accoppiate al ciclo delle variazioni di peso (denominato ciclo del peso umido-secco), costituiscono una
base razionale per modificare la prescrizione dialitica nei pazienti con migrazione del vettore all'esterno
dell'ellisse di tolleranza al 75%, sia del peso secco da raggiungere allo stacco, che del peso umido da
portare all'inizio della seduta HD. La prescrizione del peso in feedback sulla migrazione del vettore Z
all'interno dell'ellisse al 75% porterebbe modifiche al peso umido (riduzione) nel 30% e al peso secco
(aumento) nel 50% dei pazienti studiati [21].
La distribuzione dei vettori di 251 pazienti instabili (ipotensioni sintomatiche in oltre il 30% delle sedute
negli ultimi tre mesi), con lo stesso BMI degli stabili, era traslata a destra (20-25% più frequentemente i
vettori erano più lunghi con un angolo di fase minore degli stabili). L'analisi del follow-up di mortalità a due
anni stabilirà se i pazienti con vettore oscillante entro o fuori l'ellisse di tolleranza al 75% siano sottoposti a
un rischio di morte differenziato. Dati della letteratura indicherebbero un rischio maggiore di morte per i
pazienti con angolo di fase < 4.5°, valore prossimo all'angolo di fase del vettore medio del gruppo di
instabili [34,35].Negli instabili peraltro, concentrazioni minori di albumina e Hb rispetto ai pazienti stabili,
hanno riproposto il ruolo della nutrizione sulla patogenesi dell'instabilità emodinamica in HD. La
considerazione del solo angolo di fase del vettore può avere un qualche significato soltanto per R costante,
normale ed entro genere, circostanze ignorate in letteratura. In Tabella 2 e Fig. 1 è evidente come i pazienti
edematosi con sindrome nefrosica abbiano un angolo di fase intorno a 3°. Clinicamente è difficile accettare
che abbiano un rischio di morte maggiore degli instabili in HD, o di pazienti con AIDS [36].
4. Analisi vettoriale BIA in DP.
In DP l'idratazione è molto variabile e viene valutata sulla base di criteri clinici. L'applicazione della
BIA convenzionale nel paziente in DP porta a stime distorte dei compartimenti. Dai dati preliminari di uno
studio multicentrico nazionale, il vettore del paziente in DP senza edema occuperebbe una regione
corrispondente al vettore dei pazienti stabili all'inizio della seduta HD. Le soluzioni per dialisi libere in
peritoneo non modificano l'impedenza, che pertanto può essere misurata ad addome pieno o vuoto.
5. Analisi vettoriale BIA nel bambino.
Saranno disponibili a breve i valori di riferimento normale, come ellissi di tolleranza al 50%, 75% e
95% per i neonati e i bambini per classi di età fino a 15 anni. Il vettore (espresso come Z/H, Ohm/m)
segue sul Grafo RXc una traiettoria di maturazione elettrica individuata in uno studio preliminare [25], con
accorciamento progressivo fino a raggiungere il vettore medio degli adulti dello stesso genere. La
validazione clinica stabilirà se le variazioni di composizione corporea nel bambino saranno associate a
migrazioni del vettore seguendo il modello dell'adulto.
Conclusioni.
Sfruttando le misure dirette di impedenza con il metodo del Grafo RXc è possibile ottenere una
valutazione semiquantitativa (in percentili) dello stato di idratazione di un soggetto adulto e anziano, da 15 a
85 anni, confrontando il vettore impedenza misurato con la variabilità della popolazione di riferimento
descritta dalle ellissi di tolleranza, specifiche per genere.
Il metodo non richiede alcuna assunzione di modello, di composizione corporea, o di idratazione, ed
essendo indipendente dal peso corporeo ne può spiegare le variazioni.
9
L'analisi vettoriale BIA, alla stregua dell'ECG, potrebbe effettivamente diventare uno strumento di
routine nella valutazione dell'idratazione di tutti i pazienti, alla prima visita e nei controlli periodici.
Un'ulteriore e più ampia validazione clinica dovrà confermarne l'utilità nell'analisi della composizione
corporea nelle situazioni più complesse con variazioni combinate di idratazione e nutrizione.
La BIA convenzionale potrebbe avere impiego clinico in poche situazioni a composizione corporea
normale e stabile.
B:SOFT TISSUE ANALYSIS , le misure dirette
Basi Razionali
La tecnica impedenziometrica (BIA) standard consiste nel misurare la caduta di tensione causata
dall’impedenza globale di un corpo al quale viene applicata una corrente alternata e costante (modulo Z),
mentre alcuni strumenti più sofisticati misurano separatamente le sue componenti, ossia la Reattanza (Xc) e
la Resistenza (Rz). Tramite queste misure non invasive, abbinate a formule specifiche per strumento e
popolazione, vengono ottenuti i valori relativi e assoluti di Acqua Corporea e delle Masse Magra e Grassa.
Per migliorare i risultati sono state sviluppate numerose formule, specifiche per popolazione o patologia,
che includono peso, altezza, età e sesso del soggetto.
Critiche all’Analisi BIA
A causa della manipolazione matematica della misura vengono riscontrate varie problematiche che limitano
l’utilizzo clinico negli stati patologici.
Quali sono i problemi riscontrati ad oggi
1. La valutazione del grasso corporeo (ottenuta attraverso l’ausilio di formule empiriche) non
permette interpretazioni sullo stato d’idratazione e nutrizione del paziente.
2. Tutte le formule sono ottenute con metodi statistici di regressione che determinano una
propagazione d’errori dato che:
a.
I risultati ricavati dalle differenti tecniche vengono paragonati tra loro senza che esista un
vero gold standard di riferimento.
b.
Gli algoritmi vengono validati sulla base di metodi di regressione specifici per popolazione,
sesso ed età.
c.
Parametri avulsi dalla misura come l’altezza, il peso, l’età o il sesso e altre costanti inserite
nelle formule contribuiscono a determinare fino all’80% del risultato finale, relegando così la misura
ad un ruolo marginale.
d.
Le formule spesso ricavate da soggetti sani vengono applicate sui pazienti senza
considerare il loro stato di salute.
3. Le formule si basano sull’ipotesi che l’ idratazione della massa magra sia sempre il 73%. Purtroppo
qualsiasi condizione associata ad idratazione della FFM differente dal 73% introduce una distorsione
nelle stime dei compartimenti con un’imprevedibile propagazione dell’errore che influenza l’intera
l’analisi di composizione corporea.
Gli scompensi idro-elettrolitici possono essere causa o conseguenza di numerose patologie. La loro
valutazione è stata fino ad oggi di difficile esecuzione, richiedendo l’uso di tecniche invasive.
La misura diretta
10
Il sistema Akern STA (Soft Tissue Analyzer) è attualmente l’unico strumento al mondo in grado di
misurare direttamente, indipendentemente dal peso, età o altezza del soggetto, i compartimenti
fondamentali per la valutazione dello stato nutrizionale: la Massa Cellulare (BCM) e la percentuale
d’Acqua Extracellulare (ECW%), eliminando il pericolo di conclusioni sbagliate indotte dagli errori
intrinseci delle equazioni.
Attraverso la misura delle proprietà dielettriche dei tessuti conduttivi, come muscoli e parenchima, è
possibile valutare con alta sensibilità e specificità i valori relativi e assoluti di idratazione e cellularità: dalla
misura capacitiva deriva direttamente la superficie totale delle membrane cellulari, attraverso la quale viene
determinata la massa cellulare. I valori così ottenuti non derivano quindi dalla conduttività del soggetto
che è una variabile dipendente anche dalla lunghezza del conduttore.
BCM in chilogrammi e la percentuale di ECW evidenzia immediatamente lo stato fisiologico del soggetto,
in altre parole lo stato di idratazione e nutrizione.
Esecuzione de lla misura:
Dopo aver applicato 4 elettrodi al paziente, si ottengono direttamente e immediatamente sullo schermo i
seguenti risultati: BCM in chilogrammi, ECW in percentuale, Metabolismo Basale in Kcal, Reattanza,
Resistenza in Ohm ed Angolo di Fase in gradi.
Interpretazione dei dati e loro applicazione clinica
Tramite i due valori fondamentali BCMkg ed ECW% si valuta lo stato di idratazione e nutrizione del
paziente.
1.
Un valido aiuto all’interpretazione della BCM è dato dalla formula che permette di ricavare la
quantità minima teorica di massa cellulare che un individuo dovrebbe avere:
BCMmin in Kg = Altezza in cm – 100 x 0.3 (m) { 0.28 (f)}
2.
Una quantità di BCM superiore ai minimi calcolati indica uno stato di nutrizione adeguato.
Nei soggetti normonutriti l’acqua extracellulare (ECW) è considerata normale se è il 40%
dell’acqua totale (TBW). Le oscillazioni fisiologiche vanno da un minimo del 38% ad un massimo
del 45%. Percentuali superiori al 45% possono essere dovute a ritenzione idrica, malnutrizione o
ad entrambe le situazioni, mentre percentuali inferiori al 38% sono dovute a disidratazione
extracellulare.
3.
In presenza di valori di BCM normali, il valore della ECW ci permette di valutarne lo stato di
idratazione.
4.
L’Angolo di fase diminuisce quando la massa cellulare si riduce, è quindi un valore significativo per
l’interpretazione dello stato di nutrizione. La diminuzione dell’angolo di fase può inoltre essere
causata dall’aumento dei fluidi extracellulari a causa di disturbi del bilancio idrico.
L’angolo di fase di un giovane ben nutrito e ben idratato va dai 6 agli 8 gradi.
Il Nomogramma BIAVECTOR® (clinicamente validato) mostra graficamente lo stato fisiologico di un
soggetto, permettendo un veloce controllo dei risultati. Il nomogramma è composto da tre aree, definite
elissi di confidenza (50%), tolleranza (75%) anormalità (95%) ed è in grado di evidenziare con ottima
sensibilità e specificità il reale stato di idratazione in qualsiasi condizione clinica e indipendentemente dal
peso corporeo.
Il nomogramma è suddiviso in 4 settori:
11-Il vettore di
un soggetto
ben nutrito cade nei due
settori a sinistra dell’asse
STEADY STATE
DYNAMIC STATE
LESS
FLUIDS
DEHYDRATION
-3
-1
0
Xc/H, Ohm/m
Xc/H, Ohm/m
-2
MO
AN RE M A
D ST
SS
RU C
TURE
LE SS
STR U MA SS
CT U A ND
RE
+1
+2
+3
MORE
FLUIDS
ANASARCA
R/H, Ohm/m
R/H, Ohm/m
Variazioni dell’idratazione sono associate ad un accorciamento (iperidratazione) o un allungamento
(disidratazione) del vettore di impedenza lungo l’asse maggiore.
Lo stato di idratazione di un soggetto si normalizza quando il vettore si avvicina al centro del grafo.
Esempio 1:
Soggetto di sesso maschile
Risultati della misura
BCM= 16,2kg
Resistenza (Rz)= 463 Ohm
Angolo di fase (PA)= 3,4°
Altezza= 170cm
ECW%= 61,6%
Reattanza (Xc)= 28 Ohm
Ad una prima analisi dei dati il basso valore di BCM di 16,2 Kg mostra una chiara malnutrizione. Il
calcolo della BCMmin (170cm – 100) x 0,3 = 21kg) conferma questa interpretazione. Il valore
misurato di ECW del 61,6 % indica con evidenza una espansione dell’interstizio del paziente
Interpretazione dell’Analisi BiaVector®
Il grafo BIA VECTOR® evidenzia la diagnosi sopra riportata in
quanto Il vettore cade sul limite dell’ellisse di confidenza al
95% confermando una notevole iperidratazione e
malnutrizione.
Un vettore di impedenza corto, abbinato ad un angolo di fase
molto basso (3,5°), è un indice prognostico negativo
L’interpretazione delle misure fornite dal Soft Tissue Analyzer,
senza conoscere il peso e lo stato di salute del soggetto è
giusto: si tratta delle misure effettuate pre-dialisi su un
soggetto di 80 anni con un peso corporeo di 55,5 Kg.
12
Esempio 2
Soggetto di sesso femminile
Risultati della misura (post dialisi)
BCM= 22,9 Kg
Resistenza (Rz)= 702 Ohm
Angolo di Fase (PA)= 7,3°
Altezza= 156 cm
ECW%= 40,4%
Reattanza (Xc)= 90 Ohm
Solo dai dati di misura risulta un soggetto con una discreta Massa Cellulare (BCMmin teorica 15,7
Kg) ed una buona idratazione. L’angolo di fase risulta molto buono (7,3°).
Interpretazione dell’Analisi BiaVector®
Il grafo rappresenta la migrazione del vettore pre e post
dialisi. L’esame pre-dialisi (quadrato) mostra che il paziente,
con una buona situazione idrica considerata la sua patologia,
avrebbe potuto essere sottoposto alla sola purificazione.
L’esame post – dialisi (punto) mostra la migrazione del
vettore fuori dal Grafo, nella zona di estrema disidratazione.
Questo esame mostra un caso in cui l’ultrafiltrazione a cui è
stato sottoposto il paziente non era in effetti necessaria,
poiché il trattamento lo ha “asciugato” troppo portandolo alla
disidratazione.
Esempio 3
Soggetto di sesso maschile
Altezza= 177 cm
Risultati della misura (pre dialisi)
BCM=21,5 kg
Resistenza (Rz)= 491 Ohm
ECW%= 52,1%,
Reattanza (Xc)= 41 Ohm Angolo di fase (PA)= 4,8°
Risultati della misura (post dialisi)
BCM=23,6 kg
Resistenza (Rz)= 566 Ohm
ECW%= 45,5%,
Reattanza (Xc)= 60 Ohm Angolo di fase (PA)= 6,1°
Interpretazione dell’analisi Biavector®
E’ il tipico esempio di migrazione pre / post dialisi: il primo
esame (quadrato) mostra una iperidratazione (ECW =
52,2%). L’analisi post-dialisi (punto) mostra l’allungamento
del vettore di impedenza (disidratazione) lungo l’asse
maggiore. I due vettori, situati leggermente a destra dell’asse
mediano, indicano malnutrizione (BCMmin= 23,1 Kg)
L’aumento di BCM è spiegabile da una sostanziale
reidratazione intracellulare, probabilmente imputabile alla
cinetica dell’urea, che rimanendo intrappolata nelle cellule
richiama fluidi e genera successivamente il fenomeno del
“rebound”.
Esempio 4 :
Soggetto di sesso maschile
Risultati della misura
BCM= 38,7 kg
Altezza= 176cm
ECW%= 38,2%,
13
Resistenza (Rz)= 451 Ohm
Reattanza (Xc)= 63 Ohm Angolo di fase (PA)= 8,0°
La Massa Cellulare minima teorica di questo soggetto dovrebbe essere 22,8 Kg. Il valore misurato
è ben superiore, indicando perciò un’ ottima forma fisica (stato di nutrizione) con una pronunciata
muscolatura. Il valore di ECW% misurato è leggermente inferiore ai valori di normalità (dal 43 al
45% per i maschi sotto i 30 anni). L’interpretazione dei dati è confermata dall’ottimo angolo di fase
riscontrato (8°).
Interpretazione dell’analisi Biavector® :
Il vettore del soggetto cade in alto a sinistra dell’asse
mediano, identificato come il settore caratteristico di soggetti
con una ottima forma fisica (tante cellule e tanta acqua
intracellulare) tipica degli atleti.
Soggetto di questo esame è un giovane sportivo che lavora
come bagnino e che pesa 88,6 Kg.
Esempio 5
Soggetto di sesso femminile
Risultati della misura
BCM= 11,5 Kg
Resistenza (Rz)= 900 Ohm
Angolo di Fase (PA) =4,8°
Altezza = 155 cm
ECW%= 52,5%
Reattanza (Xc) = 75 Ohm
La paziente ha una massa cellulare estremamente bassa (11,5 kg contro un minimo teorico di 15
,4 kg) sintomo di una grave malnutrizione. L’elevata ECW riscontrata potrebbe essere causata
dalla sola malnutrizione (neoglucogenesi da proteine interne: acqua intracellulare divenuta
extracellulare a causa della rottura delle membrane cellulari) o anche da una forte iperidratazione.
Interpretazione dell’analisi Biavector® :
Il vettore cade al di fuori delle ellissi del 95% nel settore a
destra indice di disidratazione e malnutrizione. Questo tipo di
posizionamento del vettore in alto all’estrema destra del
Grafo è tipico dei soggetti molto magri, emaciati o affetti da
anoressia nervosa. Un angolo di fase di 4,8° indica un cattivo
rapporto tra Resistenza e Reattanza, ovvero uno
sbilanciamento tra acqua e cellule presenti.
L’interpretazione dei dati senza la conoscenza di peso,
altezza, età è giusta: trattasi di una giovane anoressica del
peso di 29 Kg.
Esempio 6
14
Soggetto di sesso maschile
Risultati della misura:
BCM= 54kg
Resistenza (Rz) = 362 Ohm
Angolo di Fase (PA)= 8,8°
Altezza= cm 173
ECW%=35%
Reattanza (Xc) =56 Ohm
L’alto valore di Massa cellulare di 54 Kg si riferisce sicuramente ad un soggetto una muscolatura
molto sviluppata (BCMmin= Kg. 21.9)Il valore della ECW% è sotto il valore ottimale (40-45%),
sintomo di leggera disidratazione.
Interpretazione dell’analisi Biavector® :
Nel nomogramma il vettore cade nel settore a sinistra (buona
nutrizione) al limite dell’ellisse del 95% di anormalità, nella
zona che indica una estesa struttura cellulare tipica di atleti e
soggetti con molta massa cellulare.
L’angolo di fase di 8,8° conferma un’ottima forma fisica
(angoli di fase superiori a 8 sono tipici di sportivi)
Anche qui l’interpretazione che abbiamo dato con i soli dati di
misura e confermato nel nomogramma è giusta: si tratta di
un Body builder professionista con un peso corporeo di 86,8
Kg.
Esempio 7:
Soggetto di sesso maschile
Risultati della misura:
BCM= 11kg
Resistenza (Rz) = 508 Ohm
Angolo di Fase (PA) = 2,5°
Altezza = 171 cm
ECW%= 70%
Reattanza (Xc) = 22 Ohm
Le misure del paziente mostrano un valore molto basso di Massa cellulare, indicante un soggetto
fortemente deperito. Il Valore di ECW del 70% mostra una iperidratazione con presenza di edema.
L’angolo di fase incredibilmente basso può risultare dall’associarsi dei fenomeni di malnutrizione ed
iperidratazione.
Interpretazione dell’analisi Biavector ®
Il vettore del soggetto cade in basso a destra fuori dall’ellisse
del 95%, nella zona tipica dell’edema con malnutrizione.
L’angolo di fase di 2,5° è indice prognostico negativo, a
conferma del grave squilibrio tra i livelli di BCM ed ECW
riscontrati .
Si tratta di un uomo di 40 anni, malato di cancro con un livello
di BCM bassissimo (11 Kg) ma di un peso corporeo totale di
91,4 Kg.
15
Esempio 8:
Soggetto di sesso feminile
Risultati della misura:
BCM= 24,8 kg
Resistenza (Rz) = 312 Ohm
Angolo di Fase (PA) = 3,5°
Altezza = 166 cm
ECW%= 61,1%
Reattanza (Xc) = 19 Ohm
Anche se il valore di BCM risulta sufficiente (BCMmin=19,8 kg)., la quota di ECW del 61,1% indica
una forte iperidratazione e la presenza di edema. I soli dati di misura elettrica, estremamente
anomali, esprimono che si tratta di un soggetto fortemente patologico. La conferma ci viene data
dall’angolo di fase estremamente basso (3,5°).
Interpretazione dell’analisi Biavector®
Il vettore cade al di fuori dell’ellisse del 95%, nella zona di
edema: ciò causa il suo basso angolo di fase. Tuttavia il suo
stato di nutrizione è ancora accettabile. Anche in questo caso
un vettore di impedenza corto, abbinato ad un angolo di fase
basso (3,5°), è indice prognostico fortemente negativo
L’esame STA – Biavector non prende in considerazione la
quantità di grasso corporeo, bensì la qualità dei tessuti
analizzati.
Il soggetto in esame è una donna di 57 anni del peso di 160 Kg che ha un assetto nutrizionale
ancora accettabile, ma con una significativa ritenzione idrica.
BIBLIOGRAFIA
1. Heymsfield SB, Wang ZM, Visser M, Gallagher D, Pierson RNJr: Techniques used in the measurement
of body composition: an overview with emphasis on bioelectrical impedance analysis. Am J Clin Nutr
64:478S-484S,1996.
2. Lukaski HC: Biological indexes considered in the derivation of the bioelectrical impedance analysis. Am
J Clin Nutr 64:397S-404S, 1996.
3. Kushner RF: Bioelectrical impedance analysis: a review of principles and applications. J Am Coll Nutr
11:199-209,1992.
4. Foster KF, Lukaski HC: Whole-body impedance - what does it measure ? Am J Clin Nutr 64:388S396S, 1996.
5. Roubenoff R, Kehayas JJ, Dawson-Hughes B, Heymsfield SB: Use of dual-energy X-ray
absorptiometry in body composition studies: Not yet a "gold standard". Am J Clin Nutr 58:589-591,
1993.
16
6. Houtkooper LB, Lohman TG, Going SB, Howell WH: Why bioelectrical impedance analysis should be
used for estimating adiposity. Am J Clin Nutr 64:436S-448S, 1996.
7. Kushner RF, Schoeller DA. Estimation of total body water by bioelectrical impedance analysis. Am J
Clin Nutr 44:417-424, 1986.
8. Kushner RF, Schoeller DA, Fjeld CR, Danford L. Is the impedance index (ht2/R) significant in
predicting total body water ? Am J Clin Nutr 56:835-839, 1992.
9. Lukaski HC, Bolonchuck WW. Estimation of body fluid volumes using tetrapolar bioelectrical
impedance measurements. Aviat Space Environ Med 59:1163-1169, 1988.
10. Lukaski HC, Bolonchuck WW, Hall CB, Siders WA. Validation of tetrapolar bioelectrical impedance
method to assess human body composition. J Appl Physiol 60:1327-1332, 1986.
11. Gray DS, Bray GA, Gemayel N, Kaplan K. Effect of obesity on bioelectrical impedance. Am J Clin
Nutr 50:255-260, 1989.
12. Heitman BL. Prediciton of body water and fat in adult Danes from measurements of electrical
impedance. Int J Obes 14:789-802,1990.
13. Deurenberg P, van der Kooy K, Leenen R, Westrate JA, Seidell JC. Sex and age specific prediction
formulas for estimating body composition from bioelectrical impedance: a cross-validation study. Int J
Obes 15:17-25, 1991.
14. Stolarczyk LM, Heyward VH, Hicks VL, Baumgartner RN. Predictive accuracy of bioelectrical
impedance in estimating body composition of Native American women. Am J Clin Nutr 59:964-970,
1994.
15. Abrahamsen B, Hansen TB, Hosberg IM, Pedersen FB, Beck-Nielsen H: Impact of hemodialysis on
dual X-ray absorpiometry, bioelectrical impedance measurements, and anthropometry. Am J Clin
Nutr 63:80-86, 1996.
16. Stenver DI, Gotfresden A, Hilsted J, Nielsen B: Body composition in dialysis patients treated with
erythropoietin, measured by dual-energy x-ray absorptiometry. Abstr XIIIth ICN, Madrid, 1995.
17. Piccoli A, Rossi B, Pillon L, Bucciante G. A new method for monitoring body fluid variation by
bioimpedance analysis: The RXc graph. Kidney Int 46:534-539,1994.
18. Piccoli A, Nigrelli S, Caberlotto A, Bottazzo S, Rossi B, Pillon L: Bivariate normal values of the
bioelectrical impedance vector in adult and elderly populations. Am J Clin Nutr 61:269-270,1995.
19. Piccoli A, Piazza P, Noventa D, Pillon L, Zaccaria M: A new method for monitoring hydration at high
altitude by bioimpedance analysis. Med Sci Sports Exerc 28:1517-1522, 1996.
20. Piccoli A, Brunani A, Savia G, Pillon L, Favaro E, Berselli ME, Cavagnini F: Discriminating between
body fat and fluid changes in the obese adult using bioimpedance vector analysis. Int J Obesity 22:97104, 1998.
21. Piccoli A, for the Italian HD-BIA Study Group: Identification of operational clues to dry weight
prescription in hemodialysis using bioimpedance vector analysis. Kidney Int 53:1036-1043,1998.
22. Piccoli A, Pittoni G, Facco E, Pillon L: Relationship between central venous pressure and
bioimpedance vector analysis in critically ill patients. Crit Care Med, in press (1999).
23. Piccoli A, Rossi B, Pillon L: Operational equivalence between segmental and whole-body bioelectrical
impedance in renal patients. Am J Clin Nutr 59:675-676,1994.
24. Lentner C: Introduction to statistics. Statistical tables. Mathematical formulae, in Geigy Scientific
Tables (vol 2, 8th ed), Basle, Ciba-Geigy Limited, 1982, pp. 215-218.
25. Piccoli A, Pillon L, Pisanello L, Zacchello G: Electrical maturation trajectory of human tissues identified
by bioelectrical impedance vector analysis. Nutrition 15:77-78,1999.
26. Barber DC: Electrical impedance tomography. In The biomedical engineering handbook, edited by
Bronzino JD, Boca Raton, CRC Press, 1995, p. 1151-1164.
17
27. Dixon WJ, Brown MB, Engelman L, Jennrich RI. BMDP statistical software manual. Berkeley,
UCLA, 1992.
28. Piccoli A, Pillon L, Favaro E: Asymmetry of the total body water prediction bias using the impedance
index. Nutrition 13:438-441,1997.
29. Lukaski HC: A new approach to estimate changes in total body water by bioelectrical impedance
analysis. Nutrition 13:474-475, 1997.
30. Gartner A, Sarda P, Dupuy RP, Maire B, Delpeuch F, Rieu D: Bioelectrical impedance analysis in
small- and appropriate-for-gestational-age newborn infants. Eur J Clin Nutr 48:425-432,1994.
31. Piccoli A, Rossi B, Pillon L, Bucciante G: Body fluid overload and bioelectrical impedance analysis in
renal patients. Miner Electrolyte Metab 22:76-78,1996.
32. Guyton AC: Human physiology and mechanisms of disease. Philadelphia, Saunders, 1982, p 240.
33. McDonald JJ, Chanduvi B, Velarde G, Cama R, Diaz F, Carrillo R, Torre V, Watanabe J, Villareal J,
Ramirez-Ramos A, Mantle R, Gilman RH: Bioimpedance monitoring of rehydration in cholera. Lancet
341:1049-1051,1993.
34. Maggiore Q, Nigrelli S, Ciccarelli C, Grimaldi C, Rossi GA, Michelassi C: Nutritional and prognostic
correlates of bioimpedance indexes in hemodialysis patients. Kidney Int 50:2103-2108, 1996.
35. Chertow GM, Lowrie EG, Lew NL, Lazarus JM: Bioelectrical impedance analysis predicts survival in
hemodialysis patients. J Am Soc Nephrol 7:1442,1996.
36. Ott M, Fischer H, Polat H, Helm EB, Frenz M, Caspary WF, Lembcke B. Bioelectrical impedance
analysis as a predictor of survival in patients with human immunodeficiency virus infection. J Acquir
Immune Defic Syndr 9:20.25, 1995.
37. Hannan WJ, Cowen SJ, Fearon KCH, Plester CE, Falconer JS, Richardson RA. Evaluation of multifrequency bio-impedance analysis for the assessment of extracellular and total body water in surgical
patients. Clin Sci 86:479-485,1994.
38. Patel RV, Peterson EL, Silverman N, Zarowitz BJ: Estimation of total body and extracellular water in
post-coronary artery bypass graft surgical patients using single and multiple frequency bioimpedance.
Crit Care Med 24:1824-1828, 1996.
39. Garosi G, Talluri T, Capotondo L, Di Paolo N: L'analisi della bioimpedenza nelle malattie renali. In: Di
Paolo N: Semeiotica del rene e delle vie urinarie. Wichtig, Milano, 1995, pp. 535-565.
40. Edefonti A, Loi S, Ardissino G, Dagnino L, Ghio L, Damiani B, Sandoval Diaz M: Use of
bioimpedance (BIA) to modify dry weight in patients on chronic hemodialysis (HD). J Amer Soc
Nephrol 9:247A, 1998.
41. P. Deurenberg, A. Tagliabue, F.J. Schouten: Multy-frequency impedance for the preiction of
extracellular water and total body water. British Journal of Nutrition 73 : 349-358, 1995.
18