19-09-2007
18:37
Pagina 397
Quorum sensing microbico
e igiene degli alimenti
Valerio Giaccone
Università di Padova
Premessa
I batteri sono esseri viventi come tutti gli altri, solo un po’ meno complessi come struttura. Per decenni sono stati visti come esseri viventi molto individualisti che conducono la loro esistenza come singole cellule
libere in un mezzo, alla costante ricerca di
nutrienti per sopravvivere e, se ci sono le
possibilità, riprodursi. In realtà oggi sappiamo che i batteri fanno parte di una società
piuttosto complessa e che sono in grado di
comunicare fra loro.
Non si può dire che parlino o cantino, così
come accade all’uomo o come fanno (in modo più elementare) delfini e balene, ma certo si scambiano informazioni rilasciando nell’ambiente una serie di messaggi che i loro
consimili percepiscono.
Per esempio, i batteri periodicamente fanno
il censimento della popolazione e tastano il
terreno, ossia verificano praticamente in tempo reale le condizioni dell’ambiente che li
circonda, sia esso l’ambiente esterno o l’interno di un essere animato come una pianta, un animale o l’uomo stesso.
In questo contesto i batteri producono e rilasciano nell’ambiente circostante alcuni
composti chimici specifici che fungono da
trasmettitori del messaggio; altri batteri li
captano, li interpretano e rispondono producendo a loro volta dei messaggi, diciamo
così, odorosi.
Nella società dei batteri (o meglio, nell’ambiente in cui una certa popolazione microbica è inserita) corrono costantemente dei
segnali chimici, molecole di piccole dimensioni simili agli anticorpi e chiamati autoinduttori. Queste molecole si accumulano al
di fuori delle singole cellule microbiche, ma
finché la carica microbica è bassa e diluita
nell’ambiente esterno non succede nulla.
Quando però la stessa popolazione si
accresce e supera un certo livello (un quorum, visto come numero legale per una votazione) le molecole che si sono accumulate possono innescare una serie di eventi
che si succedono per lo più con effetto “a
cascata” determinando qualche reazione o
qualche effetto. Questo sistema di comunicazione è chiamato, appunto, quorum sensing. Il quorum sensing, in altri termini, è un
sistema complesso di comunicazione “cellula-cellula” con il quale i batteri sono in grado di comunicare fra loro.
Grazie a questo sistema i batteri sono capaci di mettere in atto attività coordinate, una
capacità che un tempo si riteneva propria
soltanto degli esseri viventi superiori.
Questa capacità di comportarsi come un
9 / 397
Contributi scientifici
09_settembre_2007_DEF.qxp
09_settembre_2007_DEF.qxp
19-09-2007
18:37
Pagina 398
Contributi scientifici
organismo complesso coordinato ha parecchi vantaggi per una popolazione microbica, quali la capacità di migrare verso
un altro ambiente dove si trovino migliori
condizioni di habitat e di nutrienti o l’adozione di nuovi modelli di sviluppo che potrebbero costituire una difesa contro le aggressioni esterne.
Alla luce delle nuove acquisizioni in questo settore si profila all’orizzonte una nuova disciplina, la “socio-microbiologia” che
dovrebbe studiare i comportamenti di una
singola popolazione batterica che funziona come un aggregato coordinato di esseri viventi e non come un insieme caotico e
disordinato di singole entità.
Sfruttando il quorum sensing i
batteri possono regolare:
1) l’emissione di bioluminescenza
2) la formazione di biofilm sulle superfici di lavoro nelle
industrie alimentari
3) la crescita competitiva tra
differenti popolazioni e la
sporulazione
4) la sintesi di antibiotici e di
batteriocine
5) l’induzione di fattori di virulenza nelle piante o negli
umani
6) i processi di infezione degli
organismi superiori
7) la differenziazione di linee
cellulari a partire da cellule
primigenie.
Il presupposto essenziale perché i microrganismi possano
colloquiare fra loro e coordinarsi nelle loro
attività sta proprio nelle concentrazioni dei
mediatori chimici del messaggio nel mezzo in cui i batteri sono immersi.
È indispensabile qui ricordare che i batteri
possono essere presenti nell’ambiente in
due forme di vita:
a) la forma libera nel mezzo acquoso, definita forma planctonica
b) la forma sessile, adesa a una qualsiasi superficie e immersa in una matrice amorfa di sostanza organica al cui interno i
batteri possono sopravvivere e moltiplicare.
Questo speciale aggregato di batteri e
sostanza organica (EPS Extracellular Po-
lymeric Substances) è chiamato biofilm.
I biofilm sono un universo in miniatura e per
i microrganismi costituiscono un ambiente
di vita in cui la crescita o la riduzione della
popolazione microbica è regolata dal
quorum sensing in base alle condizioni più
o meno favorevoli del substrato. Come tali,
i biofilm costituiscono un aspetto importante per l’igiene degli alimenti perché è
proprio grazie ai biofilm che batteri alteranti o pericolosi per la salute (come Listeria monocytogenes, Staphylococcus aureus e Bacillus cereus) possono sopravvivere su superfici di lavoro anche in assenza di nutrienti e resistere all’azione dei disinfettanti.
Inoltre, sempre grazie al quorum sensing
all’interno della loro popolazione i batteri
possono modulare la manifestazione di determinate caratteristiche fenotipiche rispetto ad altre secondo le necessità.
Immersi in un biofilm o liberi nell’ambiente
in forma planctonica, i batteri comunicano
fra di loro sintetizzando e liberando nel
mezzo dei messaggi di tipo chimico costituiti da specifici composti.
I più conosciuti e studiati sono gli AHL ossia gli acil-omoserina-lattoni.
Posto di fronte a un sistema di comunicazione piuttosto complesso che si fonda su
una cascata di reazioni biochimiche e sulle
interazioni di geni che codificano questa
9 / 398
sintesi, un igienista degli alimenti, da buon
“praticone”, è portati a chiedersi a che cosa possa servire entrare così a fondo nella
vita intima di una comunità batterica, a
cosa serva studiare i sofisticati meccanismi
biochimici di comunicazione dei batteri.
L’importanza di una simile conoscenza diventa evidente se ricorriamo, come paragone, all’esempio dei codici cifrati utilizzati dai Comandi militari giapponesi nella Seconda Guerra mondiale per emanare ordini alle truppe dislocate lontano dalla madrepatria. Quando gli Americani riuscirono
a decifrare il codice cifrato utilizzato dai
Nipponici, le sorti della guerra si ribaltarono perché i primi riuscirono a inserirsi nelle
comunicazioni del nemico e a
scoprire quali fossero i bersagli degli attacchi.
Traslando il concetto, conoscere i meccanismi che regolano
la comunicazione tra i singoli
componenti di una popolazione microbica immersa in un
biofilm può permetterci di tenerla meglio sotto controllo e
di dominarla, facendo in modo che quella rallenti il suo sviluppo (come nel caso di germi
patogeni o alteranti) o lo accentui, nel caso di batteri utili
nelle fermentazioni microbiche.
In questa sede mi prefiggo soltanto di riassumere i concetti
essenziali del quorum sensing
rimandando i lettori ai riferimenti bibliografici citati alla
fine del documento per ulteriori approfondimenti sull’argomento.
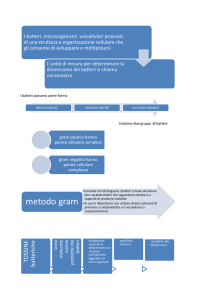
È importante sottolineare subito che i batteri possono scambiarsi messaggi sia all’interno di una stessa specie sia tra generi
microbici differenti. Tuttavia, i meccanismi
chimici sui quali si fonda il quorum sensing
dei batteri Gram negativi sono differenti da
quelli che permettono ai Gram positivi di
comunicare fra loro: in pratica, i mediatori
chimici in gioco non sono gli stessi.
Quorum sensing dei batteri
Gram negativi
Il primo meccanismo di quorum sensing
scoperto ha riguardato proprio un batterio
09_settembre_2007_DEF.qxp
19-09-2007
18:37
Gram negativo, Vibrio fischeri, un batterio
bioluminescente che vive come simbionte
negli organi luminosi specializzati di un
cefalopode decapode (Euprymna scolopes) e del pesce Monocentres japonicus.
Questo sistema è sempre preso a paradigma per dare una prima idea e spiegare meglio i meccanismi del quorum sensing.
Il gene luxI, racchiuso in un operone chiamato luxICDABE, codifica la sintesi di una
specifica sintetasi che a sua volta porta alla
sintesi di una molecola specifica, N-(3-ossoesanoil)-omoserina lattone (OHHL) che
è l’autoinduttore. Il gene luxR, a sua volta,
codifica la produzione di un fattore trascrizionale il quale, dopo avere interagito con
l’autoinduttore prima citato, va a legarsi all’operone luxICDABE rendendo possibile e
attivando la trascrizione di tutti i geni ivi
contenuti che portano alla sintesi di tutti i
componenti del sistema luciferasi così come a un aumento esponenziale della sintesi di LuxI.
Per passare alla forma attiva il trascrittore
LuxR richiede la presenza di due distinte
chaperonine, GroEL e GroESL.
In sintesi, quindi, l’autoinduttore fa sapere
a tutti i batteri che essi esistono all’interno
di un organo luminescente e che non sono,
invece, immersi nel mare dove sarebbero
così dispersi da non potere creare mai le
concentrazioni sufficienti per dare origine
al messaggio.
Nei batteri Gram negativi il quorum sensing
è mediato dagli acil-omoserina-lattoni (AHL),
la cui sintesi prende le mosse da due differenti gruppi di composti, l’S-adenosilmetionina (SAM) e una proteina acil-acil carrier (acil-ACP).
Il LuxI promuove la formazione di un legame ammidico tra acil-ACP e SAM, e dalle
successive reazioni si origina un AHL.
In tutti i segnali sinora individuati le molecole hanno come denominatore comune
proprio l’anello omoserina-lattone.
Le molecole possono poi contenere catene laterali con un numero di atomi di carbonio che varia tra 4 e 14 e altre piccole differenze strutturali e di composizione.
La membrana dei batteri Gram negativi è
permeabile agli AHL e man mano che la
cellula li sintetizza, li emette nell’ambiente
esterno, dove devono avere la possibilità
di accumularsi.
Pagina 399
Finché le concentrazioni microbiche sono
basse l’AHL diffonde passivamente al di
fuori delle singole cellule a causa del gradiente di concentrazione (maggiore all’interno della cellula e più basso al di fuori di
essa).
Quando però il numero di batteri presenti
in un ambito piuttosto ristretto comincia a
diventare notevole, la concentrazione di
AHL al di fuori delle singole cellule batteriche diventa presto superiore a quello presente all’interno di ciascuna di esse.
A questo punto, l’AHL deve prima accumularsi all’interno della cellula finché la sua
concentrazione diventa superiore a quella
presente all’esterno. Solo a quel punto potrà fuoriuscirne dell’altro.
Le principali specie batteriche di interesse
alimentare in cui è documentata la presenza di proteine LuxI sono: Vibrio fischeri,
Burkholderia cepacia, Enterobacter agglomerans, Erwinia carotovora, Escherichia
coli, Pseudomonas aureofaciens, Ps. aeruginosa, Ralstonia solanacearum, Salmonella
enterica ser. typhimurium, Serratia liquefaciens, Yersinia enterocolitica.
Quorum sensing e
alterazioni degli alimenti da
batteri Gram negativi
Con i dovuti distinguo, si può generalizzare ricordando che la flora microbica delle
carni fresche refrigerate in via di putrefazione è costituita essenzialmente da:
(1) pseudomonadacee che possono arrivare a cariche fino a 109 ufc/g se le carni sono conservate in aria
(2) batteri lattici ed enterobatteri (fino a
105-107 ufc/g) nel caso delle carni confezionate in pellicola plastica sotto
vuoto.
Parecchi autori hanno rilevato la presenza
di AHL in campioni di carni prelevati direttamente dal circuito commerciale, pervenendo alla conclusione che batteri quali
Pseudomonas possano formare dei biofilm
sulla superficie delle carni alterate e che il
quorum sensing sia uno dei meccanismi
che facilitano la formazione di questi biofilm.
È sempre grazie al quorum sensing che i
batteri regolano la produzione di enzimi
9 / 399
idrolitici e che coordinano fra loro attività
quali la loro mobilità e la colonizzazione di
un substrato.
Alla luce di queste considerazioni si è anche ipotizzato che siano proprio gli AHL a
favorire e accentuare la sintesi enzimatica
quando la carica microbica degli enterobatteri raggiunge valori soglia sufficienti, contribuendo alla comparsa di modificazioni
sensoriali sgradevoli nelle carni fresche anche se la CMT non ha ancora raggiunto
valori, diciamo così, “esplosivi”.
In effetti, nella carne si può riscontrare la
presenza evidente di AHL quando la carica ha appena raggiunto le 10 6 ufc/g, una
concentrazione microbica che non è
ancora sufficiente per parlare nelle carni di
vera e propria putrefazione.
Fra gli enterobatteri che formano una delle
due principali componenti della flora
microbica delle carni fresche confezionate
sotto vuoto, predominano Hafnia alvei e
Serratia spp.
Sottoponendo a gascromatografia il surnatante di colture di ceppi di questi due batteri isolati dalle carni, alcuni autori hanno
dimostrato che, fra tutti gli AHL presenti, la
molecola più abbondante era costituita dall’OHHL, molecola citata più sopra.
Anche Yersinia enterocolitica è in grado di
sintetizzare degli acil-omoserina-lattoni come l’OHHL e l’N-esanoil omoserina-lattone, se fatta crescere in estratti di carne e
anche di pesce.
Tutto ciò ha portato a ipotizzare che in
futuro si potrebbe aumentare la conservabilità delle carni e dei prodotti ittici freschi
e confezionati sotto vuoto utilizzando particolari additivi conservanti che siano specificamente in grado di inibire la sintesi di
AHL e che potrebbero essere definiti come “inibitori del quorum sensing”.
Va però rimarcato che non tutti i ricercatori sono concordi con queste proposte; alcuni studiosi fanno notare che il quorum
sensing, pur essendo un fattore che favorisce lo scadimento sensoriale delle carni,
non è e non può essere considerato la
causa fondamentale della putrefazione delle carni fresche.
Dal punto di vista diagnostico, il rilevamento dei AHL nei substrati in cui si sospetta
una parte attiva del quorum sensing nei processi degradativi può essere fatto con due
09_settembre_2007_DEF.qxp
19-09-2007
18:38
Pagina 400
Contributi scientifici
tipi di controlli analitici:
(a) prove biologiche che utilizzano vari
ceppi batterici, in cui si punta a inattivare il gene luxI omologo responsabile
della produzione degli AHL.
Eliminato il gene suddetto in una certa
popolazione batterica, è evidente che
l’espressione del gene sopra indicato
diventerà possibile solo se nel substrato che si vuole esaminare si ha la presenza di altro AHL
(b) vettori di plasmidi che rispondono all’inattivazione degli omologhi LuxR, come è stato fatto in colture di E. coli.
Grazie alla specificità di ciascun omologo del LuxR diventa possibile individuare le differenti molecole di AHL e di distinguerne
il profilo di produzione.
Con questi sistemi diagnostici,
i brasiliani Pinto e coll. hanno
condotto indagini sulla presenza dei principali mediatori
chimici del quorum sensing,
gli acil-omoserina-lattoni, nelle
flore microbiche Gram negative isolate dal latte crudo refrigerato.
Già Liu e Griffiths avevano rimarcato che i difetti del latte
crudo provocati da un eccessivo sviluppo di Pseudomonas
fluorescens potevano essere
correlabili alla capacità del
batterio di produrre AHL e di
sintetizzare proteasi extracellulari.
I ricercatori brasiliani hanno
studiato la liberazione di AHL da parte
della flora microbica Gram negativa isolata
da latte crudo.
In totale hanno isolato e identificato 53 differenti ceppi di batteri dei generi Acinetobacter, Aeromonas, Burkholderia, Cedecea,
Chryseomonas, Chryseobacterium, Enterobacter, Hafnia, Klebsiella, Moraxella, Pantoea, Providencia, Pseudomonas, Rahnella
e Serratia.
Gli autori hanno evidenziato che quasi
l’85% di tutti questi ceppi era in grado di
produrre AHL e che, di conseguenza, fra i
batteri Gram negativi responsabili delle alterazioni del latte crudo il quorum sensing
gioca un ruolo di estrema importanza.
Quorum sensing dei
batteri Gram positivi
I batteri Gram positivi mettono in atto il
quorum sensing utilizzando molecole “segnale” e modalità differenti da quelle utilizzate dai Gram negativi.
I Gram positivi sfruttano come molecola di
trasmissione del segnale un oligopeptide
di origine ribosomiale chiamato peptide
autoinduttore (AIP o “peptide feromone”).
Il gene che codifica la sintesi di questa
molecola messaggero, sovente è adiacente a un gene che codifica il sistema regolatore a due componenti (2CRS).
I Gram positivi che si sono sinora rivelati in
grado di produrre questo composto sono:
Bacillus subtilis, Carnobacterium maltaromaticum e C. piscicola, Enterococcus faecalis, Lactobacillus plantarum e L. casei,
Lactococcus lactis, Staphylococcus aureus,
Streptococcus pneumoniae.
Mancano ancora dati certi sull’esistenza di
un quorum sensing in Listeria monocytogenes e nelle listerie in genere, anche se ciò è
probabile.
L’insieme dei due geni associati prende nome di “sistema regolatore a 3 componenti”
(3CRS). È opportuno ricordare che in tutti i
batteri il sistema 2 CRS, formato da istidinaproteina-chinasi (HPK) di membrana e da
un regolatore di risposta (RR), è il principa9 / 400
le sistema di trasduzione di segnale attraverso la membrana cellulare.
È grazie a questo sistema 2CRS che i batteri possono percepire le modificazioni di
pH, concentrazioni di soluti, temperatura
ecc. che intervengono nell’ambiente in cui
sono inseriti.
Nei batteri Gram negativi le molecole di
AHL diffondono passivamente attraverso la
membrana del batterio, fluendo dal suo interno all’esterno; perché una seconda cellula riesca a captare questo messaggio, invece, bisogna che il mediatore chimico sia
trasportato attivamente all’interno della
cellula, se si vuole ottenerne una reazione.
Nel caso dei batteri Gram positivi, invece,
il modello peptide-feromone
non prevede questa ultima fase, proprio grazie al fatto che
la proteine sensore vista prima
è già collocata sulla faccia esterna della membrana. Il sistema 3CSR tiene sotto controllo
e regola la manifestazione di
alcuni aspetti fenotipici dei
batteri Gram positivi:
a) sintesi di batteriocine in Carnobacterium piscicola, Lactobacillus plantarum, L. casei
ed Enterococcus faecium
b) trasferimento di plasmidi
mediante coniugazione in Enterococcus faecalis
c) competenza genetica in
Streptococcus pneumoniae
e Bacillus subtilis
d) espressione dei fattori di virulenza negli stafilococchi
e) sporulazione di Bacillus subtilis
f) formazione di biofilm
g) risposte che i batteri mettono in atto
contro gli stress subletali.
Studiando le sequenze genomiche complete esistenti di Streptococcus thermophilus scopriamo che tutte comprendono
i geni che codificano la sintesi del sistema
2CRS; ne desumiamo, quindi, che tutti i
ceppi del batterio sono potenzialmente in
grado di mettere in atto il quorum sensing.
Autori giapponesi hanno segnalato, infine,
che probabilmente nei batteri Gram positivi il quorum sensing funziona anche con
altre molecole-segnale differenti dal sistema
3CRS, i gamma-butiro-lattoni.
09_settembre_2007_DEF.qxp
19-09-2007
18:38
Il fatto non deve stupire perché queste molecole sono strutturalmente simili agli AHL
dei Gram negativi e sembrano intervenire
nello stimolare la produzione di antibiotici
in Streptomyces.
Pagina 401
• la scoperta dell’esistenza del quorum sensing e le sempre maggiori conoscenze
che si accumulano su questo argomento
cominciano a rivoluzionare l’approccio
che i ricercatori hanno nello studio dei
microrganismi.
In sintesi
• Xavier e Bassler definiscono il quorum
sensing «un processo di comunicazione
tra cellule batteriche che comporta la
sintesi, la liberazione e la captazione di
“molecole segnale” extracellulari chiamate autoinduttori».
• un requisito essenziale perché il fenomeno si realizzi è il raggiungimento da parte
della popolazione microbica di un valore soglia, perché si possa contare su una
certa quantità minima di molecole antoinduttrici per trasmettere il segnale.
• con le conoscenze del quorum sensing
si cominciano a giustificare meglio comportamenti prima non ben spiegabili, come la sporulazione dei batteri sporigeni
e altri aspetti di fisiologia microbica.
• il quorum sensing ci fa comprendere che
le popolazioni microbiche non sono dei
semplici aggregati più o meno caotici di
microrganismi che vivono ciascuno per
proprio conto, bensì una comunità coordinata al cui interno fluiscono costantemente informazioni che permettono alla
comunità stessa di resistere alle condi-
zioni avverse e di avvantaggiarsi per il
loro fine.
• per altro verso, le conoscenze che si stanno accumulando sul quorum sensing microbico permetteranno all’uomo di comprendere meglio i meccanismi di colonizzazione microbica degli alimenti e
dei loro processi alterativi. Le possibilità
che si schiudono sono quelle di potere
interferire, per via chimica, con il coordinamento delle società microbiche, scardinandolo o quanto meno disturbandolo. In questo modo si dovrebbe riuscire
a tenere meglio sotto controllo le popolazioni microbiche, avendo come risultati ultimi un migliore livello di salubrità e
igiene dei prodotti e un aumento della
loro conservabilità commerciale.
La bibliografia è disponibile sul sito
www.ilprogressoveterinario.it

![5\) batteri [modalità compatibilità]](http://s1.studylibit.com/store/data/000928299_1-28a224c15810efb654d8d9e4b207aa31-300x300.png)