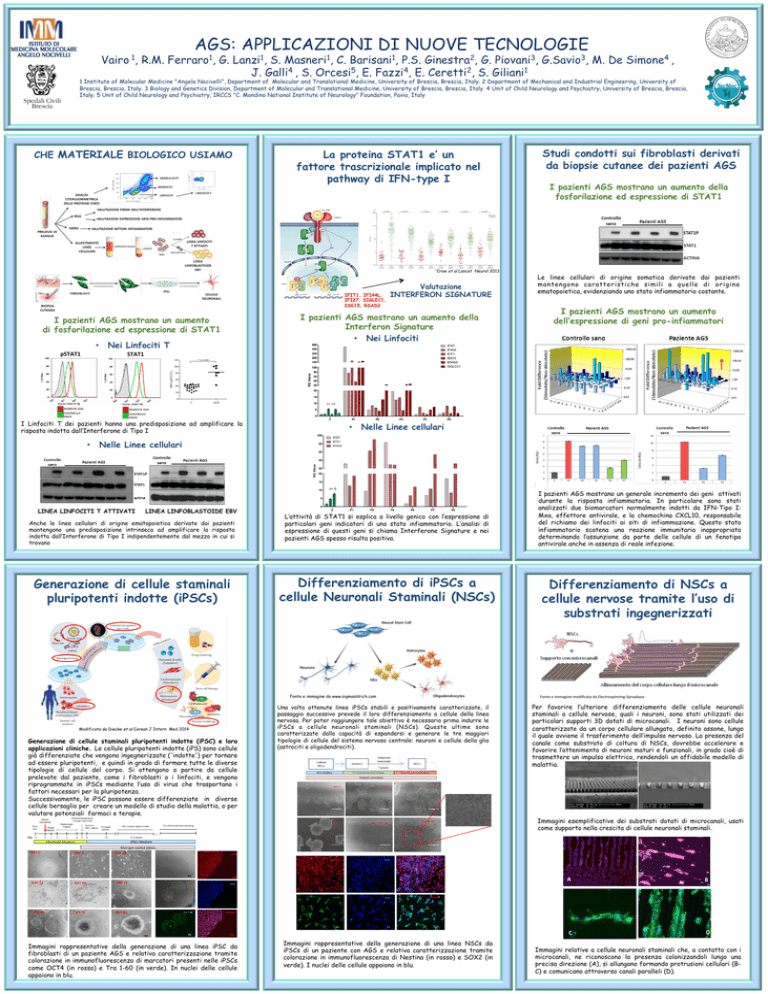
AGS: APPLICAZIONI DI NUOVE TECNOLOGIE
Vairo 1, R.M. Ferraro1, G. Lanzi1, S. Masneri1, C. Barisani1, P.S. Ginestra2, G. Piovani3, G.Savio3, M. De Simone4 ,
J. Galli4 , S. Orcesi5, E. Fazzi4, E. Ceretti2, S. Giliani1
1 Institute of Molecular Medicine "Angelo Nocivelli", Department of Molecular and Translational Medicine, University of Brescia, Brescia, Italy. 2 Department of Mechanical and Industrial Engineering, University of
Brescia, Brescia, Italy. 3 Biology and Genetics Division, Department of Molecular and Translational Medicine, University of Brescia, Brescia, Italy. 4 Unit of Child Neurology and Psychiatry, University of Brescia, Brescia,
Italy. 5 Unit of Child Neurology and Psychiatry, IRCCS "C. Mondino National Institute of Neurology" Foundation, Pavia, Italy
CHE MATERIALE BIOLOGICO USIAMO
La proteina STAT1 e’ un
fattore trascrizionale implicato nel
pathway di IFN-type I
Crow et al Lancet Neurol 2013
IFIT1, IFI44L,
IFI27, SIGLEC1,
ISG15, RSAD2
I pazienti AGS mostrano un aumento della
Interferon Signature
• Nei Linfociti
I pazienti AGS mostrano un aumento
di fosforilazione ed espressione di STAT1
• Nei Linfociti T
pSTAT1 Valutazione
INTERFERON SIGNATURE
Studi condotti sui fibroblasti derivati
da biopsie cutanee dei pazienti AGS
I pazienti AGS mostrano un aumento della
fosforilazione ed espressione di STAT1
Le linee cellulari di origine somatica derivate dai pazienti
mantengono caratteristiche simili a quelle di origine
ematopoietica, evidenziando uno stato infiammatorio costante.
I pazienti AGS mostrano un aumento
dell’espressione di geni pro-infiammatori
STAT1 120
***p<0.0005
MFI (pSTAT1)
100
80
60
40
20
0
C
AGS
n= 13 I Linfociti T dei pazienti hanno una predisposizione ad amplificare la
risposta indotta dall’Interferone di Tipo I
• Nelle Linee cellulari
• Nelle Linee cellulari
n= 6
LINEA LINFOCITI T ATTIVATI
LINEA LINFOBLASTOIDE EBV
Anche le linee cellulari di origine ematopoietica derivate dai pazienti
mantengono una predisposizione intrinseca ad amplificare la risposta
indotta dall’Interferone di Tipo I indipendentemente dal mezzo in cui si
trovano
L’attività di STAT1 si esplica a livello genico con l’espressione di
particolari geni indicatori di uno stato infiammatorio. L’analisi di
espressione di questi geni si chiama Interferone Signature e nei
pazienti AGS spesso risulta positiva.
Differenziamento di iPSCs a
cellule Neuronali Staminali (NSCs)
Generazione di cellule staminali
pluripotenti indotte (iPSCs)
Fonte e immagine da www.sigmaaldrich.com
Modificato da Diecke et al Corean J Intern Med 2014
Generazione di cellule staminali pluripotenti indotte (iPSC) e loro
applicazioni cliniche. Le cellule pluripotenti indotte (iPS) sono cellule
già differenziate che vengono ingegnerizzate ('indotte') per tornare
ad essere pluripotenti, e quindi in grado di formare tutte le diverse
tipologie di cellule del corpo. Si ottengono a partire da cellule
prelevate dal paziente, come i fibroblasti o i linfociti, e vengono
riprogrammate in iPSCs mediante l’uso di virus che trasportano i
fattori necessari per la pluripotenza.
Successivamente, le iPSC possono essere differenziate in diverse
cellule bersaglio per creare un modello di studio della malattia, o per
valutare potenziali farmaci e terapie.
Una volta ottenute linee iPSCs stabili e positivamente caratterizzate, il
passaggio successivo prevede il loro differenziamento a cellule della linea
nervosa. Per poter raggiungere tale obiettivo è necessario prima indurre le
iPSCs a cellule neuronali staminali (NSCs). Queste ultime sono
caratterizzate dalla capacità di espandersi e generare le tre maggiori
tipologie di cellule del sistema nervoso centrale: neuroni e cellule della glia
(astrociti e oligodendrociti).
I pazienti AGS mostrano un generale incremento dei geni attivati
durante la risposta infiammatoria. In particolare sono stati
analizzati due biomarcatori normalmente indotti da IFN-Tipo I:
Mxa, effettore antivirale, e la chemochina CXCL10, responsabile
del richiamo dei linfociti ai siti di infiammazione. Questo stato
infiammatorio scatena una reazione immunitaria inappropriata
determinando l’assunzione da parte delle cellule di un fenotipo
antivirale anche in assenza di reale infezione.
Differenziamento di NSCs a
cellule nervose tramite l’uso di
substrati ingegnerizzati
Fonte e immagine modificata da Electrospinning-­‐Spraybase Per favorire l’ulteriore differenziamento delle cellule neuronali
staminali a cellule nervose, quali i neuroni, sono stati utilizzati dei
particolari supporti 3D dotati di microcanali. I neuroni sono cellule
caratterizzate da un corpo cellulare allungato, definito assone, lungo
il quale avviene il trasferimento dell’impulso nervoso. La presenza del
canale come substrato di coltura di NSCs, dovrebbe accelerare e
favorire l’ottenimento di neuroni maturi e funzionali, in grado cioè di
trasmettere un impulso elettrico, rendendoli un affidabile modello di
malattia.
Immagini esemplificative dei substrati dotati di microcanali, usati
come supporto nella crescita di cellule neuronali staminali.
iPSCs Medium Fibrobalst Medium Matrigel-­‐coated plates DAY 0 DAY 7 DAY 10 OCT4 4X DAY 12 DAY 14 DAY 18 DAY 20 DAY 24 DAY 26 20X DAPI A B C D 10
X 4X Tra-­‐1-­‐60 4X 4X MERGED 20X Immagini rappresentative della generazione di una linea iPSC da
fibroblasti di un paziente AGS e relativa caratterizzazione tramite
colorazione in immunofluorescenza di marcatori presenti nelle iPSCs
come OCT4 (in rosso) e Tra 1-60 (in verde). In nuclei delle cellule
appaiono in blu.
Immagini rappresentative della generazione di una linea NSCs da
iPSCs di un paziente con AGS e relativa caratterizzazione tramite
colorazione in immunofluorescenza di Nestina (in rosso) e SOX2 (in
verde). I nuclei delle cellule appaiono in blu.
20 i
Immagini relative a cellule neuronali staminali che, a contatto con
microcanali, ne riconoscono la presenza colonizzandoli lungo X una
precisa direzione (A), si allungano formando protrusioni cellulari (BC) e comunicano attraverso canali paralleli (D).












