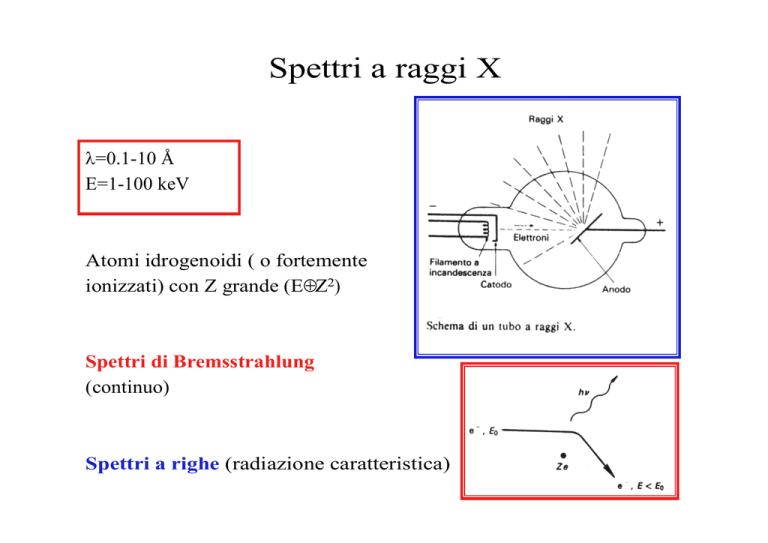
Spettri a raggi X
λ=0.1-10 Å
E=1-100 keV
Atomi idrogenoidi ( o fortemente
ionizzati) con Z grande (E≈ Z2)
Spettri di Bremsstrahlung
(continuo)
Spettri a righe (radiazione caratteristica)
Radiazione di Bremsstrahlung (frenamento)
Gli elettroni emessi dal catodo vengono
accelerati verso l’anodo (eV0).
Gli elettroni, passando vicino ai nuclei
atomici dell’anodo vengono deflessi
e rallentati.
rallentati
Emissione di radiazione e.m. nel
continuo (elettrodinamica classica).
Atomo+e- (veloce)->atomo+e- (lento) +hν
Singolo frenamento: hνmax=eV0=hc/λmin
elettrone IN ⇒ fotone OUT
Kα
Max. energia dei raggi X =
Max. energia elettrone
Spettro
caratteristico
hνmax=eV0=hc/λmin
(dipende dal
bersaglio)
Spettro caratteristico
Emissione discreta
della serie K
Bremsstrahlung
Spettro continuo dovuto al
frenamento degli elettroni
Kβ
Bremsstrahlung
λmin
Spettri dei raggi X : Diagrammi di Moseley
λ (Å)
Z
Serie L
Lα
n=3a2
Kα
n=2a1
Serie K
Kβ
n=3a1
f
Moseley scoprì che la radice quadrata della frequenza della riga Kα
era proporzionale al numero atomico degli atomi del bersaglio:
−16
ν = 0.248 ×10
(Z −1)
2
Formula di Bohr per atomi idrogenoidi:
m 0e 4 Z 2 1
1
ν=
3 2 − 2
8πε 0h n1 n 2
Kα => n1=1, n2=2; Z->Z-b con b≈1 (effetto di schermaggio del
potenziale coulombiano del nucleo da parte dell’elettrone più interno).
m 0e 4 1 1
2
ν=
−
(
Z
−
b
)
3
2
2
8πε 0 h 1 2
3m e 4 1 2
0
ν =
4 3 (Z − b )
32πε 0 h
Mα
X-ray Spectra: “Stylized”
da n = 4 a 3
n=4
Diagram of Atomic
Levels
Lα da n = 3 a 2
n=3
n=2
Kα da n = 2 a 1
α da n+1 a n
β da n+2 a n
γ da n+3 a n
Struttura fine degli
spettri dei raggi X












