Corso di Laurea Magistrale in
“Medicina e Chirurgia”
Fisiologia e Biofisica
A.A. 2016-2017
Muscolo scheletrico e
contrazione muscolare
Prof. Clara Iannuzzi
Dipartimento di Biochimica, Biofisica e Patologia Generale
[email protected]
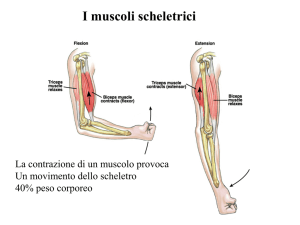
I muscoli hanno due funzioni: generare movimento
generare forza
I muscoli scheletrici generano anche calore e contribuiscono
alla termoregolazione (in ambiente freddo, il cervello ordina ai
muscoli di contrarsi e questo origina il brivido, che crea calore)
Energia chimica
Muscolo
Energia meccanica
Il muscolo ha la funzione di trasformare l’energia chimica in energia meccanica.
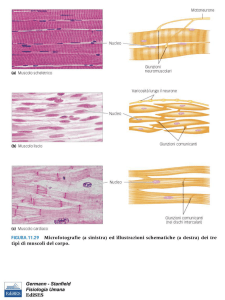
Le fibre muscolari scheletriche appaiono striate e
multinucleate. Controllano i movimenti del corpo.
Sono volontari, si contraggono in risposta
a stimoli che provengono da motoneuroni.
Le fibre muscolari cardiache sono uninucleate e striate.
Si connettono tra loro attraverso dischi intercalari.
Sono involontarie, si contraggono spontaneamente
senza stimoli esterni. L’attività è modulata dal
sistema nervoso viscerale e anche dal sistema
endocrino.
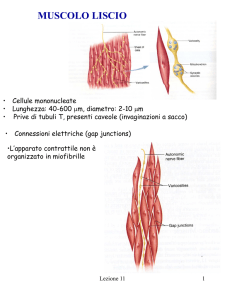
Muscolo liscio è il tipo principale di muscolo degli organi
interni e cavi, come stomaco, vescica, vasi sanguigni.
Cellule uninucleate senza evidenti striature.
Muscolo scheletrico
Connettivo
Fibre
muscolari
Vasi sanguigni
Nervi
Reticolo
sarcoplasmatico
Miofibrille
Sarcolemma
Tubuli T
Nuclei
Sarcoplasma
Mitocondri
Glicogeno
Struttura muscolo scheletrico
Struttura fibra muscolare scheletrica
Contengono
l’apparato contrattile
della fibra muscolare
Fibra (cellula) muscolare
Tubuli T
Reticolo
sarcoplasmatico
Sarcolemma
Mitocondri
Nucleo
Filamento spesso
Filamento sottile
Miofibrilla
RS e tubuli T aiutano a trasmettere i segnali dal sarcolemma alle fibrille,
rendendo la cellula muscolare capace di rispondere al segnale nervoso.
Struttura sarcomero
Quando osservate al microscopio esse presentano una striatura. Per questo motivo il
muscolo scheletrico, così come il muscolo cardiaco, viene indicato come muscolo striato.
FILAMENTI SPESSI
2 catene pesanti (heavy chains)
p.m. 200.000
MIOSINA:
proteina oligomerica
p.m. 450.000
2 coppie di catene leggere
(light chains) non identiche
p.m.16.000 e 20.000
Dominio C-terminale: α-elicoidale
lunghezza 134 nm, diametro 2 nm
(coda della miosina)
Ciascuna catena pesante
Dominio N-terminale: globulare
(testa della miosina)
Coda
Ogni coppia di catene leggere è legata al dominio globulare di ciascuna
catena pesante nel tratto che connette testa e coda.
Snodo
Testa
Assemblaggio dei filamenti spessi nelle miofibrille
Le code di molecole di miosina adiacenti si dispongono in modo sfalsato, con le teste
che sporgono in modo ordinato dal filamento spesso con un andamento ad elica.
La testa rappresenta la “parte che lavora” della molecola di miosina, essa è infatti la
parte che genera attivamente la forza meccanica sviluppata dal muscolo. Ciascuna
testa possiede due siti cruciali per la generazione della forza contrattile:
Sito di fissazione dell’actina: lega monomeri di actina
Sito ATPasico: possiede attività enzimatica e idrolizza ATP
Poichè nella porzione centrale del filamento spesso non sono presenti ponti
trasversali, questa parte viene detta zona nuda.
Nel muscolo scheletrico circa 250 molecole di miosina si uniscono a formare un
filamento spesso, il quale è sistemato in modo che le teste di miosina si raggruppano
all’estremità, mentre la regione centrale è un fascio di code di miosina
FILAMENTI SOTTILI
MONOMERI DI ACTINA G (capaci di legare la miosina)
Proteine regolatrici:
TROPOMIOSINA: proteina filamentosa che si estende al di
sopra delle molecole di actina, bloccandone il legame con la
miosina quando il muscolo è a riposo.
TROPONINA: Complesso di tre proteine;
una attacca il filamento di actina
una si fissa alla tropomiosina
una in grado di legare reversibilmente ioni Ca2+
Assemblaggio dei filamenti sottili nelle miofibrille
I monomeri di actina G (globulare) sono legati
come perle in una collana a formare strutture
filamentose dette actina F (proteina fibrosa).
A loro volta due filamenti di actina F si
intrecciano in una struttura a doppia elica in
modo da formare i filamenti di actina che
caratterizzano i filamenti sottili.
Il legame con le proteine regolatrici consente
alle fibre muscolari di iniziare e terminare la
contrazione.
FILAMENTI SOTTILI
Troponina
TnT
Legame
Tn-tropomiosina
TnI
Legame
Actina-TnC
TnC
Legame
Ioni Ca++
Disposizione dei filamenti spessi (miosina) e sottili (actina)
nel muscolo scheletrico
I filamenti spessi e sottili sono connessi da ponti trasversali, detti anche ponti crociati, costituiti dalle
teste di miosina che si legano lassamente ai filamenti di actina. Ogni molecola di G-actina ha un
singolo sito di legame per una testa di miosina.
Dischi Z: strutture proteiche a zig zag, che fungono da sito di attacco per i filamenti sottili. Un
sarcomero è composto da due dischi Z e dai filamenti tra essi compresi
Linea M: questa banda rappresenta il sito di attacco dei filamenti spessi
linea M
disco Z
disco Z
SARCOMERO
La titina è una enorme proteina elastica che occupa tutta la distanza tra disco Z e linea
M. Ha la funzione di agevolare il ritorno del sarcomero allungato alla sua lunghezza di
riposo; inoltre stabilizza la disposizione dei filamenti all’interno del sarcomero con l’aiuto
della proteina non elastica nebulina. La nebulina si trova di fianco ai filamenti sottili e si
attacca ai dischi Z. Garantisce l’allineamento dei filamenti di actina del sarcomero.
TEORIA DELLO SCORRIMENTO DEI FILAMENTI
Quando un sarcomero si contrae, i filamenti sottili e spessi non cambiano in lunghezza. Il
filamento sottile di actina scivola sul filamento spesso di miosina, spostandosi verso la
linea M al centro del sarcomero. La banda A non si modifica in lunghezza, ma sia la zona H
che la banda I si accorciano mentre i filamenti si sovrappongono.
La forza che spinge il filamento di actina è il movimento dei ponti crociati di miosina che
legano actina e miosina. La miosina è una proteina motrice che converte il legame chimico
dell’ATP in energia meccanica. Questo processo non continua all’infinito.
Da cosa è regolato questo processo? Nello stato rilassato la tropomiosina blocca parzialmente i siti
di legame dell’actina per la miosina.
La contrazione viene iniziata quando il Ca2+ si lega alla troponina C. Il legame col Ca2+ cambia la
conformazione della molecola di tropomiosina e scopre il resto del sito di legame per la miosina, così che
questa può completare la propria flessione.
Lo stimolo all’entrata del Ca2+ proviene da un potenziale di azione
che dal motoneurone che raggiunge la fibra muscolare striata.
Il potenziale di membrana di queste cellule è -90mV che coincide con il
valore del potenziale di equilibrio del cloro. Questo vuol dire che per il
cloro c’è equilibrio elettrochimico.
Sinapsi neuro-muscolare
L’arrivo di un potenziale d’azione (in rosso) è in grado di depolarizzare e
ripolarizzare la membrana. Esso agisce sui canali del Ca2+ voltaggio
dipendenti e permette l’esocitosi delle vescicole sinaptiche contenenti il
neurotrasmettitore acetilcolina.
I segnali per la contrazione muscolare arrivano dal SNC ai muscoli scheletrici per mezzo dei
motoneuroni. L’acetlcolina proveniente dal motoneurone innesca un potenziale d’azione nella fibra
muscolare che a sua volta scatena una contrazione. Questa combinazione di eventi elettrici e meccanici
viene definito accoppiamento eccitazione-contrazione.
Il Ca2+ serve come gradiente
elettrochimico
e
permette
l’esocitosi delle vescicole contenenti
il neurotrasmettitore ACh.
L’ACh
diffonde
nello
spazio
sinaptico e va a legare specifici
recettori presenti sulla membrana.
Tali recettori sono colinergici di
tipo nicotinico e sono recettori
canale: il loro legame con ACh
permette l’apertura del canale e il
passaggio di ioni positivi (K+ e Na+).
L’ACh legata viene rimossa da AChE.
Il legame dell’ACh al recettore induce una depolarizzazione della
membrana (genesi di un potenziale graduato). La polarizzazione sarà
quindi direttamente proporzionale alla quantità di ACh esocitata.
Quando il potenziale d’azione raggiunge un recettore diidropiridina (DHP), la connessione
meccanica fra il recettore e il reticolo sarcoplasmatico apre i canali per il Ca2+ .
L’apertura di questi canali rilascia Ca2+ nel citoplasma, dove gli ioni si possono combinare con la troponina
e permettere di iniziare la contrazione.
Il rilasciamento muscolare si ha quando il reticolo sarcoplasmatico riassorbe Ca2+ per mezzo di una Ca2+ATPasi. Quando la concentrazione citoplasmatica di Ca2+ scende, lo ione si stacca dalla troponina, la
tropomiosina scivola all’indietro per bloccare il sito legante la miosina, e la fibra si rilascia.
Il segnale elettrico che determina la
fuoriuscita del Ca2+ dal RS è localizzato
nella membrana del tubulo T, e non nella
membrana del RS stesso.
I recettori DHP nelle membrane dei
tubuli T funzionano da rivelatori di
voltaggio.
In seguito ad un potenziale di azione, la
conformazione dei recettori DHP si
modifica e trasmette un segnale ai
recettori per la rianodina, determinando
l’apertura dei canali per il Ca2+.
A sua volta, il Ca2+ fuoriesce dal RS e si
diffonde nel citosol dove lega il
complesso della troponina.
Nicotina: agonista dei recettori colinergici nicotinici (recettori ionotropi)
presenti sulla membrana post-sinaptica della giunzione
neuromuscolare.
Agonista: sostanza che mima l’attività di un ligando.
Legame nicotina-recettore colinergico: determina apertura dei canali ionici
delle cellule post-sinaptiche, che si
depolarizzano.
Sebbene la nicotina sia un agonista, l’esposizione a lungo termine determina
inattivazione dei recettori colinergici con conseguente up-regulation degli
stessi.
La deprivazione da nicotina consente a tutti i recettori di ritornare allo stato
attivo: il maggior numero di recettori è probabilmente responsabile dei sintomi
da astinenza.
MIASTENIA GRAVE: malattia autoimmune in cui l’organismo non
riconosce i recettori colinergici come “self”.
Gli anticorpi anti-recettore determinano una
notevole riduzione dei recettori per l’acetilcolina. Ne consegue che, anche se il rilascio
del neurotrasmettitore è normale, la risposta
è ridotta e si manifesta debolezza muscolare.
SINDROME DI LAMBERT-EATON
In questa patologia, la debolezza muscolare è causata da un attacco
autoimmune nei confronti dei canali del calcio presenti sulla membrana
presinaptica. Ciò diminuisce il flusso di ioni calcio diretti verso l’interno
della cellula limitando la fusione delle vescicole con la membrana
e, quindi, la liberazione di acetilcolina.
Stimolazioni ripetute del motoneurone facilitano l’accumulo di calcio
nel bottone sinaptico e facilitano la liberazione del
neurotrasmettitore
PARALISI PERIODICA IPERKALEMICA
Difetto genetico dei canali voltaggio dipendenti del sodio che
non si inattivano. La fibra muscolare non si ripolarizza e non
genera un nuovo potenziale d’azione. Si ha accumulo di ioni
potassio nel LEC.
I grafici a destra mostrano i potenziali d’azione nel terminale assonale e nella fibra muscolare,
seguiti dalla curva di tensione della scossa muscolare. Il periodo di latenza rappresenta il tempo
necessario perché il Ca2+ venga rilasciato dal reticolo sarcoplasmatico e diffonda verso i filamenti
della miofibrilla.
Un singolo potenziale d’azione evoca una
singola scossa muscolare.
Le scosse sono diverse da fibra a fibra
per la velocità con cui sviluppano tensione
(fase ascendente della curva della scossa),
la tensione massima raggiunta (altezza della curva)
e durata della scossa (ampiezza della curva).
Fasi della scossa singola
La stimolazione ripetuta del muscolo induce lo sviluppo di
numerose scosse singole in successione, ognuna delle quali ha
forma e grandezza uguale a quella delle altre (carattere del
tutto o nulla del potenziale di azione).
Sebbene le scosse siano riproducibili in un dato muscolo o fibra
muscolare, esse variano notevolmente da un muscolo all’altro.
T<C
La forza generata
dal muscolo non è
sufficiente
a
vincere il carico.
Contrazioni isotoniche (T = C)
Lavoro prodotto dal muscolo= 0
(Nessuno spostamento)
Lavoro prodotto dal muscolo≠ 0
Muscolo a riposo
Contrazione isometrica: il muscolo non
si accorcia. I sarcomeri si accorciano
generando forza ma gli elementi
elastici si allungano così che la
lunghezza muscolare resta costante.
Contrazione
isotonica:
I
sarcomeri
si
accorciano.
Poiché gli elementi elastici
sono
allungati,
l’intero
muscolo deve accorciarsi.
Contrazione fibre muscolari
scheletriche
Forza (Tensione)
Movimento
Resistenza ad un
carico
La tensione generata da un muscolo è direttamente proporzionale
all’interazione tra filamenti spessi e filamenti sottili (numero di
ponti trasversali).
La tensione sviluppata dalla contrazione dipende direttamente dalla lunghezza dei
sarcomeri prima che la contrazione inizi. Ogni sarcomero si contrarrà con il massimo
della forza se è alla lunghezza ottimale, né troppo lungo né troppo corto.
Se la fibra comincia la contrazione quando il sarcomero è troppo lungo, i filamenti sottili e spessi
sono scarsamente sovrapposti e formano pochi ponti trasversali quindi non possono generare
molta forza. Viceversa, se il sarcomero è più corto della sua lunghezza ottimale, i filamenti
saranno troppo sovrapposti per cui i filamenti spessi possono spostare i filamenti sottili solo per
una breve distanza. Inoltre, i filamenti spessi finiscono a contatto coi dischi Z e non possono
formare ponti trasversali per cui la tensione cala rapidamente.
Adenosintrifosfato (ATP)
Fosfato
Adenina
Ribosio
Legame ricco
d’energia
La contrazione del muscolo scheletrico dipende dal rifornimento continuo di ATP. La quantità di
ATP presente nel muscolo è sufficiente per otto contrazioni circa. Come fonte di energia di
riserva, il muscolo contiene fosfocreatina, una molecola i cui legami fosfato ad alta energia
vengono generati a partire da creatina e ATP quando i muscoli sono a riposo
Fosfocreatina
Canali del Ca2+
nella membrana
sarcoplasmatica
(per rimuovere
Ca2+ dal citosol).
Debito di O2
Durante il lavoro muscolare, i vasi sanguigni che irrorano il muscolo
si dilatano aumentando l’apporto di ossigeno. In una prima fase,
l’energia è fornita da processi aerobici ed il
consumo di O2 è proporzionale al lavoro svolto.
Se il lavoro da compiere è molto grande, la sintesi aerobica delle
riserve energetiche non è più sufficiente e l’energia è fornita
da processi anaerobici.
Al termine dello sforzo, è necessario utilizzare una quantità di O2
supplementare per rimuovere l’eccesso di acido lattico e ripristinare
i depositi di ATP e fosfocreatina. L’extraconsumo di O2 è tanto
maggiore quanto più lungo è stato il ricorso a processi anaerobici.
Produzione di calore nei muscoli
W, lavoro meccanico
Energia fornita = Energia liberata
Sintesi ATP e PC
Q, calore
Rendimento = W/Energia fornita
0≤ Rendimento ≤50%
Contrazione isometrica
Contrazione isotonica
La forza della contrazione aumenta con la sommazione delle scosse muscolari.
Una fibra muscolare risponde ad uno stimolo (▲) con una scossa. Se gli stimoli
sono separati nel tempo, il muscolo si rilassa completamente tra le scosse.
La durata della scossa è inferiore al tempo intercorrente tra
due stimolazioni successive e quindi le scosse sono identiche.
Quando gli stimoli sono ravvicinati nel tempo, la fibra muscolare non ha il tempo di
rilassarsi e le contrazioni si sommano, generando una contrazione con una tensione
maggiore.
La tensione generata da un muscolo aumenta se
si sommano più scosse singole ravvicinate
Se gli stimoli arrivano molto rapidamente, il muscolo raggiunge la sua massima
tensione. Se il muscolo ha ancora la possibilità di rilassarsi tra gli stimoli, si
realizza il tetano incompleto.
La tossina tetanica inibisce il rilascio dei neurotrasmettitori inibitori. Il
muscolo resta quindi contratto e non è più in grado di rilasciarsi.
Se il muscolo raggiunge una tensione costante, è nella condizione di tetano completo.
Tetano completo
E’ quindi possibile aumentare la tensione sviluppata da una singola fibra muscolare
variando la frequenza dei potenziali d’azione nella fibra, che sono scatenati dal
rilascio di acetilcolina da parte dei motoneuroni.
CARATTERISTICHE DEI VARI TIPI DI FIBRE MUSCOLARI
Ossidative lente
muscolo rosso (I)
Velocità
contrazione
Ossidative rapide
muscolo rosso (IIa)
Glicolitiche rapide
muscolo bianco (IIb)
molto lenta
intermedia
Attività
ATPasica
lenta
rapida
molto rapida
Diametro
piccolo
medio
grande
Durata
contrazione
molto lunga
lunga
breve
Metabolismo
ossidativo
Colore
rosso scuro
glicolitico/ossidativo
rosso
molto rapida
glicolitico
pallido
Fibre muscolari
ossidative lente
Fibre muscolari
glicolitiche rapide
La grande quantità di mioglobina , numerosi mitocondri(M) e un’estesa
rete di capillari sanguigni (cap) distinguono il muscolo ossiodativo a lenta
contrazione (R) dal muscolo glicolitico a contrazione rapida (W).
Unità motoria: gruppo di fibre
innervate da un solo motoneurone
Unità motoria: è l’unità fondamentale della contrazione nel muscolo
scheletrico
Fibre dello stesso tipo.
La contrazione di un’unità è
un evento tutto o nulla.
Il numero di fibre muscolari in un’unità motoria è
variabile. Nei muscoli che governano i movimenti fini,
come quelli oculari o della mano, un’unità motoria può
contenere anche solo 3-5 fibre. Se l’unità motoria viene
attivata, solo poche fibre si contraggono e la risposta
muscolare è piccola. Se vengono attivate altre unità, la
risposta aumenta di poco perché si aggiungono solo poche
fibre. Ciò consente graduazioni fini nei movimenti.
Nei muscoli usati per movimenti grossolani, come stare in
piedi o camminare, un singolo motoneurone può
innervare centinaia di fibre muscolari.
Il muscolo può generare contrazioni graduate di varia forza e durata in quanto è
composto da molte unità motorie di diversi tipi. Questa varietà gli permette di variare
tipo di contrazione cambiando i tipi di unità motorie in attività e il numero di unità che
rispondono in un certo tempo.
Muscolo : insieme
di unità motorie.
La tensione sviluppata da un muscolo è in relazione al numero e al tipo di unità
motorie reclutate.
Principio della dimensione
S (slow)
Tipo I
FR(fast resistent)
Tipo IIa
FR(fast fatigable)
Tipo IIb
Il reclutamento dell’unità motoria è in relazione alla soglia di eccitabilità che
ha il motoneurone che innerva quella classe di fibra.
Muscolo liscio
Muscolo
cardiaco
scheletrico
liscio
MUSCOLO LISCIO
La muscolatura liscia si trova nelle pareti degli organi cavi. La sua
contrazione genera forza per spostare materiale attraverso il lume degli
organi cavi o per modificare la conformazione dell’organo.
Il muscolo liscio si contrae e rilascia molto più lentamente rispetto al
muscolo striato, ma può sostenere la contrazione per lunghi periodi di tempo.
Questa facoltà consente alla parete degli organi di mantenere la tensione
con un carico continuato. Es. vescica urinaria.
Alcuni muscoli lisci sono tonicamente contratti e mantengono costantemente
la tensione. Es. sfinteri.
Eterogeneità: muscolo liscio vascolare
“
“ gastrointestinale
“
“
urinario
“
“
respiratorio
“
“
riproduttivo
“
“
oculare
Anatomia: le fibre contrattili del muscolo liscio sono disposte in fasci
intrecciati. Gli strati di muscolo liscio all’interno di un organo
sono disposti in varie direzioni.
Controllo della contrazione: neurotrasmettitori, ormoni, segnali paracrini.
Poiché diversi segnali possono raggiungere la
fibra simultaneamente, questa agisce come
centro di integrazione dei segnali.
Variabilità delle proprietà elettriche: la contrazione può avvenire in seguito
ad un potenziale d’azione, oppure dopo
un potenziale elettrotonico sotto-soglia
o anche in assenza di variazioni del
potenziale di membrana.
Accoppiamento eccitazione-contrazione: ingresso di Ca2+ attraverso canali
controllati dalla depolarizzazione,
stiramento e segnali chimici. Rilascio
dal reticolo sarcoplasmatico mediato
da recettori accoppiati all’IP3.
Le fibre muscolari liscie sono piccole e a forma di fuso. Le fibre contrattili non
sono disposte in sarcomeri organizzati, quindi i muscoli lisci non hanno un
aspetto a bande. Actina e miosina sono disposte in lunghi fasci che si
estendono in diagonale alla periferia cellulare, tenuti insieme da corpi densi di
natura proteica, formando una struttura a rete intorno al nucleo centrale.
Il rapporto actina/miosina è 10-12:1 contro 2-4:1 nel muscolo scheletrico.
La linea continua di teste di miosina consente ai filamenti di actina
di scorrere lungo la miosina senza interruzione (assenza di zona
nuda), mantenendo una tensione continua grazie all’interazione dei
ponti trasversali
La disposizione obliqua delle fibre fa sì che la cellula diventi tondeggiante
quando si contrae.
La funzione di deposito di calcio da parte del reticolo sarcoplasmatico
è integrata da caveole, piccole vescicole vicine alla membrana cellulare
che contengono canali a cancello
Meccanismo eccitazione-contrazione
Il Ca++ entra nelle fibre muscolari lisce attraverso:
♦ canali voltaggio-dipendenti attivati
dalla depolarizzazione
♦ canali attivati meccanicamente
♦ canali a controllo di neurotrasmettitore
Il Ca++ viene anche rilasciato dal R.S.
Il Ca++ si lega alla calmodulina
Il complesso Ca-calmodulina si lega alla chinasi
della catena leggera della miosina attivandola
La chinasi attivata fosforila la miosina
ripristinandone l’attività ATPasica.
Gli eventi molecolari della contrazione nel muscolo liscio sono simili a
quelli del muscolo scheletrico con alcune differenze:
-Sia nel m. liscio che in quello scheletrico, il segnale di inizio della
contrazione è un aumento del calcio citoplasmatico
-Nel m. liscio il calcio entra da liquido extracellulare oltre a venire
rilasciato dal reticolo sarcoplasmatico
-Nel m. liscio il calcio si lega alla calmodulina. Nel m. scheletrico si lega
alla troponina che manca nel m. liscio
-Nel m. liscio il calcio, che si lega alla calmodulina, è solo il primo passo
della cascata che termina con la contrazione. Nel m. scheletrico il calcio
che si lega alla troponina avvia immediatamente la contrazione
-Nel m. liscio la fosforilazione delle proteine è caratteristica essenziale del
processo contrattile
- Nel m. liscio la regolazione della miosina è il principale controllo della
contrazione. Nel m. scheletrico è l’actina a essere regolata.
Il Ca++ viene rimosso dal citoplasma usando una
proteina di antiporto Ca++-Na+ ed una Ca++-ATPasi
La calmodulina rilascia il calcio e si stacca dalla
chinasi delle catene leggere.
La miosina fosfatasi rimuove il fosfato dalla miosina
diminuendone l’attività ATPasica
La miosina ha una attività ATPasica più lenta quindi la fase contrattile
è più lunga (fenomeno del blocco dei ponti trasversali)
MUSCOLO LISCIO UNITARIO
L’onda di depolarizzazione
diffonde nel tessuto
attraverso le giunzioni che
collegano le cellule.
MUSCOLO LISCIO MULTI-UNITARIO
Nell’iride e nel corpo ciliare dell’occhio, nel tratto genitale maschile e nell’utero tranne che
prima del travaglio e del parto.
Cellule non connesse elettricamente. Ogni cellula deve essere stimolata indipendentemente.
Ciò consente un controllo fine e contrazioni graduate, visto che rende possibile l’attivazione
selettiva di singole fibre.
Fibre colinergiche
Fibre adrenergiche
SISTEMA NERVOSO AUTONOMO
A seconda del recettore coinvolto si indurrà vasocostrizione o
vasodilatazione nell’arteriola.
Frequenza contrattile costante nel
tempo genera vasocostrizione.