Progetto dal titolo: “Produzione di anticorpi ingegnerizzati contro macromolecole espresse sulla
membrana cellulare”.
Responsabile della Ricerca: Annarosa Arcangeli
Negli ultimi venti anni, sta prendendo campo un nuovo modello di riferimento nella ricerca
oncologica, basato sul concetto che canali ionici e trasportatori controllano molti aspetti del fenotipo
neoplastico in diversi tipi di tumori umani (1-3). Le ricerche condotte dalla Prof. Arcangeli hanno
fortemente contribuito a dimostrare l’importanza che i canali Kv11.1 (hERG1) rivestono
nell’acquisizione del fenotipo neoplastico. A tale proposito, è noto che queste proteine sono iperespresse
in alcuni tumori umani, in cui controllano vari aspetti della fisiologia della cellula neoplastica (4-12).
L’attività del canale è in grado di modulare i) i fenomeni di proliferazione e di apoptosi regolando
conseguentemente la chemioresistenza, ii) la secrezione di VEGF con un chiaro impatto sulla
progressione tumorale, iii) l’acquisizione di un fenotipo invasivo. Il fatto che la proteina hERG1 sia in
grado di influenzare cosi tanti e differenti aspetti è imputabile alla sua capacità di modulare la
segnalazione intracellulare e ciò è reso possibile dal fatto che a livello della membrana plasmatica delle
cellule tumorali si lega con i recettori integrinici e in alcuni casi anche con recettori per fattori di crescita
e citochine a formare complessi macromolecolari.
In collaborazione con il Prof. Ermanno Gherardi del Medical Research Council di Cambridge, l’oggetto
di questo progetto è quello di produrre un nuovo anticorpo anti-hERG1, da poter essere utilizzato in
diagnostica e clinica. Tale anticorpo sarà il risultato di un’ingegnerizzazione di una proteina anticorpale
già prodotta nel nostro laboratorio (vedi sotto) e sarà costituito da una singola catena polipeptidica che
include il dominio variabile della catena pesante dell’ immunoglobulina (VH) legato mediante un
polipeptide flessibile (linker) ad un dominio variabile della catena leggera (VL). Per questo motivo verrà
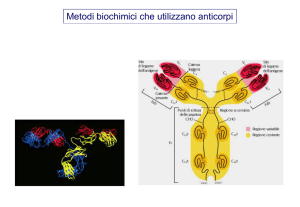
indicato come “single chain variable fragment o scFv” (Fig. 1).
Fig.1
Gli anticorpi scFv hanno molte applicazioni pratiche, comprese l’immunodiagnosi e la terapia. In
particolare, sono spesso preferibili rispetto agli anticorpi completi, poiché la regione Fc può determinare
il riconoscimento di bersagli non desiderati quali le cellule esprimenti i recettori Fc.
In particolare, la prima fase sperimentale consisterà nell’ingegnerizzazione di un anticorpo
monoclonale murino anti-hERG1 prodotto in passato nel nostro laboratorio, la cui specificità ed efficacia
in vivo è stata già dimostrata con ricerche finanziate con fondi del progetto Grant Proposal 2007
assegnato alla Prof. Arcangeli dall’Istituto Toscano Tumori (ITT), con i quali sarà finanziato anche tale
Assegno di Ricerca.
Tale ingegnerizzazione consiste nella clonazione e nel sequenziamento del cDNA codificante i domini
VH e VL dell’anticorpo murino di interesse a partire dall’RNA estratto dagli ibridomi secernenti gli
anticorpi anti-hERG1 (Mab A7, prodotto brevetto N° FI2006A000008). Questo obiettivo sarà raggiunto
mediante PCR usando primers specifici capaci di riconoscere le regioni costanti e le sequenze leader a
monte delle regioni V. Usando oligonucleotidi specifici per le sequenze esterne al DNA codificante i
domini variabili espressi, saranno ottenuti i geni-V specifici dell’ibridoma. I prodotti di PCR saranno
direttamente clonati in un vettore appropriato (pCRII, Invitrogen), senza bisogno di alcuna purificazione.
Dopo il sequenziamento di almeno due diversi cloni positivi per ciascuna regione V, al fine di identificare
possibili errori dovuti alla reazione di amplificazione, le sequenze clonate verranno modificate alle
estremità 5’ e 3’ (usando primers opportuni), in modo da inserire le sequenze di restrizione necessarie per
il loro trasferimento in vettori di espressione. Il prodotto finale sarà trasfettato transientemente in modelli
cellulari e dopo un’opportuna selezione, saranno eseguiti test ELISA per valutare la capacità di secernere
l’anticorpo di interesse.
BIBLIOGRAFIA:
1) Fraser & Pardo, EMBO Rep. 9: 512–5 (2008).
2) Becchetti &Arcangeli, J. Gen. Physiol. 132, 313-4 (2008).
3) Arcangeli et al., Curr Med Chem 16: 66-93 (2009).
4) Arcangeli, et al., J.Physiol., 489, 455-471 (1995).
5) Bianchi et al., Cancer Res., 58, 815-822 (1998).
6) Cherubini et al. Br. J. Cancer, 83, 1722-1729 (2000).
7) Pillozzi et al.,Leukemia, 16, 1791-1798 (2002).
8) Crociani et al., J. Biol. Chem., 278, 2947-2955 (2003).
9) Lastraioli et al., Cancer Res. 64:606-611 (2004).
10) Masi et al. Br. J. Cancer, 93, 781-792 (2005).
11) Pillozzi et al. Blood, 110, 1238-1250 (2007).
12) Crociani et al., submitted to Cancer Cell.
Il Responsabile della Ricerca
Prof. Annarosa Arcangeli