UNIVERSITÀ DEGLI STUDI DI GENOVA
Facoltà di scienze matematiche, fisiche e naturali
Corso di Laurea Triennale in Fisica
SPETTROSCOPIA ELETTRONICA
SU FILM PER GLI SPECCHI
DI RIVELATORI DI ONDE
GRAVITAZIONALI
Candidato: Giulio Pizzigoni
Relatori:
Dott. Gianluca Gemme
Dott. Mirko Prato
Anno Accademico 2008/2009
Indice
Introduzione
1
2
Spettroscopia Elettronica a raggi X
1.1 Principi fisici . . . . . . . . . . . . . . . . . . .
1.1.1 Modellizzazione delle shell atomiche
1.1.2 Effetto fotoelettrico . . . . . . . . . . .
1.2 Strumento di misura: spettrometro XPS . . .
1.2.1 Lampada a raggi X . . . . . . . . . . .
1.2.2 Schema dell’analizzatore di elettroni .
1.2.3 Sistema di vuoto . . . . . . . . . . . .
1.2.4 Profondità d’analisi . . . . . . . . . . .
1.2.5 Compensazione della carica . . . . . .
5
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
Analisi dei campioni
2.1 Modalità di analisi del campione . . . . . . . . . . . . . .
2.2 Analisi del film . . . . . . . . . . . . . . . . . . . . . . . .
2.2.1 Campione as received . . . . . . . . . . . . . . . . .
2.2.2 Campione trattato tramite bombardamento ionico
2.2.3 Polvere di pentossido . . . . . . . . . . . . . . . .
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
9
9
9
10
10
11
13
14
14
15
.
.
.
.
.
17
17
19
19
26
36
Conclusioni
41
Bibliografia
43
Introduzione
L’esistenza delle Onde Gravitazionali è una delle previsioni della teoria della Relatività Generale formulata da Einstein nel 1916. La prima osservazione indiretta del
fenomeno fu compiuta da Hulse e Taylor nel 1975, in seguito alla scoperta del sistema binario di pulsar PSR1913+16 [1]. Essi attribuirono la diminuzione del periodo
orbitale della pulsar alla perdita di energia e momento angolare attraverso l’emissione di onde gravitazionali. Un’intensa attività sperimentale è stata dedicata negli
ultimi quarant’anni alla rivelazione diretta di onde gravitazionali, con lo sviluppo di rivelatori risonanti e della prima generazione di rivelatori interferometrici
(Virgo, LIGO) [2, 3].
Attualmente la comunità scientifica sta lavorando allo sviluppo dei rivelatori
interferometrici di seconda generazione (Advanced Virgo, Advanced LIGO), con
lo scopo di migliorare la sensibilità di un’ordine di grandezza rispetto agli attuali
interferometri di prima generazione. Il volume di Universo osservabile si espanderà di un fattore 1000, con un incremento corrispondente del numero di eventi
rivelabili (v. Fig. 1).
Figura 1: Confronto fra la sensibilità di un interferometro di prima generazione (Virgo) ed
uno di seconda generazione (Advanced Virgo). A destra è illustrato l’aumento
del volume dell’Universo osservabile corrispondente.
Per realizzare la futura generazione di interferometri è necessario studiare tutte
le possibili fonti di rumore che limitano la sensibilità dell’apparato, nel tentativo di
trovare tecniche per ridurli ulteriormente. Nella regione di frequenza intermedia,
dove ci si aspetta l’emissione di onde gravitazionali da un gran numero di sorgenti,
la sensibilità di un tipico interferometro è limitata dall’eccitazione termica dei gradi
di libertà meccanici degli specchi sospesi e delle loro sospensioni. In particolare da
circa 40 Hz a 150 Hz il contributo dominante al rumore termico viene dagli specchi
(v. Fig. 2).
6
Introduzione
Figura 2: Principali limitazioni alla sensibilità di un interferometro di seconda generazione
(Advanced Virgo).
L’origine fisica del rumore termico è descritta dal teorema FluttuazioneDissipazione di Callen e Welton [4]. In sintesi, il teorema mette in relazione le
fluttuazioni all’equilibrio termodinamico di un corpo con le proprietà dissipative
del corpo stesso. In altre parole, quanto maggiori sono le dissipazioni meccaniche
di un materiale, tanto maggiori saranno le fluttuazioni all’equilibrio termico dei
suoi gradi di libertà meccanici, ossia il rumore termico ad essi associato. Per questa ragione, per ridurre il rumore termico degli specchi si utilizzano materiali con
ridottissime dissipazioni meccaniche.
Negli interferometri di prima generazione gli specchi sono formati da un substrato di ossido di silicio, SiO2 (Herasil), del peso di circa 20 Kg, sul quale è depositato per sputtering un multistrato riflettente formato da una decina di strati sottili
(spessore d ≈ 100 nm), alternando un materiale a basso indice di rifrazione, ossido
di silicio, ed un materiale ad alto indice di rifrazione, ossido di tantalio Ta2 O5 (v.
Fig. 3).
Figura 3: Struttura schematica di uno specchio. Si notano gli strati alternati di materiale a
basso indice di rifrazione, n L e ad alto indice di rifrazione, n H . Lo spessore dei
singoli strati è scelto in modo da soddisfare la relazione n · d = λ/4, dove λ =
1064 nm, è la lunghezza d’onda della luce nell’interferometro.
Al rumore termico degli specchi contribuiscono sia il substrato (bulk) sia il multistrato riflettente (coating). Mentre negli attuali rivelatori il fattore limitante è il rumore termico del bulk, negli interferometri di seconda generazione saranno impiegati substrati con minori dissipazioni meccaniche (Suprasil) e di massa maggiore
(circa 40 Kg), e il rumore termico del coating diventerà dominante. Studi recenti
Introduzione
7
hanno mostrato come il rumore termico del coating sia a sua volta dominato dal
materiale ad alto indice di rifrazione, il Ta2 O5 [5].
Per questa ragione uno studio sistematico delle tecniche di deposizione e delle
caratteristiche ottiche e meccaniche dei materiali utilizzati per il coating, e in particolare dell’ossido di tantalio, assume una grande importanza, con lo scopo di identificare i meccanismi delle dissipazioni meccaniche e migliorare le caratteristiche
meccaniche senza degradare le proprietà ottiche.
Il gruppo di ricerca nel quale ho lavorato opera all’interno della collaborazione
Virgo, con lo scopo di identificare le cause delle dissipazioni meccaniche nei coating
dielettrici degli specchi e di migliorare le loro caratteristiche, utilizzando diverse
tecniche di analisi dei materiali. Nell’ambito di questa collaborazione, nel mio lavoro di tesi, mi sono occupato della caratterizzazione chimica dei film di pentossido
di tantalio mediante spettroscopia foto-elettronica a raggi X (X-ray Photoelectron
Spectroscopy, XPS).
Sono stati analizzati due campioni di pentossido: un film di spessore nominale di 200 nm, depositato su ossido di silicio (ATFilms) e una polvere (dimensione < 5 µm) di Ta2 O5 puro al 99, 99%. Il film è stato analizzato prima e dopo un
bombardamento con ioni Argon.
Nel Capitolo 1 sono brevemente illustrati i principi fisici sui quali si basa l’analisi XPS, e il funzionamento dello spettrometro utilizzato. Nel Capitolo 2 sono
presentate le misure e la relativa analisi per identificare le specie chimiche presenti.
Infine nelle Conclusioni si cerca di fornire un’interpretazione dei risultati ottenuti
e una descrizione dei possibili sviluppi futuri.
Capitolo 1
Spettroscopia Elettronica a raggi X
1.1
1.1.1
Principi fisici
Modellizzazione delle shell atomiche
La struttura elettronica di un elemento è descritta dal modello a shell. Un orbitale
è univocamente identificato da tre numeri quantici: n, l e j. Questi danno informazioni sull’energia del livello, sul suo momento angolare orbitale e su quello totale.
Può essere considerato anche il numero quantico magnetico m, proiezione sull’asse
z del momento angolare orbitale (l).
I numeri quantici sono legati dalle seguenti relazioni:
n = 1, 2, ....
l<n
j = l±s
−l < m < l
(1.1)
dove s è lo spin dell’elettrone (= 12 ).
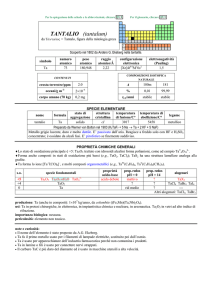
La tabella 1.1 lega i numeri quantici con notazioni usate in spettroscopia elettronica:
Figura 1.1: Tabella di nomenclatura
Gli elettroni si dispongono su questi livelli secondo il principio di Pauli: in un
orbitale vi può essere un unico elettrone con numeri quantici n, l, m e s.
Ogni coppia di n e l corrisponde a due valori differenti di momento angolare
totale j. Se l 6= 0, come conseguenza dell’interazione spin-orbita, il livello j = l + s
ha un’energia differente dal quello con j = l − s; per l = 0 i due livelli coincidono.
10
Spettroscopia Elettronica a raggi X
1.1.2
Effetto fotoelettrico
Il fenomeno fisico che rende possibile l’analisi del campione è l’effetto fotoelettrico:
un quanto di energia, hν, è in grado di estrarre un elettrone da un atomo, purché
sia verificato:
hν > EB + W
(1.2)
dove W è la funzione lavoro per estrarre un elettrone dal materiale, ed EB è l’energia di legame dell’elettrone estratto, caratteristica dell’elemento da cui proviene
l’elettrone e dal suo stato chimico.
Figura 1.2: Nella figura è rappresentato lo schema di emissione di un elettrone per effetto
fotoelettrico
Si ricava che l’energia cinetica di un elettrone emesso per effetto fotoelettrico è
data da:
Ek = hν − W − EB
(1.3)
Se W e hν sono noti è possibile conoscere l’energia di legame, risalendo così
al materiale dal quale è stato emesso l’elettrone. Quindi, sfruttando l’effetto fotoelettrico, è possibile effettuare l’analisi chimica di un campione, identificando gli
elementi da cui è composto ed il loro stato chimico.
1.2
Strumento di misura: spettrometro XPS
Lo spettrometro utilizzato, come si vede dalla Fig. 1.3, è costituito da tre parti
fondamentali:
• camera sperimentale e campione;
• sorgente di raggi X;
• rivelatore.
Strumento di misura: spettrometro XPS
11
Figura 1.3: Schema dello spettrometro XPS
1.2.1
Lampada a raggi X
L’analisi si basa sull’interazione di raggi X con il campione. Per generare questa
radiazione esistono diverse tecniche. Nel nostro caso è stata utilizzata una lampada, costituita da un tubo sotto vuoto avente agli estremi anodo e catodo (nel caso
dell’XPS il catodo è a terra e l’anodo è fissato ad un potenziale compreso fra 10 ÷ 15
KV). Nella regione del catodo è posto un filamento metallico (e.g. tungsteno) che,
per effetto termico, rilascia elettroni.
Questi vengono accelerati e portati ad energie cinetiche comprese fra 4 ÷ 15
KeV. Lungo la direzione degli elettroni è posto un bersaglio (e.g. magnesio,
alluminio,...); gli elettroni interagiscono con questo materiale, ionizzandolo.
Figura 1.4: Lampada a raggi X
La ionizzazione porta l’atomo in una configurazione eccitata. L’atomo, per tornare in una posizione di equilibrio, richiama un elettrone dalla shell più esterna nel
livello ionizzato; questo fenomeno emette un fotone di energia:
hν = En − EK
(1.4)
12
Spettroscopia Elettronica a raggi X
dove En è l’energia dell’elettrone meno legato e EK è quella del livello ionizzato.
Di seguito è riportata una tabella con diversi materiali usati come target con le
relative energie dei raggi X prodotti:
Figura 1.5: Magnesio e alluminio sono i materiali comunemente usati per la realizzazione
dell’anodo
Nel nostro caso il target è di alluminio. Questo materiale presenta un buon
rapporto fra energia prodotta e larghezza del picco e siamo in grado di ottenere
fotoemissione per tutte le energie di legame a cui siamo interessati. Inoltre la risoluzione sulle energie cinetiche selezionate (da cui dipende quella sull’energia di
legame) è data da:
2
∆EK = (∆EB2 + ∆Eν2 + ∆EXPS
)0.5
(1.5)
dove ∆EB è la larghezza intrinseca dovuta al tempo di vita medio finito della
lacuna, ∆EXPS è la risoluzione dell’analizzatore di elettroni e ∆Eν è la larghezza del picco dei raggi X prodotti. Quindi, fissati gli altri due errori, maggiore è
l’indeterminazione dei raggi X, maggiore sarà l’errore sull’energia cinetica.
Per migliorare ulteriormente la larghezza della riga dei raggi X prodotti è necessario introdurre un monocromatore. Questo permette la selezione di una lunghezza d’onda attraverso la diffrazione su un reticolo cristallino. Questo è possibile
perchè la radiazione presenta una lunghezza d’onda comparabile col passo reticolare. La legge, proposta nel 1913 da Bragg [6], lega l’angolo di diffrazione alla
Strumento di misura: spettrometro XPS
13
lunghezza d’onda:
2d sin θ = nλ
(1.6)
Figura 1.6: Diffrazione sul cristallo
dove d è la distanza fra due piani del cristallo, θ è l’angolo rispetto al piano di
incidenza e n é l’ordine del picco selezionato.
1.2.2
Schema dell’analizzatore di elettroni
L’apparato per la selezione e il conteggio degli elettroni di energia fissata è formato
da: lenti elettrostatiche, condensatore emisferico e detector.
Figura 1.7: Schema analizzatore
La selezione degli elettroni con energia cinetica fissa (di seguito pass energy) è
data dalla differenza di potenziale applicata (di seguito d.d.p.) al condensatore
emisferico:
R1 R2
EK =
e∆V = ke∆V
(1.7)
R22 − R21
dove R1 e R2 sono rispettivamente il raggio minore e quello maggiore del condensatore, e la carica dell’elettrone e ∆V la differenza di potenziale. I campioni di
Ta2 O5 sono stati analizzati a pass energy costante, quindi a d.d.p. e relativo errore
fissi. Questa scelta porta ad avere un ∆EXPS anch’esso costante in tutta la misura,
in quanto proporzionale all’errore commesso sulla differenza di potenziale.
Ricordando l’eq. 1.5 è facile notare come ad alte pass energy la risoluzione dello
strumento diminuisca mentre aumenta a basse pass energy.
14
Spettroscopia Elettronica a raggi X
Le lenti elettrostatiche, poste anteriormente al condensatore, hanno la proprietà
di collimare e variare l’energia cinetica degli elettroni. Con queste caratteristiche le
lenti sono in grado, variando il potenziale applicatogli, di presentare all’entrata del
condensatore elettroni con la giusta pass energy.
Lo stadio finale consta di un channel plates: un disco con una serie di piccoli
fori. Ognuno di questi fori ha un piccolo channel electron multiplier. Questo oggetto
è in grado di moltiplicare gli elettroni in entrata.
Figura 1.8: Schema channel electron multiplier
Il guadagno di questo componente è funzione della tensione applicatagli. Utilizzando valori tipici di tensione fra 2 e 4 KV, il guadagno è circa di un fattore
100.
1.2.3
Sistema di vuoto
La camera in cui il campione è analizzato si trova ad una pressione di 10−8 ÷ 10−9
mbar. Se non si lavorasse in queste condizioni, gli elettroni, che dal campione viaggiano verso l’analizzatore, continuerebbero a scambiare energia col gas; questo porterebbe ad una diminuzione del segnale e ad un conseguente aumento del rumore.
Un altro dato importante è il fattore di ricoprimento: alla pressione di 10−6 mbar il
gas residuo è capace di legarsi alla superficie del solido creando un monolayer di
gas in 1 secondo. A queste pressioni il fenomeno presenta una scala temporale decisamente inferiore al tempo di analisi ed è in grado di introdurre così una sorgente
di rumore non trascurabile.
L’inserimento del campione nella camera viene fatto servendosi di una
pre-camera, per evitare tutte le volte di depressurizzare l’intero volume.
1.2.4
Profondità d’analisi
La relazione che lega l’intensità di emissione degli elettroni alla profondità di
analisi nel materiale è data da:
I ( x ) = I0 e− x/λ cos θ
(1.8)
dove x è la distanza, I0 è l’intensità per x = 0, λ il libero cammino medio degli
elettroni e θ l’angolo fra la normale alla superficie e l’analizzatore.
Vediamo che dopo uno spessore superiore 3λ il fascio si attenua di circa il 95%.
Questo parametro è funzione dell’energia degli elettroni e del materiale analizzato,
secondo la legge empirica proposta da Seah e Dench (1979):
λ=
538a A
+ 0.361a A ( a A E A )0.5
E2A
(1.9)
Strumento di misura: spettrometro XPS
15
La profondità di analisi, fissato il libero cammino medio, varia in funzione
dell’angolo di take-off, θ, come mostrato in figura 1.3.
Figura 1.9: La profondità di analisi dipende dell’angolo di take-off, θ
L’analisi di un film, effettuata a diversi angoli, porta informazioni sulla
composizione chimica in funzione della profondià nel campione.
1.2.5
Compensazione della carica
L’analisi sul campione porta ad un accumulo di carica, positiva, sulla sua superfice, vista la continua estrazione di elettroni. Questa genera un campo elettrico che
modifica le energie degli elettroni rilevati. Pertanto è necessario mantenere neutro
il nostro campione, onde evitare questa causa di errore.
Se esso ha proprietà metalliche allora basterà collegarlo a terra perchè si mantenga elettricamente neutro. Se il materiale è invece un dielettrico (come nel caso dei
campioni di Ta2 O5 ), la neutralizzazione richiede una tecnica differente: investire la
zona analizzata con un fascio di elettroni di bassa energia (5 eV) emessi per effetto
termico da un filamento metallico riscaldato.
Capitolo 2
Analisi dei campioni
Scopo dell’analisi è caratterizzare la composizione chimica di un film di Ta2 O5 (dello spessore nominale di 200 nm) depositato mediante Double Ion Beam sputtering (v.
Fig. 2.1) su un substrato di SiO2 (Corning 7980r , ATFilms).
Figura 2.1: Schema Double Ion Beam sputtering. (1) Fascio di ioni Argon, (2) target, (3) substrato, (4) Fascio secondario di ioni Argon, (5)(6) raggio di elettroni per neutralizzare l’Argon, (7) controllo ottico per controllare lo spessore durante la
crescita
Il campione, così realizzato, è stato analizzato as received a due angoli di take-off:
45◦ e 32◦ . Successivamente è stato bombardato con ioni Argon (sputtering). Dopo
questo trattamento è stato nuovamente analizzato a 45◦ e 32◦ .
Infine è stata analizzata una polvere di pentossido di tantalio prodotta da Aldrich, pura al 99, 99% e con grani di grandezza nominale inferiore a 5 µm. Questa
analisi è servita per confrontare i dati ottenuti sul film con le caratteristice del Ta2 O5
bulk.
2.1
Modalità di analisi del campione
All’interno della camera principale il campione ha 4 gradi di libertà: tre di traslazione e uno di rotazione. I primi sono necessari per la messa a fuoco dell’analizzatore sul campione, in modo da massimizzare il numero di elettroni raccolti dallo
stesso; la rotazione varia l’angolo fra la normale alla superficie del campione e l’analizzatore e permette così di effettuare misure a diverse profondità (v. sezione
1.2.4).
18
Analisi dei campioni
Per prima cosa viene fatta una misura di pochi minuti a bassa risoluzione (survey) dove si analizza uno spettro di energia di legame (binding energy, B.E.) compresa fra pochi eV e 1000 eV. Per realizzare questa misura si usa un’alta pass energy
(v. sezione 1.2.2) (nel nostro caso 187.85 eV):
Figura 2.2: Esempio di survey su campione di pentossido as received; è possibile vedere già
gli elementi presenti
In figura è riportato lo spettro XPS del campione as received. Come si può vedere presenta dei picchi in determinate regioni di B.E. che identificano la presenza
di un particolare elemento. L’intensità di questi picchi è direttamente proporzionale alla concentrazione dell’elemento. Il fattore di proporzionalità, detto fattore
di sensibilità dell’elemento, dipende dall’efficienza e dalla funzione di trasmissione dell’analizzatore e dalla sezione d’urto propria del processo di foto-emissione
considerato.
In tutto lo spettro è presente anche un fondo. Questo è causato da tutti quegli
elettroni che hanno subito scattering anelastico prima di uscire dal campione.
Una volta realizzata questa misura è necessario capire in quali regioni di B.E.
sono presenti gli elementi da analizzare. Per fare questo si cercano, in letteratura [8–10], i valori di B.E. degli elementi che possono essere nel campione e si
confrontandoli coi valori dei picchi propri dello spettro.
Dalla misura di Fig. 2.2, si osserva la presenza di Ossigeno, Tantalio e Carbonio. Quest’ultimo elemento è probabilmente presente a causa dell’esposizione del
campione all’ambiente.
Una volta identificate le posizioni degli elementi viene effettuata una misura ad
alta risoluzione (di seguito HRES), nel nostro caso con pass energy di 5.85 eV.
Per analizzare i dati così raccolti ho utilizzato due programmi, MultiPak (fornito
assieme allo strumento di misura) e Fityk [11].
Il primo programma sfruttando i fattori di sensibilità degli elementi analizzati permette, nota l’intensità dei picchi, di calcolare il rapporto stechiometrico fra
gli elementi di interesse. Il secondo programma permette di sottrarre il fondo
(utilizzando il modello di Shirley [7]), e analizzare i dati così ottenuti.
L’analisi consiste nell’approssimare la curva sperimentale con una base di N
gaussiane. Per ogni legame chimico il numero di gaussiane dipende dal momento
angolare l del livello. Se questo ha l = 0 ogni specie chimica sarà rappresentata
da una gaussiana. Nel caso di livello con l 6= 0, per il principio di interazione
spin-orbita, ogni specie chimica è rappresentata da un doppietto. La distanza fra i
picchi del doppietto è propria della separazione del livello e il rapporto fra aree è
Analisi del film
19
dato dalla relazione:
S.O. =
2.2
2.2.1
2( l + s ) + 1
2( l − s ) + 1
(2.1)
Analisi del film
Campione as received
La prima misura è stata effettuata sul campione as received ad un angolo di 45◦ .
Dal survey (v. es. in Fig. 2.2) si identificano sul campione i seguenti elementi:
Tantalio, Ossigeno, e Carbonio. I livelli orbitali che portano informazioni su questi
elementi e sui loro legami sono, rispettivamente, Ta 4f, O 1s e C 1s.
Dalla letteratura si assumono le seguenti B.E. [8–10]:
Elemento
Ta
C
O
Origine
Ta2 O5
avventizio
Ta2 O5
Livello
4f7/2
1s
1s
B.E. (eV)
26.40
284.80
530.60
Tabella 2.1: B.E. note dalla letteratura. La B.E. del carbonio sarà quella su cui ci baseremo
per calibrare la nostra scala energetica
La scala dell’energia di legame sarà calibrata imponendo la posizione del livello
C 1s come trovata da letteratura (v. Tab. 2.1).
Una volta eseguito il survey, si decide di effettuare l’HRES nelle regioni di B.E.:
a) Ta4f: [15 ÷ 35] eV;
b) C1s: [275 ÷ 295] eV;
c) O1s: [520 ÷ 540] eV.
A causa dell’accoppiamento spin-orbita mi aspetto di trovare una curva avente
due picchi nella regione ’a’, mentre ne avrò solo uno in ’b’ e ’c’ (v. sezione 1.1.1).
Questi i dati raccolti:
Figura 2.3: Livello 4f del Tantalio
20
Analisi dei campioni
Figura 2.4: Livello 1s del Carbonio
Figura 2.5: Livello 1s dell’Ossigeno
Come atteso, in Fig. 2.3, si osserva la separazione dei sotto livelli j = 7/2 e
j = 5/2.
Inoltre il rapporto stechiometrico calcolato fra Tantalio e Ossigeno vale circa
0.47. Questo dato mostra un deficit di Ossigeno nel campione, in quanto il valore
Ta/O nel Ta2 O5 deve valere 0.4.
Successivamente viene fatto un survey a 32◦ e si decide eseguire l’HRES sulle
seguenti regioni di B.E.:
a) Ta4f: [15 ÷ 35] eV;
b) C1s: [273 ÷ 293] eV;
c) O1s: [520 ÷ 540] eV.
Questi i dati raccolti:
Analisi del film
21
Figura 2.6: Livello 4f del Tantalio
Figura 2.7: Livello 1s del Carbonio
Figura 2.8: Livello 1s dell Ossigeno
Il rapporto stechiometrico calcolato fra Tantalio e Ossigeno vale circa 0.45.
Questo dato conferma la carenza di Ossigeno nel campione, precedentemente
osservata.
È utile confrontare i dati delle due misure. Per eseguire questa operazione
22
Analisi dei campioni
bisogna prima normalizzare le aree dei dati.
Figura 2.9: Confronto Ta 4f. Si osserva una diversa forma nei punti 1 e 2.
Figura 2.10: Confronto O 1s. Si osserva una diversa forma nel punto 1.
Per quanto riguarda i dati del carbonio non vi sono particolari differenze, mentre per quelli del tantalio e dell’ossigeno si notano forme differenti (v. Fig. 2.9
e Fig.2.10), questo porta a pensare ad una composizione chimica funzione della
profondità (v. sezione 1.2.4).
Con queste informazioni è possibile iniziare ad analizzare i dati.
Osservando i dati relativi al livello Ta 4f, presi ad un angolo di 45◦ , risulta evidente la necessità di utilizzare più di una specie chimica per riprodurre l’andamento sperimentale dei dati. Ogni specie chimica è rappresentata da una coppia di
gaussiane. Fra loro sono fissate le seguenti relazioni: il rapporto delle aree vale
0.75 (v. eq. 2.1), la distanza fra i picchi è stata impostata a 1.91 eV, come da letteratura [8, 10]. Fra loro si è imposta la stessa larghezza a metà altezza(full width at
half height, FWHM), in quanto i dati sono affetti tutti dalla stessa indeterminazione
(provengono dallo stesso livello, i raggi X con cui è stato eccitato il campione hanno sempre la stessa indeterminazione e durante la misura l’indeterminazione dello
strumento è stata tenuta costante) (vedi eq. 1.5). L’analisi migliore, su questi dati, è
stato ottenuto con tre specie chimiche.
Questi i risultati ottenuti:
Analisi del film
23
Ta2 O5
Ta2 O5− x
Ta
Center (eV)
26.491 ± 0.025
28.401 ± 0.025
25.153 ± 0.025
27.053 ± 0.025
21.863 ± 0.025
23.773 ± 0.025
Area
1662
1246
113
85
68
51
FWHM (eV)
1.185 ± 0.025
1.185 ± 0.025
1.185 ± 0.025
1.185 ± 0.025
1.185 ± 0.025
1.185 ± 0.025
Tabella 2.2: Analisi sul livello 4f del tantalio a 45◦ su campione as received con chi-quadro
di 2.83
Figura 2.11: Analisi dei dati su campione as received a 45◦ su Ta 4f
Confrontando con la letteratura i risultati ottenuti [9] si deduce che la gaussiana
con centro a 26.491 eV è il pentossido di tantalio, mentre quella a 21.863 eV è tantalio
metallico. La terza specie si suppone essere subossido di tantalio (Ta2 O5− x ).
Da questa analisi la specie chimica dominante è il pentossido. Inoltre questo fit
determina la B.E. del subossido e del metallo (confrontato con la letteratura [9]); i
sotto livelli con j = 7/2 sono ad una distanza da quello del pentossido di 1.338
eV (subossido) e di 4.628 eV (metallo). Questi valori sono stati imposti nei fit
successivi.
Per analizzare i dati a 32◦ sono state usate le stesse famiglie chimiche usate
nell’analisi dei dati a 45◦ . Ad ogni specie chimica sono imposte le generalità del
livello (rapporto e separazione spin-orbita). Inoltre la specie chimica del subossido
è stata imposta distante da quella del pentossido di 1.338 eV (valore trovato dall’analisi precedente), mentre la specie chimica del metallo è stata imposta distante dal
pentossido di 4.628 eV (valore trovato dall’analisi precedente).
Questi i risultati ottenuti:
24
Analisi dei campioni
Ta2 O5
Ta2 O5− x
Ta
Center (eV)
26.397 ± 0.025
28.307 ± 0.025
25.057 ± 0.025
26.967 ± 0.025
21.74 ± 0.025
23.65 ± 0.025
Area
1856
1392
30
23
66
50
FWHM (eV)
1.038 ± 0.025
1.038 ± 0.025
1.038 ± 0.025
1.038 ± 0.025
1.038 ± 0.025
1.038 ± 0.025
Tabella 2.3: Analisi sul livello 4f del Tantalio a 32◦ su campione as received con chi-quadro
di 4.27
Figura 2.12: Analisi dei dati su campione as received a 32◦ su Ta 4f
Per confrontare l’abbondanza delle tre specie vanno normalizzate le aree trovate, rispetto a quella del pentossido. Questi i dati normalizzati (rispetto al
pentossido) e confrontati:
Elemento
Ta2 O5− x
Ta
Analisi a 45◦
6.8%
4.1%
Analisi a 32◦
1.6%
3.6%
Tabella 2.4: Confronto fra aree normalizzate rispetto al pentossido di tantalio
Da questo confronto si nota come il metallo abbia una percentuale quasi costante in funzione della profondità. Vi è, invece, una diminuzione di subossidi
all’aumentare della profondità di analisi.
Osservando, invece, i dati relativi al livello O 1s (ad un angolo di 45◦ ), risulta
evidente la necessità di utilizzare più di una specie chimica per riprodurre l’andamento sperimentale dei dati. La migliore analisi è stata fatta utilizzando tre specie
chimiche. Ogni specie chimica è rappresentata da una gaussiana. Fra loro si è imposta la stessa FWHM, in quanto i dati sono affetti tutti dalla stessa indeterminazione
(provengono dallo stesso livello, i raggi X con cui è stato eccitato il campione hanno sempre la stessa indeterminazione e durante la misura l’indeterminazione dello
strumento è stata tenuta costante) (vedi eq. 1.5).
Questi i risultati ottenuti:
Analisi del film
25
Ta2 O5
H2 O
Ta2 O5− x
Center (eV)
530.555 ± 0.025
532.955 ± 0.025
532.010 ± 0.025
Area
1858
69
170
FWHM (eV)
1.584 ± 0.025
1.584 ± 0.025
1.584 ± 0.025
Tabella 2.5: Valori dei parametri trovati analizzando i dati del livello 1s dell’Ossigeno a
45◦ . Il chi-quadro è di 1.87
Figura 2.13: Analisi sui dati del livello 1s dell’Ossigeno a 45◦
Confrontando con la letteratura i risultati ottenuti [9] si deduce che la gaussiana con centro a 530.555 eV è Ta2 O5 , mentre quella a 532.955 eV è H2 O [9]. La terza
specie è subossido di tantalio (Ta2 O5− x ). Si osserva come la specie chimica dominante sia il pentossido, mentre le altre due specie hanno un numero di conteggi
ridotto. Inoltre la specie chimica legata ai subossidi ha un B.E. maggiore di quella
del pentossido di 1.455 eV. Quest’ultima informazione è servita per impostare, nei
fit successivi, la distanza relativa fra il centro della gaussiana dei subossido e quello
dei pentossidi.
Per analizzare i dati presi a 32◦ si sono usate le stesse specie chimiche trovate
con l’analisi precedente.
Questi i risultati ottenuti:
Ta2 O5
H2 O
Ta2 O5− x
Center (eV)
530.621 ± 0.025
533.021 ± 0.025
532.076 ± 0.025
Area
2059
64
254
FWHM (eV)
1.312 ± 0.025
1.312 ± 0.025
1.312 ± 0.025
Tabella 2.6: Valori dei parametri trovati analizzando i dati del livello 1s dell’Ossigeno a
32◦ . Il chi-quadro è di 2.44
26
Analisi dei campioni
Figura 2.14: Analisi sui dati del livello 1s dell’Ossigeno a 32◦
Anche qui si osserva come la specie chimica dominante sia il pentossido.
Si nota una differenza non trascurabile della FWHM fra i due fit (maggiore del
10%). Questa potrebbe essere dovuto ad una differente neutralizzazione.
Per confrontare l’abbondanza delle tre specie vanno normalizzate le aree
rispetto al pentossido di tantalio. Questi i dati normalizzati e confrontati:
Elemento
H2 O
Ta2 O5− x
Analisi a 45◦
3.7%
9.1%
Analisi a 32◦
3.1%
12.3%
Tabella 2.7: Confronto fra aree normalizzate rispetto al pentossido di tantalio
Da questo confronto si osserva una diminuzione di acqua e un aumento dei subossidi all’aumentare della profondità di analisi. Il primo dato porta ad ipotizzare
la presenza di acqua in superficie, mentre il secondo porta a pensare ad un aumento
di subossidi negli strati più profondi.
I risultati ottenuti dell’analisi fatta sui dati presi a 45◦ e a 32◦ del campione as
received fanno:
1. supporre una presenza di Carbonio avventizio e acqua nei primi strati del
campione, dovuta ad un deposito superficiale avvenuto successivamente alla
realizzazione del film;
2. osservare che l’andamento della specie dei subossidi, in funzione dell’angolo, nel livello 1s dell’ossigeno e opposta a quella misurata nel livello 4f del
tantalio. Questo porta a pensare che la specie ipotizzata nell’ossigeno (vedi
B.E. del subossido in Tab. 2.5 e Tab. 2.6) abbia una componete di bulk.
2.2.2
Campione trattato tramite bombardamento ionico
Con l’analisi precedente si è trovato che:
1. ci sono materiali diversi dal pentossido di tantalio, in particolare carbonio
avventizio e acqua;
Analisi del film
27
2. i fit sui dati relativi al livello 4f del tantalio portano a ipotizzare la presenza
di subossidi nei primi strati superficiali. Per quanto riguarda la componente metallica invece si osserva un andamento più uniforme in funzione della
profondità;
3. la specie inserita per rappresentare i subossidi nel livello 1s dell’Ossigeno
presenta un comportamento diverso. Questa infatti si comporta al contrario
di quanto visto nel livello 4f del Tantalio; all’aumentare della profondità di
analisi aumenta.
Con i dati fino qui raccolti non è possibile stabilire una relazione fra specie
chimiche e profondità di analisi.
Una tecnica che può fornire evidenze sperimentali ulteriori, eliminando le impurezze superficiali, è un bombardamento ionico sul campione. L’idea è di investire la superficie del campione con ioni di Argon (Ar+ ) di energia cinetica nota
(nel nostro caso 3 KeV). In questo modo lo sputtering è in grado di eliminare i primi strati superficiali, lasciando come zona di analisi strati più profondi, privi di
contaminazione dovuta all’esposizione del film all’ambiente.
Il bombardamento ionico è stato eseguito in intervalli di 6 secondi. Alla fine
di ogni intervallo si è analizzato il campione nella regione di B.E. contenente il
segnale del carbonio (275 e 295 eV). Dopo la terza esecuzione del bombardamento
(18 secondi) il segnale proveniente dal livello 1s del Carbonio è stato eliminato.
Questo trattamento conferma che il Carbonio, sul campione, si è depositato
successivamente alla realizzazione del film.
Una volta eseguito lo sputtering si eseguono due survey, a 45◦ e a 32◦ . Le regioni
di B.E. di interesse rimangono quella del livello 4f del Tantalio e quella 1s dell’Ossigeno. Ad entrambi gli angoli vengono scelte le stesse regioni energetiche, su cui
eseguire l’HRES:
a) Ta 4f: [15 ÷ 35] eV;
b) O 1s: [520 ÷ 540] eV.
Avendo eliminato il carbonio avventizio si è persa la specie chimica di riferimento per calibrare la nostra scala energetica. Per quest’analisi prendiamo come
B.E. di riferimento quella relativa al livello 4f7/2 del Tantalio, nota dalla letteratura
(v. Tab. 2.1), in quanto è una zona ben identificata nel nostro spettro.
La misura ad alta risoluzione, effettuata a 45◦ , da i seguenti risultati:
28
Analisi dei campioni
Figura 2.15: Misura HRES eseguita sul livello 4f del Tantalio
Figura 2.16: Misura HRES eseguita sul livello 1s del Ossigeno
Già da questa misura si vede come lo sputtering abbia alterato le specie chimiche presenti nel campione. Infatti il rapporto stechiometrico Ta/O vale circa
0.53. Questo mostra come il bombardamento ionico abbia aumentato il deficit di
Ossigeno.
L’area dei dati presi a questo angolo è stata poi normalizzata. I dati così ottenuti
sono stati confrontati con quelli precedentemente presi allo stesso angolo sul campione as received. Fra i due livelli, quello che ha modificato maggiormente i suoi
legami chimici è il 4f del Tantalio. Per questo livello si osserva una diminuzione
dei massimi legati al pentossido, mentre nella zona di B.E. legata ai subossidi vi è
un aumento di questa specie (vedi punto 2, Fig. 2.17). Vi è una forma differente
anche nel punto 1 (Fig. 2.17), legata alla comparsa di specie chimiche differenti.
Per il livello O 1s, nei punti 1 e 2 di Fig. 2.18, i dati del campione as received
presentano una forma più larga rispetto a quelli del campione bombardato con
ioni Ar+ . Questo indica che in quelle zone era presente un deposito superficiale,
eliminato dallo sputtering.
Di seguito è riportato il confronto fra i dati presi a 45◦ fra campione non trattato
e trattato:
Analisi del film
29
Figura 2.17: Confronto fra i dati del campione as received e quello trattato, presi a 45◦ . In
questo caso i dati sono quelli del livello Ta 4f
Figura 2.18: Confronto fra i dati del campione as received e quello trattato, presi a 45◦ . In
questo caso i dati sono quelli del livello O 1s
La misura ad alta risoluzione, effettuata a 32◦ , da i seguenti risultati:
Figura 2.19: Misura HRES eseguita sul livello 4f del Tantalio
30
Analisi dei campioni
Figura 2.20: Misura HRES eseguita sul livello 1s del Ossigeno
Anche questi dati presentano un valore di Ta/O pari a 0.53, a conferma del
risultato trovato ad un angolo di 45◦ .
I dati sono stati normalizzati in modo da confrontarli poi coi dati
precedentemente ottenuti dalla misura a 32◦ sul campione as received.
Anche a quest’angolo il livello che ha modificato maggiormente i suoi legami
chimici è il 4f del tantalio. Anche qui vi è una diminuzione dei massimi legati al
pentossido, mentre nella zona di B.E. legata ai subossidi vi è un aumento di questa
specie (vedi punti 2 e 3 di Fig. 2.21). Vi è una forma differente nel punto 1 (v. Fig.
2.21), legata sempre ad una redistribuzione dei legami chimici.
Per il livello O 1s, nel punto 1 di Fig. 2.22, i dati del campione non trattato hanno
una forma leggermente più larga rispetto a quelli del campione sputterato. Questo,
come detto precedentemente, indica che in quella zona era presente un deposito
superficiale, eliminato dallo sputtering.
Di seguito è riportato il confronto coi i dati presi a 32◦ fra campione non trattato
e trattato:
Figura 2.21: Confronto fra i dati del campione as received e quello trattato, presi a 32◦ . In
questo caso i dati sono quelli del livello Ta 4f
Analisi del film
31
Figura 2.22: Confronto fra i dati del campione as received e quello trattato, presi a 32◦ . In
questo caso i dati sono quelli del livello O 1s
Confrontiamo ora fra loro i dati, normalizzando le aree, presi a 45◦ e a 32◦ dal
campione trattato.
Questa volta il confronto dei livello 1s dell’Ossigeno, ai due angoli, non presenta evidenti differenze. Questo porta a pensare che la specie chimica inserita in
questo livello, per rappresentare i subossidi, ha anche una componente superficiale
(probabilmente impurezze) che lo sputtering ha eliminato.
Per quanto riguarda i dati relativi al livello 4f del Tantalio, questi presentano
ancora differenze (punto 1 di Fig. 2.23). Questa è un’ulteriore osservazione che
porta a pensare ad una popolazione di specie chimiche funzione della profondità
di analisi anche dopo il bombardamento ionico.
Figura 2.23: Confronto dei dati presi a 45◦ e 32◦ sul libello Ta 4f . Si osserva una diversa
forma nel punto 1.
32
Analisi dei campioni
Figura 2.24: Confronto dei dati presi a 45◦ e 32◦ sul libello O 1s. Non si osserva nessuna
differenza
Osservando i dati relativi al livello Ta 4f, relativi alla misura a 45◦ , risulta evidente la necessità di usare più di tre specie chimiche per riprodurre l’andamento
sperimentale dei dati.
La migliore analisi è stata con cinque specie chimiche (corrispondenti a 10 gaussiane). Tre di queste sono quelle usate nell’analisi precedente. Alle 6 gaussiane,
rappresentanti queste specie, è stata imposta la stessa FWHM, al contrario delle
rimanti 4 gaussiane. Fra le tre famiglie chimiche sono state imposte le distanze
trovate nelle analisi precedenti (v. sezione 2.2.1).
In generale (per tutte e 10 le curve) ad ogni coppia di gaussiane, rappresentante
una specie chimica, sono stati imposti i valori caratterizzanti del livello 4f del tantalio: rapporto fra le aree S.O.= 0.75 (v. eq. 2.1) e split fra sotto-orbitale con j=7/2 e
con j=5/2 di 1.91 eV [8].
Questi i dati ottenuti dall’analisi:
Formula
Ta2 O5
Ta2 O5− x
Ta
Taa Ob
Tac Od
Center (eV)
26.400 ± 0.025
28.310 ± 0.025
25.062 ± 0.025
26.972 ± 0.025
21.772 ± 0.025
23.682 ± 0.025
23.630 ± 0.025
25.540 ± 0.025
22.138 ± 0.025
23.048 ± 0.025
Area
1382
1037
192
144
102
76
664
498
30
23
FWHM (eV)
1.416 ± 0.025
1.416 ± 0.025
1.416 ± 0.025
1.416 ± 0.025
1.416 ± 0.025
1.416 ± 0.025
2.142 ± 0.025
2.142 ± 0.025
0.794 ± 0.025
0.794 ± 0.025
Tabella 2.8: Valori dei parametri ottenuti analizzando i dati del livello 4f del Tantalio a 45◦
con chi-quadro di 1.96
Analisi del film
33
Figura 2.25: Analisi sui dati presi a 45◦ sul livello Ta 4f
Le prime tre famiglie, precedentemente inserite, sono note. Le rimanenti due
sono in una zona di B.E. legata ai subossidi, tipo Taa Ob e Tac Od .
Per l’analisi sui dati presi a 32◦ si impostano le stesse relazioni usate per l’analisi
a 45◦ . In più vengono impostate le relazioni trovate con questa nuova analisi a 45◦ ,
ossia le posizioni di Taa Ob e Tac Od rispetto alla posizione del pentossido di tantalio.
Questa l’analisi dei dati:
Formula
Ta2 O5
Ta2 O5− x
Ta
Taa Ob
Tac Od
Center (eV)
26.400 ± 0.025
28.310 ± 0.025
25.062 ± 0.025
26.972 ± 0.025
21.772 ± 0.025
23.682 ± 0.025
23.630 ± 0.025
25.540 ± 0.025
22.138 ± 0.025
23.048 ± 0.025
Area
1483
1113
214
160
100
75
561
421
20
15
FWHM (eV)
1.327 ± 0.025
1.327 ± 0.025
1.327 ± 0.025
1.327 ± 0.025
1.327 ± 0.025
1.327 ± 0.025
2.142 ± 0.025
2.142 ± 0.025
0.794 ± 0.025
0.794 ± 0.025
Tabella 2.9: Valori dei parametri ottenuti analizzando i dati del livello 4f del Tantalio a 45◦
con chi-quadro di 1.96
34
Analisi dei campioni
Figura 2.26: fit su campione sputterato a 32◦ su Ta4f
L’analisi sui dati presi a 32◦ porta informazioni quantitative fra specie chimiche
presenti nel campione (v. Tab. 2.9). Siamo interessati al confronto di queste con
quelle ottenute con l’analisi dati acquisita a 45◦ . Per farlo normalizziamo tutte le
aree rispetto a quella del pentossido di tantalio.
Formula
Ta2 O5− x
Ta
Taa Ob
Tac Od
Analisi a 45◦
13.9%
7.4%
48.0%
2.2%
Analisi a 32◦
14.4%
6.7%
37.8%
1.3%
Tabella 2.10: Confronto fra aree, normalizzate rispetto a quella del pentossido
Da questo confronto vediamo che la famiglia dei subossidi, al diminuire dell’angolo di misura, aumenta, comunque in modo non significativo. Questa specie però
non è l’unica componente che può contenere dei subossidi. Infatti se si confrontano
le somme delle aree, ai due diversi angoli, relative al subossido e alle ultime due
famiglie (Taa Ob e Tac Od ), troviamo, come già osservato in Fig. 2.23, che vi è una diminuzione di queste specie all’aumentare della profondità di analisi. La presenza
della famiglia metallica rimane invece costante, questa caratteristica era già stata
osservata nell’analisi sul campione non sputterato (v. sezione 2.2.1).
Si è dunque portati a pensare che le specie chimiche legate ai subossidi siano
presenti negli strati più superficiali del campione, mentre la componente metallica
sia presente in maniera più uniforme nel campione.
Osservando, invece, i dati relativi al livello O 1s (ad un angolo di 45◦ ), risulta
evidente la necessità di utilizzare più di una specie chimica per riprodurre l’andamento sperimentale dei dati. La migliore analisi è stata fatta utilizzando tre specie
chimiche. Ogni specie chimica è rappresentata da una gaussiana. Fra loro si è imposta la stessa FWHM, in quanto i dati sono affetti tutti dalla stessa indeterminazione
(provengono dallo stesso livello, i raggi X con cui è stato eccitato il campione hanno sempre la stessa indeterminazione e durante la misura l’indeterminazione dello
strumento è stata tenuta costante) (vedi eq. 1.5).
Questi i risultati ottenuti:
Analisi del film
35
Ta2 O5
H2 O
Ta2 O5− x
Center (eV)
530.661 ± 0.025
533.061 ± 0.025
532.116 ± 0.025
Area
2002
36
142
FWHM (eV)
1.311 ± 0.025
1.311 ± 0.025
1.311 ± 0.025
Tabella 2.11: Valori dei parametri ottenuti analizzando i dati a 45◦ con chi-quadro di 1.25
Figura 2.27: Analisi sui dati del livello O 1s a 45◦
Dopo lo sputtering si registra una diminuzione di acqua sul campione, in accordo con l’ipotesi precedente che identificava questo materiale nelle regioni più
superficiali.
Vediamo ora cosa si ottiene analizzando i dati presi a 32◦ :
Ta2 O5
H2 O
Ta2 O5− x
Center (eV)
530.706 ± 0.025
533.106 ± 0.025
532.161 ± 0.025
Area
2189
22
105
FWHM (eV)
1.352 ± 0.025
1.352 ± 0.025
1.352 ± 0.025
Tabella 2.12: Valori dei parametri ottenuti analizzando i dati a 32◦ con chi-quadro di 1.26
36
Analisi dei campioni
Figura 2.28: Analisi sui dati del livello O 1s a 32◦
Anche in questa analisi l’acqua presenta una diminuzione di area rispetto a
quelli trovati sul campione as received.
Confrontiamo le aree dei subossidi e dell’acqua normalizzandole rispetto a
quella del pentossido di tantalio:
Formula
H2 O
Ta2 O5− x
Analisi a 45◦
1.8%
7.1%
Analisi a 32◦
1.0%
4.8%
Tabella 2.13: Confronto fra aree, normalizzate rispetto a quella del pentossido di tantalio
Entrambe le specie chimiche presentano una diminuzione di acqua e di
subossido all’aumentare della profondità di analisi.
Mentre il primo comportamento era stato già osservato, analizzando il campione as received, il secondo andamento risulta essere opposto a quello osservato
precedentemente. Una spiegazione possibile è che questa componente presentava,
sul campione analizzato as received, specie chimiche superficiali legate a impurezze,
dovute ad esposizione all’ambiente, che lo sputtering ha eliminato.
2.2.3
Polvere di pentossido
L’ultima analisi è stata fatta su polvere di pentossido di tantalio puro al 99.99%.
Il survey eseguito su questo campione indica presenza di Carbonio, Ossigeno e
Tantalio. Visto che questa analisi è fatta per confrontare i dati ottenuti sul film con
le caratteristiche del Ta2 O5 bulk, l’HRES viene eseguito solamente sulle seguenti
regioni di B.E. (escludendo il segnale del Carbonio):
a) Ta4f: [15 ÷ 35] eV;
b) O1s: [517 ÷ 537] eV.
La scala delle energie è calibrata sul livello 4f7/2 del Tantalio (v. Tab. 2.1), non
avendo analizzato il livello 1s del Carbonio.
Questi i dati raccolti:
Analisi del film
37
Figura 2.29: Dati relativi al livello 4f del Tantalio
Figura 2.30: Dati relativi al livello 1s dell’Ossigeno
Il valore Ta/O vale circa 0.41 per la polvere. Questo si avvicina molto al valore
che deve avere il materiale (0.4), ma è dovuto all’alto rapporto superficie volume
che permette all’acqua di essere fortemente presente nel campione, abbassando così
il deficit di Ossigeno.
I dati così ottenuti vengono confrontati con quelli precedentemente ottenuti
analizzando il campione a 32◦ , prima e dopo il bombardamento ionico.
Come si vede in Fig. 2.31 i dati della misura sul campione as received non presentano differenze con quelli presi sulla polvere, se non nella zona di B.E. compresa
fra 26.4 e 28.4 eV. Per quanto riguarda il confronto fra le misure prese sul campione
trattato e la polvere (v. Fig. 2.31) osserviamo le stesse differenze viste confrontando
i dati del campione dopo lo sputtering con quelli dell’as received.
I dati relativi al livello 1s dell’Ossigeno, presi sulla polvere, presentano una larghezza decisamente maggiore di quelli relativi al film. Questa evidenza è dovuta al
rapporto superficie volume, che nel caso della polvere è maggiore rispetto a quello
del film.
38
Analisi dei campioni
Figura 2.31: Confronto dei dati ottenuti sul film e con quelli del bulk, riguardanti il livello
4f del Tantalio
Figura 2.32: Confronto dei dati ottenuti sul film e con quelli del bulk, riguardanti il livello
1s dell’Ossigeno
Per analizzare i dati del livello Ta 4f si sono inserite le tre specie chimiche usate
nell’analisi sui dati presi dal campione as received.
Questi i risultati dell’analisi:
Ta2 O5
Ta2 O5− x
Ta
Center (eV)
26.400 ± 0.025
28.310 ± 0.025
25.062 ± 0.025
26.972 ± 0.025
21.772 ± 0.025
23.682 ± 0.025
Area
1346
1010
23
17
42
31
FWHM (eV)
0.99 ± 0.025
0.99 ± 0.025
0.99 ± 0.025
0.99 ± 0.025
0.99 ± 0.025
0.99 ± 0.025
Tabella 2.14: Risultati dell’analisi dati relativi alla polvere di tantala sul livello 4f del
Tantalio, con chi-quadro di 3.08
Analisi del film
39
Figura 2.33: Analisi dati sul livello Ta 4f
Segue il confronto delle aree, normalizzate rispetto a quella del pentossido, fra
film e polvere:
Formula
Ta
Ta2 O5− x
Taa Ob
Tac Od
as received 32◦
3.6%
1.6%
-
Trattato 32◦
6.7%
14.4%
37.8%
1.3%
polvere 32◦
3.1
1.7%
-
Tabella 2.15: Confronto fra aree normalizzate rispetto a quella del pentossido di tantalio
Dal confronto fra le aree trovate, analizzando i dati fino a qui raccolti, si può
vedere come i dati relativi al film as received a 32◦ , sono simili a quelli della polvere. Questa evidenza porta a pensare che le specie chimiche presenti nei materiali
analizzati non dipendono dal tipo di tecnica usata per costruirli.
Per analizzare i dati del livello O 1s si sono inserite le tre specie chimiche usate
nell’analisi sui dati presi dal campione as received.
Questi i risultati dell’analisi:
Ta2 O5
H2 O
Ta2 O5− x
Center (eV)
530.566 ± 0.025
532.966 ± 0.025
532.021 ± 0.025
Area
1489
208
134
FWHM (eV)
1.331 ± 0.025
1.331 ± 0.025
1.331 ± 0.025
Tabella 2.16: Risultati dell’analisi dati relativi alla polvere di tantala sul livello 1s
dell’Ossigeno, con chi-quadro di 1.44
40
Analisi dei campioni
Figura 2.34: Analisi dati sul livello O 1s
Questo il confronto delle aree, normalizzate rispetto a quella del pentossido, fra
film e polvere:
Formula
H2 O
Ta2 O5− x
as received 32◦
3.1%
12.3%
Trattato 32◦
1.0%
4.8%
polvere 32◦
14.0%
9.0%
Tabella 2.17: Confronto fra aree, normalizzate rispetto a quella del pentossido di tantalio
Da questo confronto fra le aree, sulle specie relative all’ossigeno, si vede come
l’umidità presente nella polvere è molto maggiore di quella sul film. La specie
chimica subossido è presente anche nella polvere in quantità non trascurabile.
Conclusioni
Lo scopo di questo lavoro di tesi è dare un contributo all’identificazione delle cause
delle dissipazioni meccaniche nei coating dielettrici degli specchi, attraverso la caratterizzazione chimica dei film di pentossido di tantalio, mediante spettroscopia
XPS.
Sono state effettuate misure XPS di un film di Ta2 O5 di spessore 200 nm
(ATFilm) a due angoli di take-off, prima e dopo un processo di bombardamento
ionico.
La prima differenza evidenziata dall’analisi riguarda il rapporto stechiometrico
Ta/O. Questo valore dovrebbe essere uguale a 0.4; quello trovato analizzando i dati
raccolti sul campione as received vale circa 0.47 (per θ = 45◦ ) e 0.45 (per θ = 32◦ ).
Questo indica che il nostro materiale ha una carenza di Ossigeno rispetto ad un
campione puro di Ta2 O5 . Il deficit di Ossigeno aumenta ulteriormente una volta
eseguito il bombardamento ionico sul campione; si passa a un valore Ta/O=0.53
(per entrambi gli angoli di analisi).
Questa anomalia del rapporto stechiometrico è spiegata dall’analisi del livello 4f del Tantalio che indica una presenza nel materiale di un legame metallico.
Questa caratteristica, già presente nel campione as received, viene confermata dopo il bombardamento ionico, che aumenta l’intensità di questo segnale. Inoltre, ad
entrambi gli angoli di take-off, la presenza del legame metallico appare costante.
Questo dato porta a pensare che questa sia una componente di bulk.
L’analisi XPS evidenzia anche la presenza di legami chimici intermedi nel Ta
che si attribuisce a subossidi del tipo Ta2 O5− x . L’analisi del campione as received indica che i subossidi hanno una bassa concentrazione, che mostra forte dipendenza
dall’angolo di analisi (v. Tab. 2.4). Anche questa componente è accentuata dopo il
bombardamento ionico.
Per confrontare i risultati ottenuti sul film con le caratteristiche del Ta2 O5 bulk,
si è analizzato un campione di polvere di pentossido di Tantalio, pura al 99.99%
(Aldrich).
Dall’analisi di questi dati si trovano gli stessi legami chimici osservati sul film.
Ciò suggerisce che la composizione chimica del film osservata non dipende dalla
tecnica di deposizione ma è una caratteristica del materiale.
L’analisi sul livello O 1s del pentossido di tantalio ha mostrato la presenza di tre
legami chimici. Due di questi sono stati identificati come Ta2 O5 e H2 O. Il restante
legame, in analogia con i risultati dell’analisi del livello 4f del Tantalio, si attribuisce
alla presenza di subossidi del tipo Ta2 O5− x .
In conclusione, la presenza di un legame metallico e di subossidi suggerisce che
le cause di dissipazione meccanica nel film di Ta2 O5 possano essere associate a queste impurezze. Per verificare questa ipotesi è necessario realizzare un’analisi più
complessa. Per esempio, per cercare di eliminare metallo e subossidi si può pensare
di scaldare il campione in un’atmosfera ricca di ossigeno e di effettuare analisi chi-
42
Conclusioni
miche e misure di dissipazione meccanica per vedere se dopo questo trattamento
queste componenti sono eliminate e le dissipazioni meccaniche diminuite.
Bibliografia
[1] R. A. Hulse and J. H. Taylor. The Astrophysical Journal, vol. 195 51, (1975).
[2] Virgo. http://www.virgo.infn.it/.
[3] LIGO - Laser Interferometer
http://www.ligo.caltech.edu/.
Gravitational
Wave
Observatory.
[4] Herbert B. Callen and Theodore A. Welton. Physical Review, vol. 83(1), 34,
(1951).
[5] S. D. Penn, P. H. Sneddon, H. Armandula, J. C. Betzwieser, G. Cagnoli,
J. Camp, D. R. M. Crooks, M. M. Fejer, A. M. Gretarsson, and G. M. Harry.
Class. Quant. Grav, vol. 20, 2917, (2003).
[6] John Wolstenholme John F. Watts. An introduction to surface analysis by XPS
and AES. WILEY, (2003).
[7] D.A. Shirley. Phys. Rev. B, vol. 5, 4709, (1971).
[8] M. Prato E. Cesarini A. Chincarini G. Cagnoli M. Canepa F. Vetrano and
G. Gemme. Proc. 8th Amaldi Conference on Gravitational Waves, New York,
(2009)
[9]
NIST
X-ray
Photoelectron
http://srdata.nist.gov/xps/
Spectroscopy
Database,
[10] E. Atanassova, D. Spassov. Appleied Surface Science, vol. 135, 71, (1998)
[11] fityk, http://www.unipress.waw.pl/fityk/.