CancerStat Umbria
Anno III No. 3-4
Marzo-Aprile2012
Registro Tumori
Umbro di Popolazione
ISSN 2039-814X
Registro Nominativo
delle Cause di Morte
Registro Regionale
dei Mesoteliomi
Direttore:
Francesco La Rosa
I tumori delle alte vie
aero-digestive
Coordinatore:
Fabrizio Stracci
Antonio Frenguelli, Giampiero Ricci,
Maria Cristina Cristi
Dipartimento di
Specialità MedicoChirurgiche e Sanità
pubblica.
Sezione di Sanità
Pubblica.
Università degli Studi
di Perugia.
Nicola Buonora, Antonella Monsignori
Fabrizio Stracci, Fortunato Bianconi,
Valerio Brunori, Francesco La Rosa
INDICE:
Parte I
Regione dell’Umbria.
Direzione regionale
Salute, coesione sociale
e società della
conoscenza
Introduzione e materiali e metodi
pag.
97
Epidemiologia e fattori di rischio
pag.
98
Bibliografia
pag. 105
Parte II
Anatomia patologica e management clinico
pag. 106
Bibliografia
pag. 124
CANCERSTAT UMBRIA, ANNO III NO. 3
CANCERSTAT UMBRIA, ANNO III NO. 3
CancerStat Umbria
Registro Tumori
Umbro di Popolazione
Registro Nominativo
delle Cause di Morte
Registro Regionale
dei Mesoteliomi
Direttore:
Anno III No. 3-4, Marzo-Aprile 2012
ISSN 2039-814X
Codice CINECA-ANCE E205269
Pubblicato da:
Registro Tumori Umbro di Popolazione
Francesco La Rosa
Coordinatore:
Fabrizio Stracci
Collaboratori:
Anna Maria Petrinelli
Daniela Costarelli
Fortunato Bianconi
Valerio Brunori
Daniela D’Alò
Silvia Leite
Maria Saba Petrucci
Francesco Spano
Dipartimento di Specialità Medico-Chirurgiche e Sanità
Pubblica. Sezione di Sanità Pubblica.
Università degli Studi di Perugia.
Via del Giochetto
06100 Perugia
Tel.: +39.075.585.7329 - +39.075.585.7366
Fax: +39.075.585.7317
Email: [email protected]
URL: www.rtup.unipg.it
Segreteria:
Luisa Bisello
Regione dell’Umbria.
Direzione regionale
Salute, coesione sociale
e società della
conoscenza
Emilio Duca
Paola Casucci
Marcello Catanelli
Mariadonata Giaimo
CANCERSTAT UMBRIA, ANNO III NO. 3
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
I tumori delle alte vie aero-digestive
Antonio Frenguelli1, Giampiero Ricci1, Maria Cristina
Cristi1, Nicola Buonora2, Antonella Monsignori2, Fabrizio
Stracci3, Fortunato Bianconi3, Valerio Brunori3, Francesco
La Rosa3
1
2
3
Clinica Otorinolaringoiatrica, Azienda Ospedaliera di Perugia
Scuola di Specializzazione in Igiene e Medicina preventiva,
Università di Perugia
Registro Tumori Umbro di Popolazione, Dipartimento di Specialità
medico-chirurgiche e Sanità pubblica, Università di Perugia
Parte I
Nicola Buonora, Antonella Monsignori
Fabrizio Stracci, Fortunato Bianconi, Valerio Brunori, Francesco
La Rosa
Introduzione
Materiali e Metodi
Tra le Vie Aero-Digestive Superiori (VADS) si
includono le seguenti sedi anatomiche: cavità
orale (C01-06), faringe (ipofaringe, orofaringe e
rinofaringe) (C09-14), cavità nasali e seni
paranasali (C30-C31) e laringe (C32)[1].
Nell’ambito dei tumori maligni delle vie aerodigestive superiori il tipo istologico più
frequentemente riscontrato è il carcinoma
epidermoidale, che prende origine dall’epitelio
superficiale delle mucose e che, da solo,
costituisce l’80-90% circa di tutti i tumori maligni
(il 70% dei tumori del distretto cervico-cefalico).
Si tratta di tumori maligni che rivestono un
particolare significato, in quanto coinvolgono
funzioni essenziali della vita, quali la respirazione,
la deglutizione, la fonazione, gli aspetti relazionali
e la qualità di vita. Le problematiche relative ai
pazienti con tumori epiteliali delle VADS
richiedono la collaborazione interdisciplinare di
numerosi
specialisti:
otorinolaringoiatri,
odontostomatologici, oncologi, radiologi e
radioterapisti, patologi, anestesisti ed altri ancora.
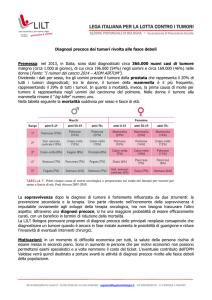
In questo lavoro vengono illustrati i tassi
d’incidenza e di mortalità per tumori maligni
delle vie aero-digestive superiori nella regione
Umbria, i trend temporali degli stessi indicatori
per il periodo 1994-2009 ed il confronto con i
trend italiani 1998-2005[2-3].
I dati relativi al numero di nuovi casi sono quelli
del database del Registro Tumori Umbro di
Popolazione (RTUP), quelli relativi ai deceduti
del Registro Nominativo delle Cause di Morte
(ReNCaM) dell’Umbria.
I tumori sono stati codificati secondo la decima
classificazione internazionale delle malattie (ICD
X)[1].
I trend temporali sono stati calcolati sui tassi
standardizzati per sesso ed età, con la
popolazione europea con il metodo della
“jointpoint regression”. Questa analisi temporale
mette in evidenza i cambiamenti statisticamente
significativi dei trend e quantifica la variazione
media annuale dei tassi (annual percent change =
APC)[4].
Nelle tabelle l’asterisco (*) accanto al valore
dell’APC indica la significatività (P≤0.05)
dell’incremento o del decremento calcolato.
97
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
EPIDEMIOLOGIA
I tumori maligni delle prime vie aero-digestive
superiori rappresentano per frequenza il settimo
tumore nella popolazione mondiale.
Ogni anno si registrano più di mezzo milione di
nuovi casi nel mondo.
Si stima che intorno al 2020, l’aumento della vita
media della popolazione porterà al raddoppio di
questa patologia fino a più di 1 milione di nuovi
casi e a più di 500.000 morti ogni anno[5].
I tumori delle vie aero-digestive superiori sono i
più comuni tra gli uomini al di sotto dei 55 anni.
Nei paesi dell’Europa Occidentale tali neoplasie,
come per gli altri tumori delle vie respiratorie,
hanno fatto registrare il loro picco d’incidenza e
mortalità tra il 1950 ed 1980, soprattutto nei
maschi. A partire dalla fine degli anni ottanta la
mortalità ha iniziato progressivamente a
declinare.
Nell’Europa centrale e soprattutto dell’Est,
continua invece a registrarsi un aumento del
tasso d’incidenza e di mortalità che rispecchia il
diffondersi dell’epidemia dei tumori correlata
all’abitudine al fumo[6].
In Italia, tra il 2002 e il 2005, sono stati registrati,
in media, 29.2 casi all’anno ogni 100.000 uomini,
e 6.9 casi ogni 100.000 donne, rappresentando,
rispettivamente, il 4.2% e l’1.3% di tutti i tumori
diagnosticati.
Come per gli altri tumori delle vie respiratorie, gli
ultimi 20 anni sono stati caratterizzati da un
ormai
consolidato
trend
decrescente
dell’incidenza e della mortalità nel sesso maschile.
Incidenza e mortalità si riducono in modo
statisticamente significativo con un APC
rispettivamente di 3.2 e 3.4 (figura 1). Tra le
donne prosegue il leggero e non significativo
trend crescente dell’incidenza (APC +1.4),
mentre le variazioni della mortalità non sono più
apprezzabili dai primi anni ’90 (APC +1.4)
(figura 2).
Nei trend recenti non si notano importanti
differenze per età, tuttavia i VADS
rappresentano nei maschi, per frequenza, il 5°
tumore nella fascia di età 50-69 anni.
In particolare, l’incidenza e la mortalità sono più
alte nei maschi al nord che al centro e al sud.
Anche tra le femmine si osserva un gradiente
decrescente nord-sud[3].
Figura 1. Trend temporali dei tassi standardizzati di
incidenza e mortalità per 100.000 abitanti nel sesso
maschile in Italia. Periodo 1998-2005.
Figura 2. Trend temporali dei tassi standardizzati di
incidenza e mortalità per 100.000 abitanti nel sesso
femminile in Italia. Periodo 1998-2005.
Andamenti temporali dell’incidenza e della
mortalità in Umbria.
Il trend umbro non si discosta dal quadro
epidemiologico italiano. A partire dal 1994, anno
d’inizio dell’attività del Registro Tumori Umbro
di Popolazione, al 2009 l’incidenza e la mortalità
per i tumori maligni delle alte vie aero-digestive
superiori presentano un andamento decrescente,
statisticamente significativo nei maschi, mentre
nelle femmine il trend decresce lievemente.
98
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Incidenza e mortalità nei maschi si riducono, in
maniera significativa, dal 1994 al 2009 con APC
rispettivamente -3.2* e -2.3* (figura 3). Nelle
femmine il trend è decrescente, ma non in
maniera significativa. Incidenza e mortalità
diminuiscono con APC rispettivamente -0.3 e 0.6 (figura 4).
I tassi standardizzati d’incidenza e mortalità sono
molto più elevati nella ASL 1 sia per la
popolazione maschile che per la popolazione
femminile ed il valore riscontrato si discosta in
maniera apprezzabile dal valore complessivo
della regione (Tabelle 1-6). Tuttavia il trend
d’incidenza è sfavorevole nella fascia d’età 35-59
(APC 1.2), confermando in tal modo
l’andamento degli altri registri nazionali (figura
5).
Tabella 1. Numero annuo medio di nuovi casi, tassi
grezzi e standardizzati di incidenza e mortalità in
Umbria. Periodi 1978-1982, 1994-1998, 2004-2008;
Maschi.
30
25
20
15
Anni di
riferimento
10
1978-1982
1994-1998
2004-2008
N.
casi
128
124
102
Anni di
riferimento
1978-1982
1994-1998
2004-2008
N.
morti
69
57
53
5
20
08
20
06
20
04
20
02
20
00
19
98
19
96
19
94
0
INCIDENCE 1994-2009 APC (95%CI) -3.2* (-4.2;-2.0)
MORTALITY 1994-2009 APC (95%CI) -2.3* (-4.1;-0.4)
Figura 3. Trend umbro di incidenza e mortalità nei
maschi (triangolo: tasso osservato d’incidenza; linea
continua: trend stimato d’incidenza; rombo: tasso
osservato di mortalità; linea continua: trend stimato
di mortalità).
Mortalità
Tasso
Tasso
grezzo
standard.
17.4
15.1
14.4
10.3
12.6
7.9
Tabella 2. Numero annuo medio di nuovi casi, tassi
grezzi e standardizzati di incidenza e mortalità in
Umbria. Periodi 1978-1982, 1994-1998, 2004-2008;
Femmine.
5
4
Anni di
riferimento
1978-1982
1994-1998
2004-2008
3
2
1
N.
casi
15
24
21
0
Incidenza femmine
Tasso
Tasso
grezzo
standard.
3.5
2.9
5.7
3.8
4.7
2.6
20
08
20
06
20
04
20
02
20
00
19
98
Mortalità
19
96
19
94
Incidenza Maschi
Tasso
Tasso
grezzo
standard.
32.3
28.5
31.5
22.9
24.3
17.4
INCIDENCE 1994-2009 APC (95%CI) -0.3 (-2.6;2.0)
MORTALITY 1994-2009 APC (95% CI) -0.6 (-3.9;2.8)
Figura 4. Trend umbro di incidenza e mortalità
nelle femmine (triangolo: tasso osservato
d’incidenza; linea continua: trend stimato
d’incidenza; rombo: tasso osservato di mortalità;
linea continua: trend stimato di mortalità).
99
Anni di
riferimento
N.
morti
Tasso
grezzo
Tasso
standard.
1978-1982
1994-1998
2004-2008
7
11
11
1.6
2.5
2.4
1.3
1.3
1.3
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Tabella 3. Numero annuo medio di nuovi casi, tassi
grezzi e standardizzati di incidenza e mortalità per
ASL in Umbria. Maschi. Periodo 1994-1998.
19941998
INCIDENZA
Tabella 5. Numero annuo medio di nuovi casi, tassi
grezzi e standardizzati di incidenza e mortalità per
ASL in Umbria. Maschi. Periodo 2004-2008
20042008
MORTALITA'
M
N.
casi
Tasso Tasso N.
Tasso
grezzo stand. morti grezzo
ASL1
28
46.3
35.6
70
ASL2
48
31.1
22.6
ASL3
22
29.4
ASL4
26
Umbria
124
MORTALITA'
Tasso
stand.
M
N.
casi
23.2
16.5
ASL1
22
34.9
26.2
65
20.3
13.9
111
14.3
10.9
ASL2
38
21.9
15.8
95
10.9
7.1
21.3
51
14.0
9.1
ASL3
16
20.6
15.3
39
10.2
6.1
24.5
17.4
53
10.1
6.7
ASL4
26
23.8
16.2
65
12.2
6.8
31.5
22.9
285
14.4
10.3
Umbria
102
24.3
17.4
264
12.6
7.9
Tabella 4. Numero annuo medio di nuovi casi, tassi
grezzi e standardizzati di incidenza e mortalità per
ASL in Umbria. Femmine. Periodo 1994-1998
19941998
INCIDENZA
INCIDENZA
Tasso
stand.
Tabella 6. Numero annuo medio di nuovi casi, tassi
grezzi e standardizzati di incidenza e mortalità per
ASL in Umbria. Femmine. Periodo 2004-2008
20042008
MORTALITA'
Tasso
Tasso Tasso N.
grezzo stand. morti grezzo
Tasso Tasso N.
Tasso
grezzo stand. morti grezzo
INCIDENZA
MORTALITA'
Tasso
stand.
F
N.
casi
2.5
1.4
ASL1
4
5.4
3.5
9
2.7
1.3
27
3.3
1.9
ASL2
7
3.9
2.2
18
1.9
1.1
2.7
10
2.7
1.1
ASL3
3
3.9
2.3
9
2.2
1.2
5.9
3.6
11
2.1
0.8
ASL4
7
6.2
3.8
18
3.1
1.7
5.7
3.8
56
2.5
1.3
Umbria
21
4.7
2.6
54
2.4
1.3
F
N.
casi
ASL1
5
7.2
5.0
8
ASL2
9
5.5
3.7
ASL3
4
4.7
ASL4
6
Umbria
24
100
Tasso Tasso N.
Tasso
grezzo stand. morti grezzo
Tasso
stand.
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
25
APC: -3.36*
20
15
APC: 1.2
10
5
20
08
20
06
20
04
20
02
20
00
19
98
19
96
0
19
94
Tasso d'incidenza 35-59
30
Figura 5. Trend umbro di incidenza nei maschi
(triangolo: tasso osservato d’incidenza; linea continua:
trend stimato d’incidenza) e nelle femmine (rombo:
tasso osservato di incidenza; linea continua: trend
stimato di incidenza) per la classe d’età 35-59.
Figura 7. Distribuzione regionale dei tumori
delle VADS nelle femmine. SIR 2004-2008.
FATTORI DI RISCHIO
L’analisi geografica della distribuzione regionale
evidenzia l’ormai ben nota presenza di aree a
rischio più elevato (figure 6-7), riconfermando
l’elevata incidenza, di tali patologie, per quanto
riguarda il sesso maschile, in una vasta area che
insiste nel territorio della ASL1.
I principali fattori di rischio sono: il fumo,
l’alcool, la cattiva igiene orale, gli squilibri
nutrizionali,
l’esposizione
a
cancerogeni
occupazionali e alle radiazioni.
Il tabacco
L’utilizzo di tabacco è associato all’incremento
del rischio di carcinoma delle vie aero-digestive
superiori. Dalla combustione del tabacco
vengono prodotte nitrosamine cancerogene e
radicali liberi che provocano l’alterazione degli
enzimi antiossidanti protettivi e favoriscono il
danno cellulare. Essi agiscono sia come sostanze
iniziatrici che come fattori promuoventi il
processo di cancerogenesi. Inoltre il fumo di
tabacco esercita un effetto cancerogeno anche
per l’effetto termico della sigaretta, infatti il
contatto con il calore della combustione provoca
fenomeni irritativi che spesso sono all’origine di
modificazioni cellulari. I fumatori abituali hanno
un rischio incrementato di 5-25 volte di contrarre
una neoplasia cervicofacciale. L’aumento del
rischio è proporzionale all’età di inizio, alla durata
dell’esposizione e alla quantità di sigarette fumate
Figura 6. Distribuzione regionale dei tumori
delle VADS nei maschi. SIR 2004-2008
101
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
al giorno[7]. Anche il fumo passivo incrementa il
rischio: ad esempio per una esposizione al fumo
passivo >15 anni, il rischio incrementa di 1,6
volte. Il rischio declina sostanzialmente circa
dieci anni dopo la cessazione del fumo[8]. Nella
popolazione italiana gli uomini che smettono di
fumare prima dei 50 anni riducono di più del
50% il rischio attribuibile al fumo di tumore
cervicofacciale, se smettono prima dei 30 anni il
rischio si riduce del 90%, tornando vicino ai
livelli di un soggetto non esposto al fumo. Un
maggiore quantitativo quotidiano di fumo per un
breve periodo è meno dannoso di un
quantitativo minore per un lungo tempo.
L’associazione è forte oltre che con il consumo
di sigarette, con l’uso di pipa e sigari nonché,
nelle aree dell’Asia dove questa abitudine è
diffusa, con la masticazione delle foglie di Betel.
utilizzato come stimolante per sopprimere la
fame, ridurre lo stress e aumentare i sensi. La
maggior parte delle famiglie lo coltiva nell’orto[9].
L’alcool
L’alcool è un fattore di rischio indipendente per
l’insorgenza
dei
tumori
cervicofacciali
(soprattutto per oro-ipofaringe e laringe). Esso
esercita un’azione tossica diretta: l’etanolo, infatti,
ossidato ad acetaldeide diviene un potente agente
cancerogeno. Esso inoltre aumenta l’attività dei
pro-cancerogeni presenti nel fumo grazie
all’induzione enzimatica epatica e il fumo da
parte sua incrementa la formazione di
acetaldeide. L’associazione di alcool e di fumo
aumenta di 7 volte il rischio di sviluppare una
neoplasia del cavo orale e della laringe. Il rischio
di tumore è proporzionale alla quantità di etanolo
assunta e non dipende dal tipo di bevanda
alcoolica (vino, birra o super alcoolici)
consumato in prevalenza. Alcool e tabacco
hanno azione sinergica rispetto al rischio di
malattia cosicché la presenza di individui che
consumano quantità eccessive di bevande
alcooliche e fumano, configura l’esistenza di
gruppi a rischio elevato. Aumenti moderati di
rischio sono stati dimostrati anche in forti
bevitori non fumatori[10].
Il Betel
L’elevato tasso di cancro del cavo orale in Asia
meridionale è dovuto alla masticazione di
preparati a base di Betel (Piper betle). Il Betel nei
paesi asiatici è noto per avere proprietà
medicinali, stimolanti e anti-settiche. Infatti,
viene utilizzato per trattare il dolore nella cefalea,
nell’artrite, per le odontalgie, come antibiotico,
per aiutare la digestione, per la stipsi, per aiutare
l’allattamento. Si dice abbia proprietà
afrodisiache. Il Betel è la foglia di una vite
appartenente alla famiglia delle Piperaceae nota
per le sue proprietà medicinali. E’ diffusa
soprattutto in Bangladesh, India e Sri Lanka. Le
foglie sono masticate insieme in un pacchetto
avvolto con il dado di areca (che dall’associazione
viene impropriamente chiamato “Betel nut”,
noce di betel). Il Betel e l’areca svolgono un
ruolo importante nella cultura indiana,
soprattutto tra gli indù. Molte cerimonie
tradizionali che regolano la vita degli indù
utilizzano questi componenti, ad esempio,
quando si donano soldi, questi per rispetto
vengono riposti all’interno di un involucro di
Betel e areca. Il “Betel nut” gioca anche un ruolo
importante nella cultura vietnamita. Un
proverbio dice che “il Betel inizia la
conversazione” e fa riferimento alla pratica delle
persone di masticare il Betel in occasioni formali
o “per rompere il ghiaccio” in situazioni
scomode. In Papua Nuova Guinea il Betel viene
Altri fattori
Molte
indagini
epidemiologiche
hanno
dimostrato che una carente igiene orale,
un’alimentazione poco equilibrata e un basso
indice di massa corporea (BMI) contribuiscono
sostanzialmente ad aumentare la probabilità di
insorgenza di un tumore maligno dell’orofaringe.
I fenomeni di displasia e l’insorgenza del
carcinoma sono associati alla scarsa igiene orale,
infatti, sono molto meno frequenti in pazienti
sottoposti a regolari cure odontoiatriche. Le
parodontiti e i fenomeni di riassorbimento osseo
alveolare sono associati all’incremento di
sviluppo dei tumori della lingua di circa 5 volte.
Le placche polimicrobiche possono avere
un’azione mutagena sull’epitelio di rivestimento e
la presenza di batteri nel cavo orale sembra
favorire la sintesi di sostanze cancerogene, come
ad esempio l’acetaldeide (dalla trasformazione
dell’alcool).
102
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
E’ ormai nota l’associazione tra alcuni virus e i
tumori delle vie aero-digestive superiori. Il virus
di Epstein-Barr è associato al carcinoma
nasofaringeo (WHO III; UNPC). Tale forma è
caratterizzata dalla presenza di cellule tumorali
indifferenziate con un prominente infiltrato
linfocitico. Il carcinoma nasofaringeo di tipo
WHO III è particolarmente comune in alcune
aree della Cina e del sud-est asiatico con picchi
d’incidenza di 20-30 casi per 100.000 abitanti[11].
Una recente review sulla prevalenza delle
infezioni HPV nei tumori del distretto cervicofacciale ha rilevato che il 25.9% di tutti questi
tumori sono positivi per HPV DNA, con una
prevalenza di HPV più alta nel carcinoma
orofaringeo (35.6%) rispetto a quello della cavità
orale (23.5%) o al cancro della laringe (24%).
HPV 16 è il sottotipo più frequentemente
riscontrato. Esso era presente nel 90% dei tumori
orofarigei, nel 69% dei laringei e nel 68% dei
tumori della cavità orale[12].
carcinomi squamocellulari e sarcomi. Il periodo
di latenza medio tra l’irradiazione e lo sviluppo
della neoplasia è 30 anni. Una caratteristica
peculiare dei carcinomi della testa e del collo è il
riscontro sincrono (5-10% dei casi) o metacrono
(10-20% dei casi entro 5 anni) di un altro
carcinoma a carico della stessa regione o
dell’esofago o del polmone. L’alta frequenza di
tumori multipli si spiega con la persistente
influenza dei fattori di rischio coinvolti
(soprattutto del fumo) a livello di ampie aree
degli epiteli delle alte vie digerenti e del tratto
respiratorio che hanno già subito le prime
trasformazioni preneoplastiche (cosiddetta field
cancerization)[13-15].
Discussione
Dai dati sopra esposti, risulta di tutta evidenza
che la diminuzione dell’APC dell’incidenza e
conseguentemente della mortalità nel sesso
maschile è espressione dell’effetto positivo legato
ad una minore esposizione ai principali fattori di
rischio. Nel sesso femminile, l’aumento
dell’incidenza
è
attribuibile
soprattutto
all’incremento dell’abitudine al fumo, che
testimonia un’inversione di tendenza delle
abitudini nei due sessi. Nella regione Umbria, le
variazioni di esposizione ai fattori di rischio si
traducono in variazioni degli indicatori
epidemiologici con la conferma di aree ben note
a rischio più elevato. Il controllo dei fattori di
rischio, per quanto difficile, si tradurrebbe in un
forte impatto sulla salute della popolazione.
Nonostante ci siano molti dati che mostrano
frequenti ritardi nella diagnosi dei tumori maligni
delle alte vie aero-digestive e un’influenza
sfavorevole di questo fenomeno sull’esito del
trattamento, non è ancora chiaro se un
programma di screening sia fattibile ed
efficace[16]. Screening per i tumori maligni del
cavo orale sono stati condotti in molte centinaia
di migliaia di individui in alcuni paesi poveri
(India e Cuba) ed in migliaia di soggetti ad alto
rischio (forti fumatori e bevitori) in paesi
sviluppati (Stati Uniti, Gran Bretagna ed Italia).
E’ stato possibile in tal modo identificare alte
percentuali (intorno al 10%) di soggetti con
lesioni sospette, per lo più leucoplachie. Le
L’epitelio delle alte vie digerenti e respiratorie è
tra i più vulnerabili ai deficit di varie sostanze
anti-ossidanti. Questa circostanza è molto
frequente nei forti bevitori per i quali circa un
quarto delle calorie quotidiane deriva dall’alcool.
Mentre è ben dimostrato l’effetto favorevole di
un consumo abitualmente elevato (>3-4 porzioni
al giorno) di verdura e frutta, soprattutto di
colore giallo/arancio, contenente anti-ossidanti
(carotene, carotenoidi, flavonoidi, vitamine A, C,
E). L’elevato consumo di frutta e verdura ha un
effetto protettivo anche su soggetti fumatori e
bevitori; questo effetto viene perso al consumo
degli stessi alimenti non freschi ma conservati. Il
consumo di carne e uova sembrerebbe
aumentare il rischio di tumore delle vie aerodigestive superiori. Un altro fattore di rischio è
un basso BMI, che è verosimilmente collegato a
una
bassa
classe
socio-economica
di
appartenenza. Altri fattori di rischio sono
l’esposizione occupazionale a percloroetilene,
utilizzato nel lavaggio a secco (correlato
soprattutto al carcinoma della laringe) e altre
sostanze a rischio quali l’asbesto, i pesticidi, le
fibre di vetro lavorate a mano, gli idrocarburi
aromatici policiclici, le polveri tessili, l’etanolo, la
formaldeide, la naftalina, l’acido solforico. Anche
un’irradiazione precedente correla con lo
sviluppo di tumori delle ghiandole salivari,
103
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
maggiori difficoltà sono state incontrate nel
follow-up di questi soggetti e nello stabilire un
intervallo realistico tra gli esami di screening,
tenuto conto che la fase preinvasiva sembra
essere abbastanza rapida (intorno a un anno).
Ovviamente, l’organizzazione di screening
sarebbe sostanzialmente favorita dalla scoperta di
un test capace di identificare la fase preclinica
prima della semplice ispezione visiva del cavo
orale. Inoltre, a causa della frequente
multicentricità delle lesioni preneoplastiche, il
controllo chirurgico della malattia sarebbe più
difficile per i tumori maligni del cavo orale e
faringe che per quelli del collo dell’utero e
mammella[17-18]. Per quanto concerne il carcinoma
della laringe, le esperienze di screening sono
minori che per cavo orale e faringe ma minore è
anche il fenomeno del ritardo diagnostico.
Infatti, alcuni sintomi, quali la disfonia, portano
più precocemente all’osservazione i tumori
maligni della laringe di quelli del cavo orale.
104
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
to cancers of the upper aerodigestive tract in
northern Italy. Tumori 2010; 96(1): 1-10.
BIBLIOGRAFIA
1. WHO. International statistical classification of
diseases and related health problems, tenth
revision (ICD-10). Geneva, 1992.
2. La Rosa F and RTUP Working Group.
L’incidenza del cancro in Umbria 2006-2008.
Regione dell'Umbria eds, Perugia (Italy); 2009.
3. AIRTum Working Group. I trend storici di
incidenza e mortalità 1986-2005. AIRTum
Longterm incidence and mortality AIRTum
cancer trend, 1986-2005 in Trend dei tumori
negli anni 2000. Epidemiol Prev 2009; 33: (45) suppl 1.
4. Kim HJ, Fay MP, Feuer EJ, Midthune DN.
Permutation tests for joinpoint regression
with application to cancer rates. Stat. Med
2000; 19, 335. Correction: 2001, 20, 655.
5. Marron M, Boffetta P, Zhang ZF, Zaridze D
et al. Cessation of alcohol drinking, tobacco
smoking and the reversal of head and neck
cancer risk. Int J Epidemiol 2010; 39(1): 18296. Epub 2009 Oct 5.
6. La Vecchia C, Lucchini F, Negri E. Trends in
oral cancer mortality in Europe. Oral
Oncology 2004; 40: 433-439.
7. Pelucchi C, Gallus S, Garavello W, Bosetti C,
La Vecchia C. Alcohol and tobacco use, and
cancer risk for upper aerodigestive tract and
liver. Eur J Cancer Prev 2008; 17(4):340-4.
8. Gandini S, Botteri E, Iodice S, Boniol M,
Lowenfels AB, Maisonneuve P, Boyle P.
Tobacco smoking and cancer: A meta-analysis
Int J Cancer 2008;122(1):155-64.
9. Lee CH, Lee KW, Fang FM et al. The use of
tobacco-free betel-quid in conjunction with
alcohol/tobacco impacts early-onset age and
carcinoma distribution for upper aerodigestive
tract cancer. J Oral Pathol Med 2011; 8. doi:
10.1111/j.1600-0714.2011.01022.x.
11. Young LS, Murray PG. Epstein-Barr virus
and oncogenesis: from latent genes to
tumours. Oncogene 2003; 22(33):5108-21.
12. Giuliano AR, Anic G, Nyitray AG.
Epidemiology and pathology of HPV disease
in males. Gynecol Oncol 2010; 117(2
Suppl):S15-9. Epub 2010 Feb 6.
13. Park SL, Lee YC, Marron M, Agudo A et al.
The association between change in body mass
index and upper aerodigestive tract cancers in
the ARCAGE project: multicenter casecontrol study.Int J Cancer 2011; 128(6):144961. doi: 10.1002/ijc.25468.
14. Giuliano AR, Anic G, Nyitray AG.
Epidemiology and pathology of HPV disease
in males.
Gynecol Oncol 2010; 117(2
Suppl):S15-9. Epub 2010 Feb 6.
15. Franceschi S, Muñoz N, Bosch XF, Snijders
PJ, Walboomers JM. Human papillomavirus
and cancers of the upper aerodigestive tract: a
review of epidemiological and experimental
evidence. Cancer Epidemiol Biomarkers Prev
1996; 5(7):567-75.
16. Franceschi S, Barzan L, Talamini R.
Screening for cancer of the head and neck: if
not now, when? Oral. Oncol 1997; 33: 313316.
17. Shuman AG, Entezami P, Chernin AS,
Wallace NE, Taylor JM, Hogikyan ND.
Demographics and efficacy of head and neck
cancer screening. Otolaryngol Head Neck
Surg 2010; 143(3):353-60.
18. Gourin CG, Kaboli KC, Blume EJ, Nance
MA, Koch WM. Characteristics of
participants in a free oral, head and neck
cancer screening program. Laryngoscope
2009; 119(4):679-82.
10. Canova C, Richiardi L, Merletti F. Alcohol,
tobacco and genetic susceptibility in relation
105
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Parte II
Antonio Frenguelli, Giampiero Ricci, Maria Cristina Cristi
ANATOMIA PATOLOGICA E MANAGEMENT CLINICO
infiltranti invece è necessario ricorrere alla terapia
radiante o all’exeresi chirurgica.
- Carcinomi anaplastici, papillomi maligni,
papillomi invertiti, adenocarcinomi, epiteliomi a
cellule cilindriche.
Più rari sono i tumori di derivazione connettivale,
cartilaginea ed ossea: sarcomi, angiosarcomi,
condrosarcomi,
osteosarcomi
e
emangiopericitomi.
Sono invece rarissimi i meningiomi, i neuroestesio-epiteliomi
(derivati
dalla
mucosa
olfattiva), i linfomi e i melanomi.
TUMORI MALIGNI DEL NASO E
DEI SENI PARANASALI
I tumori maligni del naso e dei seni paranasali
costituiscono l'1% circa di tutte le neoplasie
maligne.
La maggior parte delle neoplasie derivano
dall'epitelio
di
rivestimento.
Si
tratta
prevalentemente di:
Carcinomi
ad
epitelio
pavimentoso
(corneificante o non corneificante), che insorge
spesso su cicatrici da ustione e su manifestazioni
del Lupus eritematoso volgare, ha per lo più,
nello stadio iniziale, forma di verruca sessile o
peduncolata, che lentamente si può ulcerare.
I margini di questa lesione ulcerativa che prende
il nome di cancroide, formano di solito un
cercine netto e sono in parte incassati nella cute,
in parte rilevati, mentre il fondo è costituito da
granulazioni grigiastre e sanguinanti. A questo
stadio la neoplasia ha rapido accrescimento e
metastatizza ai linfonodi sottomandibolari e
parotidei[1-2].
- Carcinoma ad epitelio pavimentoso non
cornificante o basalioma, che insorge su
manifestazioni di cheratosi senile, evolve
lentamente senza metastatizzare. La forma
vegetante non presenta caratteri obiettivi di
particolare rilievo, mentre quella piana cicatriziale
può presentare attorno ad una zona centrale di
atrofia cicatriziale, una estensione periferica a
mezzo di bottoni vegetanti, spesso ulcerati
superficialmente. Il tumore si estende lentamente
ma può distruggere in profondità ossa e
cartilagini. Nella forma terebrante, la neoplasia ha
netta e precoce tendenza ad invadere i piani
profondi, mentre nell’ulcus rodens, si ha di solito
una unica formazione ulcerata ad andamento
lento e serpiginoso. Nei casi iniziali e superficiali
è indicata la diatermocoagulazione, nelle forme
SINTOMATOLOGIA
I sintomi sono in rapporto con la zona di
insorgenza della neoplasia.
La sintomatologia più comune è sovrapponibile a
quella di una sinusite purulenta cronica con
sintomi legati al seno interessato, le epistassi
sono tuttavia più frequenti e più abbondanti. Nei
melanomi l'epistassi può costituire il primo
sintomo lamentato dal paziente. In altri casi
l'interessamento diretto di tronchi nervosi da
parte del tumore può dare luogo a fenomeni
nevralgici o ad ipoestesia cutanea (perdita del
tatto) nel territorio di distribuzione dei nervi
interessati dalla neoplasia.
L'ostruzione nasale unilaterale e progressiva,
quasi sempre accompagnata da epistassi e da
rinopiorrea (fuoriuscita dal naso di materiale
mucoso e purulento), costituisce il sintomo più
importante della fase iniziale delle neoplasie
insorte nelle cavità nasali[1].
Ogni neoplasia maligna nasale o sinusale ha
tendenza, nel suo ulteriore decorso, ad invadere
le strutture anatomiche circostanti e la
sintomatologia quindi dipenderà dalle varie
modalità di propagazione.
Potranno esistere sintomi a carico dell'orbita
(edema delle parti molli con spostamento del
bulbo oculare, paralisi oculare, disturbi visivi), a
106
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
l'oggetto di un impegno terapeutico notevole sia
per la complessità della sede anatomica su cui
insorgono ed i rapporti di contiguità con
importanti strutture limitrofe, sia per la diagnosi
spesso tardiva e conseguentemente lo stadio
avanzato in cui giungono alla prima
osservazione[1]. È stato documentato un eccesso
di rischio nei lavoratori del legno e del cuoio (con
latenze anche molto lunghe), nell'industria tessile,
metallurgica, metalmeccanica, chimica.
I progressi compiuti nella diagnosi e cura sono
stati:
a) l'endoscopia naso-sinusale con possibilità di
anticipare la diagnosi, di definire meglio
l'estensione della malattia e di monitorare durante
il follow-up la sede trattata e l'efficacia delle
terapie;
b) l'imaging (TC, RM), con gli stessi vantaggi
dell'endoscopia applicati allo studio dei piani
profondi anziché delle superfici mucose;
c) la resezione cranio-facciale che ha cambiato la
prognosi dei tumori ad interessamento etmoidale;
d) l'associazione sistematica di chirurgia e
radioterapia in tutti i casi non iniziali;
e) il contributo della chemioterapia seno frontale
seno sfenoidale etmoide seno mascellare orbita
etmoide fossa nasale.
carico del cranio (cefalea e paralisi multiple dei
nervi cranici) e a carico del massiccio facciale e
della arcata dentaria superiore (nevralgia della II
branca del trigemino, deformità estetica della
regione canina o nella regione degli zigomi,
progressiva caduta dei denti).
DIAGNOSI
La diagnosi delle neoplasie maligne delle fosse
nasali e dei seni paranasali si formula con la visita
otorinolaringoiatrica
(esame
obiettivo)
completata
da
tecniche
endoscopiche
(endoscopia
nasale
a
fibre
ottiche,
videoendoscopia) e confermata da accertamenti
radiologici (TAC).
Il tipo istologico verrà determinato mediante un
prelievo bioptico con esame istologico.
Le metastasi a distanza (ossee, polmonari,
epatiche) verranno diagnosticate mediante
radiografia
del
torace,
ecotomografia
dell'addome, scintigrafia ossea total body,
scintigrafia a positroni (PET).
Le metastasi linfonodali loco regionali (molto più
frequenti di quelle a distanza) saranno svelate
dall'esame ecotomografico del collo eseguito con
sonde ad elevata frequenza e con tecniche
ecocolordoppler.
TERAPIA
La terapia è essenzialmente chirurgica e si avvale
di interventi endoscopici (eseguiti dall'interno
delle fosse nasali) e di interventi con accesso
esterno (a cielo aperto). Frequentemente le due
tecniche, per avere un assoluto controllo della
radicalità di asportazione, si abbinano[3].
In base al caso clinico sarà programmata anche
l'asportazione delle stazioni linfonodali satelliti
alla zona di insorgenza della neoplasia
(svuotamento linfonodale). Dopo l'intervento
potranno essere eseguiti cicli di radioterapia e di
chemioterapia variamente abbinati a giudizio
dello specialista in oncologia.
RICHIAMO ANATOMOPATOLOGICO
La complessità delle strutture anatomiche che
concorrono alla formazione dei seni paranasali
contribuisce all'ampio spettro di istotipi che si
possono osservare in queste sedi.
Il carcinoma squamocellulare è anche in questa
sede la neoplasia più frequente, seguita da
adenocarcinomi con vari aspetti differenziativi,
carcinomi cosiddetti transizionali, carcinomi ad
insorgenza da ghiandole salivari minori, tumori
derivanti dal neuroepitelio olfattorio con aspetti
differenziativi
che
possono
andare
dall'estesioneuroblastoma
al
carcinoma
neuroendocrino a piccole cellule; ancor più rari
melanomi, sarcomi, linfomi.
TUMORI MALIGNI DELLE
CAVITÀ PARANASALI
SINTOMI ED EVOLUZIONE
In relazione al fatto che la sede di insorgenza o
sviluppo sia nelle fosse nasali o all'interno di un
seno, i sintomi dei tumori naso-paranasali sono:
ostruzione nasale, dolore locale, epistassi,
secrezione nasale, tumefazione della guancia o
gengivale-palatina. Qualsiasi sintomo anche
I tumori maligni naso-paranasali sono rari: meno
dell'1% di tutti i tumori e circa il 3% dei tumori
delle vie aero-digestive superiori. Rappresentano
107
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
apparentemente banale (ostruzione nasale
monolaterale, secrezione nasale corpuscolata,
modico dolore locale), non altrimenti spiegabile e
non risolto dopo 3 settimane, richiede un esame
specialistico. Dovrebbe essere raccomandato
l'uso sistematico dell'endoscopio nasale in ogni
visita specialistica ORL ed il ricorso alla TC/ RM
per qualsiasi sintomo o quadro clinico non
migliorato dopo 15 giorni di trattamento medico
e non chiarito dall'endoscopia nasosinusale.
Particolare sospetto devono destare disturbi
unilaterali, in pazienti di età superiore ai 35 anni
con
anamnesi
negativa
per
patologie
infiammatorie
rinosinusali
ricorrenti[4].
L'evoluzione della malattia è locale: le metastasi
laterocervicali alla prima osservazione (<10%) o
a distanza, sono poco frequenti anche con tumori
molto avanzati.
comprenda orbita-nervo ottico, in particolare per
valutare la funzione dell'occhio controlaterale),
anestesista.
CLASSIFICAZIONE
DEL
TUMORE
PRIMITIVO
Esiste solo per il seno mascellare e l'etmoide. La
classificazione di N ed il raggruppamento in stadi
sono uguali alle altre sedi ORL.
Seno mascellare (TNM, UICC 1997)
T1
T2
DIAGNOSI
Talora si giunge alla diagnosi di neoplasia in
corso di approccio chirurgico per patologia
presunta diversa (sinusopatia cronica, poliposi).
In tale evenienza è opportuno sospendere la
procedura, attendere l'istologia definitiva, stadiare
correttamente la malattia, programmare la
terapia.
La stadiazione comprende: anamnesi ed esame
fisico, attribuzione di un punteggio di
performance status, esame fibroendoscopico
naso-paranasale, esame ORL completo, TC/
RM, (con particolare attenzione alla distinzione
tra opacizzazione dei seni paranasali da raccolta
di secrezioni e da massa tumorale, e per questi
dettagli la risoluzione della RM è migliore)
ecografia (o TC/ RM) delle aree linfatiche
cervicali, esami generali ematochimici, ECG,
radiografia del torace, eventuali altri esami
indicati dalla situazione clinica per il giudizio di
operabilità (spirometria, ecocardiogramma). La
biopsia può quasi sempre essere eseguita per via
transnasale, eventualmente con l'aiuto di fibre
ottiche per chirurgia endoscopica; per evitare
alterazioni dovute ad edema, sanguinamento,
tamponamento, andrebbe sempre programmata
dopo la TC/ RM.
Consulti: radioterapista, oncologo medico,
odontostomatologo (se è prevista radioterapia
che comprenda il cavo orale non edentulo o
riabilitazione protesica), oculista (se prevista
exenteratio-orbitae o radioterapia con campo che
T3
T4
Tumore limitato alla mucosa
antrale, senza interessamento
osseo
Tumore con erosione o
distribuzione ossea, esclusa la
parete posteriore del seno, ma
compreso il palato duro o/e il
meato medio
Tumore invadente una delle
seguenti formazioni: parete
posteriore del seno, pavimento
o parete mediale dell'orbita,
tessuti sottocutanei e cute della
guancia
Tumore invadente il contenuto
orbitario oltre le sue pareti,
compreso l'apice o/e una delle
seguenti strutture: lamina
cribrosa, seno sferoidale,
rinofaringe, seno frontale, base
cranica
Etmoide
T1
T2
T3
T4
108
Tumore limitato all’etmoide,
con o senza erosione ossea
Tumore esteso alla fossa nasale
Tumore esteso alla parte
anteriore dell'orbita o/e al seno
ascellare
Tumore con estensione
intracranica, nell'orbita
compreso l'apice, con
interessamento dello sfenoide
o/e del seno frontale o/e della
cute del naso
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
mascellare, le pareti posteriore e laterale del seno
mascellare devono essere indenni.
Maxillectomia totale (subtotale se la resezione
dell'emipalato duro è incompleta, eventualmente
allargata
alla
fossa
infratemporalepterigomascellare, all'orbita, ai tegumenti facciali):
indicata per invasione delle pareti del seno
mascellare e per estrinsecazioni oltre a queste.
Etmoidectomia monolaterale subtotale per via esterna:
indicata per neoplasie limitate all'etmoide
anteriore.
Resezione cranio-facciale: per neoplasie etmoidali
anche se ancora totalmente extracraniche, ma
molto contigue al pavimento della fossa cranica
anteriore, per consentire una escissione con
margine di sicurezza ed in tutte le neoplasie
etmoidali con estensione alla rinobase fino alla
dura madre.
Ricostruzione
L'impiego di lembi è raccomandato per
rimpiazzare i difetti da ampie escissioni cutanee,
per creare sostegno all'orbita o al cervello, per
separare la cavità cranica dalle vie aeree. La
riabilitazione palatina può avvenire con protesi
mobili (richiedono pulizia, consentono una facile
ispezione della cavità chirurgica) o con lembi
(non richiedono pulizia non consentono l'esame
diretto del letto operatorio).
TERAPIA
Chirurgia
Gran parte della letteratura concorda
nell'attribuire i risultati migliori in termini di
sopravvivenza
all'associazione
chirurgiaradioterapia, anche se non vi è unanimità di
indicazioni su quando (prima o dopo
l'intervento) effettuare la radioterapia. La
chirurgia da sola può forse essere considerata in
casi molto selezionati di neoplasie iniziali[1].
L'indicazione chirurgica non è uguale per tutti gli
istotipi: in casi localmente molto avanzati di
tumori ad alto grado di malignità quali il
carcinoma indifferenziato, andrebbe sempre
valutata la possibilità di un trattamento
alternativo ad una chirurgia estesamente
demolitiva. Per il carcinoma adenoide cistico
invece, con elevata tendenza alla recidiva locale
ed alle metastasi a distanza, ma con un'evolutività
particolarmente lenta, una resezione chirurgica
con finalità palliative potrà essere presa in
considerazione per migliorare la qualità di vita
anche in presenza di metastasi. Vengono anche
qui perseguiti i principi generali della chirurgia
oncologica: resezione in monoblocco con
margini adeguati e ben definiti in tessuto sano. Vi
sono però estensioni tumorali ed aree
anatomiche che costringono a qualche
compromesso, richiedendo una rimozione a parti
staccate e dei margini di tessuto sano esigui, in
particolare a livello di seno cavernoso, clivus,
orbita. Da qui l'importanza di una integrazione
terapeutica postoperatoria.
Il trattamento chirurgico profilattico delle aree
linfatiche cervicali non trova indicazioni.
RADIOTERAPIA
Il trattamento radiante come singola modalità è
riservato alle forme inoperabili, o per estensione
locale o per condizioni generali del paziente. Di
regola, pertanto, si adotta in associazione alla
chirurgia. Non vi è una preferenza tra eseguire il
trattamento radiante prima o dopo la chirurgia. Il
volume da trattare con RT deve comprendere la
sede clinicamente evidente di malattia e le aree in
cui è sospettata la presenza di malattia subclinica.
Il trattamento radiante postoperatorio è erogato a
2Gy/frazione per 5 frazioni alla settimana. La
dose totale è di 50Gy/25frazioni/5 settimane sul
letto chirurgico; ulteriori 10 Gy/1 settimana sono
erogati sulla sede del tumore primitivo, se i
margini chirurgici sono negativi. Se i margini
chirurgici sono positivi per residuo neoplastico è
previsto un sovradosaggio di 16- 20 Gy/8- 10
frazioni.
La dose totale nei pazienti inoperabili varia da 50
a 70 Gy in 25-35 frazioni.
Modalità chirurgiche
Il tipo di resezione chirurgica varia in relazione
alla sede di origine ed alle strutture coinvolte.
Drenaggio: esperienze giapponesi degli ultimi
decenni sono state confermate da uno studio
prospettico dell'Università di Rotterdam, in cui la
chirurgia consiste nel solo debulking della massa
tumorale attraverso un’antrotomia e successiva
ripetuta rimozione del tessuto necrotico,
associata a chemioterapia locale ed a
radioterapia[3].
Maxillectomia parziale, con possibili estensioni
inferiore e mediale: indicata per neoplasie della
parete mediale del seno mascellare o per
neoplasie dell'infrastruttura. La tuberosità
109
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Non è indicato trattamento radiante profilattico
del collo nei casi N0. È prevista la radioterapia
post-operatoria sul collo nei casi con
interessamento linfonodale[1].
Tossicità: la dose totale erogabile è limitata dalla
tolleranza di organi a rischio. È possibile un
danno retinico per dosi superiori a 44 Gy in 22
frazioni, un deficit dei nervi ottici per dosi
superiori a 54Gy-27 frazioni e un'encefalopatia
post attinica per dosi superiori a 60Gy in 30
frazioni. Con tecniche adeguate di trattamento
radiante, quando applicabili, il manifestarsi di
trisma, insufficienza ipofisaria, ipoacusia, danno
al chiasma ottico sono attesi in una percentuale
inferiore al 10%.
reperti clinici, la Rx del torace e gli esami generali
ematochimici, incluso la funzionalità tiroidea se
la parte bassa del collo è stata irradiata,
annualmente. Altri eventuali esami potranno
essere eseguiti in relazione al quadro clinico.
RISULTATI
Il controllo locale è di circa il 50%, a 5 anni la
sopravvivenza libera da malattia è del 20-25%. La
sopravvivenza globale media è attorno al 35%, e
quella per la specifica malattia attorno al 45%,
con ampie variazioni in relazione all'istotipo (dal
70% per l'adenocarcinoma ben differenziato al
15% per il melanoma e il carcinoma
indifferenziato), alla classe di T (dall’80% ed oltre
per i T1, T2 a meno del 20% per i T4), alla classe
di N (meno del 20% per gli N2, N3), alla
fattibilità di un trattamento con intento radicale.
La radioterapia da sola, impiegata usualmente in
neoplasie avanzate non resecabili per estensione
od in pazienti non operabili per condizioni
generali, comporta sopravvivenze a 5 anni
inferiori al 20%.
STRATEGIA TERAPEUTICA
T1: Chirurgia + eventuale ERT se
adenocarcinoma poco differenziato, carcinoma
indifferenziato, melanoma se margini di
resezione infiltrati o “stretti” (<5 mm);
•
T2,3,4: Chirurgia + ERT (nota: il ruolo
della chemioterapia loco-regionale o sistemica
associata alla radioterapia con l'intento di evitare
la demolizione chirurgica ed il ruolo della
chemioterapia
neoadiuvante
prima
del
trattamento definitivo per migliorare i risultati in
termini di sopravvivenza, sono oggetto di
studio);
•
T inoperabili: ERT (l'associazione con
chemioterapia è limitata a studi clinici)
•
N0: nessuna terapia;
•
N>0: svuotamento laterocervicale dei
livelli da 1 a 5 + ERT.
•
FATTORI PROGNOSTICI
Fattori prognostici individuabili nelle casistiche
chirurgiche sono l'età, l'istotipo (con una
prognosi peggiore per melanoma e carcinoma
indifferenziato), la sede di origine (più favorevole
per le fosse nasali rispetto ai seni paranasali per la
diagnosi più precoce), le dimensioni e
conseguentemente l'estensione a strutture
anatomiche limitrofe, la diffusione perineurale, le
metastasi linfonodali cervicali ed a distanza, la
possibilità di un trattamento adeguato (chirurgia
radicale con margini microscopicamente liberi e
radioterapia adiuvante a dosi >55Gy)[5]. Le
recidive locali sono la causa più frequente di
morte: il trattamento delle recidive dà risultati
sconfortanti. Per migliorare la sopravvivenza
sono necessari diagnosi precoce, stadiazione
iniziale accurata, trattamento “aggressivo”.
FOLLOW- UP
Le visite di controllo sono programmate
individualmente in base alla tossicità dei
trattamenti, rischio di recidiva, sorveglianza per
diagnosi precoce di secondi tumori, comorbidità.
In linea generale la frequenza dei controlli viene
effettuata ogni 1-3 mesi nel primo anno dopo il
trattamento, ogni 2-4 mesi nel secondo e terzo
anno, ogni 4-6 mesi nel quarto e quinto e negli
anni successivi. Il controllo consiste in un esame
ORL completo.
La valutazione preferibilmente va attuata
congiuntamente dall'otorinolaringoiatra e dal
radioterapista (e dall'oncologo medico se il
paziente ha ricevuto chemioterapia). La TC e/o
RM sarà eseguita annualmente o in relazione a
110
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Ecografia: permette di visualizzare le parti
interne del corpo. Utilizza onde sonore ad alta
frequenza (ultrasuoni) che rimbalzano contro gli
organi o le parti che si vogliono indagare
producendo un'eco, che viene tradotta in
immagini a due dimensioni. E’ un esame
assolutamente indolore e privo di effetti
collaterali.
Risonanza magnetica (RM): utilizza onde
magnetiche che rivelano immagini di organi
interni del corpo.
Tomografia a emissione di positroni (PET):
un computer elabora i segnali che arrivano da
una macchina, la quale rileva la distribuzione di
uno zucchero radioattivo (glucosio) iniettavo in
vena nel paziente. Questa tecnica permette di
evidenziare chiaramente le cellule tumorali,
poiché esse reagiscono allo zucchero più delle
altre cellule.
Dosaggio di EBV DNA nel sangue: nei casi in
cui il tumore è legato alla presenza del virus di
Epstein-Barr (EBV) può essere utile dosare i
livelli di questo virus nel sangue, sia per la
prognosi che per valutarne l’andamento dopo la
terapia.
TUMORI MALIGNI NASO- E
RINO-FARINGEI
Il cancro del rinofaringe ha origine più
comunemente dalle cellule squamose che
rivestono l’orofaringe .
A seconda del tessuto e del tipo di cellule colpite
si distinguono tipi diversi di cancro:
Tipo I: carcinoma squamocellulare
cheratinizzante;
Tipo II: carcinoma non cheratinizzante;
Tipo III: carcinoma spinocellulare basaloide.
SEGNI E SINTOMI
Per il tumore del rinofaringe difficilmente i
sintomi compaiono nella fase iniziale della
malattia. Potenziali segni di malattia sono la
difficoltà di respirazione, di eloquio e di udito,
sanguinamento, ostruzione nasale, adenopatie
cervicali.
Negli stadi più avanzati compaiono i seguenti
sintomi: cefalea, interessamento dei nervi del
cranio, noduli cervicali di grosse dimensioni su
entrambi i lati, tumefazione al collo o alla gola,
faringodinia, difficoltà di respirazione o di
eloquio, epistassi, difficoltà di udito, dolore o
ronzio all’orecchio, cefalea.
•
DIAGNOSI
Rinofaringoendoscopia:
permette
di
visualizzare l’interno di naso e gola grazie a un
tubicino rigido o flessibile che termina con un
dispositivo
illuminante
(rinofaringoscopio)
inserito dal naso. E’ un esame fastidioso e per
questo è consigliabile eseguirlo in anestesia locale
somministrata tramite uno spray. Se si ha il
sospetto di tumore si può procedere ad una
biopsia (prelevamento di cellule da analizzare al
microscopio).
Panendoscopia: con un tubicino flessibile
(endoscopio) permette di visualizzare tutte le vie
aeree superiori, dal naso fino a trachea ed
esofago. L’esame richiede anestesia generale.
Ago aspirato: una siringa fornita di un ago
sottile viene usata per prelevare cellule o fluidi
dal tessuto che si vuole analizzare.
Tomografia computerizzata (Tc): tecnica
radiografica che fotografa parti interne del corpo
con l’aiuto di un computer.
•
•
•
111
esame obiettivo: il medico palperà il collo
per accertare l’eventuale presenza di
linfonodi ingrossati ed esaminerà la gola
inserendo nel cavo orale uno specchietto dal
manico lungo per visualizzare eventuali
anomalie;
rinoscopia: è una procedura che consente di
visualizzare le strutture interne del naso
attraverso un rinoscopio (un tubo flessibile
dotato di un apparato illuminante) allo scopo
di rilevare eventuali anomalie. Il medico
potrà procedere al prelievo di campioni di
tessuti da analizzare al microscopio (biopsia);
esame neurologico: esame in cui il paziente
è sottoposto ad una serie di semplici quesiti e
test per verificare le capacità cerebrali, la
funzionalità del sistema nervoso e del
midollo spinale. L’esame consente di valutare
la salute mentale del paziente, la
coordinazione motoria, la deambulazione
nonché la condizione dei muscoli, dei sensi e
dei riflessi;
radiografia della testa e del torace: è
un’indagine radiologica del cranio e degli
organi e delle ossa che si trovano nel torace. I
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
•
•
raggi X consistono in un fascio di energia in
grado di attraversare il corpo e fissarsi su una
pellicola
fotografica,
visualizzando
l’immagine
delle
strutture
interne
dell’organismo;
RMN (risonanza magnetica nucleare): è
una particolare tecnica radiografica che
utilizza i campi magnetici per trasmettere a
un computer i dati, che poi questo rielabora
per dare immagini dettagliate delle strutture
interne del corpo;
Stadio 0 (carcinoma in situ)
Nello stadio 0, le cellule neoplastiche sono
presenti unicamente nella mucosa del rinofaringe.
Lo stadio 0 si definisce anche carcinoma in situ.
Stadio I
Nello stadio I, il tumore è circoscritto al
rinofaringe.
Stadio II
Lo stadio II si divide convenzionalmente in
stadio IIA e stadio IIB:
• stadio IIA: il tumore si è diffuso all’orofaringe
(la porzione mediana della gola che
comprende il palato molle, la base della
lingua e le tonsille), e/o alla cavità nasale;
• stadio IIB: il tumore è presente nel rinofaringe
e ha invaso i linfonodi (i linfonodi sono
piccole strutture del sistema linfatico, a forma
di fagiolo, presenti in tutto il corpo, che
producono e conservano le cellule che
combattono le infezioni) omolaterali, ossia
localizzati nella stessa parte del collo dove è
presente il tumore, oppure ha invaso l’area
circostante il rinofaringe e potrebbe aver
compromesso anche i linfonodi omolaterali. I
linfonodi compromessi hanno un diametro
pari o inferiore a 6 cm.
TAC (tomografia computerizzata o
tomografia assiale computerizzata):
consiste in una serie di immagini dettagliate
delle strutture interne dell’organismo, prese
da angoli diversi Le immagini sono rilevate
da
un
computer
collegato
a
un’apparecchiatura per raggi X. In alcuni casi,
si usa un mezzo di contrasto (che vi sarà
iniettato in vena oppure dato da assumere
oralmente) per migliorare la visualizzazione
degli organi o dei tessuti;
• esami di laboratorio: si eseguono allo scopo
di valutare i campioni di tessuto, sangue,
urina o di altre sostanze presenti
nell’organismo e aiutano a formulare la
diagnosi, a pianificare il trattamento e a
monitorarne gli effetti e a seguire il decorso
della malattia nel tempo;
• biopsia: consiste nel prelievo di un campione
di cellule o di tessuto che sarà esaminato al
microscopio per accertare l’eventuale
presenza di cellule tumorali.
Alcuni fattori influiscono sulla scelta del
trattamento e sulla prognosi, ossia sulla
probabilità di guarigione [3].
La probabilità di guarigione (prognosi) e il
trattamento dipende dai seguenti fattori:
• dallo stadio del tumore (se è circoscritto o
esteso a tutto il rinofaringe, se si è diffuso ad
altri organi);
• dal tipo di tumore:
• dalle dimensioni del tumore;
• dall’età e dalle condizioni generali di salute.
Stadio III
Nello stadio III il tumore:
• è presente nel rinofaringe e ha invaso i
linfonodi su entrambi i lati del collo. Detti
linfonodi hanno un diametro pari o inferiore
a 6 cm; oppure
• ha invaso i tessuti molli (orofaringe e/o
cavità nasale) e i linfonodi su entrambi i lati
del collo, i quali hanno un diametro pari o
inferiore a 6 cm; oppure
• si è diffuso oltre i tessuti molli invadendo le
aree circostanti la faringe e i linfonodi su
entrambi i lati del collo, i quali hanno un
diametro pari o inferiore a 6 cm; oppure
• ha invaso le strutture ossee limitrofe o i seni
mascellari e potrebbe aver invaso i linfonodi
di uno o di entrambi i lati del collo. Detti
linfonodi hanno un diametro pari o inferiore
a 6 cm.
STADIAZIONE DELLA MALATTIA
Il cancro del rinofaringe si classifica secondo i
seguenti stadi:
112
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Stadio IV
Lo stadio IV si divide convenzionalmente in
stadio IVA, stadio IVB e stadio IVC:
• stadio IVA: il tumore si è diffuso oltre il
rinofaringe e potrebbe aver invaso i nervi
cranici, l’ipofaringe (la porzione inferiore
della gola), il cranio o la mascella e le aree
circostanti e/o l’osso che circonda l’occhio. Il
tumore potrebbe essersi diffuso anche ai
linfonodi di uno o di entrambi i lati del collo
e i linfonodi interessati hanno un diametro
pari o inferiore a 6 cm;
• stadio IVB: il tumore ha invaso i linfonodi
sovraclaveari (localizzati sopra la clavicola)
e/o i linfonodi interessati hanno un diametro
maggiore di 6 cm;
- stadio IVC: il tumore si è diffuso oltre i
linfonodi e ha invaso altri organi.
Radioterapia
La radioterapia consiste nell’applicazione di
radiazioni ad alta frequenza per distruggere le
cellule neoplastiche. Esistono due tipi di
radioterapia: radioterapia esterna: le radiazioni
possono essere erogate da una macchina esterna
all’organismo e orientate sulla zona interessata
dal tumore; oppure radioterapia interna o
intracavitaria: le radiazioni vengono erogate
internamente a partire da sostanze radioattive
(radioisotopi) impiantate tramite aghi, tubicini o
cateteri all’interno o a breve distanza dal tumore.
La modalità di attuazione della radioterapia
dipende dal tipo e dallo stadio del tumore da
trattare.
L’irradiazione esterna sulla tiroide o sull’ipofisi
può alterare il funzionamento della ghiandola
tiroidea. La funzionalità della tiroide sarà,
pertanto, controllata prima e dopo il trattamento.
Prima dell’inizio della radioterapia, è molto
importante sottoporsi a visita odontoiatrica per
risolvere eventuali problemi.
Cancro del rinofaringe recidivante.
Si definisce recidivante il tumore del rinofaringe
che si ripresenta dopo il trattamento. La recidiva
può svilupparsi nella stessa sede del tumore
primitivo oppure in un altro organo.
Chemioterapia
La chemioterapia è la modalità terapeutica che
distrugge le cellule neoplastiche o blocca la
divisione cellulare attraverso la somministrazione
di farmaci, che possono essere assunti per bocca
in forma di compresse, oppure iniettati per via
endovenosa o intramuscolare. In questi casi, la
chemioterapia si definisce trattamento sistemico,
perché il farmaco entra nella circolazione
sanguigna, si diffonde nell’organismo e in questo
modo può raggiungere e distruggere le cellule
neoplastiche che si sono diffuse a distanza.
Quando
il
farmaco chemioterapico
è
somministrato direttamente nella colonna
spinale, in una cavità organica, quale l’addome, o
in un organo, esso agisce principalmente sulle
cellule neoplastiche presenti in quella regione. La
modalità di attuazione della chemioterapia
dipende dal tipo e dallo stadio del tumore da
trattare.
OPZIONI TERAPEUTICHE
Esistono trattamenti diversi per i pazienti
portatori di cancro del rinofaringe.
Alcuni trattamenti sono standard (il trattamento
attualmente praticato), altri sono in fase di
sperimentazione nell’ambito di studi clinici.
Prima dell’inizio del trattamento, potreste
prendere in considerazione la possibilità di
partecipare a uno studio clinico[4]. Lo studio
clinico è una ricerca che ha come scopo quello di
migliorare i trattamenti attualmente applicati o di
ottenere informazioni su modi più efficaci di
trattamento dei pazienti oncologici. Se gli studi
clinici dimostrano che un nuovo trattamento è
migliore dei trattamenti attualmente impiegati
come trattamento “standard”, il nuovo
trattamento potrà diventare il trattamento
“standard”.
Idealmente, la scelta del trattamento oncologico
più adatto alle vostre esigenze è una decisione
che dovrebbe coinvolgere il paziente, i familiari e
il personale medico.
Chirurgia
La chirurgia consiste nell’asportazione del
tumore. Nel trattamento dei tumori del
rinofaringe, la chirurgia è utilizzata talvolta nel
caso in cui il tumore non risponda alla
radioterapia. Se i linfonodi sono compromessi, il
chirurgo potrebbe asportare i linfonodi e altri
Esistono tre opzioni terapeutiche standard, che
sono:
113
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
tessuti nella zona del collo. Sono attualmente in
corso alcuni studi clinici miranti a valutare
l’efficacia di nuove modalità terapeutiche.
•
TERAPIA BIOLOGICA
La terapia biologica mira a stimolare le difese
naturali dell’organismo per combattere il tumore
attraverso la somministrazione di sostanze
prodotte dall’organismo stesso oppure di origine
sintetica. La funzione di tali sostanze è quella di
stimolare, orientare o ripristinare il sistema
immunitario dell’organismo a difendersi dalla
malattia. La terapia biologica è detta anche
terapia con somministrazione di modificatori
della risposta biologica (BRM, acronimo per
Biological response modifier) o immunoterapia.
Radioterapia con fasci ad intensità modulata. La
radioterapia con fasci ad intensità modulata è una
radioterapia
tridimensionale
che
utilizza
immagini computerizzate per visualizzare la
dimensione e la forma del tumore.
•
radioterapia
seguita
dalla
dissezione
linfonodale per rimuovere i linfonodi del
collo che persistono o si riformano dopo
l’irradiazione;
chemioterapia per tumori che hanno
metastatizzato, ossia che si sono diffusi ad
altri organi.
TUMORI MALIGNI DEL CAVO
ORALE
Il cavo orale comprende i due terzi anteriori della
lingua, le gengive, la superficie interna delle
guance e delle labbra, la parte inferiore della
bocca sotto la lingua (il pavimento orale), la
parte superiore ossea della bocca (il palato duro)
e la zona oltre i denti del giudizio (il trigono
retro molare)[6].
LABBRO
TRATTAMENTO IN BASE ALLO
STADIO
La patologia oncologica del labbro di interesse
chirurgico è costituita dalle lesioni precancerose
con
displasia-carcinoma
in
situ,
macroscopicamente evidenti in forma di
leucoplachia, eritroplasia, eritroleucoplachia,dal
carcinoma basocellulare e dal carcinoma
squamoso.
Il carcinoma del labbro è una patologia
relativamente rara (circa il 2 per cento di tutti i
tumori del distretto cervico-cefalico), la cui
incidenza attualmente sembra manifestare una
tendenza alla diminuzione,grazie ad un maggior
controllo dei fattori di rischio (fumo, sole, traumi
dentari).
Colpisce prevalentemente il sesso maschile (circa
l’80 per cento dei casi) con maggior incidenza tra
i 50 e 70 anni, si sviluppa soprattutto in persone
dalla pelle chiara che trascorrono molto tempo al
sole (per esempio i muratori, gli agricoltori o i
pescatori) e colpisce preferibilmente il labbro
inferiore a livello del vermiglio.
I tumori del labbro inferiore prediligono il sesso
maschile e sono per lo più carcinomi squamosi,
l’insorgenza è subdola e lentamente evolutiva,
manifestandosi in circa il 10-30 per cento dei casi
come degenerazione carcinomatosa di una
lesione precancerosa asintomatica. L’incidenza di
Stadio I:
Il trattamento consiste generalmente nella
radioterapia con irradiazione del tumore e dei
linfonodi del collo.
Stadio II:
Le opzioni terapeutiche sono le seguenti:
-chemioterapia più radioterapia;
-radioterapia con irradiazione del tumore e dei
linfonodi del collo.
Stadio III
Le opzioni terapeutiche sono le seguenti:
-chemioterapia associata a radioterapia
-radioterapia con irradiazione del tumore e dei
linfonodi del collo
-radioterapia seguita da dissezione linfonodale
per rimuovere i linfonodi del collo che
persistono o si riformano dopo la terapia
radiante.
Stadio IV
Le opzioni terapeutiche sono le seguenti:
• chemioterapia associata a radioterapia;
• radioterapia con irradiazione del tumore e dei
linfonodi del collo;
114
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
metastasi linfonodali locoregionali è del 10-20
per cento, con comparsa tardiva e prevalente
localizzazione
sottomandibolare
e
sottomentoniera. I tumori del labbro superiore
colpiscono in eguale misura i due sessi , sono per
lo più carcinomi basocellulari e il più delle volte
insorgono sulla cute del labbro. L’incidenza di
metastasi locoregionali è più alta dei precedenti
con sede preferenziale per i linfonodi
preauricolari e intraparotidei.
La chirurgia dei tumori del labbro deve
soddisfare la radicalità oncologica, che prevede
ampie resezioni, e quella estetico funzionale,
assicurando
la
continenza
salivare
e
un’articolazione comprensibile delle consonanti
labiali e quindi della parola. Le resezioni possono
essere
superficiali
quando
prevedono
l’asportazione del vermiglio che può inoltre
essere ricostruito con lembo linguale o con
lembo mucoso prelevato dal labbro opposto, e si
effettuano per perdite di sostanza inferiori o
uguali a un terzo. Si può effettuare inoltre una
resezione a tutto spessore del labbro inferiore
con escissione a cuneo o escissione a W e
successiva sutura dei due lembi[1]. Quando la
perdita di sostanza è invece compresa tra un
terzo e due terzi del labbro, si effettua
l’intervento di Estlander, di Von Bruns, di
Camille Bernard o la tecnica a gradino.
LINGUA
ORALE
MOBILE
E
provocando algie soprattutto per le lesioni del
bordo linguale. Le neoplasie infiltranti arrivano
successivamente a compromettere la motilità
linguale, con ripercussioni sulla fonazione e sulla
deglutizione. I tumori linguali vengono trattati
chirurgicamente con interventi di resezioni
parziali per via intraorale, emiglossectomia
transorale e successiva riparazione a sutura
diretta o con lembo nasogenieno o radiale.
In caso di lesioni molto estese si può effettuare
l’intervento di Commando che prevede
l’asportazione dell’emimandibola insieme con il
pavimento orale e l’emilingua omolaterale. Data
l’elevata incisione di metastasi del collo,
l’intervento viene sempre accompagnato o
preceduto dallo svuotamento laterocervicale
funzionale o demolitivo[6].
GUANCIA
Sono molto rari, rappresentano il 5 per cento e
sono frequenti nei fumatori e nei masticatori di
tabacco, nonché nei soggetti portatori di protesi
dentarie in cui è frequente il traumatismo.
l’evoluzione carcinomatoso delle leuco e delle
eritroplachie avviene nel 18% dei casi e sembra
interessare la porzione centrale o posteriore della
guancia, il più spesso lungo il piano occlusale. Il
comportamento clinico di questi tumori è
insidioso perché molto spesso risulta
asintomatico, senza dolore e ulcerazioni. Evolve
verso la mandibola con interessamento dei
fornici gengivali, del trigono retro molare e della
gengiva. L’estensione profonda può raggiungere
la fossa pterigoidea e quella infratemporale. Il
drenaggio linfatico avviene verso i linfonodi
sottomascellari, seguiti da quelli iugodigastrici,
preparotidei e dalle catene medio giugulari.
L’incidenza di metastasi linfonodale è del 50 per
cento[7].
Nei casi di limitata estensione tumorale si opta
per la radioterapia più tosto che per la chirurgia,
altrimenti si asporta in toto il tumore e si associa
lo svuotamento linfonodale sottomandibolare e
laterocervicale.
PAVIMENTO
La lingua mobile e il pavimento orale sono le
sedi di più frequente riscontro del carcinoma del
cavo orale e ne rappresentano il 30 per cento
circa di tutti i carcinomi orali. Nella lingua le
lesioni iniziali sono localizzate principalmente nei
due terzi posteriori della superficie ventrale e
marginale. Rari sono i carcinomi del dorso
linguale in quanto meno ricco di cheratina. I
tumori del pavimento possono restare a lungo
asintomatici data la differente innervazione
rispetto la lingua, con un numero minore di
terminazioni sensitive dolorifiche. Il dolore
compare
tardivamente
ma
solo
con
l’interessamento del periostio mandibolare. Nella
lingua viceversa il dolore è il primo sintomo,
essendo un organo mobile, il movimento
favorisce il traumatismo contro i denti,
115
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
TRIGONO RETROMOLARE
tumori maligni sono più frequenti, e
costituiscono un grave problema clinico
soprattutto per la diagnosi tardiva. La tonsilla
palatina è costituita da epitelio di rivestimento e
da tessuto linforeticolare, per cui i tumori che
possiamo riscontare sono: epiteliomi (85-95%),
sarcomi (linfosarcomi e reticolosarcomi) (1015%), melanomi e cilindromi (molto rari).
Rappresentano il 7 per cento dei tumori della
cavità orale e sono costituiti da adenocarcinomi a
cellule squamose.
Colpiscono per lo più il sesso maschile con un
incidenza di 4:1 e prediligono le fasce d’età
comprese tra i 60 e i 70. i fattori di rischio sono il
tabacco, alcool, protesi dentarie e la cattiva igiene
orale. Il 60 per cento dei tumori viene
diagnosticato quando è ancora confinato alla
regione di partenza in quanto il trigono retro
molare è facilmente esplorabile, tendono alla
diffusione locale precoce in sede tonsillare, base
lingua, guancia e osso mandibolare. Il sintomo
d’esordio è il trisma. Nel 50 per cento dei
pazienti affetti da questa neoplasia vi è
interessamento linfonodale metastatico. Il
trattamento chirurgico può prevedere dall’exeresi
limitata alla sede con resezione della mandibola o
nei casi più estesi si predilige la radioterapia[1].
Cilindromi.
Sono tumori a cavallo tra malignità e benignità;
sebbene biologicamente siano benigni (bassa
tendenza alle metastasi e all’infiltrazione), essi
tendono alla recidiva ostinata anche quando la
demolizione è estesa, cosicché si è costretti a
operare ripetutamente il paziente finché egli non
ne risente dal punto di vista funzionale (danno
digestivo, fonatorio e respiratorio).
Melanomi.
Hanno le stesse caratteristiche dei melanomi
cutanei.
OROFARINGE
Epiteliomi.
Aspetto macroscopico: appaiono come una
massa di colore “rosso pesante”, congesto, e
possono presentare zone ulcerose o zone
biancastre di necrosi. La scarsità dei vasi rende il
tumore suscettibile a superinfezioni.
Negli ultimi anni si è manifestato un aumento
dell’incidenza di tumori orofaringei nei giovani; è
stato dimostrato che queste neoplasie non sono
correlate con il consumo di alcool e di tabacco,
ma con la presenza del virus HPV (herpes virus).
STADIAZIONE
L’aspetto più importante è l’infiltrazione fino
all’eventuale superamento della capsula tonsillare;
questa infatti rappresenta la barriera naturale
della neoplasia, e quando viene superata consente
al tumore di accrescersi all’interno del connettivo
lasso peritonsillare, senza che il soggetto avverta
dolore. I sintomi iniziano a farsi evidenti solo
quando la massa infiltra anche i piani muscolari
sottostanti, per cui il paziente si reca dal medico
in uno stadio molto avanzato. La stadiazione
TNM è così definita in base alla biopsia: T1s
(tumore in situ), T1 (tumore <> 4 cm), T4
(tumore che invade le strutture adiacenti).
LOGGIA TONSILLARE E TONSILLA
PALATINA
Sono i tumori maligni di più frequente
osservazione nell’ambito dell’orofaringe e
costituiscono il 45-50 per cento dei tumori di
questa regione anatomica. L’età di insorgenza è
compresa tra i 55 e i 65 anni con una netta
prevalenza del sesso maschile.
I tumori benigni sono molto rari; i più comuni
sono i papillomi dell’epitelio tonsillare, che in
genere sono piccoli ma possono crescere di
volume o, in casi rari, diventare maligni.
Entrambe le condizioni sono favorite dal
traumatismo esercitato da parte del cibo che
entra in contatto con la tonsilla[8]. Data la
semplicità
dell’intervento,
si
procede
all’escissione per evitare qualsiasi problema. I
METASTASI:
linfonodali (in genere molto precoci, possono
essere sia monolaterali che bilaterali, per la
connessione tra i due lati; possono interessare i
linfonodi
sotto-angolo-mandibolari,
laterocervicali, cervicali trasversi, spinali) e polmonari
116
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
(spesso si tratta di tumori coesistenti in due o più
punti della linea epiteliale).
(l’aspetto della tonsilla è diverso, nei sarcomi la
superficie è liscia, le cripte sono scomparse, a
causa della crescita imponente interna del tessuto
linfatico neoplastico).
SOTTOTIPI
ISTOLOGICI:
epitelioma
malpighiano
basocellulare,
epitelioma
malpighiano spinocellulare, epitelioma a stroma
linfomatoide, linfoepitelioma di RegandSchmincke (tipico della tonsilla faringea, più
frequente nei giovani, a prognosi severa).
- Prognosi: la sopravvivenza a 5 anni oggi si
aggira attorno al 60-70%, molto di più rispetto a
qualche anno fa. Ciò è da mettere in relazione,
più che alla diagnosi precoce, alla possibilità di
effettuare interventi chirurgici più demolitivi,
grazie ai progressi della chirurgia ricostruttiva.
SINTOMATOLOGIA
Assodato che può essere anche tardiva, può
comprendere: sensazione di corpo estraneo,
disfagia unilaterale (il tumore è grande almeno
quanto un cece; questo sintomo può essere
trascurato perché il paziente può fisiologicamente
già da prima preferire l’altro lato per la
deglutizione, infatti ognuno tende a preferire un
lato per la deglutizione), adenite sotto-angolomandibolare (data la ricchezza di tessuto linfatico
della tonsilla, può comparire anche molto prima
degli altri sintomi) [9]. Questi sintomi sono
importanti soprattutto se permangono dopo la
risoluzione di un episodio infiammatorio acuto;
ovvero la febbre e i segni di infiammazione
scompaiono, mentre permangono uno o più di
questi sintomi. In una seconda fase, quando il
tumore è più grosso, possono comparire:
odinofagia
e
dolore
spontaneo
(da
interessamento dei muscoli sottostanti), otalgia
riflessa
(da
interessamento
del
nervo
mandibolare), sputo ematico (per rottura dei
vasi), trisma (per blocco dei muscoli respiratori),
alito fetido (spesso trascurato, deriva soprattutto
dalla necrosi del tumore).
Terapia del focolaio primitivo: la terapia medica e
la radioterapia hanno uno scopo palliativo, e si
usano
per
malattie
estese
intrattabili
chirurgicamente. La terapia chirurgica può essere
fatta tramite due tipi di accessi, che vanno scelti
in base allo stadio della malattia: accesso
endobuccale (solo se il tumore è limitato al corpo
tonsillare e non ha superato la capsula; si esegue
una tonsillectomia extracapsulare), oppure
accesso esterno (quando il tumore ha superato la
capsula invadendo i tessuti vicini, l’unica
soluzione è la faringectomia transmascellare,
ovvero l’asportazione in blocco della parete della
faringe e del palato molle; a questo scopo è
necessario demolire la mandibola, ma oggi questo
non è più un problema grazie alla possibilità di
prelevare lembi cutanei e alla disponibilità di ogni
tipo di protesi).
- Terapia delle metastasi linfonodali: può essere
profilattica o terapeutica. Quella profilattica può
essere fisica (radioterapia transcutanea) o
chirurgica
(svuotamento
laterocervicale
funzionale). Quella terapeutica è necessariamente
chirurgica
(svuotamento
laterocervicale
funzionale oppure radicale). La differenza tra lo
svuotamento radicale e funzionale è basata sulla
presenza o meno di infiltrazione della capsula
linfonodale; se questa è presente, si deve
asportare l’intera stazione linfonodale comprese
le fasce e i tessuti molli vicini (svuotamento
radicale); se non è presente, si possono scollare le
fasce che si dicotomizzano per accogliere i
linfonodi, e asportare solamente i linfonodi
(svuotamento funzionale)
DIAGNOSI
- Diagnosi: endoscopia (orofaringoscopia,
laringofaringoscopia), palpazione (consente di
individuare la massa e l’adenopatia, e di valutare
la durezza e la mobilità; più la massa è mobile,
minore è l’adesione ai piani sottostanti, minore è
quindi il grado di infiltrazione), biopsia (è
necessaria per verificare la diagnosi e la
stadiazione).
- Diagnosi differenziale: le forme ulceroinfiltranti vanno differenziate da TBC e sifilide
(anamnesi, test sierologici); le forme ulcerative
dall’angina di Plaut-Vincent (interessa i giovani);
le forme vegetanti e infiltrative dai sarcomi
117
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
ganglionare deve essere sospettata se il paziente
ha la TBC.
Sarcomi.
- Aspetto: la tonsilla appare come una palla a
superficie liscia, con scomparsa delle cripte a
causa della pressione dall’interno delle cellule
linfatiche in proliferazione. La tonsilla si gonfia
come un palloncino, e la capsula non viene
direttamente infiltrata finché il volume non si
accresce troppo e finisce per far “scoppiare” la
capsula stessa; in quel momento inizia
l’infiltrazione come per gli epiteliomi.
- Terapia: è medica e radiante, e dato che il
tumore è già diffuso al momento della diagnosi
non ha senso l’approccio chirurgico
TUMORI DELLA LARINGE
- Sottotipi e caratteristiche istologiche:
linfosarcoma (sovvertimento o scomparsa dei
centri germinativi, sostituiti da una proliferazione
linfoblastica diffusa), reticolosarcoma (cellule
reticolo-istiocitarie in proliferazione, presenza
tipica di un reticolo argentaffine, scomparsa dei
centri germinativi).
Il carcinoma della laringe rappresenta la più
frequente
neoplasia
del
distretto
otorinolaringoiatrico.
Le più comuni sedi di origine del carcinoma a
cellule squamose sono le corde vocali vere,
l’epiglottide, il seno piriforme.
Il cancro della laringe colpisce elettivamente il
sesso maschile (solo il 5-8% dei casi è infatti
riscontrabile nelle donne). La maggiore incidenza
di carcinoma laringeo si verifica nella quinta,
sesta e settima decade di vita. Si è visto che gli
abitanti delle zone più industrializzate presentano
una incidenza di carcinoma laringeo 2-3 volte
superiore che non gli abitanti delle zone rurali.
- Sintomatologia: anche in questo caso è molto
tardiva, e di solito non è presente la sensazione di
corpo estraneo. La massa che si accresce diventa
infine troppo grande e determina un ostacolo
fisico alla deglutizione. Allora si rileveranno:
disfagia unilaterale, tumefazione linfoghiandolare
(anche in questo caso precoce e diffusa), voce
nasale (per diminuzione della risonanza faringea
causata dalla presenza della massa).
I tumori benigni
I processi benigni che coinvolgono la laringe
sono per lo più noduli vocali detti anche noduli
dei cantanti, Polipi, Papillomi, fibromi, angiomi,
condromi, linfomi,neurinomi e cisti( congenite e
acquisite).
Si possono inoltre individuare a livello
istopatologico,le seguenti lesioni precancerose,
con un crescendo di alterazioni morfologiche e,
da un punto di vista biologico-clinico, di
potenzialità evolutive: la cheratosi e la iperplasia
squamosa benigna, la displasia da lieve a severa.
Quest’ultima è considerata anche sinonimo di
carcinoma in situ.
- Esame obiettivo: aumento globale della tonsilla,
con mucosa violacea e senza segni di flogosi; solo
tardivamente compaiono ulcerazione e necrosi,
perché questi tumori hanno una maggiore
disponibilità di vasi, per la loro origine più
profonda[10].
- Diffusione: questi tumori hanno una precoce e
imponente diffusione nel torrente linfatico, per
cui le metastasi linfoghiandolari saranno precoci
e soprattutto molto diffuse: sotto-angolomandibolari, sotto-mandibolari, latero-cervicali,
iliache e lombo-sacrali, altre.
I tumori maligni
Il cancro laringeo può svilupparsi in qualsiasi
zona della laringe: glottide,sopraglottide e
subglottide. Nella regione sovraglottica vanno
distinte le sottosedi seguenti: epilaringe che
comprende l’epiglottide sovraioidea, la plica
arepiglottica, il versante laringeo e l’aritenoide;
sovraglottide che comprende l’epiglottide
- Diagnosi: è semplice in soggetti giovani con
sintomatologia disfagica e tonsilla aumentata di
volume, in assenza di segni di flogosi; viene
comunque accertata dalla biopsia.
- Diagnosi differenziale: l’ipertrofia banale è
semplice da differenziale, perché sebbene spinta,
non porta mai alla scomparsa delle cripte; la TBC
118
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
Le caratteristiche istopatologiche sono di solito
quelle del carcinoma ad epitelio pavimentoso
corneificante o non corneificante (80-90% dei
casi). Solo raramente si osservano forme
indifferenziate ed altrettanto rari sono i casi di
adenocarcinoma. Obiettivamente la neoplasia
può presentare carattere vegetante, che viene
anche descritto sotto il nome di forma esofitica,
ha l’aspetto di una massa proliferante esuberante,
a grossi mammelloni, o moriforme, villosa o a
cavolfiore facilmente sanguinante.
La forma infiltrante o interstiziale ha
accrescimento sottomucoso, a seconda che
l’infiltrazione sia più o meno profonda, si ha una
placca più o meno indurita e più o meno rilevata
in superficie, a limiti imprecisi, ricoperta da
mucosa non ulcerata ne vegetante. La forma
ulcerativa altro non è che l’inevitabile evoluzione
delle due forme precedenti, specialmente della
infiltrante, si può presentare sotto l’aspetto di
una perdita di sostanza più o meno estesa, a
bordi frastagliati sopraelevati [13]. La superficie
ulcerata è di solito irregolare, talvolta ricoperta da
granulazioni esuberanti o da masse proliferanti
simili a cavolfiore, sì da poter parlare di una
forma ulcero-proliferante. Gli epiteliomi possono
a loro volta venir distinti istologicamente in due
tipi fondamentali: lo spino-cellulare ed il basocellulare.
Con il termine di tumori intrinseci, endolaringei
o cavitari, si debbono intendere i tumori che si
sviluppano nella zona della laringe che va dal
piede della faccia laringea dell’epiglottide alla
regione ipoglottica. Si definiscono, invece, tumori
estrinseci, marginali, esolaringei o faringolaringei, quelli a sviluppo sul bordo libero o sulla
metà superiore dell’epiglottide, sulle pliche ariepiglottiche o sulle aritenoidi, come pure quelli
del seno piriforme, delle docce feringo-laringee e
del solco glosso-epiglottico. Gli epiteliomi
endolaringei sono due o tre volte più frequenti
degli estrinseci, risiedono comunemente sulle
corde vocali, procedono con infiltrazione diffusa,
che porta ad un aumento del volume della corda,
che si presenta ora granulosa, ora mammellonata,
talvolta l’infiltrazione è sormontata da
un’ulcerazione più o meno estesa.
Comprendiamo
nella
denominazione
di
epiteliomi marginali o faringo-laringei i tumori a
sede sul margine e sul bordo libero
dell’epiglottide, sulle pliche ari-epiglottiche, sulle
infroioidea e le pieghe ventricolari o false
corde[11]. Tenuto conto di tali presupposti
anatomici, si suddividono ulteriormente le forme
tumorali in relazione alla loro sede e alla relativa
diffusione locale, come segue:
T1: tumore limitato ad una sola sottosede della
sovraglottide con normale mobilità delle corde
vocali;
T2: tumore che invade la mucosa di più di una
delle sottosedi adiacenti della sovraglottide o
della glottide o di una regione al di fuori della
sovraglottide, senza fissità della laringe;
T3: tumore limitato alla laringe con fissità delle
corde vocali e invasione dell’area postcricoidea o
dei tessuti preepiglottidi;
T4: tumore che invade la cartilagine tiroidea e si
estende nei tessuti molli del collo, alla tiroide e
all’esofago. Le forme ipoglottiche dei tumori
laringei incidono con valori percentuali molto
bassi rispetto a quelli relativi alle neoplasie
glottiche o ai tumori sopraglottici. Spesso i
tumori rilevati nella regione ipoglottica sono in
continuità con il piano glottico, nei pazienti con
carcinomi cordali si può praticamente escludere
un interessamento della regione ipoglottica
soprattutto in quelle forme circoscritte ( T1 ) in
cui il processo neoplastico resta localizzato in
corrispondenza della faccia superiore della corda
vocale vera. Nelle forme glottiche più estese, T2
o T3, nelle quali il tumore si diffonde dalla
regione glottica a quella sottoglottica , non vi
sono elementi che consentano di stabilire se il
tumore si origini nell’una o nell’altra regione. In
definitiva si ha un’impossibilità di identificare i
confini tra la regione ipoglottica e quella glottica,
e quindi l’esatta delimitazione dei tumori di
ciascuna di queste due regioni, ci inducono a
considerare in un unico gruppo i carcinomi che
interessano tali sedi[12].
Quando il tumore diffonde colpisce in primo
luogo i linfonodi presenti nel collo (cervicali
profondi e cervicali anteriori). Si può avere una
diffusione del tumore alla base della lingua,in
altre regioni della gola e del collo, ai polmoni e
organi a distanza.
ISTOPATOLOGIA
La maggior parte delle neoplasie maligne
laringee è costituita da carcinomi derivanti
dall’epitelio di rivestimento, più rari i sarcomi e
gli endoteliomi.
119
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
aritenoidi, sui seni piriformi e nelle docce glossoepiglottiche o faringo-epiglottiche. Nel 30-40%
dei casi si osserva una localizzazione della zona
vestibolare mentre nel 25% dei casi il cancro
colpisce la zona cordale e nel 10% la zona
ventricolare. Il cancro della zona commissurale
anteriore incide solo per l’1-2% del totale dei
carcinomi laringei,nel 2-3% dei casi è colpita la
zona sottoglottica. Il 95% dei tumori ipofaringei
insorgono nelle docce faringo-laringee o seni
piriformi, la diffusione può venire per continuità,
per metastasi loco-regionali che avvengono per
via linfatica. Le metastasi per via ematica in altri
organi ed apparati sono più rare e tardive.
dovrà essere allargata alle condizioni ambientali,
allo stile di vita e a tipo di lavoro. Anche alcune
abitudini voluttuarie (fumo), l’abuso o il cattivo
uso della voce, possono fornire elementi utili ad
una corretta diagnosi. Per ognuno dei sintomi
accertati dovranno essere inoltre valutate le
modalità d’insorgenza, le sue modificazioni nel
tempo, la successione cronologica con cui si
sono verificate e sovrapposte ad altre
manifestazioni morbose. I sintomi fondamentali
della patologia laringea sono tre: dispnea,
disfonia e disfagia. La dispnea laringea presenta
caratteri tipici[15]. È di tipo inspiratorio
accompagnata da un movimento di discesa della
laringe, per contrazione abnorme dei muscoli
sterno-tiroideo e sterno-ioideo. Il carattere
inspiratorio della dispnea è legato alla riduzione
del lume laringeo per la presenza di una
neoformazione endolaringea. Spesso la dispnea
laringea si accompagna a stridore respiratorio
(cornage) ed al rientramento di alcune zone del
torace (tirage), dovuto alla contrazione forzata
dei muscoli respiratori, particolarmente evidente
in corrispondenza della fossetta del giugolo e
nelle regioni sopraclavicolari.
Per quanto riguarda la disfonia, questa può
insorgere improvvisamente o progressivamente,
può avere carattere continuo, o manifestarsi in
alcune ore della giornata. La voce disfonica può
assumere un timbro aspro, legnoso come si
verifica in caso di neoplasie laringee, o in alcune
forme di laringite cronica alla vibrazione delle
corde vocali vere può sovrapporsi la vibrazione
delle false corde ipertrofiche per cui in questi casi
si può avere la cosiddetta voce di false corde[1].
La paralisi di una corda vocale può essere invece
responsabile di una diplofonia. La disfonia che è
un fenomeno esclusivamente laringeo deve
essere distinta da modificazioni del timbro della
voce, legate ad abnorme funzionamento della
cavità di risonanza nasali.
La disfagia costituisce il terzo tra i sintomi
fondamentali della patologia laringea. Essa è
legata a lesioni che interessano l’epiglottide e
l’ipofaringe. Questo tipo di disfagia può essere
meccanica o dolorosa e può verificarsi sia per i
cibi solidi che liquidi. Accanto a questi tre
sintomi fondamentali possono essere presenti
sintomi collaterali secondari quali: tosse,
adenopatia latero-cervicale spesso legata a
metastatizzazione linfonodali .
SINTOMI
La sintomatologia del cancro laringeo è in
rapporto inizialmente con la sede d’insorgenza,
con il suo accrescimento, e con le modalità di
diffusione. Il più frequente sintomo che
caratterizza i tumori della laringe coinvolgenti le
corde vocali è la disfonia, dapprima saltuaria e
tende a farsi più frequente ed intensa fino a
trasformarsi in una mancanza completa della
voce[14]. Quando il tumore interessa la regione
sopraglottica, i sintomi sono tardivi e costituiti
prevalentemente da disfagia con un dolore che
può irradiarsi verso l’orecchio. Se la neoplasia è
ulcerata alla disfagia spesso si associano scialorrea
riflessa intensa e alito fetido. Altrettanto
importante è la comparsa di una dispnea di tipo
inspiratorio, che compare in caso di tumore
subglottico. In rari casi il primo sintomo è
rappresentato da una adenopatia metastatica.
DIAGNOSI
La diagnosi del cancro della laringe spesso è
basata sul riscontro di una neoformazione
vegetante o ulcerata, su di una riduzione della
motilità o fissità laringea, sul ristagno di saliva in
un seno piriforme. Essa si avvale di:
Anamnesi: Il primo approccio ad un paziente
che presenta una sintomatologia laringea è
rappresentato dall’anamnesi e dall’esame
obiettivo e semeiologico. Per anamnesi s’intende
la raccolta dettagliata a scopo clinico-diagnostico
di tutte le notizie sulla vita del paziente, su
abitudini e patologie pregresse che possono
essere messe in relazione con l’inizio o con il
decorso della malattia. L’indagine anamnestica
120
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
visita ORL nel caso in cui non è stato possibile
ispezionare completamente la laringe o
semplicemente per conoscere con maggior
precisione l’estensione della malattia e la mobilità
delle corde vocali. La laringoscopia a fibre ottiche
permette di effettuare un’ispezione diretta della
laringe che viene eseguita tramite l’introduzione
in faringe, attraverso le fosse nasali, di endoscopi
flessibili a fibre ottiche o mediante l’uso di
endoscopi rigidi con ottiche angolate a 70° o 90°,
introdotti in faringe attraverso il cavo orale.
L’immagine della laringe così visualizzata viene
vista attraverso un monitor o un oculare posto
all’estremità dell’apparecchio.
Esame obiettivo: si compie con l’ispezione, la
palpazione, con l’esplorazione digitale ed anche
con l’ascoltazione. L’ispezione permette di
valutare la normale motilità laringea nella
deglutizione, l’eventuale esteriorizzazione di un
processo suppurativo o neoplastico o l’esistenza
di adenopatie latero-cervicali. Essa non deve
essere disgiunta dall’ascoltazione che può farci
rilevare l’esistenza di rumori particolari (tirage).
La palpazione permette, di valutare la mobilità
della laringe in ambedue i sensi verticale e
trasversale, di precisare le deviazioni laterali o gli
spostamenti in avanti del condotto laringotracheale, l’asimmetria dello scheletro, l’aumento
di volume per pericondrite. Con la palpazione è
possibile inoltre valutare l’eventuale presenza di
masse patologiche.
Laringoscopia diretta: si effettua in anestesia
generale con paziente curarizzato con apposita
spatola, dotata di illuminazione distale, vengono
avvicinate la base della lingua e l’epiglottide,
l’esaminatore può osservare la laringe con visione
diretta o attraverso microscopi ingranditori. In
questo modo è possibile, oltre che ad osservare
l’organo eseguire delle biopsie o interventi
chirurgici per piccole neoformazioni (polipi,
noduli, leucoplachie). I campioni di tessuto
vengono affidati successivamente ad un
anatomo-patologo per l’analisi microscopica.
Laringoscopia indiretta: Si esegue a malato
seduto, con capo esteso. Si invita il paziente a
protudere la lingua: con tale manovra la base
della lingua si porta in alto ed in avanti,
sollevando contemporaneamente la laringe, che è
ad
essa
ancorata,
e
facilitando
la
visualizzazione[16]. Si afferra la punta della lingua
con interposizione di garza affinché non scivoli.
Lo specchietto laringeo, opportunamente
riscaldato perché non si appanni, viene
introdotto davanti all’ugola con una inclinazione
di circa 40°-50°. I raggi luminosi proiettati dallo
specchio frontale vengono deviati verso la
laringe. Per ottenere un innalzamento della
laringe e quindi una migliore visualizzazione il
paziente viene invitato a pronunciare la vocale
“e” o “i”. Si ottiene un’immagine speculare, la
commissura anteriore della laringe viene
proiettata nella parte superiore dello specchietto.
Mentre il paziente pronuncia la vocale “e”, per il
sollevamento dell’epiglottide, si riuscirà a vedere
le corde vocali nella posizione di fonazione, cioè
nella posizione di adduzione e di tensione. Con
l’atto di inspirazione, si vedrà il movimento
opposto delle corde, quello cioè di abduzione. Il
contatto tra lo specchietto e il palato molle può
provocare riflessi particolarmente vivaci, tosse e
conati di vomito. In questi casi può essere utile
effettuare un’anestesia di superficie
Esame radiografico: l’indagine radiografica
della laringe dà la possibilità di un’analisi delle
varie parti della laringe in condizioni normali e
patologiche. Per questo studio la migliore
proiezione è quella laterale o di profilo. Un
progresso notevole nello studio della radiografia
laringea si è ottenuto con la tomografia
computerizzata (TC) e con la RMN la quale
mette meglio in evidenza eventuali alterazioni dei
tessuti molli laringei nei confronti delle strutture
cartilaginee. Particolarmente utile risulta l’
indagine radiografica per la ricerca di eventuali
corpi estranei laringo-tracheali.
Laringostroboscopia: Permette di analizzare nei
dettagli le caratteristiche fisiologiche e
patologiche della vibrazione glottica che si
basano fondamentalmente sulla teoria mucoondulatoria [17]. Le corde vocali hanno due
movimenti traverso e verticale. Le fasi del ciclo
vibratorio sono tre: apertura, avvicinamento e
chiusura. Dal rapporto tra la durata delle vari fasi
si individuano le modalità di vibrazione: normale,
Laringoscopia a fibre ottiche: Questa tecnica
viene utilizzata come completamento di una
121
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
ipercinetica, ipocinetica. La videostroboscopia
permette di visualizzare fenomeni non visibili a
occhio nudo quali segmenti cordali non vibranti,
rigidità delle mucose ecc.
Laringectomia totale: nell'intervento si esegue
l'asportazione completa della laringe e la
tracheostomia che consiste nell'abboccamento
della trachea alla cute del collo. La procedura può
essere associata alla asportazione dei linfonodi
loco-regionali (svuotamento linfonodale)[1]. La
laringectomia totale si esegue solo nei casi più
avanzati dove non esistono alternative
terapeutiche con interventi meno mutilanti. Tali
tipi di interventi si prefiggono lo scopo di
asportare radicalmente la laringe con le regioni
contigue verso cui il tumore è sconfinato. In
particolare sono possibili allargamenti dell’exeresi
verso:
- Ipofaringe
- Base lingua
- Cute della regione anteriore del collo.
La successiva riparazione della breccia faringea
residua, la ricostruzione dei tegumenti e
l’abboccamento della trachea al giugulo,
consentono la definitiva separazione delle vie
respiratorie da quelle digestive.
TERAPIA
La terapia delle neoplasie della laringe si basa
sulla terapia chirurgica, sulla radioterapia e sulla
chemioterapia.
Terapia chirurgica
Si articola in interventi di vario tipo in base alla
estensione locale della neoplasia e alla presenza o
meno di linfonodi sospetti o invasi.
•
Interventi endoscopici: laringoscopia
diretta in sospensione; si può eseguire con
tecnica tradizionale microchirurgica o con
tecnica Laser. E' utile nei casi iniziali, senza
diffusione
linfonodale
del
tumore.
Cordectomia endoscopica laser: questo tipo
di intervento è riservato a quelle lesioni del
piano glottico che coinvolgono la corda
vocale, preferenzialmente nel suo bordo
libero,
senza
interessamento
della
commissura anteriore , dello spazio
sottoglottico, della regione aritenoidea e del
pavimento del ventricolo di Morgagni. La
motilità della corda vocale deve essere del
tutto conservata. Nel suo funzionamento il
Laser CO2 emette radiazioni non visibili del
campo infrarosso, può essere considerato a
tutti gli effetti un bisturi ottico e permette di
intervenire in maniera completamente
esangue.
Radioterapia
Si utilizza solo nelle forme iniziali delle corde
vocali in alternativa alla chirurgia.
Chemioterapia
Si utilizzano protocolli basati soprattutto sull'uso
del Cisplatino.
Le forme tumorali più maligne (CA
indifferenziati) sono le più sensibili alla
chemioterapia.
Essa inoltre rappresenta l'unica alternativa in tutti
i casi non operabili[18].
I migliori risultati nella terapia del cancro laringeo
si raggiungono quando la malattia viene
affrontata
in
equipe
dal
chirurgo
otorinolaringoiatra, dall'oncologo e dal
radioterapista.
Laringectomie parziali: sono interventi
conservativi in cui si esegue l'asportazione di
parti della laringe con conservazione dell'organo.
Le procedure chirurgiche possono prevedere o
non prevedere l'asportazione dei linfonodi locoregionali
(svuotamento
linfonodale).
Laringectomia orizzontale glottica secondo
Calearo Teatini: prevede l’asportazione in
monoblocco tutta la glottide prearitenoidea
(corde vocali e commissura anteriore) con la
porzione di cartilagine tiroide su cui si inserisce.
La successiva ricostruzione della continuità
laringea consente il recupero fonatorio,
respiratorio e la decannulazione definitiva del
paziente.
FOLLOW-UP
(controlli
successivi
ai
trattamenti)
Un corretto follow-up dovrebbe prevedere:
• Visita di controllo ORL nel corso della quale
deve essere eseguito un esame endoscopico
con tecniche tradizionali o, meglio, con la
Videofibrolaringoscopia con registrazione
delle immagini..
122
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
•
•
•
Esami ematici idonei (C.E.A., alfa feto
proteina,
marcatori
tumorali,
VES,
transaminasi, LDH..)
Radiografia del torace
Ecotomografia dell'addome
123
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
11. Ferlito A, Carbone A, De Santo LW, et al.
"Early" cancer of the larynx: the concept as
defined by clinicians, pathologists, and
biologists. Ann. Oto Rhinol. Laryn 1996;
105: 245-250.
BIBLIOGRAFIA
1. De Campora E, Marzetti F. La chirurgia
oncologica della testa e del collo. Pacini Editore.
1996.
12. Gnepp D, Barnes L, Crissman J, Zarbo R.
Recommendations for the reporting of larynx
specimens containing laryngeal neoplasms.
Virchows Arch 1997;431: 155-157.
2. Ridge JA, Glisson BS, Lango MN, et al. Head
and Neck Tumors in Pazdur R, Wagman LD,
Camphausen KA, Hoskins WJ (Eds) Cancer
Management: A Multidisciplinary Approach. 11
ed. 2008.
13. Wennerberg J. Predicting response to therapy
of squamous cell carcinoma of the head and
neck (review). Anticancer Res 1996;16: 23892396.
3. Parkin DM, Whelan SL, Ferlay J, Raymond L,
Young J. (eds.). Cancer Incidence in Five
Continents. Vol. VII. IARC Scientific
Publication No. 143. Lyon. International Agency
for Research on Cancer, 1997.
14. Baretton G, Li X, Stoll C, et al. Prognostic
significance of DNA ploidy in oral squamous
cell carcinomas. A retrospective flow and
image cytometric study with comparison of
DNA ploidy in excisional biopsy specimens
and resection specimens, primary tumours
and lymph node metastases. Oral Surg Oral
Med Oral Pathol Oral Radiol Endod 1995;
79: 68-76.
4. Forastiere AA, Ritter MA, Herscher LL, Cook J,
Wheeler RH, Spencer S, Buchsbaum D, Robert
F, Gillison M, Koch WM, Shah KV, Laccourreye
O, Bassot V, Brasnu D, Laccourreye H. Head
and Neck. Curr Opin Oncol 1999; 11: 175-203.
5. Barzan L, Talamini R. Analysis of prognostic
factors for recurrence after neck dissection.
Arch. Otolaryngol Head Neck Surg 1996;122:
1299-1302.
15. Brennan JA, Mao L, Iiruban RH, et al.
Molecular assessment of histopathological
staging in squamous-cell carcinoma of the
head and neck. New Engl. J Med 1995;332;
7: 429-435.
6. Franceschi S, Barzan L, Talamini R. Screening
for cancer of the head and neck: if not now,
when? Oral. Oncol 1997;33:313-316.
16. Adelstein DJ. Recent randomized trials of
chemoradiation in the management of locally
advanced head and neck cancer. Current
Opinion in Oncology 1998; 10: 213-218.
7. Schottenfeld D, Fraumeni JF Jr. (eds). Cancer
Epidemiology and Prevention. Second Edition.
New York: Oxford University Press, 1996.
17. Carbone A, Volpe R, Barzan L. Superficial
extending carcinoma (SEC) of the larynx and
hypopharynx. Pathol. Res Pract 1992;188:
729-735.
8. Yun Oh and Li Mao. Biomarkers in head and
neck carcinoma. Curr. Opin Oncol 1997;9: 247256.
9. Terrell JE. Quality of life assessment in head and
neck cancer patients. Hematol Oncol Clin North
Am 1999; 13: 849-865.
18. Samuel W. Beenken, MD. "Laryngeal Cancer
(Cancer of the larynx)". Laryngeal
Cancer
(Cancer of the larynx). Armenian Health
Network,
Health.am.
http://www.health.am/cr/laryngeal-cancer/.
Retrieved 2007-03-22.
10.Annual Report on the Rare Diseases and
Conditions Research. National Institutes of
Health.
http://rarediseases.info.nih.gov/.
Retrieved 2007-03-22.
124
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
CancerStat Umbria
ISSN 2039-814X
Anno III, 2012
Numero 1
I tumori della vescica
Numero 2
Trend di mortalità per cause in Umbria. 1994-2010.
125
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
CancerStat Umbria
ISSN 2039-814X
Anno II, 2011
Numero 1
Mortalità per cause nelle ASL dell’Umbria. 2005-2009.
Numero 2
Anni di vita potenziale persi (YPLL) in Umbria. 1995-1999 e 2005-2009.
Numero 3-4
Il cancro della prostata.
Numero 5
Ciò che bisogna sapere per decidere se sottoporsi allo screening per il cancro
della prostata.
Partecipazione al IV round dello screening citologico della AUSL 2 dell’Umbria.
Numero 6
Il cancro del rene.
Numero 7
Fumo o salute. I sessione.
Numero 8
I tumori della tiroide.
Numero 9
Fumo o salute. II e III sessione.
Numero 10
GISCoR. I sessione
Numero 11
GISCoR. II sessione
Numero 12
Il cancro del pene e del testicolo
126
I TUMORI DELLE ALTE VIE AEREO-DIGESTIVE
CancerStat Umbria
Anno I, 2010
Numero 0
Le statistiche del cancro e della mortalità in Umbria.
Numero1
- Ultime pubblicazioni dei collaboratori del RTUP.
- Technology assessment della metodica di prelievo e di preparazione della citologia in fase
liquida (LBC – Liquid Based Citology) per l’utilizzo routinario nello screening per la
prevenzione del tumore della cervice uterina in tutte le fasce di età e per la ricerca del Papilloma
Virus Umano ad alto rischio oncogeno (HPV – DNA HR) come test primario nelle fasce di età
da 35 a 64 anni durata prevista: 12 mesi / 8000 donne).
Numero 2
L’incidenza del cancro in Umbria, 2006-2008.
Numero 3
- Il Registro Rumori Infantili Umbro-Marchigiano.
- La ricerca dei tumori professionali nell’ambito del progetto OCCAM.
Numero 4
Il quadro epidemiologico per la programmazione della prevenzione oncologica regionale in Umbria.
Numero 5
- Incontro con il Gruppo multidisciplinare regionale per le neoplasie tiroidee in Umbria. Perugia
28/29 ottobre 2010.
Tavola rotonda: Utilità della creazione di registri regionali dei carcinomi della tiroide.
o L’esperienza del gruppo multidisciplinare regionale per le neoplasie della tiroide.
o Registro Tumori Umbro di Popolazione (RTUP) e carcinoma della tiroide.
Numero 6
- Incontro con il Gruppo multidisciplinare regionale per le neoplasie tiroidee in Umbria. Perugia
28/29 ottobre 2010.
Tavola rotonda: Utilità della creazione di registri regionali dei carcinomi della tiroide.
o Registro Siciliano dei Tumori della tiroide.
- Convegno: Nuove acquisizioni nella gestione clinica del carcinoma della tiroide di origine
follicolare: cosa dicono le linee guida?
Numero 7
- Neoformazioni della cute e del cavo orale. Melanoma.
Terni 13.11.2010
o L’epidemiologia dei tumori cutanei in Umbria.
o Prevenzione primaria e secondaria dei tumori cutanei.
127