Farmacologia
Glucocorticoidi
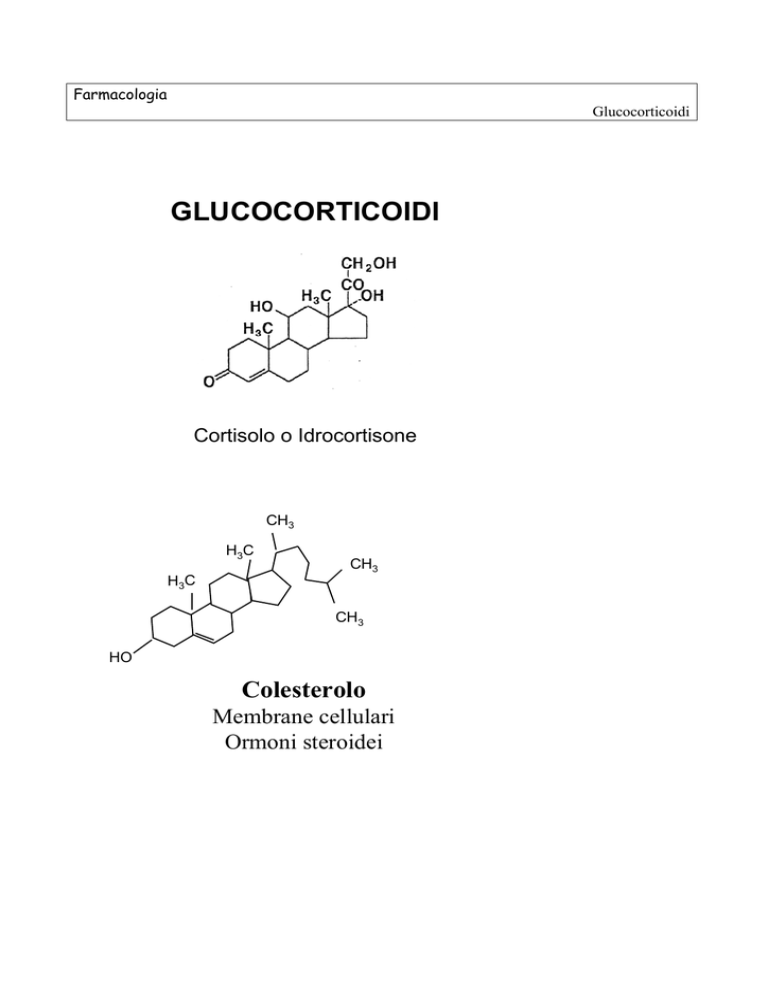
GLUCOCORTICOIDI
Cortisolo o Idrocortisone
CH3
H3C
CH3
H3C
CH3
HO
Colesterolo
Membrane cellulari
Ormoni steroidei
Cortisolo o Idrocortisone
Cholesterol
Steroid20α hydroxylase
20α-OH-cholesterol
P450sccCYPXIA
Colesterol Side Chain cleavage enzyme
Pregnenolone
Progesterone
Aldosterone
P45017αCYPXVIIA
Steroid17α hydroxylase
17α-OH-pregnenolone
Dehydroepiandrosterone
3β-HSD
3beta-hydroxysteroid dehydrogenase
17α-OH-progesterone
Androstenedione
Oestrone
P45021CYPXXIA
Steroid21 hydroxylase
11-deoxycortisol
Testosterone
Oestradiol
P45011βCYPXIB
Steroid11β hydroxylase
Cortisol (hydrocortisone)
+
+
IL-1
IL-2
TNF-α
Sistema immunitario
Linfociti, neutrofili
monociti/macrofagi
___
Cortisolo
•Il cortisolo è sintetizzato dalla zona fascicolata/reticolare del surrene
•La biosintesi e la liberazione è indotta dall’ormone adrenocorticotropo (ACTH), rilasciato
dall’ipofisi, a sua volta sotto il controllo dell’ipotalamo via CRH (corticotropin-releasing hormone).
•L’ACTH (via un recettore serpentino, Gs):
•1) aumenta la traslocazione (?) del substrato nella membrana interna dei mitocondri, dove sono
localizzati gli ormoni biosintetici (P450scc)
•2) aumenta la trascrizione genica degli enzimi biosintetici
Leung & Bloom, J Allergy Clin Immunol. 111, 3-22, 2003
Leung & Bloom, J Allergy Clin Immunol. 111, 3-22, 2003
Glucocorticoidi
Recettore Glucocoiticoidi
GR dimero
Transattivazione
Trascrizione genica
Proteine antiinfiammatorie,
ma anche effetti collaterali
GR monomero
Inibizione fattori di
trascrizione
NF-kB, AP-1, NF-AT
Transrepressione
da Barnes, Nature, 402(S), 1999
Glucocorticoid regulated genes
a)
•
•
•
•
•
Increased gene trascription
Lipocortin-1 (annexin-1)
β2-adrenoceptor
Secretory leucocyte inhibitory protein, CC10
IL-RII, IL1ra
IkB-α
b) Decreased gene transcription
• Cytokines (IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-11,
IL-13, TNF-α, GM-CSF
• Chemokines (RANTES, eotaxin, MIP-1α, MIP-1, MCP-3
• Enzymes (iNOS, COX-2, cPLA2)
• Adhesion molecules (ICAM-1, VCAM-1
• Receptors (IL-2R, NKiR)
Adcock & Caramori (2001)
Goodman & Gilman’s, 2001
Principali usi terapeutici dei GC
a) Patologie endocrine
Terapia sostitutiva dell’insufficienza surrenalica primaria e secondaria
b) Patologie non endocrine
Malattie reumatiche (Lupus e. sistemico, poliartrite nodosa, artrite a cellule giganti,
osteoartrite, artrite reumatoide, sindromi vasculitiche, cardite reumatica)
Malattie renali (Sindrome nefrotica, glomerulonefrite mebranosa e membranoproliferativa)
Malattie allergiche
Asma bronchiale
Malattie infettive (Polmonite da Pneumocystis carinii, meningite da H. influenzae tipoB)
Malattie cutanee (Dermatosi su base allergica)
Malattie oculari
b) Patologie non endocrine
Malattie gastrointestinali (Colite ulcerosa cronica, Malattia di Crohn)
Malattie epatiche (Epatite cronica su base autoimmune attiva)
Malattie neoplastiche (Leucemia linfatica acuta, linfoma)
Edema cerebrale (Neoplasie, parassiti, traumi e accidenti vascolari?)
Altre malattie (Sarcoidiosi, trombocitopenia, anemia emolitica su base autoimmune, stroke
e lesioni del m. spinale, trapianti d’organo)
GC e metabolismo intermedio
a) Inibizione utilizzo glucosio nei t. periferici
(t. adiposo, cute, fibroblasti, timociti, PMN)
Meccanismo: translocazione trasportatori del glucosio dalla
membrana plasmatica a sedi intracellulari
b) Promozione gluconeogenesi
(fegato)
Meccanismo: nel fegato induzione della trascrizione di enzimi
coinvolti nel metabolismo degli a.a. e nella gluconeogenesi
(fosfoenolpiruvato carbossichinasi, glucosio-6-fosfattasi, fruttosio2,6-bifosfonati)
effetti catabolici (atrofia t. linfoide, diminuzione masse
muscolari, assotigliamento cute, bilancio negativo azoto
GC e metabolismo intermedio (segue)
c) Facilitazione permissiva effetto lipolitico di agonisti β-adrenergici e
GH; induzione della lipolisi negli adipociti ed aumento ac. grassi
liberi
Redistribuzione del grasso nell’organismo
(ipercorticismo, sindrome di Cushing –”buffalo hump,
“moon facies”, area sopraclavicolare e perdita si grasso
alle estremità)
Effetti collateri della terapia con GC
•Obesità e ridistribuzione del grasso nell’organismo (”buffalo hump, “moon facies”, area
sopraclavicolare, strie addominali);
•Riduzione dello spessore ed atrofia della cute con difficoltà nella cicatrizzazione delle ferite;
•Riduzione delle masse muscolari
•Osteoporosi (inibizione osteoblasti, attivazione osteoclasti indiretta, diminuito assorbimento calcio,
difetti nella mineralizzazione);
•Modificazioni dell’umore (euforia e psicosi);
•Cateratta;
•Immunosoppressione con diminuzione delle difese naturali contro le infezioni;
•Ritenzione idrosalina ed ipertensione (per effetto mineralcorticoide di alcune molecole ed aumento
epatico della sintesi di angiotensinogeno)
•Ritardo della crescita nei bambini (?)
•Dopo trattamento prolungato, inibizione e soppressione dell’asse ipotalamo-ipofisi-surrene ed
atrofia surrenalica. L’interruzione della somministrazione deve avvenire gradualmente;
•Ulcere peptiche;
•Iperglicemia e diabete mellito iatrogeno
Vie di somministrazione dei glucocorticoidi
•Via orale (per tutte le molecole)
•Topica cutanea: desametasone, idrocortisone, triamcinolone
•Topica inalatoria: beclometasone, budesonide, flunisolide, fluticasone, triamcinolone
•Topica nelle malattie infiammatorie del tratto intestinale: budesonide
•EV e IM: desametasone, idrocortisone, metilprednisone, metilprednisolone
Goodman&Gilman’s
Cellular effect of corticosteroids, Barnes et al., Ann. Int. Med., 139, 359-370, 2003