13
Cardiopatie da malattie sistemiche,
infettive, da farmaci
Il cuore è spesso interessato da numerose
malattie sistemiche o infettive, dall’effetto di
farmaci o di sostanze chimiche che causano
alterazioni morfologiche, funzionali ed emodinamiche che si manifestano come cardiomiopatie secondarie (dilatativa, restrittiva,
infiltrativa), valvulopatie, patologie del pericardio (versamento, tamponamento, costrizione), masse intracardiache, endocardite
marantica o di Libman-Sacks, carcinoide, ipereosinofilia. L’endocardite infettiva è trattata
separatamente nel capitolo 11. L’ecocardiografia è la metodica di scelta per il riconoscimento e la valutazione di queste alterazioni.
L’eco 2D fornisce informazioni di carattere
morfologico e funzionale; con il Doppler e il
color Doppler si ottengono le pressioni intracardiache, si valuta la severità di una stenosi
e di un rigurgito valvolare e la modalità di
riempimento diastolico ventricolare. Non è
raro che il riscontro ecocardiografico di un’alterazione cardiaca sia il primo indizio diagnostico di una determinata malattia sistemica,
ad esempio il coinvolgimento tipico della valvola tricuspidale e della valvola polmonare
nella malattia da carcinoide, o l’aumentato
spessore e l’aspetto granulare delle pareti
ventricolari nell’amiloidosi. Nella tabella 13.1
sono elencate diverse manifestazioni cardiache di patologie sistemiche di riscontro fre-
quente nel laboratorio di ecocardiografia; le
loro caratteristiche saranno discusse in dettaglio in questo capitolo con l’aiuto di materiale illustrativo.
Amiloidosi
L’amiloidosi è dovuta alla deposizione di sostanza amiloide in diversi organi. Può coinvolgere il miocardio, dove è causa di cardiomiopatia infiltrativa (figura 13.1). Contrariamente all’opinione comune, non tutte le cardiomiopatie infiltrative sono responsabili di
quadri cardiaci morfologici ed emodinamici di
tipo restrittivo. Nell’amiloidosi, l’infiltrazione miocardica interessa principalmente
l’interstizio, e l’aspetto morfologico predominante è l’aumento dello spessore parietale
senza dilatazione della cavità ventricolare sinistra1 (figura 13.2). La funzione sistolica ventricolare non è significativamente ridotta se
non nello stadio avanzato, quando lo spessore parietale raggiunge i 15 mm. Anche se l’ipertrofia parietale visibile all’eco 2D è uno dei
parametri più importanti nei pazienti con amiloidosi, tale diagnosi non può essere esclusa
anche in presenza di normali spessori parietali.2 I depositi cardiaci di amiloide sono diffusi
e coinvolgono il miocardio, il setto interatriale, il pericardio e le valvole,3 dove causa insuf-
225
MANUALE
DI
ECOCARDIOGRAFIA
ficienza valvolare che è un reperto comune in
questa patologia. I depositi di amiloide rendono il tessuto miocardico ecoriflettente all’eco
2D, per cui le immagini appaiono molto definite, ma il solo aspetto luminoso non è di per
sé diagnostico, dal momento che è presente
anche nella malattia ipertensiva (specialmente nei pazienti con coinvolgimento renale),
nella malattia da accumulo di glicogeno4 e
nella cardiomiopatia ipertrofica. I pazienti con
amiloidosi cardiaca hanno bassi voltaggi del
QRS o un aspetto elettrocardiografico pseudoinfartuale (figura 13.3), mentre l’ipertrofia
del ventricolo sinistro, la cardiomiopatia ipertrofica e l’accumulo di glicogeno si accompagnano con il reperto elettrocardiografico di alti voltaggi del QRS tipici dell’ipertrofia del
ventricolo sinistro. Nelle fasi iniziali della malattia la funzione sistolica ventricolare può essere iperdinamica e non è insolito riscontrare
Tabella 13.1 - ASPETTI ECOCARDIOGRAFICI DELLE MALATTIE SISTEMICHE
Amiloidosi
• Aumento dello spessore (moderato-marcato) delle
pareti del ventricolo sinistro e del ventricolo destro
• Cavità ventricolare sinistra di normali dimensioni
• Graduale deterioramento della funzione sistolica
ventricolare
• Aspetto granulare del miocardio
• Versamento pericardico
• Disfunzione diastolica
• Ispessimento delle valvole e insufficienza di più
valvole
Spondilite anchilosante
• Dilatazione dell’anulus aortico
• Dilatazione dei seni di Valsalva
• Ispessimento della valvola aortica con insufficienza
Carcinoide
• Ispessimento e retrazione della valvola tricuspidale con insufficienza severa
• Stenosi tricuspidale, di solito lieve
• Ispessimento e retrazione della valvola polmonare
con stenosi
• Sovraccarico di volume del ventricolo destro.
• Ispessimento delle valvole del cuore sinistro
(< 15%)
Atassia di Friedreich
• Ipertrofia del ventricolo sinistro, di solito concentrica (68%), che simula la cardiomiopatia ipertrofica
• Dilatazione del ventricolo sinistro con disfunzione
sistolica (7%)
Emocromatosi
• Aspetto di cardiomiopatia dilatativa, ventricolo sinistro dilatato con ridotta funzione sistolica
• Normale spessore parietale del ventricolo
• Caratteristiche di riempimento diastolico di tipo restrittivo negli stadi avanzati
Infezione da HIV o AIDS
• Versamento pericardico
• Cardiomiopatia dilatatativa
• Ipertensione polmonare
Sindrome da ipereosinofilia
• Ispessimento e imbrigliamento del lembo mitralico
posteriore
226
• Trombo nell'apice del ventricolo sinistro con obliterazione della cavità
• Raramente, miocardite diffusa con dilatazione del
ventricolo sinistro e disfunzione sistolica
Ipertiroidismo o ipotiroidismo
• Versamento pericardico
• Disfunzione sistolica del ventricolo sinistro
Sindrome di Marfan
• Dilatazione dell'aorta ascendente
• Dilatazione dell'anulus aortico e del seno di Valsalva
• Dissezione aortica
• Prolasso valvolare mitralico
Distrofia muscolare (Duchenne)
• Fibrosi basale posteriore e laterale
Feocromocitoma
• Ipertrofia concentrica del ventricolo sinistro (20%)
• Miocardite (acuta) per crisi catecolaminica
Artrite reumatoide
• Versamento pericardico
• Pericardite costrittiva
• Granuloma cardiaco
Sarcoidosi
• Alterazione della cinesi parietale regionale
• Assottigliamento della parete basale e posterolaterale
• Aneurisma posterobasale
• Morfologia di tipo restrittivo
Sclerodermia
• Versamento pericardico
• Ipertensione polmonare
• Sclerosi valvolare
Lupus eritematoso sistemico
• Pericardite
• Tamponamento
• Miocardite
• Endocardite, Libman-Sacks
Sclerosi tuberosa
• Rabdomioma
• Cardiomiopatia
Cardiopatie da malattie sistemiche, infettive, da farmaci
B
A
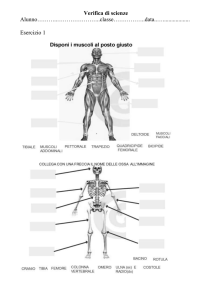
FIGURA 13.1
Amiloidosi. A: sezione istologica di un prelievo bioptico del miocardio colorato con «sulfated alcian blue». L’amiloide
(frecce) si deposita intorno alle miocellule. B: aspetto macroscopico che mostra l’infiltrazione di amiloide (frecce
bianche) e l’ispessimento delle pareti ventricolari sinistre. (Riproduzione autorizzata da Click RL, Olson LJ, Edwards
WD, et al. Echocardiography and systemic diseases. J Am Soc Echocardiogr 1994; 7: 201-16).
B
A
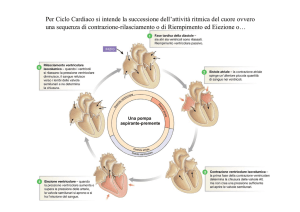
FIGURA 13.2
A: proiezione parasternale asse lungo che mostra aspetti tipici dell’amiloidosi cardiaca: ipertrofia concentrica del
ventricolo sinistro (LV), aspetto granulare del miocardio e ispessimento delle valvole. Il seno coronarico (CS,
freccia) è dilatato per l’aumentata pressione atriale destra. B: nella proiezione parasternale asse corto è visibile la
marcata ipertrofia concentrica del ventricolo sinistro. La freccia a doppia punta indica lo spessore (18 mm) del setto
interventricolare (VS). AV = valvola aortica; MV = valvola mitralica; PW = parete posteriore.
227
13
MANUALE
DI
ECOCARDIOGRAFIA
un movimento sistolico anteriore della mitrale e un’ostruzione intraventricolare, tipici della cardiomiopatia ipertrofica.5 Con il progredire della malattia, però, la funzione sistolica
si deteriora progressivamente.
Il Doppler a onda pulsata è utile nella valutazione delle alterazioni diastoliche dell’amiloidosi cardiaca. Il dato iniziale è l’alterato
rilasciamento dovuto all’ipertrofia ventricolare (disfunzione diastolica di grado 1); il pattern diviene di tipo restrittivo (disfunzione
diastolica di grado 3-4) quando la progressiva infiltrazione di amiloide riduce la distensibilità del ventricolo sinistro e aumenta la
pressione atriale sinistra6 (figura 13.4). Il
riempimento ventricolare può temporaneamente normalizzarsi («pseudonormalizzazione»; disfunzione diastolica di grado 2) per la
contemporanea presenza di alterato rilasciamento e aumentata pressione di riempimento atriale sinistra, prima di assumere un pattern francamente restrittivo. Il tempo di decelerazione (DT) è una delle più importanti
variabili diagnostiche della malattia.7 Un DT
breve peggiora la prognosi. La sopravvivenza
media dei pazienti con DT inferiore o uguale
a 150 ms è inferiore a 1 anno, rispetto ai 3 anni dei pazienti con DT superiore a 150 ms (figura 13.5). Pertanto l’ecocardiografia forni-
A
FIGURA 13.3
A: tracciato elettrocardiografico (ECG)
di una paziente di 78 anni con dispnea.
L’esame ecocardiografico è stato
eseguito nel sospetto di un infarto
miocardico anteriore. L’ECG mostra QRS
di basso voltaggio nelle derivazioni
periferiche e segni di pregresso infarto
miocardico anteriore.
L’ecocardiogramma mostrava un tipico
aspetto dell’amiloidosi cardiaca, che è
stata successivamente confermata con la
biopsia. B: ECG della stessa paziente,
eseguito 2 anni prima. Si può osservare
un’onda Q in D3, ma i voltaggi non sono
ridotti.
228
B
sce informazioni complete, sia morfologiche,
sia funzionali (funzione sistolica e diastolica),
sia prognostiche.
Carcinoide
La malattia cardiaca da carcinoide è dovuta a
una lenta crescita metastatica di un tumore di
solito localizzato all’ileo. Il coinvolgimento cardiaco avviene quasi esclusivamente ad opera
di metastasi epatiche che rilasciano serotonina e bradichinina. Poiché queste sostanze tumorali sono inattivate dal polmone, le strutture cardiache maggiormente interessate sono quelle destre; ma talvolta possono essere
colpite anche le sezioni sinistre (7% dei casi),
quando un forame ovale pervio consente il
passaggio di queste sostanze dall’atrio destro
al sinistro, oppure quando esistano metastasi
polmonari.8 L’aspetto patologico predominante è la fibrosi delle valvole, specialmente la
tricuspide e la polmonare, e dell’endocardio.9
L’ispessimento (fibrosi) e le ridotte escursioni valvolari sono responsabili di insufficienza
tricuspidale severa, di stenosi tricuspidale solitamente moderata e di stenosi polmonare di
vario grado (figure 13.6 e 13.7).
Questi aspetti sono facilmente individuabili
con eco 2D. La valvola tricuspidale è ispessita
13
Cardiopatie da malattie sistemiche, infettive, da farmaci
e retratta, con limitata mobilità e incompleta
coaptazione dei lembi; il rigurgito valvolare
che ne consegue determina sovraccarico di
volume del ventricolo destro con dilatazione
della cavità e movimento anomalo del setto interventricolare, se l’insufficienza tricuspidale
è severa. La valvola polmonare, anch’essa
ispessita e retratta, diviene progressivamente
stenotica; talvolta è difficile da visualizzare
con approccio transtoracico, per cui può essere necessaria una proiezione transesofagea
asse lungo del tratto di efflusso ventricolare
destro. Le pareti del ventricolo destro sono
generalmente di normale spessore, ma la ETE
potrebbe mostrare la presenza di una placca
carcinoide sopra l’endocardio delle camere di
Afflusso ventricolare sinistro
Afflusso ventricolare sinistro
B
A
Studio iniziale
6 mesi dopo
Studio iniziale
7 mesi dopo
FIGURA 13.4
Doppler spettrale dell’afflusso mitralico in due pazienti con amiloidosi cardiaca. A: inizialmente (a sinistra) il
Doppler mostrava un alterato rilasciamento con diminuzione dell’onda E, aumento dell’onda A e allungamento del
tempo di decelerazione (DT). Sei mesi dopo (a destra) lo spettro Doppler si pseudonormalizzava con il progredire
dell’amiloidosi cardiaca. B: in un altro paziente, il DT inizialmente (a sinistra) era di 190 ms con normale onda E ed
A. Sette mesi dopo (a destra) comparve il tipico aspetto di tipo restrittivo (aumento dell’onda E, diminuzione
dell’onda A e riduzione del DT) a indicare che l’aspetto iniziale era di pseudonormalizzazione. (Riproduzione
autorizzata da Klein AL, Hatle LK, Taliercio CP, et al. Serial Doppler echocardiographic follow-up of left ventricular
diastolic function in cardiac amyloidosis. J Am Coll Cardiol 1990; 16: 1135-41).
(1)
(23)
Sopravvivenza (%)
100
FIGURA 13.5
(19)
80
(8)
60
(4)
(7)
40
20
0
0,0
(4)
DT > 150 ms
E/A ≥ 2,1 (n=1)
DT ≤ 150 ms
E/A ≥ 2,1 (n=14)
DT > 150 ms
E/A < 2,1 (n=29)
DT ≤ 150 ms
E/A <2,1 (n=16)
0,5
1,0
1,5
Anni
2,0
2,5
Curve di sopravvivenza di pazienti con
amiloidosi cardiaca. I pazienti con
tempo di decelerazione (DT) inferiore o
uguale a 150 ms avevano una mortalità
del 50% a 1 anno, mentre la
sopravvivenza era del 90% se il DT
superava i 150 ms. (Riproduzione
autorizzata da Klein AL, Hatle LK,
Taliercio CP, et al. Prognostic
significance of Doppler measures of
diastolic function in cardiac amyloidosis:
a Doppler echocardiography study.
Circulation 1991; 83: 808-16).
229
MANUALE
DI
ECOCARDIOGRAFIA
destra. Un altro reperto è la metastasi miocardica8 (figura 13.8). Gli aspetti eco 2D della malattia cardiaca da carcinoide sono ben
definiti e facilmente distinguibili da altre patologie che determinano insufficienza ventricolare destra, come l’anomalia di Ebstein,
traumi e infarto del ventricolo destro, displasia della tricuspide, insufficienza tricuspidale
severa da alterazioni valvolari intrinseche. In
casi più rari, alterazioni valvolari simili a quelle da carcinoide possono derivare da un eccessivo uso di ergotamina o, più recentemente, di farmaci anoressizzanti («fen-phen»)
(vedi il paragrafo successivo).
Cardiopatie indotte da farmaci
Alcuni farmaci sono stati identificati come
agenti responsabili di cardiomiopatie e valvulopatie. È ben noto come la doxorubicina
(Adriamicina), un agente chemioterapico,
produca dilatazione e disfunzione sistolica
del ventricolo sinistro.10 La tossicità cardiaca
è in relazione con la dose somministrata ed è
potenziata dalla somministrazione, precedente o contemporanea, di radioterapia. Pa-
zienti che necessitano di chemioterapia con
doxorubicina dovrebbero essere sottoposti a
un primo esame ecocardiografico 2D di base
e a successivi controlli a intervalli di tempo regolari. La disfunzione sistolica del ventricolo
sinistro da doxorubicina può essere irreversibile e generalmente compare dopo una dose
superiore a 450 g/m2. Un analogo quadro di
cardiomiopatia è prodotto dalla daunorubicina (> 600 mg/m2) e dalla ciclofosfamide (> 6,2
g/m2).11 Il trattamento con ciclofosfamide può
provocare anche versamento pericardico o
tamponamento cardiaco. Una severa disfunzione ventricolare sinistra può essere inoltre
riscontrata in pazienti bulimici che ingeriscono sciroppo di ipecacuana:12 il principale
componente dell’ipecacuana, l’emetina, causa danno mitocondriale e inibizione della fosforilazione ossidativa. La terapia cronica con
steroidi ad alte dosi può causare disfunzione
sistolica del ventricolo sinistro; la funzione
cardiaca può essere compromessa inoltre dalle fenotiazine e dagli antidepressivi triciclici.
La tossicità da farmaci può coinvolgere
anche le valvole cardiache. Gli alcaloidi dell’ergotamina possono produrre lesioni valvo-
FIGURA 13.6
Carcinoide. A sinistra: reperto anatomopatologico di carcinoide cardiaco. I lembi della valvola polmonare sono
ispessiti, retratti ed accorciati, con apertura fissa. Si notino le placche di fibrosi endocardica (frecce). A destra: i
lembi della tricuspide e le corde tendinee sono ispessiti e retratti. (Riproduzione autorizzata da Click RL, Olson LJ,
Edwards WD, et al. Echocardiography and systemic diseases. J Am Soc Echocardiogr 1994; 7: 201-16).
230
Cardiopatie da malattie sistemiche, infettive, da farmaci
A
13
B
C
D
FIGURA 13.7
A: a sinistra, fotogramma sistolico 2D dell’afflusso
ventricolare destro che mostra il coinvolgimento della
tricuspide (TV) nella malattia da carcinoide. I lembi
anteriore e settale della tricuspide non collabiscono
perché retratti e ispessiti; ne deriva un’insufficienza
tricuspidale severa. A destra, immagine color Doppler
di un jet da insufficienza tricuspidale severa. B: Doppler
a onda continua del flusso transtricuspidale in soggetto
con carcinoide. La velocità del rigurgito tricuspidale è di
2,5 m/s, valore più alto di quello atteso per
un’insufficienza tricuspidale pura. Considerando una
pressione atriale destra (RA) di circa 20 mmHg, la
pressione sistolica del ventricolo destro è di 45 mmHg, a
causa di una moderata stenosi polmonare nel
carcinoide. La concavità (frecce) del profilo Doppler del
rigurgito tricuspidale corrisponde all’onda «V», a causa
del rigurgito severo; di conseguenza la velocità di flusso
anterogrado tricuspidale è aumentata. C: proiezione
parasternale asse corto a livello della valvola polmonare
interessata dal carcinoide. L’anulus (freccia) è ristretto
e la valvola è retratta. Ao = aorta; PA = arteria
polmonare; RA = atrio destro. D: moderata stenosi
polmonare rilevata dal Doppler a onda continua; la
velocità massima è 2 m/s e il flusso rigurgitante ha un
tempo di decelerazione molto breve, per il rapido
azzeramento del gradiente pressorio (freccia verso il
basso) fra ventricolo destro e arteria polmonare. Inoltre
si osserva un flusso diastolico (freccia verso l’alto)
polmonare dovuto a una rapida ascesa della pressione
diastolica nel ventricolo destro.
FIGURA 13.8
Metastasi miocardica
(M) nella parete del
ventricolo sinistro
(LV) in un uomo di 61
anni con carcinoide
della tricuspide e della
polmonare,
confermati dal reperto
autoptico.
(Riproduzione
autorizzata da Pellikka
PA, Tajik AJ,
Khandheria BK, et al.
Carcinoid heart
disease: clinical and
echocardiographic
spectrum in 74
patients. Circulation
1993; 87: 1188-96).
231
MANUALE
DI
ECOCARDIOGRAFIA
lari simili a quelle della malattia reumatica o
del carcinoide.13 Nei pazienti che hanno assunto alcaloidi dell’ergotamina, i reperti ecocardiografici 2D sono simili a quelli delle patologie sopracitate, ma l’esame microscopico
mostra placche fibrose adese su valvole relativamente normali. Farmaci anoressizzanti
sono stati individuati come causa di valvulopatie e/o ipertensione polmonare. In Europa,
negli ultimi anni ’60 e all’inizio degli anni ’70,
è stato dimostrato che l’aminorex era causa di
ipertensione polmonare. Più recentemente,
un lavoro di Connolly et al.14 condotto nel nostro istituto ha riscontrato la presenza di insufficienza aortica, mitralica o tricuspidale in
24 pazienti che avevano assunto «fen-phen»
(figura 13.9). Le implicazioni di questi dati sono potenzialmente enormi in quanto è noto
che dai 4 ai 6 milioni di persone nel mondo sono state esposte a fenfluramina e dexfenfluramina con o senza phentermina. Studi successivi hanno documentato un’incidenza tra
l’8% e il 30% di insufficienza mitralica in pazienti che hanno assunto «fen-phen» per vari periodi di tempo; insufficienza valvolare o
ipertensione polmonare sono state riscontrate in pazienti che hanno assunto tale farmaco
per meno di 1 mese. Qualora i pazienti che abbiano assunto fenfluramina e dexfenfluramina con o senza phentermina sviluppino sintomi o segni di insufficienza valvolare, viene
posta l’indicazione all’esecuzione di un esame
ecocardiografico. Un’insufficienza valvolare
può essere considerata associata all’assunzione di «fen-phen» qualora l’esame ecocardiografico dimostri la presenza di insufficien-
B
A
C
FIGURA 13.9
A: reperto anatomico di una valvola mitralica di una donna di 45 anni che aveva assunto farmaci anoressizzanti con
«fen-phen» per 11 mesi. I lembi e le corde tendinee sono lucenti e ispessiti. B: reperto istologico di una valvola
mitralica di una donna di 44 anni che aveva assunto terapia anoressizzante con «fen-phen» per 12 mesi. La struttura
valvolare è integra, ma presenta placche «adese» sulla superficie (frecce). C: aspetti ecocardiografici tipici di una
valvola mitralica dopo trattamento con «fen-phen». Sia la valvola aortica (AV) che mitralica (MV) sono ispessite; il
lembo anteriore mitralico (freccia) presenta un movimento a cupola in diastole, come nella valvulopatia reumatica. Il
color Doppler mostra insufficienza aortica severa (AR). (B: riproduzione autorizzata da Connolly HM, Crary JL,
McGoon MD, et al. Valvular heart disease associated with fenfluramine-phentermine. N Engl J Med 1997; 337: 581-8).
232
Cardiopatie da malattie sistemiche, infettive, da farmaci
za aortica modesta o insufficienza mitralica di
grado moderato; il riscontro di insufficienza
aortica è più comune di quello di insufficienza mitralica.
Emocromatosi
L’emocromatosi idiopatica è una malattia autosomica recessiva con incidenza del 2-3 per
1000. È caratterizzata da una vasta deposizione di ferro in vari organi, tra cui cuore, fegato, testicoli e pancreas. Quando è il cuore
ad essere interessato, la malattia è di solito in
uno stadio avanzato e ha coinvolto molti organi. La severità della disfunzione miocardica
è proporzionale alla quantità di ferro che si
deposita nel miocardio e che altera la funzione contrattile delle miocellule determinando
disfunzione sistolica e dilatazione del ventricolo sinistro come nella cardiomiopatia dilatativa (figura 13.10). La causa di morte più
frequente nei pazienti con emocromatosi è
l’insufficienza cardiaca ingravescente. Nei pazienti che presentano insufficienza cardiaca e
A
un quadro di cardiomiopatia dilatativa di eziologia sconosciuta, è importante valutare il dosaggio del ferro, la capacità di legare il ferro e
il livello di ferritina sierica. Gli aspetti eco 2D
dell’emocromatosi cardiaca sono: moderata
dilatazione ventricolare sinistra, disfunzione
sistolica del ventricolo sinistro, normale spessore parietale e normale aspetto delle valvole, dilatazione biatriale15 (figura 13.11). Alla
dilatazione delle camere cardiache conseguono vari gradi di insufficienza valvolare tricuspidale e mitralica. Alla Mayo Clinic il 37%
dei pazienti con emocromatosi presentava
un quadro di insufficienza cardiaca congestizia con riempimento diastolico ventricolare
sinistro di tipo restrittivo, con aspetto morfologico da cardiomiopatia dilatativa.15 La maggior parte di questi malati è morta entro 6 mesi, ma la disfunzione del ventricolo sinistro
può essere reversibile, a volte anche completamente, praticando frequenti salassi. È pertanto utile seguire nel tempo la funzione ventricolare sinistra con ecocardiografia.
B
FIGURA 13.10
Emocromatosi. A: reperto bioptico che mostra la deposizione di ferro (pigmentazione nera) all’interno dei miociti
(frecce). B: reperto autoptico tipico di cardiopatia dilatativa da emocromatosi cardiaca con caratteristica colorazione
ferro-ruggine. (Riproduzione autorizzata da Click RL, Olson LJ, Edwards WD, et al. Echocardiography and systemic
diseases. J Am Soc Echocardiogr 1994; 7: 201-16).
233
13
MANUALE
DI
ECOCARDIOGRAFIA
Immunodeficienza da infezione
virale nell’uomo
Nei pazienti affetti da immunodeficienza acquisita da infezione virale sono state descritte varie patologie del sistema cardiovascolare, tra cui il versamento pericardico, il tamponamento cardiaco, la cardiomiopatia dilatativa, l’ipertensione polmonare, l’endocardite e
i tumori cardiaci16-17 (figura 13.12). Uno studio prospettico eseguito con esami ecocardiografici seriati ha mostrato che l’incidenza
di versamento pericardico in pazienti, sopravvissuti, con immunodeficienza acquisita raggiunge l’11% per anno. Il versamento pericardico è generalmente modesto e asintomatico;
tuttavia è stato dimostrato che la sopravvivenza è più breve nei pazienti in cui il versamento pericardico si sviluppa indipendentemente dai livelli sierici di albumina e di CD4.17
l’interessamento di alcuni organi; molto comune è l’interessamento del cuore, sia nelle
sezioni destre che sinistre, con ispessimento
endocardico nelle aree di afflusso e obliterazione fibrotrombotica degli apici ventricolari.
Gli aspetti ecocardiografici tipici sono: ridotto movimento del lembo mitralico posteriore
(che determina insufficienza valvolare di vario grado) con ispessimento della parete inferobasale del ventricolo sinistro, lesioni fibrotrombotiche dell’endocardio e obliterazione
trombotica degli apici18 (figura 13.13). Questi
due ultimi fattori sono alla base della riduzione sia della distensibilità ventricolare che del
riempimento diastolico, quindi di un quadro
Doppler di tipo restrittivo. Più raramente la
crisi ipereosinofila acuta causa una miocardite diffusa con dilatazione ventricolare e marcata riduzione della funzione sistolica; la morte avviene di solito per insufficienza cardiaca
severa oppure per aritmie ventricolari.
Sindrome da ipereosinofilia
Cardiopatie indotte da radiazioni
La sindrome da ipereosinofilia è caratterizzata dalla presenza di un’elevata concentrazione di eosinofili (superiore a 1500/mm3) e dal-
FIGURA 13.11
Ecocardiogramma 2D (proiezione
parasternale asse corto) di emocromatosi
cardiaca; l’aspetto è simile a quello della
cardiomiopatia dilatativa. VS = setto
interventricolare.
FIGURA 13.12
Immagine ecocardiografica transtoracica,
proiezione parasternale asse lungo (a sinistra) e
asse corto (a destra), che evidenzia una
cardiomiopatia dilatativa e versamento pericardico
(PE) in un paziente giovane con sindrome da
immunodeficienza acquisita (AIDS).
234
Radiazioni al mediastino possono danneggiare le arterie coronarie, il pericardio, le valvo-
Cardiopatie da malattie sistemiche, infettive, da farmaci
le cardiache o il miocardio e causare stenosi
coronariche prossimali, versamento pericardico, pericardite costrittiva, insufficienza valvolare, cardiomiopatia restrittiva o tali patologie in associazione. Il danno valvolare indotto da radiazioni si manifesta con ispessimento e insufficienza valvolare, che interessa prevalentemente la tricuspide. Una
manifestazione cardiaca più severa è costituita dall’insufficienza del cuore destro per
pericardite costrittiva o cardiomiopatia restrittiva o entrambe. Parametri eco Doppler
di patologia costrittiva e restrittiva vengono
discussi in dettaglio nel capitolo 14.
Insufficienza renale
I pazienti affetti da insufficienza renale cronica sono generalmente ipertesi; in tali pazienti il principale reperto ecocardiografico è
costituito dall’aumento degli spessori parietali del ventricolo sinistro. L’aspetto del miocardio nell’ipertrofia ventricolare sinistra mostra caratteristiche simili a quelle dell’amiloi-
dosi, ma queste due entità patologiche possono essere distinte l’una dall’altra. L’insufficenza renale cronica è associata a ipertrofia
ventricolare sinistra e amiloidosi con riduzione dei voltaggi elettrocardiografici. Nell’insufficienza renale, anche se la funzione sistolica è normale nei primi stadi della malattia, si
ha una ridotta funzione diastolica e ridotto
rilasciamento del miocardio. Negli stadi più
avanzati di tale patologia, con la riduzione
della distensibilità miocardica si ha un aumento della pressione di riempimento del
ventricolo sinistro, e il pattern di riempimento diastolico può assumere un aspetto di
pseudonormalizzazione o di tipo restrittivo.
La funzione sistolica del ventricolo sinistro
può diminuire in caso di ipertensione presente da molti anni. È di frequente riscontro
la presenza di piccoli versamenti pericardici,
soprattutto in pazienti sottoposti a emodialisi. L’insufficienza renale cronica comunemente causa sclerocalcificazione delle valvole; anche l’anulus mitralico può presentare
calcificazioni.
B
A
FIGURA 13.13
Proiezioni quattro camere apicali di due pazienti con sindrome ipereosinofila; è presente obliterazione dell’apice per
depositi eosinofili e trombotici. La contrattilità miocardica sottostante non è alterata. A: rispetto al fotogramma
diastolico (a sinistra), in quello sistolico (a destra) si osserva un ispessimento notevole delle pareti. Il materiale
trombotico oblitera solo l’apice. La diagnosi differenziale andrebbe fatta con la cardiomiopatia ipertrofica
coinvolgente l'apice, in cui l’apice è obliterato dal miocardio ipertrofico, ma presenta ancora una piccola cavità (a
forma di fessura) nel contesto di un miocardio iperdinamico. B: sia l’apice del ventricolo sinistro (LV) che del destro
(RV) sono obliterati dal trombo (frecce).
235
13
MANUALE
DI
ECOCARDIOGRAFIA
Sarcoidosi
La sarcoidosi è una malattia granulomatosa
ad eziologia sconosciuta, che coinvolge più organi, in particolare il polmone, dove causa
una fibrosi diffusa, insufficienza del cuore destro e ipertensione polmonare.19 Più raro è
l’interessamento cardiaco (meno del 20% dei
pazienti) che si manifesta con un quadro di fibrosi miocardica e alterazioni della cinesi parietale regionale dovute a granulomi non caseosi nel miocardio. La fibrosi colpisce prevalentemente le porzioni medie e basali del ventricolo sinistro, ma può interessare anche tutto il ventricolo. Ne consegue assottigliamento
parietale e formazione di sacche aneurismatiche soprattutto nelle porzioni basali inferiori
e laterali del ventricolo sinistro. Tutti questi
aspetti sono visibili all’eco 2D,20 ma la loro
presenza è stata rilevata solo nel 14% dei pazienti con sarcoidosi esaminati alla Mayo Clinic; i sintomi di insufficienza congestizia sono
più comuni in questi pazienti.20 La diagnosi di
sarcoidosi si basa sul dosaggio dell’enzima di
conversione dell’angiotensina (ACE), ma
molti pazienti con quadri ecocardiografici di
coinvolgimento cardiaco avevano livelli normali di ACE e granulomi non caseosi nelle biopsie endomiocardiche. Pertanto un normale
dosaggio di ACE non esclude la sarcoidosi in
fase attiva sul cuore; per formulare la diagnosi si dovrebbe eseguire una biopsia.
Sclerodermia
La patologia cardiaca più comunemente associata alla sclerodermia è costituita dalla lesione pericardica, riscontrabile nel 78% circa
dei pazienti.21 È di comune riscontro la presenza di versamento pericardico, anche se
questo difficilmente raggiunge il tamponamento cardiaco che richiede pericardiocentesi. Una delle maggiori complicanze della sclerodermia è costituita dall’ipertensione polmonare, che causa dispnea. In tutti i pazienti
con sclerodermia dovrebbe essere misurata la
velocità di rigurgito tricuspidale. Il miocardio
236
può essere coinvolto con fibrosi o sclerosi, e
questo comporta una disfunzione sistolica o
diastolica. Dunque, in pazienti con sclerodermia una valutazione della funzione diastolica
e sistolica dovrebbe costituire parte fondamentale della valutazione ecocardiografica.
Sepsi
Nei pazienti con sepsi o shock settico è frequente il riscontro di ridotta frazione di eiezione e di dilatazione del ventricolo sinistro.22
Pazienti che sopravvivono a uno shock settico presentano una ridotta frazione di eiezione.23 Nei pazienti sopravvissuti, la dilatazione
del ventricolo sinistro e la disfunzione sistolica sono reversibili. Non è chiara la causa di disfunzione miocardica dovuta a sepsi; potrebbe essere legata a fattori circolanti con effetto depressivo sul miocardio, come endotossine, fattori tumorali di necrosi o interleuchine.
Nei pazienti con sepsi è di frequente riscontro, all’esame ecocardiografico, la dilatazione
del ventricolo sinistro e la ridotta frazione di
eiezione. Tuttavia, a causa delle ridotte resistenze vascolari sistemiche, la gittata sistolica si mantiene normale (l’integrale tempo-velocità del tratto di efflusso del ventricolo sinistro e la velocità sono normali). Alcune infezioni presentano caratteristiche anomalie
cardiache ed ecocardiografiche: nell’echinococcosi e nella tubercolosi è possibile rilevare la presenza di una massa intracardiaca (vedi capitolo 16); infezioni virali, batteriche o
tubercolotiche sono associate a pericardite;
la malattia di Chagas è associata ad aneurismi
ventricolari.
La malattia di Chagas (tripanosomiasi
americana) è poco conosciuta in Nord America, ma è endemica in tutti i paesi latinoamericani. Nei pazienti infetti, il tessuto muscolare
cardiaco è invaso dal parassita protozoario
Trypanosoma cruzi, responsabile di caratteristiche anomalie: dilatazione di entrambi i
ventricoli, aneurisma ventricolare, assottigliamento delle pareti cardiache e trombi intramurali.24 Anche il sistema di conduzione
Cardiopatie da malattie sistemiche, infettive, da farmaci
viene interessato, determinando anomalie di
conduzione. L’immigrazione ha portato nel
Nord America un numero crescente di persone affette da Trypanosoma cruzi; per tale
motivo è importante che medici e sonografisti
conoscano gli aspetti ecocardiografici di questa malattia infettiva.
Spondiloartropatie
Le spondiloartropatie che presentano coinvolgimento cardiaco sono la spondilite anchilosante e la sindrome di Reiter. Le manifestazioni cardiache della spondilite anchilosante
sono insufficienza aortica, versamento pericardico e anomalie di conduzione; l’insufficienza aortica è causata dall’ispessimento
delle cuspidi valvolari, dalla dislocazione delle cuspidi provocata dal tessuto fibroso e dalla dilatazione dell’anello aortico. L’insufficienza aortica può essere di grado severo e
necessitare della correzione chirurgica. Nei
pazienti con sindrome di Reiter o artrite psoriasica è possibile osservare anche insufficienza aortica e dilatazione dell’aorta.
Lupus eritematoso sistemico
Il lupus è una malattia sistemica da immunocomplessi per la presenza di anticorpi antinucleo (ANA), che causano reazioni infiammatorie in vari organi. Per quanto riguarda il
cuore, il coinvolgimento maggiore è la pericardite (in oltre i due terzi dei pazienti), per
cui un criterio diagnostico della malattia è il riscontro ecocardiografico di versamento pericardico. Più rari invece sono il tamponamento o la pericardite costrittiva. Il miocardio può
essere interessato da un processo vasculitico
responsabile di un quadro di miocardite, ma è
raro trovare una significativa disfunzione sistolica del ventricolo sinistro. Altra lesione caratteristica è l’endocardite di LibmanSacks con verruche valvolari di solito sulla mitrale,25 generalmente nella porzione basale
con possibile estensione alle corde e ai muscoli papillari (figura 13.14). Non è invece co-
13
mune il coinvolgimento dell’aorta. Le lesioni
endocarditiche sono scarsamente visibili con
l’eco transtoracica, mentre il loro rilievo è facilitato dall’approccio transesofageo. Le valvole cardiache sono interessate anche da metastasi tumorali, che producono lesioni simili
a quelle osservate nell’endocardite di LibmanSacks; tale patologia, denominata endocardite marantica, è comune nel morbo di Hodgkin, nell’adenocarcinoma del polmone, del
pancreas, dello stomaco e del colon.
Altre patologie
Molte malattie sistemiche, reumatiche, endocrine, genetiche e infettive interessano il
cuore. Sia il feocromocitoma che la malattia di
Friedreich determinano un’ipertrofia concentrica del ventricolo sinistro.26 27 L’atassia di
Friedreich è una malattia autosomica recessiva che causa atassia cerebellare e, nel 90%
dei pazienti, anche un interessamento cardiaco; nella maggior parte dei casi gli aspetti
ecocardiografici sono simili alla cardiomiopatia ipertrofica, ma l’ipertrofia del ventricolo sinistro è più spesso concentrica mentre sono
insolite sia l’ipertrofia asimmetrica del setto
che l’ostruzione all’efflusso ventricolare sinistro. In una piccola parte (7%) dei pazienti il
ventricolo sinistro è dilatato e la funzione sistolica è ridotta per fibrosi interstiziale diffu-
FIGURA 13.14
Endocardite di
Libman-Sacks in una
donna di 36 anni con
lupus eritematoso
sistemico, senza segni
clinici di endocardite
batterica. Il fotogramma
diastolico, nella
proiezione orizzontale
transesofagea della
mitrale, mostra ampie
vegetazioni verrucose
(frecce).
237
MANUALE
DI
ECOCARDIOGRAFIA
sa.15 La maggior parte dei pazienti con feocromocitoma presenta un quadro ecocardiografico normale, fatta eccezione per una funzione sistolica iperdinamica e occasionalmente un’ipertrofia concentrica del ventricolo sinistro.26 La crisi catecolaminica può provocare miocardite acuta con dilatazione del
ventricolo sinistro e riduzione della funzione
sistolica, peraltro reversibile con il trattamento del feocromocitoma.
Anche alcune malattie neuromuscolari
colpiscono il miocardio, come la distrofia di
Duchenne che determina la fibrosi del segmento inferobasale, con aspetti ecocardiografici simili a quelli dell’infarto miocardico
inferiore. I pazienti con ipotiroidismo e più raramente quelli con ipertiroidismo possono
sviluppare una cardiomiopatia dilatativa che
si risolve con la correzione dell’alterazione
endocrina.
Bibliografia
1. Siqueira-Filho AG, Cunha CL, Tajik AJ,
Seward JB, Schattenberg TT, Giuliani ER.
M-mode and two-dimensional echocardiographic features in cardiac amyloidosis. Circulation 1981; 63: 188-96.
2. Gertz MA, Grogan M, Kyle RA, Tajik AJ.
Endomyocardial biopsy-proven light
chain amyloidosis (AL) without echocardiographic features of infiltrative cardiomyopathy. Am J Cardiol 1997; 80: 93-5.
3. Roberts WC, Waller BF. Cardiac amyloidosis causing cardiac dysfunction: analysis of 54 necropsy patients. Am J Cardiol
1983; 52: 137-46.
4. Olson LJ, Reeder GS, Noller KL, Edwards
WD, Howell RR, Michels VV. Cardiac involvement in glycogen storage disease
III: morphologic and biochemical characterization with endomyocardial biopsy.
Am J Cardiol 1984; 53: 980-1.
5. Oh JK, Tajik AJ, Edwards WD, Bresnahan
JF, Kyle RA. Dynamic left ventricular outflow tract obstruction in cardiac amyloi-
238
6.
7.
8.
9.
10.
11.
12.
13.
14.
dosis detected by continuous-wave Doppler echocardiography. Am J Cardiol
1987; 59: 1008-10.
Klein AL, Hatle LK, Taliercio CP, et al. Serial Doppler echocardiographic follow-up
of left ventricular diastolic function in
cardiac amyloidosis. J Am Coll Cardiol
1990; 16: 1135-41.
Klein AL, Hatle LK, Taliercio CP, et al.
Prognostic significance of Doppler measures of diastolic function in cardiac amyloidosis: a Doppler echocardiography
study. Circulation 1991; 83: 808-16.
Pellikka PA, Tajik AJ, Khandheria BK, et
al. Carcinoid heart disease: clinical and
echocardiographic spectrum in 74 patients. Circulation 1993; 87: 1188-96.
Callahan JA, Wroblewski EM, Reeder GS,
Edwards WD, Seward JB, Tajik AJ. Echocardiographic features of carcinoid heart
disease. Am J Cardiol 1982; 50: 762-8.
Bristow MR, Mason JW, Billingham ME,
Daniels JR. Doxorubicin cardiomyopathy: evaluation by phonocardiography,
endomyocardial biopsy, and cardiac
catheterization. Ann Intern Med 1978;
88: 168-75.
Gottdiener JS, Appelbaum FR, Ferrans
VJ, Deisseroth A, Ziegler J. Cardiotoxicity
associated with high-dose cyclophosphamide therapy. Arch Intern Med 1981; 141:
758-63.
Schiff RJ, Wurzel CL, Brunson SC, Kasloff
I, Nussbaum MP, Frank SD. Death due to
chronic syrup of ipecac use in a patient
with bulimia. Pediatrics 1986; 78: 412-6.
Redfield MM, Nicholson WJ, Edwards
WD, Tajik AJ. Valve disease associated
with ergot alkaloid use: echocardiographic and pathologic correlations. Ann Intern Med 1992; 117: 50-2.
Connolly HM, Crary JL, McGoon MD, et
al. Valvular heart disease associated with
fenfluramine-phentermine. N Engl J Med
1997; 337: 581-8.
Cardiopatie da malattie sistemiche, infettive, da farmaci
15. Olson LJ, Baldus WP, Tajik AJ. Echocardiographic features of idiopathic hemochromatosis. Am J Cardiol 1987; 60: 885-9.
16. Hoit BD, Ramrakhyani K. Pulmonary venous flow in cardiac tamponade: influence of left ventricular dysfunction and the
relation to pulsus paradoxus. J Am Soc
Echocardiogr 1991; 4: 559-70.
17. Heidenreich PA, Eisenberg MJ, Kee LL,
et al. Pericardial effusion in AIDS: incidence and survival. Circulation 1995; 92:
3229-34.
18. Gottdiener JS, Maron BJ, Schooley RT,
Harley JB, Roberts WC, Fauci AS. Two-dimensional echocardiographic assessment of the idiopathic hypereosinophilic
syndrome: anatomic basis of mitral regurgitation and peripheral embolization.
Circulation 1983; 67: 572-8.
19. Newman LS, Rose CS, Maier LA. Sarcoidosis. N Engl J Med 1997; 336:1224-34.
20. Burstow DJ, Tajik AJ, Bailey KR, DeRemee RA, Taliercio CP. Two-dimensional
echocardiographic findings in systemic
sarcoidosis. Am J Cardiol 1989; 63: 478-82.
21. Byers RJ, Marshall DA, Freemont AJ. Pe-
22.
23.
24.
25.
26.
27.
ricardial involvement in systemic sclerosis. Ann Rheum Dis 1997; 56: 393-4.
Bunnell E, Parrillo JE. Cardiac dysfunction during septic shock. Clin Chest Med
1996; 17: 237-48.
Parker MM, Suffredini AF, Natanson C, et
al. Responses of left ventricular function
in survivors and nonsurvivors of septic
shock. J Crit Care 1989; 4: 19-25.
Kirchhoff LV. American trypanosomiasis
(Chagas disease) – a tropical disease now
in the United States. N Engl J Med 1993;
329: 639-44.
Libman E, Sacks B. A hitherto undescribed form of valvular and mural endocarditis. Arch Intern Med 1924; 33: 701-38.
Shub C, Williamson MD, Tajik AJ, Eubanks DR. Dynamic left ventricular outflow tract obstruction associated with
pheochromocytoma. Am Heart J 1981;
102: 286-90.
Alboliras ET, Shub C, Gomez MR, et al.
Spectrum of cardiac involvement in Friedreich’s ataxia: clinical, electrocardiographic and echocardiographic observations.
Am J Cardiol 1986; 58: 518-24.
239
13