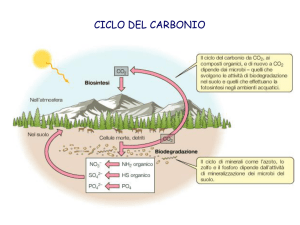
CICLO DEL CARBONIO 1. L’anidride carbonica è incorporata, o fissata, nei composti organici dai
fotoautotrofi e dai chemoautotrofi.
2. Questi composti organici rappresentano i nutrienti per i chemoeterotrofi.
3. I chemoeterotrofi rilasciano CO2 che è utilizzata dagli autotrofi.
4. Il carbonio è rimosso dal ciclo quando è incorporato in CaCO3 e
combustibile fossile.
La maggior parte del C degli organismi viene dalla CO2 dell’aria.
L’atmosfera ne contiene lo 0.03 %.
La più grande riserva di C non è l’atmosfera ma la crosta terrestre e
non è accessibile agli organismi. Ci sono essenzialmente 4 reazioni
coinvolte nel ciclo del C che devono bilanciarsi in natura. Queste sono
l’assorbimento e l’evoluzione della CO2 e del metano CH4.
PRIMA TAPPA DELLA DEGRADAZIONE DELLA S.O.
Tra i più importanti batteri del suolo eterotrofi:
Attinomiceti (Streptomyces, G+ aerobio filamentoso, rappresenta dal 5
al 20% dei coltivabili), Bacillus (G+ aerobio, rappresenta 2-10% dei
coltivabili), Clostridium (G+ anaerobio), Arthrobacter (aerobio, fino al
40% dei batteri coltivabili), Pseudomonas (G- , rappresenta 10-20% dei
coltivabili).
La fissazione del Carbonio comporta la incorporazione del carbonio dalla
anidride carbonica in molecole organiche.
A. FISSAZIONE DI CO2 .
La fissazione fotosintetica del C è responsabile della grande
maggioranza del C fissato in natura. Coinvolge l’uso dell’energia luminosa
per fissare il C negli zuccheri (e successivamente nelle altre molecole
biologiche):
CO2 + H2O + energia -----> (CH2O)n + O2
La fissazione fotosintetica del C può avvenire in ambiente aerobio o anaerobio.
Nella reazione descritta, l’uso dell’acqua come donatore di elettroni ha come
risultato la formazione di ossigeno. Questo tipo di reazione è portata avanti da
organismi ossigenici come alghe, cianobatteri, e piante verdi. Donatori di
elettroni alternativi sono utilizzati da altri fissatori di C fotosintetici, come i
batteri sulfurei fototrofi verdi e rossi, che vivono in un ambiente anossigenico.
Distinguiamo due gruppi di organismi:
Fototrofi
aerobi - cianobatteri, alghe, piante verdi
anaerobi – batteri fototrofi verdi e rossi
Litotrofi
batteri che ossidano substrati inorganici – idrogeno batteri, batteri nitrificanti,
solfo ossidanti.
(CH2O)n + O2 -----> CO2 + H2O + energia
La Respirazione comporta l’ossidazione dei carboidrati
per ottenere energia. Può avvenire in ambiente aerobio o
anaerobio. Nella reazione descritta, l’ossigeno serve come
accettore di elettroni, e si ha la formazione di acqua.
Questa reazione avviene in tutti gli organismi viventi in
ambienti aerobi, compresi piante, animali e microorganismi.
Questa reazione è l’inverso della reazione di fissazione del
C in ambiente aerobio. Accettori di elettroni alternativi
sono usati dagli organismi che effettuano una respirazione
anaerobia in ambienti anossici.
La Fermentazione è un processo portato avanti dai
microrganismi in ambienti anossici, dove l’energia è
ottenuta dalla parziale ossidazioone delle molecole
organiche.
I PIU’ COMUNI POLIMERI VEGETALI
COMPONENTE
% IN PESO SECCO DELLA PIANTA
Cellulosa
Emicellulosa
Lignina
Proteine e acidi nucleici
15-60
10-30
5-30
2-15
A QUESTI SI DEVONO AGGIUNGERE: Chitina e Peptidoglicano
COMPOSIZIONE DI DIVERSI MATERIALI LIGNOCELLULOSICI
COMPONENTE
FAGGIO ABETE PAGLIA RISO PAGLIA GRANO
% IN PESO SECCO DELLA PIANTA
Cellulosa
Emicellulosa
Lignina
47-48
30-33
21-24
42-44
27-28
26-30
36-38
28-30
11-12
40-41
28-29
16-17
PRIMA TAPPA DELLA DEGRADAZIONE DELLA S.O.
Tra i più importanti batteri del suolo eterotrofi:
Attinomiceti (Streptomyces, G+ aerobio filamentoso, rappresenta dal 5
al 20% dei coltivabili), Bacillus (G+ aerobio, rappresenta 2-10% dei
coltivabili), Clostridium (G+ anaerobio), Arthrobacter (aerobio, fino al
40% dei batteri coltivabili), Pseudomonas (G- , rappresenta 10-20% dei
coltivabili).
BIOMASSA DEI MAGGIORI COMPONENTI DEL BIOTA IN UN
SUOLO TEMPERATO COLTIVATO A PRATO
SOIL BIOTA
BIOMASSA (ton/ha)
Radici piante
Batteri
Attinomiceti
Funghi
Protozoi
Nematodi
Lombrichi
Altri animali
fino a 90, ma generalmente circa 20
1-2
0-2
2-5
0-0.5
0-0.2
0-2.5
0-0.5
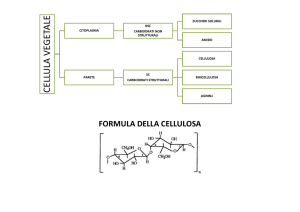
CELLULOSA
- Il + abbondante polimero di origine vegetale, costituente della parete
piante, alghe, alcuni funghi
MOLECOLA LINEARE, COMPOSTA DA 1.000-10.000 SUBUNITA' DI
GLUCOSIO - PESO MOLECOLARE: CIRCA 1.8x106
Insolubile in acqua
IN NATURA LA MAGGIOR PARTE E' DEGRADATA IN AEROBIOSI:
C6H12O6+6H2O = 6CO2+6H2O
I microrganismi cellulosolitici, sono in natura sempre associati ad altri
non cellulosolitici, che utilizzano il glucosio, rimuovendolo dal substrato ed
impedendo la inibizione della degradazione.
Esempio: Sporocytophaga sp. ed un batterio non cellulosolitico come
Flavobacterium sp., vivono in consorzio. Isolati in co-coltura da fanghi,
trasferita la co-coltuta per mesi in lab., è stabile. E molto più efficiente
della Sporocytophaga da sola.
La degradazione della cellulosa dipende dalla azione sinergica dei 3 enzimi.
Cooperazione tra ENDO di un organismo e la ESO di un altro.
Es. Trichoderma koningi e Fusarium solani
ENZIMI EXTRACELLULARI - INDUCUBILI
Glucosio prodotto finale, causa la repressione da cataboliti della
produzione di ENDO, alla concentrazione di 50 mg/l.
I tre principali enzimi per la degradazione della cellulosa:
(1) Una endoglucanasi (endo-ß-1,4-glucanasi), che agisce a caso all’interno
della catena di cellulosa, rompendo le molecole in frammenti più piccoli. Questo
enzima si trova in diverse forme –da circa 11.000 a 65.000 Da.
(2) Una esoglucanasi (eso-ß-1,4-glucanasi o cellobiohydrolase) che agisce
solo alle estremità della catena, rilasciando unità di cellobiosio. Questo enzima è
più uniforme della endoglucanasi, e va da 50,000 a 60,000 Da.
(3) ß-glucosidasi (o ‘cellobiasi’), che rompe il disaccaride cellobiosio in due
molecole di glucosio, che può essere assorbito dal fungo. Questo è un enzima
legato alla parete, come molti enzimi coinvolti negli stadi finali della degradazione
dei polimeri.
I tre enzimi agiscono sinergicamente e sono strettamente regolati, per assicurare che un fungo
che degrada la cellulosa non rilasci zuccheri ad un tasso più veloce di quello di assorbimento.
Le endoglucanasi, attaccando le catene di cellulosa a random, progressivamente creano più
estremità libere sulle quali può agire la cellobioidrolasi.
Il cellobiosio prodotto può legarsi al sito attivo della cellobioidrolasi, e inibire competitivamente
l’azione enzimatica. Così, se il cellobiosio si accumula, il tasso di degradazione della cellulosa
diminuisce automaticamente, and questo tipo di regolazione lega il tasso di degradazione al
tasso di assorbimento ed utilizzazione del glucosio da parte del fungo.
Inoltre, la regolazione della degradazione della cellulosa è ottenuta attraverso il sistema
comunemente utilizzato a feedback, chiamato repressione da cataboliti, in cui i geni che
codificano per gli enzimi sono repressi quando substrati più prontamente utilizzabili (come il
glucosio) sono disponibili nell’ambiente.
IL 5-10% DELLA CELLULOSA E' COVERTITA ANAEROBICAMENTE IN METANO:
C6H12O6 = 3CH4+3CO2
ALCUNI MICRORGANISMI CAPACI DI UTILIZZARE LA CELLULOSA
FUNGHI
BATTERI
Chaetomium cellulolyticum
Aerobi
Humicola grisea
Cellulomonas
Thrichoderma reesei
Bacillus
Trichoderma koningii
Cellvibrio
Polyporus versicolor
ATTINOMICETI
Cytophaga
Anaerobi
Clostridium cellobioparum
Clostridium thermocellum
Streptomyces
Micromonospora
Nocardia
Thermoactinomyces e Thermomonospora più efficienti di T. viride, attivi anche a 65°C.
BATTERI ANAEROBI
Dove? Rumine, digestori di fanghi, terreno, compost, sedimenti marini.
Acetovibrio cellulolyticus, anaerobio obbligato, attivo a temperature da 20 a 40°C. Prodotti finali:
H2, CO2, acetato, tracce etanolo, butanolo, fino a CH4.
CO2+4H2 = CH4+2H2O
2CO2+4H2 = CH3COOH+2H2O
METANOBATTERI
ACETOGENICI
l'ACETATO, FORMATO DIRETTAMENTE DALLA CELLULOSA PER FERMENTAZIONE, è UN
PRECURSORE DEL CH4 in anaerobiosi.
ACETATO CONVERTITO IN CH4 E CO2 DAI METANOGENI Methanosarcina, Methanobacterium,
Methanococcus:
CH3COOH = CH4+CO2
SE E' PRESENTE SOLFATO, E' RIDOTTO PREFERENZIALMENTE INVECE DELLA CO2, CIOE'
ESISTE COMPETIZIONE PER H2 TRA SOLFATO-RIDUTTORI E METANOGENI
Clostridi, anaerobi stretti.
C. thermocellum, termofilo: i suoi enzimi danno come prodotti CELLOBIOSIO E DESTRINE che
entrano nella cellula e attraverso la cellobiosio fosforilasi producono glucosio-1-fosfato e glucosio,
poi fermentati attraverso la glicolisi, = piruvato, ed in seguito a fermentazione H2, CO2, acetato,
galattosio) E PENTOSI (xilosio, arabinosio) E DI ACIDI URONICI (glucuronico, galatturonico).
POLIMERI NON LINEARI COME LA CELLULOSA, MA RAMIFICATI. Esempi: xilani, mannani,
galattani.
Processo di degradazione simile a quello della cellulosa. Siccome la molecola è più eterogenea,
sono coinvolti più enzimi extracellulari.
ENDOENZIMI che tagliano i legami interni a caso
ESOENZIMI che erodono la molecola dall'esterno, come nella cellulosa.
PRODOTTI DI DEGRADAZIONE: anidride carbonica, acqua, piccoli carboidrati monomeri e
dimeri.
NEL COMPLESSO PRENDONO IL NOME DI EMICELLULASI
MICRORGANISMI CHE UTILIZZANO LE EMICELLULOSE
_________________________________________________________________
BATTERI
Bacillus
Pseudomonas
Cytophaga
Mannano, xylano
Xylano
Galattano
ATTINOMICETI
Streptomyces
FUNGHI
Mannano, xylano
Composto da amilosio, a struttura lineare come la cellulosa ma con legami alfa 1, 4, + amilopectina,
molecola ramificata, che consta di catene analoghe a quelle dell'amilosio, legate alla catena principale
con legami alfa 1, 6.
Degradato dalle AMILASI: enzimi extracellulari, consistenti in
Alfa- 1, 4 eso ed endoglucanasi.
- AMILOSIO degradato completamente. AMILOPECTINA decomposta parzialmente per la presenza
dei legami 1, 6, su cui le AMILASI sono inattive. Intervangono enzimi del tipo AMILO- ALFA- 1, 6
GLUCOSIDASI.
Batteri: Bacillus subtilis, B. cereus, Clostridium.
Funghi: moltissimi.
LIEVITI NON SONO AMILOLITICI.
CHITINA
E' UN AMINOZUCCHERO ACETILATO. COSTITUITA DA SUBUNITA' DI NACETILGLUCOSAMINA LEGATE DA LEGAMI BETA I, 4.
MOLECOLA LINEARE
ENZIMI: CHITINASI, che rompono il polimero a partire dalle estremità, dando luogo alla formazione
di unità di DIACETILCHITOBIOSIO, che è successivamente idrolizzato al monomero di
acetilglucosammina da ACETILGLUCOSAMINIDASI.
Dopo diacetilazione, si hanno: GLUCOSAMINA, ACIDO ACETICO, GLUCOSIO, AMMONIACA.
Microrganismi piu' attivi: ATTINOMICETI
alcool cumarilico, sinapilico e coniferilico.
Circa 500-600 subunità di fenilpropani diversi sono polimerizzate a caso, tenute insieme da legami C-C
oppure C-O-C, in struttura tridimensionale, e danno luogo alla formazione di un polimero amorfo:
Nelle piante la LIGNINA circonda le microfibrille di cellulosa e rinforza la parete cellulare.
La casualità del processo di polimerizzazione rende il processo enzimatico di degradazione piu' difficile.
I tassi di degradazione sono molto più lenti di quelli della cellulosa. Si degrada lentamente anche perché
oltre ad essere un polimero eterogeneo contiene molti residui aromatici.
UN ENZIMA EXTRACELLULARE NON SPECIFICO, LA LIGNINA-PEROSSIDASI H2O2-DIPENDENTE
E' USATO CON UN ENZIMA EXTRACELLULARE, UNA OSSIDASI CHE GENERA H2O2. LA
PEROSSIDASI E LA H2O2 GENERANO RADICALI LIBERI CHE REAGISCONO CON LA LIGNINA E
RILASCIANO RESIDUI DI FENILPROPANO, SUCCESSIVAMENTE DEGRADATI DAI
MICRORGANISMI.
LA DEGRADAZIONE DELLA LIGNINA E' AEROBIA, IN QUANTO E' NECESSARIO L'OSSIGENO
ATTIVO PER POTER RILASCIARE I RESIDUI
Il legno intatto è prima attaccato dagli enzimi dei funghi del marciume bruno, che agiscono su cellulose
ed emicellulose: i rami si spezzano e rilasciano una polvere scura consistente in LIGNINA liberata.
Contemporaneamente e sequenzialmente agiscono gli enzimi dei funghi del marciume bianco, che
degradano la lignina ad anidride carbonica ed acqua, rilasciando residui di cellulosa morbidi e fibrosi.
Componenti strutturali della lignina, con le tre unità di fenil-propano e con
i tre principali tipi di legame chimico che li unisce. Nel riquadro rosso, una
una piccola parte della molecola della lignina.
Rottura degli anelli aromatici. A sinistra: durante la degradazione della lignina, per il processo
di orto fissione. A destra: durante la degradazione dei pesticidi e altri xenobiotici, per meta
fissione. Initialmente l’anello è sostituito da due gruppi idrossili sugli atomi di C adiacenti. Poi
l’anello è aperto sia tra questi due C (orto fissione) o vicino ad uno di essi (meta fissione).
DEGRADAZIONE LIGNINA: PROCESSO OSSIDATIVO COMPLESSO
COME PER LA FORMAZIONE, E' INDIRETTO E CASUALE
Fungo del marciume bianco più studiato:basidiomicete Phanerochaete chrysosporium
LA DEPOLIMERIZZAZIONE DELLA LIGNINA PRODUCE UNA VARIETA' DI FENOLI, ALCOOL,
ACIDI AROMATICI. ALCUNI SONO MINERALIZZATI A CO2 ED H2O, MA ALTRI DANNO LUOGO
A COMPOSTI UMICI.
Si hanno anche processi di ripolomerizzazione spontanea, o catalizzati da polifenolossidasi, laccasi e
perossidasi microbiche.
I RESIDUI DEI FENILPROPANI, COMPOSTI AROMATICI, SONO SIMILI IN STRUTTURA A
DIVERSI TIPI DI MOLECOLE INQUINANTI ORGANICHE COME BENZENE, TOLUENE, XYLENE,
COMPOSTI POLIAROMATICI. Le vie naturali per la loro biodegradazione sono importanti per la
Bioremediation. Ad esempio, Phanerochete chrysosporium è capace di degradare diverse molecole
inquinanti con strutture simili a quelle della lignina.
MICRORGANISMI CHE DEGRADANO E/O MODIFICANO LA LIGNINA
Organismo
Modifica p.mol.
EUCARIOTI
Funghi marciume bianco
Pleorotus osteratus
Phanerochaete chrysosporium
Coriolus verisicolor
Funghi marciume bruno
Lenzites trabea
Lentinus lepideus
Funghi marciume molle
Thielavia terrestris
Chaetomium piluliferum
PROCARIOTI
Sreptomyces badius
Bacillus megaterium
Pseudomonas spp.
Degradazione completa
+
+
+
+
+
+
+
+
-
+
+
nd
nd
+
+
+
nd
nd
nd