Scuola di Scienze mediche e Farmaceutiche
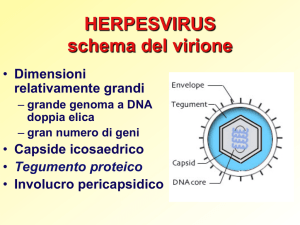
HERPESVIRUS
www.microbiologia.unige.it
Prof. Oliviero E. Varnier
2014
Sezione di Microbiologia – Dipartimento di Scienze Chirurgiche R Diagnostiche Integrate (DISC)
INTRODUZIONE
! Gli Herpesvirus sono una delle principali cause di malattie
virali umane, secondi solo ai virus influenzali e del
raffreddore.
! Sono in grado di causare malattie sintomatiche o di rimanere
silenti per molti anni in attesa di essere riattivati.
! Il nome herpes deriva dal latino herpes che, a sua volta,
deriva dalla parola greca herpein che significa “diffondersi”.
La natura di avanzare e diffondersi è caratteristica delle
lesioni della cute causate da molti herpesvirus.
2
di
44
SONO NOTE 25 FAMIGLIE DI HERPESVIRUS
MA SOLO 8 SONO CAPACI DI INFETTARE L’UOMO
TIPI DI HERPESVIRUS CHE INFETTANO L’UOMO
Virus Herpes simplex di Tipo 1 (HSV-1)
Virus Herpes simplex di Tipo 2 (HSV-2)
Virus Varicella Zoster (VZV)
Virus di Epstein Barr (EBV)
Citomegalovirus (CMV)
Herpes virus umano 6 (esantema subitum o sesta malattia)
Herpes virus umano 7
Herpes virus umano 8 (associato al sarcoma di Kaposi)
3
di
44
PROPRIETÀ DEGLI HERPESVIRUS
Herpes
Virus
Umano
Tipo
Nome
Sub Familia
Cellule Bersaglio
Latenza
Trasmissione
1
Herpes simplex-1 (HSV-1)
Alphaherpesvirinae
Mucose epiteliali
Neuroni
Contatto stretto
2
Herpes simplex-2 (HSV-2)
Alphaherpesvirinae
Mucose epiteliali
Neuroni
Contatto stretto di solito
sessuale
3
Varicella Zoster virus (VZV)
Alphaherpesvirinae
Mucose epiteliali
Neuroni
Contatto o
via respiratoria
4
Epstein-Barr Virus (EBV)
Gammaherpesvirinae
Linfociti B, epiteliali
Linfociti B
Saliva
5
Cytomegalovirus (CMV)
Betaherpesvirinae
Epiteliali, monociti,
linfociti
Monociti, linfociti e
altre
Contatto, trasfusioni di
sangue, trapianti,
congenita
6
Human herpes virus-6 (HHV-6)
Betaherpesvirinae
Linfociti T e altre
Linfociti T e altre
Contatto,
via respiratoria
7
Human herpes virus-7 (HHV-7)
Betaherpesvirinae
Linfociti T e altre
Linfociti T e altre
Sconosciuta
8
Human herpes virus-8 (HHV-8)
Kaposi's sarcoma- associated
herpes virus (KSHV)
Gammaherpesvirinae
Cellule endoteliali
sconosciuta
Scambio di liquidi
corporei ?
4
di
44
HERPESVIRUS: GENERALITÀ
! Gli Herpesvirus sono classificati in base alla loro
localizzazione nello stato di latenza.
! Quando un soggetto viene infettato da un virus
erpetico, l’infezione rimane per tutta la vita.
! L’infezione primaria può essere seguita da una
latenza con successive riattivazioni.
! Gli herpesvirus infettano la maggior parte della
popolazione umana e le persone di mezza età quasi
sempre hanno anticorpi verso la maggior parte degli
herpesvirus ad eccezione di HHV-8.
5
di
44
HERPES VIRUS: CAPSIDE E PERICAPSIDE
Virus Herpes Simplex tipo 1
Un capside (400kV Spot-scan Electron
Cryomicroscopy)
Virus Herpes Simplex tipo 1 Colorazione
negativa
Il CAPSIDE è icosaedrico composto da 162 capsomeri,
che hanno una forma a ciambella
6
di
44
RICOSTRUZIONE 3-D AL COMPUTER DA MICROFOTOGRAFIE
CRIO-ELETTRONICHE DI CAPSIDI DI VIRUS HERPES SIMPLEX Gli Herpesvirus hanno un pericapside che circonda un capside icosaedrico,
circa 100nm di diametro, che contiene il genoma a DS DNA. Quando il
pericapside si rompe e collassa allontanandosi dal capside, i virioni colorati
negativamente hanno un tipico aspetto di un uovo all’occhio di bue.
7
di
44
HERPES VIRUS: PERICAPSIDE
Gli Herpesvirus hanno il pericapside: gemmano dalla membrana nucleare, che
è stata modificata con l’inserzione di glicoproteine erpetiche (nel virus maturo,
queste glicoproteine funzionano da antirecettori per i recettori cellulari e
determinano il tropismo).
8
di
44
HERPES VIRUS: PERICAPSIDE
! Il pericapside è molto fragile e un virus con un
pericapside danneggiato non è infettivo.
! La principale implicazione è la trasmissibilità: il virus
può essere “preso” solo per contatto diretto con le
superfici mucose o con le secrezioni di un soggetto
infetto.
! Il virus è sensibile a: disidratazione, acidi, detergenti e
solventi organici per la presenza di lipidi nel
pericapside.
9
di
44
HERPES VIRUS: PERICAPSIDE
Le glicoproteine (spikes) sulla superficie di HSV: la glicoproteina B
(gB) è chiaramente visualizzata in clusters di spine lunghe circa 10 nm.
Tegumento: è lo spazio tra pericapside e capside. Contiene
proteine virali ed enzimi necessari nelle prime fasi della
replicazione.
10
di
44
HERPES VIRUS: MORFOLOGIA
Genoma:
un DNA a doppio filamento: il CMV ha il genoma di maggiori dimensioni
11
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
MORFOLOGIA del VIRUS HERPES SIMPLEX
HSV è un virus a DNA, che si replica nel nucleo, con un capside
e pericapside. Il pericapside contiene almeno 8 glicoproteine.
La matrice o tegumento, che aderisce sia al capside sia al
pericapside, contiene almeno 15-20 proteine.
12
di
44
AZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
Il genoma di HSV deve entrare nella cellula per
iniziare l’infezione. L’adsorbimento avviene tra
i proteoglicani della superficie cellulare e la
glicoproteina gC.
Questo evento è seguito da una specifica
interazione con uno o più recettori cellulari
chiamati "HVEM" (Herpes Virus Entry
Mediators), che sono simili ai recettori i “nerve
growth factors” e il “tumor necrosis factor”.
È necessaria la specifica interazione con la
glicopoteina gD seguita dalla fusione con la
membrana cellulare.
La fusione richiede l’intervento dellee
glicoproteine virali: gB, gH, gI e gL.
13
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
! Il capside virale con alcune protei-
ne del tegumento migra verso i pori
nucleari attraverso microtubuli
cellulari utilizzando il sistema di trasporto cellulare.
! Questo “attracco” dovrebbe compor-
tare l’iniezione del DNA virale dentro
i pori, mentre il capside rimane nel
citoplasma. Alcune proteine del tegumento (alfa-TIF) entrano nel nucleo con il genoma virale.
14
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
z La trascrizione del genoma HSV utilizza l’apparato trascrizionale cellulare e promotori virali che impiegano i siti leganti
dei fattori trascrizionali cellulari.
z Ci sono due fasi principali della trascrizione:
v PRECOCE, che avviene prima della replicazione del genoma,
v TARDIVA, che avviene dopo la formazione di copie di genomi
nelle aeree di replicazione virale nel nucleo cellulare infettato.
15
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
La trascrizione PRECOCE si divide in due fasi:
1. PRECOCISSIMA:
dopo l’entrata del genoma virale nel nucleo, nel quale l’alfa-TIF associato al virione si lega al recettore cellulare Oct-1, che ha legato le sequenze
TAATGARAT nella parte upstream degli enhancers dei promotori precoci
immediati.
Questo evento causa un efficiente assemblaggio del complesso di preiniziazione nella TATA box e nella trascrizione mediata da pol II.
I trascritti precocissimi sono trasportati nel citoplasma, tradotti
e le proteine precocissime migrano nel nucleo.
16
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
2. PRECOCE
Tutta la successiva trascrizione richiede l’azione delle proteine
precoci: in particolare la proteina alfa 4, che è un attivatore
generico della trascrizione, funziona legandosi a siti multipli
del genoma, interagisce con le vicine TATA boxes e facilita
l’assemblaggio dei complessi di preiniziazione.
17
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
La trascrizione PRECOCE procede e le proteine precoci sono
tradotte nel citoplasma, migrano nel nucleo e mediano la
replicazione del genoma virale (DNA-polimerasi).
Con la replicazione dei genomi, si concentrano in aree
delimitate dove inizia la TRASCRIZIONE TARDIVA.
La trascrizione precoce si esaurisce con la replicazione del
genoma.
18
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
I trascritti TARDIVI sono divisi in due gruppi
generali:
PARZIALMENTE TARDIVI e
STRETTAMENTE TARDIVI.
Essi differiscono per la quantità di trascrizione
osservata prima della replicazione del genoma.
Sono controllati da promotori con diverse
architetture funzionali.
Alcuni promotori STRETTAMENTE TARDIVI
contengono un elemento DAS (Downstream
Activating Sequence) che interagisce con uno
o più fattori cellulari DBF (DAS Binding Factor)
per mediare la formazione efficiente di complessi tardivi di trascrizione.
19
di
44
ANIMAZIONE DELL’INFEZIONE E REPLICAZIONE DI HSV
Le proteine procapsidiche (UL18, UL19 e UL38) si assemblano attorno alle
proteine di uno scheletro (UL26 e UL26.5), che successivamente sono
eliminate.
I capsidi vuoti incorporano il DNA mediante l’azione di proteine di clivaggio e
di assemblaggio.
I capsidi migrano verso la membrana nucleare e gemmano nel lume dei due
foglietti della membrana.
Questo virione con pericapside entra nel cito-plasma mediante uuna fusione
con la membrana esterna.
20
di
44
L’INFEZIONE E REPLICAZIONE DI HSV
21
di
44
LATENZA VIRALE
.
22
di
44
Percorso dell’Infezione Erpetica
L’Herpesvirus entra
nell’organismo
L’Herpesvirus entra nell’
organismo attraverso la
cute o le membrane mucose
L’Herpesvirus è latente
nei nervi
L’Herpesvirus viene riattivato
Dopo l’infezione primaria,
l’herpesvirus rimane latente nei nervi spinali
L’herpesvirus viaggia lungo
i nervi, ritornando nella cute
dove forma nuove vescicole
23
di
44
I siti nei quali HSV-1 e HSV-2
24 di 44
causano malattia nell’uomo
MALATTIE CAUSATE DA HSV
I virus Herpes simplex 1 e 2 sono frequentemente
asintomatici, ma possono anche causare gravi malattie.
La lesione iniziale è la stessa. Un vescicola trasparente
su una base eritematosa contenente virus infettivo.
Questa è spesso indicata come “una goccia di rugiada
su un petalo di una rosa”, che si trasforma in pustola e
poi in ulcera, che infine si ricopre di croste.
25
di
44
PROGRESSIONE DELLE LESIONI DA ALFA HERPESVIRUS
Arrossamento con rigonfiamento
Vescicole trasparenti
contenenti liquido e pustole
Risoluzione delle vescicole,
erosioni e ulcere
26
di
44
PROGRESSIONE DELLE LESIONI DA ALFA HERPESVIRUS
Formazione di croste
Lesione coperta di croste
guarigione
27
di
44
MALATTIE CAUSATE DA HSV
HERPES ORALE
! Può essere il risultato di una infezione da HSV-1 o da HSV-2.
Poichè l’HSV-2 è trasmesso sessualmente, le infezioni nei
bambini sono quindi causate da HSV-1.
! Nella gengivostomatite erpetica primaria, le lesioni iniziano
come vescicole chiare che si trasformano rapidamente in
ulcere, caratterizzate da un aspetto biancastro. L’infezione
inizia sulle labbra, poi si diffonde intorno alla bocca, e
raggiunge palato,faringe, gengive e la lingua.
! La riattivazione dai gangli del trigemino può dare manifestazioni
mucocutanee ricorrenti (ulcere fredde).
! La faringite erpetica è spesso associata ad altre infezioni virali
delle vie aeree superiori.
! La malattia è più grave nei soggetti immunosoppressi.
28
di
44
MALATTIE CAUSATE DA HSV
CHERATITE ERPETICA
La cheratite erpetica, principalmente causata da HSV-1, è
quasi sempre limitata ad un solo occhio.
Può dare episodi ricorrenti causando cicatrici permanenti,
danno corneale e cecità.
29
di
44
HERPES ORALE
Il virus herpes simplex può iniziare un’infezione primaria nelle
labbra e quindi raggiungere il ganglio trigemino, dove rimane
latente.
Il virus può successivamente riattivarsi, ritornare nel sito
originario dell’infezione e indurre le lesioni tipiche della febbre
erpetica labbiale.
30
di
44
EPIDEMIOLOGIA
! Le infezioni da HSV 1 e 2 durano tutta la vita e sebbene
l’instaurarsi della latenza sia iniziale, il soggetto infetto può
trasmettere l’infezione ad altri durante la riattivazione.
! Il virus si trova nelle lesioni della cute, ma può essere presente
anche in numerosi liquidi biologici (saliva e secrezioni vaginali).
! Entrambi I virus possono infettare le mucose orali e genitali:
HSV-1 di solito si diffonde “bocca-bocca” (con il bacio e l’uso
di utensili contaminati da saliva) o con il traferimento di virus
infettivo con le mani e la sua entrata nell’organismo attraverso
qualsiasi lesione o la mucosa degli occhi.
! La maggior parte della popolazione ha contratto l’infezione da
HSV-1, come dimostrato dalla presenza di anticoopri specifici.
Oltre il 90% dei bambini hanno anticorpi anti HSV-1 per la
scarsa igiene dei paesi in via di sviluppo.
31
di
44
EPIDEMIOLOGIA
! L’HSV-2 si trasmette per via sessuale e si ritrova nell’ano,
retto, e apparato digerente e nell’area genitale.
! Un neonato può essere infettato alla nascita dalla madre con
un’infezione genitale, ma anche in utero se la madre ha una
infezione sistemica. Poichè il neonato ha un sistema immune
immaturo, l’infezione può essere grave e talvolta letale.
! Tutti coloro che vengono a contatto con un liquido contenente
virus infettivo sono a rischio d’infezione.
! Il PATERECCIO erpetico è una infezione delle dita e l’herpes
dei GLADIATORI è una infezione del corpo. Il virus penetra
attraverso tagli o abrasioni della cute. Il personale sanitario
spesso contrae il patereccio da pazienti con infezioni erpetiche.
! Le infezioni da HSV-2 sono prevalenti negli adulti con l’aumento dell’attività sessuale con percentuali dell’80% nelle
prostitute.
32
di
44
PATOGENESI
! L’esposizione al virus di superfici mucose o di cute abrasa ne
permette l’inizio della replicazione all’interno delle cellule del
derma e dell’epidermide.
! Una replicazione virale sufficiente per permettere l’infezione
delle terminazioni nervose sensoriali e autonome si può
verificare in presenza e in assenza di lesioni clinicamente
evidenti.
! Si pensa che il virus o più probabilmente il nucleocapside, sia
successivamente trasportato, per via intraassonale, nella
cellula nervosa, a livello dei gangli.
! Nell’uomo non è conosciuto l’intervallo che intercorre fra
l’inoculazione del virus in un tessuto periferico e la sua
diffusione ai gangli.
33
di
44
PATOGENESI
! Durante le fasi iniziali dell’infezione, la replicazione virale
avviene a livello dei gangli e nel tessuto nervoso adiacente.
! Il virus diffonde poi ad altre superfici mucose e cutanee con una
migrazione di tipo centrifugo dei virioni infettanti attraverso il
sistema nervoso periferico.
! Questa diffusione del virus dai nervi sensoriali alla cute aiuta a
spiegare la vasta superficie e l’elevata frequenza di nuove
lesioni distanti dalla sede iniziale dell’infezione, caratteristiche
in pazienti con infezione primaria da HSV a livello orolabiale o
genitale e l’isolamento del virus nel tessuto nervoso distante dai
neuroni che innervano il sito di inoculazione.
! Si può inoltre avere diffusione per contiguità del virus inoculato
localmente e ciò può permettere un’ulteriore estensione
mucocutanea della malattia.
34
di
44
PATOGENESI
! Al termine dell’infezione primaria non è più possibile
isolare il virus dai gangli sebbene in una certa
percentuale di casi sia possibile trovare DNA virale
nelle cellule gangliari nella sede dell’infezione iniziale.
! L’HSV può poi essere riattivato da vari stimoli quali
immunodepres-sione, traumi, luce ultravioletta, ecc.; i
meccanismi di tale riattivazione sono sconosciuti.
35
di
44
HSV
! Gli Herpes simplex virus sono molto grandi e i loro genomi
codificano almeno 80 proteine, metà delle quali non fanno parte
della struttura virionale e neppure controllano la replicazione
virale, ma interagiscono con l’ospite o con la risposta immune
dell’ospite.
! Esistono due tipi: HSV-1 e HSV-2 con caratteristiche simili.
! Il genoma di HSV codifica per numerosi enzimi:
! DNA-polimerasi DNA-dipendente
! Timidina chinasi (fosforila la timidina e altri nucleosidi)
! Riduttasi dei ribonucleotidi (converte i ribonucleotidi in
deossiribonucleotidi)
! Serino-proteasi (converte una proteina dello scheletro nella
sua forma finale) è essenziale per la produzione di virioni
maturi infettivi
36
di
44
HSV
Il genoma codifica 11 glicoproteine di superficie, che sono
coinvolte in:
u Adsorbimento (gB, gC, gD e gH)
u Fusione della membrana virale con quella della cellule
ospite (gB)
u Escape immunitario
! Un esempio di funzione di escape immune è gC che si lega
alla proteina C3 del complemento e quindi la allontana dal
siero dell’ospite e inibisce le reazioni mediate dal
complemento.
! altre funzioni (gC, gE e gI).
! Le proteine virali gE e gI possono anche legare il frammento FC delle IgG. Il
virus si copre di immunoglobuline e si nasconde al sistema immune.
37
di
44
INFEZIONE LATENTE
! Il virus HSV risiede nei gangli infetti, nei quali non è in grado di
replicarsi e solo pochi geni virali sono espressi. HSV persiste
nei gangli infetti per tutta la vita, ma determinati stimoli sono in
grado di riattivare il virus.
! Nelle infezioni secondarie il virus segue gli assoni in direzione
centrifuga e si ha un ciclo di replicazione sulla cute o sulle
mucose.
! Riattivazioni spontanee avvengono nonostante la presenza
nell’ospite di immuntità umorale e cellulare, che comunque
limita la replicazione virale locale cosicchè le infezioni
riccorrenti sono meno estese e meno severe.
! Molte infezioni ricorrenti sono asintomatiche e caratterizzate
solamente da presenza virale nelle secrezioni.
38
di
44
INFEZIONE LATENTE
! Sebbene la base molecolare della riattivazione non sia nota,
si conoscono numerosi stimoli scatenanti quali: febbre,
stress fisico o psichico, esposizione alla luce ultravioletta,
traumi e variazioni ormonali.
! Più dell’80% della popolazione ospita HSV-1 nella forma
latente, ma solamente una piccola parte va incontro a
infezioni ricorrenti.
39
di
44
LA RISPOSTA IMMUNE VERSO HSV 1 e 2
! Interferone è importante nel limitare l’infezione primaria e le cellule
natural killer sono coinvolte in questa fase.
! Le cellule T citotossiche e i macrofagi sono il braccio cellulare della
risposta e uccidono le cellule infettate.
! La risposta umorale (di solito anticorpi anti glicoproteine di superficie)
conferisce la neutralizzazione.
! HSV evita il sistema immune coprendosi con IgG utilizzando i
recettori FC e quelli del complemento.
! Il virus può anche diffondersi passando da una cellula all’altra senza
entrare negli spaci intercellulari e venire a contatto degli anticorpi
umorali.
! Le risposte cellulo-mediate sono vitali nel controllo delle infezioni
erpetiche.
40
di
44
DIAGNOSI
! Esame microscopico diretto delle cellule prelevate dalla
lesione, mediante striscio di Tzanck (un raschiamento alla base
della lesione), che evidenzia cellule giganti multinucleate e
corpi inclusi di Cowdry di tipo A.
! Un rapida e definitiva diagnosi può essere ottenuta
dimostrando al presenza di antigeni virali (mediante tecniche di
immunofluorescenza o di immunoperossidasi) oppure di DNA
(ibridizzazione o PCR) nel tessuto o nel liquido delle vescicole.
! Isolamento in colture cellulari (HeLa, Hep2 e fibroblasti con
comparsa di effetto citopatico in 1-3 giorni.
! I test sierologici sono utili per la diagnosi di una infezione
primaria da HSV e per studi epidemiologici.
41
di
44
TERAPIA
! L’acyclovir (acicloguanosina) è il farmaco di scelta, è un
analogo nucleosidico, ma ha un’invidiabile reputazione di nontossicità. Le sue proprietà farmacologiche anti-virali si rivelano
solo quando viene fosforilato nella sua forma monofosfato e
successivamente nel derivato trifosfato (acyclo-GTP).
! La fosforilazione avviene nelle cellule che contengono le
deossicitidina chinasi codificata da HSV, ma non in presenza
dell’analogo enzima presente nelle cellule di mammifero.
! La fosforilazione è quindi una prerogativa delle cellule infettate
da HSV e non avviene in modo significativo nelle cellule non
infettate! L’acyclo-GTP è un potente inibitore selettivo della DNA
polimerasi di HSV e causa un arresto della catena,
competendo con il guanosintrifosfato per l’incorporazione nel
DNA virale neosintetizzato.
42
di
44
43
di
44
VACCINI
! La ricerca di un vaccino anti-HSV non è un fatto nuovo.
! Tentativi in tal senso risalgono a mezzo secolo fa e circa venti
anni fa alcuni vaccini, costituiti da virus interi inattivati, furono
commercializzati in Europa.
! È interessante notare che il principale beneficio di questi primi
prodotti sembra essere stato più terapeutico che profilattico
(servirono a ridurre l’ipersensibilità alle proteine di HSV e perciò
attenuarono la gravità delle ricadute).
! Per la possibile oncogenicità di HSV, sono stati prodotti vaccini
privi di DNA, sia per purificazione sia per ingegneria genetica.
! Questi vaccini composti da subunità o da glicoproteine sono senza
dubbio antigenici e gli anticorpi che evocano possono essere
protettivi.
44
di
44