Batteriologia generale.
Introduzione allo studio dei microrganismi.
Differenze tra organismi procarioti ed eucarioti.
Morfologia e struttura della cellula batterica:
Accrescimento batterico: conta dei batteri, curva di crescita, terreni di
coltura.
Genetica Microbica: scambio genetico tra batteri
(trasformazione,coniugazione, trasduzione).
Fattori di virulenza dei batteri
Modalità di trasmissione delle malattie infettive.
Virologia generale.
Virus: classificazione, struttura, .interazione virus-cellula, ciclo biologico
della replicazione virale
Micologia generale
Miceti: caratteristiche generali, struttura, riproduzione, fattori di virulenza e
patogenicità.
Immunologia
ruolo e funzione del sistema immune, risposta immune aspecifica e
specifica. Organi linfoidi primari e secondari Antigeni, Anticorpi ,
sistema maggiore istocompatibilità, citochine, sistema del
complemento, reazioni di ipersensibilità risposta immune alle
infezioni.
Vaccini e sieri immuni.
Strategie di controllo delle infezioni
disinfezione, sterilizzazione. Antibiogramma.
Principali batteri , funghi e virus responsabili di malattie
nell’uomo
Storia della microbiologia
differenze tra procarioti ed
eucarioti
Microbiologia
È la scienza che studia i microorganismi
I microorganismi sono organismi di dimensioni talmente
piccole da risultare invisibili ad occhio nudo
Per osservare tali microrganismi si utilizza il microscopio
MICROSCOPIO
Il microscopio (dal greco : μικρόν (micron) piccolo e
σκοπεῖν (skopein) guardare) è uno strumento che
consente di ingrandire oggetti di piccole dimensioni
per permetterne l'osservazione diretta o indiretta
tramite fotografia e sistemi elettronici. Può essere
ottico, e quindi basato sull'osservazione nell'ambito
dello spettro della luce o elettronico basato
sull'osservazione tramite fasci di elettroni , o di altro
tipo.
MICROSCOPIO
• Il microscopio ottico (light microscope LM) è il più semplice.
Per mezzo di due sistemi di lenti :uno situato vicino
all’oggetto da esaminare-OBIETTIVO- uno vicino all’occhio
dell’osservatore –OCULARE
Il potere di risoluzione di un microscopio è la capacità di
vedere punti vicini come distinti e dipende dalla lunghezza
d’onda della luce utilizzata per illuminare l’oggetto
Oculare
Obiettivo
Preparato
Microscopio ottico composto mono
oculare del tipo più semplice
rappresentato schematicamente;
La messa a fuoco avviene variando la
distanza preparato/obiettivo spostando il
tubo ottico..
A - Oculare ; B - Obiettivo; C Preparato; D - Condensatore; E Tavolino portaoggetti; F - Specchio
Tavolino portaoggetti
Specchio
Un modello base di microscopio ottico La
messa a fuoco avviene variando la
distanza preparato/obiettivo muovendo il
preparato.
Illuminatore incorporato nello strumento.
1 - Tubo verticale per fotografia; 2 - Testa
binoculare; 3 - Stativo; 4 - porta obbiettivi;
5 - Tavolino portaoggetti; 6 Condensatore; 7 - Manopole di messa a
fuoco; 8 - Sorgente di luce.
Microscopi
•
•
•
•
•
•
•
Tipo
Potere risolutivo Ingrandimento
Ottico
0,2m
1000
In campo oscuro 0,2m
1000
A contrasto di fase 0,2m
1000
A fluorescenza
0,2m
1000
MET
0,0005m
200.000
MES
0,02m
10.000
• Ottico
• In campo oscurosistema di
illuminazione che raggiunge il preparato
lateralmente
• A contrasto di fase
si basa
sul fatto che differenti popolazioni hanno indice di
rifrazione diversa e quindi la luce viene ritardata
• A fluorescenza possono essere
campioni trattati con sostanze fluorescenti
• Elettronico a
trasmissione
• Elettronico a scansione
Microscopi
MICROSCOPIO A FLUORESCENZA
• Sostanze fluorescenti hanno la capacità di
assorbire luce a lunghezze d’onda corta e la
restituiscono a lunghezze d’onda più lunga
Questo tipo di microscopio serve per osservare
preparati naturalmente fluorescenti, o legati con
molecole fluorescenti o rese tali da particolari
coloranti detti fluorocromi. Questi composti
vanno selettivamente a legarsi con strutture
cellulari definite.
Microscopio Elettronico a Scansione
• Il microscopio elettronico a scansione,
ricava l'immagine illuminando con un fascio
di elettroni il campione
Dal campione vengono emesse numerose
particelle fra le quali gli elettroni secondari.
Questi elettroni vengono rilevati da uno
speciale rilevatore
Immagine del campione in 3D
Pollini
Microscopio elettronico a
trasmissione
• Il microscopio elettronico a trasmissione fa attraversare
un campione molto sottile (da 5 a 500 nm) da un fascio di
elettroni, ingrandisce l'immagine ottenuta che viene infine
proiettata su uno schermo.
• Ingrandisce anche un milione di volte
• L’immagine che ne risulta è il risultato dell’assorbimento
selettivo degli elettroni da parte dei vari componenti del
campioni
• Dà immagini della struttura interna dell'oggetto
esaminato
Electron micrograph of a thin section of the Gram-positive showing the thick
peptidoglycan cell wall (cw), underlying cytoplasmic (plasma) membrane
(cm), mesome (m), and nucleus (n).
Dimensioni dei batteri e dei virus
batteri 0,5 e 5 μm
virus 10 nm, i più grandi possono
raggiungere i 450 nm
I MICROORGANISMI svolgono un ruolo importante nel
nostro ecosistema e la loro presenza puo’ avere
Un ruolo positivo o negativo
POSITIVO I microorganismi sono necessari per.
1. produzione di alcuni alimenti ( birra, pane, formaggi)
2. produzione di alcuni farmaci (antibiotici, vaccini)
3. i microorganismi sono indispensabili per il nostro
ecosistema( rendono possibili i cicli dell’azoto,
zolfo,carbonio)
NEGATIVO sono responsabili di malattie infettive che
hanno avuto anche un notevole impatto sociale :
1. peste detta anche morte nera
2. oggi continua la lotta contro l’AIDS e la malaria
Trionfo della morte, già a palazzo sclafani, galleria
regionale di Palazzo Abbatellis, palermo (1446)
la grande pandemia che uccise tra un terzo
e un quarto della popolazione europea
durante il XIV secolo Black death
• Il numero totale di cellule microbiche
presenti in un organismo umano può
superare di dieci volte il numero di cellule
dell'organismo stesso.
• Se si presuppone che i prodotti genici di
tali cellule microbiche possano interagire
con le cellule umane, si può dire che i geni
di origine microbica possono superare di
molto il numero di geni presenti nel
genoma umano
• Il progetto microbioma umano (human
microbiome project) è una iniziativa dei
• National Institutes of Health statunitensi con il
fine di identificare e caratterizzare i microrganismi
ed il loro rapporto con lo stato di salute e di
malattia dell'uomo. È un progetto di 5 anni con un
budget complessivo di 115 milioni di dollari.
• Il microbioma può essere definito come la
somma dei geni tutti i microorganismi presenti in
un determinato organismo superiore
• In quest'ottica, un essere umano va concepito
come composto da cellule umane e microbiche.
• I microrganismi del microbioma umano possono
essere,funghi ,protozoi , elminti e virus (tra cui
anche batteriofagi che infettano lo stesso
microbioma).
• Molti di questi geni, provenienti da organismi
non ancora allevati in coltura, identificati od
altrimenti caratterizzati.
• Il progetto microbioma umano, che si propone di
caratterizzare tutti questi geni di origine esterna,
• Lo studio del genoma umano implica il
sequenziamento del DNA , cioè
l'identificazione della sequenza dei 3 miliardi
di coppie di basi azotate che ne compongono
la molecola
• La comprensione della funzione dei geni e di
quali malattie possono derivare dalle loro
alterazioni costituisce l'obiettivo finale del
progetto.
FeatureThe Human Microbiome Project
Peter J. Turnbaugh1, Ruth E. Ley1, Micah Hamady2,
Claire M. Fraser-Liggett3, Rob Knight4 & Jeffrey I.
Gordon1
Abstract
A strategy to understand the microbial components of
the human genetic and metabolic landscape and
how they contribute to normal physiology and
predisposition to disease.
Science Daily
Relative abundance of common microbes
living in the gut may contribute to the obesity
(Dec. 21, 2006)
— A link between obesity and the microbial
communities living in our guts is suggested by
new research at Washington University School
of Medicine in St. Louis. The findings indicate
that our gut microbes are biomarkers,
mediators and potential therapeutic targets in
the war against the worldwide obesity
epidemic.
•
J Autoimmun. 2013 Sep 24. pii: S0896-8411(13)00091-7. doi: 10.1016/j.jaut.2013.07.001. [Epub ahead of
print]
•
Role of the intestinal microbiome in liver disease.
•
•
•
•
Henao-Mejia J, Elinav E, Thaiss CA, Licona-Limon P, Flavell RA.
Source
Department of Immunobiology, Yale University School of Medicine, CT 06520, USA.
Abstract
•
The liver integrates metabolic outcomes with nutrient intake while preventing harmful signals
derived from the gut to spread throughout the body. Direct blood influx from the
gastrointestinal tract through the portal vein makes the liver a critical firewall equipped
with a broad array of immune cells and innate immune receptors that recognize microbialderived products, microorganisms, toxins and food antigens that have breached the
intestinal barrier. An overwhelming amount of evidence obtained in the last decade
indicates that the intestinal microbiota is a key component of a wide variety of physiological
processes, and alterations in the delicate balance that represents the intestinal bacterial
communities are now considered important determinants of metabolic syndrome and
immunopathologies. Moreover, it is now evident that the interaction between the innate
immune system and the intestinal microbiota during obesity or autoimmunity promotes
chronic liver disease progression and therefore it might lead to novel and individualized
therapeutic approaches. In this review, we discuss a growing body of evidence that highlights
the central relationship between the immune system, the microbiome, and chronic liver
disease initiation and progression.
I ricercatori hanno dimostrato che
la comunità microbica degli obesi
ha una incrementata capacità di
raccogliere calorie dalla dieta
The Bacteria Thrive in Inner Elbow; No Harm Done
Published: May 23, 2008
by Nicholas Wade
goals of the human microbiome project include analyzing the
normal makeup of bacterial species in each niche on the human
body. “The focus in microbiology has been on pathogenic bacteria,
but we are trying to identify the commensal bacteria so that we
can begin to understand what proteins they make and how they
contribute to our health,” Dr. Segre said.
Another goal is to understand how pathogenic bacteria manage
to usurp power from the tribes of beneficial commensals in the
skin or gut, causing disease
•
•
•
•
•
Structure, Function and Diversity of the Healthy Human Microbiome
The Human Microbiome Project Consortium
The publisher's final edited version of this article is available at Nature
See other articles in PMC that cite the published article.
Abstract
•
Studies of the human microbiome have revealed that even healthy individuals differ
remarkably in the microbes that occupy habitats such as the gut, skin, and
vagina. Much of this diversity remains unexplained, although diet, environment, host genetics,
•
and early microbial exposure have all been implicated. Accordingly, to characterize the ecology of
human-associated microbial communities, the Human Microbiome Project has analyzed the largest cohort
and set of distinct, clinically relevant body habitats to date. We found the diversity and abundance of each
habitat’s signature microbes to vary widely even among healthy subjects, with strong niche specialization
both within and among individuals. The project encountered an estimated 81–99% of the genera, enzyme
families, and community configurations occupied by the healthy Western microbiome.
Metagenomic carriage of metabolic pathways was stable among individuals despite variation in
community structure, and ethnic/racial background proved to be one of the strongest associations of both
pathways and microbes with clinical metadata. These results thus delineate the range of structural and
functional configurations normal in the microbial communities of a healthy population, enabling future
characterization of the epidemiology, ecology, and translational applications of the human microbiome.
Genus- and phylum-level
classification of bacteria
colonizing a composite subject,
showing that human
microbiome diversity is
dependent on the site sampled.
Sites in the oral cavity share
greater similarity than other
types of sites, such as the skin,
Firmicutes
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
Di seguito sono riportati i più importanti tra i 274 generi compresi nel phylum Firmicutes:
Bacilli, ordine BacillalesBacillus
Listeria
Cocchi, ordine Coccacea Enterococcus
Lactococcus
Micrococcus
Staphylococcus
Streptococcus
Sarcina
Bacilli, ordine Lactobacillales Lactobacillus
Leuconostoc
Pediococcus
Clostridia Acetobacterium
Clostridium
Eubacterium
Heliobacterium
Heliospirillum
Megasphaera
Pectinatus
Selenomonas
Zymophilus
Sporomusa
ErysipelotrichiErysipelothrix
Before birth, the human intestinal tract is
sterile, but babies immediately begin to acquire
the microbial denizens of the gut from their
environment -- the birth canal, mothers' breast,
and even the touch of a sibling or parent.
Microbiologia
• Scienza che studia gli esseri viventi microscopici, unicellulari
• Presenti nel suolo, aria, acqua, corpo umano, animali, piante
• Microbiologi Batteriologia
•
Virologia
•
Micologia
•
Protozoologia
•
Elmintologia
Un campo importante della Microbiologia è
rappresentato dalla microbiologia medica
che si occupa delle malattie dell’uomo e degli
animali
Di questo campo si occupa il microbiologo
clinico che è in grado di identificare l’agente
eziologico di una malattia infettiva e
programma le misure per eliminarla
1. STORIA DELLA MICROBIOLOGIA
Generazione spontanea o Biogenesi
Aristotele (384-322 a.C.) pensava che gli
animali potessero originarsi spontaneamente
dalle piante e dal terreno.
Fino al XVII secolo si pensava che gli
organismi viventi potevano generarsi
spontaneamente
dalla
materia
in
decomposizione.
Generazione spontanea o Biogenesi
Francesco Redi (1626-1697) confutò la teoria
della Biogenesi
Il concetto di generazione
tuttavia persistette ancora
spontanea
Il primo da ossrvare queste forme viventi fu un olandese
Antony van Leeuwrnhoek(1632-1723). Nel 1673 invio’ alla
Royal Society di Londra numerose lettere in cui descriveva
dettagliatamente alcuni microorganismi
Generazione spontanea o Biogenesi
Spallanzani (1729-1799) introduce la pratica
della sterilizzazione dei terreni e nel 1799
attacca la teoria della Biogenesi,
Generazione spontanea o Biogenesi
.
John Tyndall (1820-1893) nel 1877 dimostra
che la polvere può trasportare i germi.
Fernand Cohn nel 1877 scopre le endospore
termoresistenti.
Robert Koch nel 1876 introduce il concetto di
eziologia.
1881- Koch dimostra che il
carbonchio è provocato da
B. anthracis
1881-Koch coltiva i batteri
1882-Koch scopre il bacillo
tubercolare
1884- sono pubblicati i 4
postulati di Koch
Postulati di Koch
1. L’agente causale deve essere presente in
tutti i casi della malattia di cui è ritenuto
responsabile e deve essere invece assente
negli individui sani.
2. L’agente causale deve essere isolato
dall’individuo affetto e, posto in coltura,
deve dare origine ad una popolazione
cellulare omogenea (una sola specie).
Postulati di Koch
3. L’inoculo di una coltura pura dell’agente
causale in individui sani deve dare luogo
alla comparsa della malattia di cui si ritiene
responsabile.
4. L’agente causale deve essere re-isolato
dall’individuo infettato sperimentalmente.
Scoperta del ruolo dei microorganismi
come agenti di malattia
• La prima evidenza diretta che i
microorganismi svolgevano un ruolo come
agenti di malattia fu fornita
• da Robert Koch( 1843-1910) Queste
evidenze si riferiscono ai suoi esperimenti
fatti su B. antrhracis Koch fu anche in grado
di evidenziare le spore di B. antrhracis e di
capire la diffusione della malattia
Scoperta del ruolo dei microorganismi
come agenti di malattia
1. Utilizzando questi postulati Koch ha potuto riconoscere
l’eziologia di alcune malattie come il carbonchio, il colera ,
la tubercolosi
2. Un altro importante contributo per quanto riguarda le
tecniche di laboratorio fu dato dall’impiego dell’agar per
ottenere colture pure
Scoperta del ruolo dei microorganismi
come agenti di malattia
Robert Koch fu il primo a stabilire una causa
effetto tra microorganismo e malattia.
Louis Pasteur e Robert Koch
1861-Luis Pasteur dimostra che i
microorganismi non si generano
spontaneamente e riesce anche a
dimostrare come mantenere sterili
le soluzioni
1885-Luis Pasteur allestisce il vaccino
antirabbico
1903- Wright e coll. scoprono la presenza di
anticorpi nel sangue di animali immunizzati
1929 -Fleming scopre la penicillina
1953- Watson e Crick propongono la struttura a
doppia elica del DNA
1982- allestimento del vaccino per l’Epatite B
1983-4 Gallo e Montagnier Identificazione dell’HIV
Microbiologia
• Scienza che studia gli esseri viventi microscopici, unicellulari
• Presenti nel suolo, aria, acqua, corpo umano, animali, piante
• Microbiologia:
•
Batteriologia
•
Virologia
•
Micologia
•
Protozoologia
•
Elmintologia
• Un campo importante della Microbiologia è
rappresentato dalla microbiologia medica
che si occupa delle malattie dell’uomo e
degli animali
Di questo campo si occupa il microbiologo
clinico che è in grado di identificare
l’agente eziologico di una malattia infettiva
e programma le misure per eliminarla
A che serve conoscere i
microorganismi?
Diagnosi
?
Referto batteriologico
Paziente:
Campione biologico:
Rossi Mario
Liquor
Esame microscopico dopo colorazione di GRAM: presenti
numerosi leucociti polimorfonucleati e rari diplococchi Gramnegativi, anche intraleucocitari.
POSSIBILE DIAGNOSI EZIOLOGICA DI MENINGITE!
Il liquor cerebrospinale è un fluido incolore e
trasparente che circonda il cervello, il midollo spinale
e le radici dei nervi periferici.
L'analisi cellulare, biochimica e
microbiologica del liquor è in grado di
dimostrare o escludere soprattutto processi
infiammatori o infettivi del sistema nervoso
L'esame del liquor è inoltre indicato con cefalea
improvvisa quando clinicamente si sospetta
un'emorragia cerebrale (subaracnoidale) e la TAC non
riesce a dimostrarla. In questo caso, l'esame del
liquor può dimostrare la presenza di emoglobina e
confermare la diagnosi.
Puntura lombare: inserzione dell'ago tra i processi spinosi di due vertebre
lombari per raccogliere il liquor cerebro-spinale che riempie il canale spinale.
Procarioti
dal greco nucleo “primitivo”
Eucarioti
Dal greco nucleo “ben definito”
(morfologicamente distinto)
I PROCARIOTI rappresentano circa l’80% di tutte le cellule
presenti sulla terra . La pelle umana è ricoperta di batteri e
inoltre i batteri si trovano nella bocca e nel tratto gastrointestinale
La differenza fondamentale che intercorre tra PROCARIOTI ed
EUCARIOTI consiste nel fatto che tutte le attività della
cellula avvengono in un unico compartimento al contrario
nella cellula eucariota le varie attività si svolgono in
compartimenti diversi delimitati da membrana
L’introduzione e l’estromissione di sostanze puo’avvenire nei
procarioti solo sotto forma molecolare , mediante trasporto
attraverso la membrana citoplasmatica,
mentre negli eucarioti oltre al trasporto molecolare sono
presenti processi di ENDOCITOSI ed ESOCITOSI
Strutture della cellula batterica
Strutture fondamentali:
• parete cellulare
• acido nucleico
• citoplasma
• membrana citoplasmatica
• mesosomi
Strutture facoltative:
• capsula
• fimbrie o pili
• flagelli
• spore
Principali caratteristiche strutturali e
funzionali dei procarioti
•
•
•
•
•
•
•
•
•
•
•
Nucleo: nucleoide privo di membrana nucleare
Nucleolo: Assente
DNA : Cromosomi singoli
Parete cellulare :presente
Membrana citoplasmatica : Steroli assenti
Granuli citoplasmatici: Assenti
Mitosi : Assenti
Ribosomi :70S( due subunità 50 30 S) (azione della streptomicina)
Motilità: Flagelli,
Riproduzione: Asessuata ( scissione binaria)
Dimensioni. 1-5 micron
Principali caratteristiche strutturali e
funzionali degli eucarioti
•
•
•
•
•
•
•
•
•
•
•
Nucleo: presente
Nucleolo: Presente
DNA: diverse molecole di DNA
Parete cellulare: presente nei funghi
Membrana citoplasmatica:Contiene steroli
Mitosi: Presente
Ribosomi : 80S( 60 e 40S)
Respirazione: Associata ai mitocondri
Mobilità: Flagellare, Ameboide,Ciglia
Riproduzione: Asessuata, sessuata
Dimensioni: media 20 micron
Eucarioti
• Paia di
cromosomi,
all’interno di una
membrana
nucleare
• Istoni
• Organelli
• Parete
(polisaccaridi)
• Mitosi
Procarioti
• Un solo cromosoma
circolare, non
all’interno di
membrana nucleare
• Non istoni
• Non organelli
• Parete
(peptidoglicano)
• Scissonie binaria
Trasporto delle proteine, dei
lipidi attraverso la cellula
Confeziona le molecole preparandole alla
secrezione
I BATTERI DIFFERISCONO PER:
1.
2.
3.
4.
5.
Morfologia
Dimensione
Caratteristiche metaboliche
Caratteristiche antigeniche
Caratteristiche genetiche
Grandezze dei microrganismi
•
•
•
•
•
Batteri : Micron (1/1000 di mm)
Virus : Nanometri ( 1/1000 di micron)
Funghi : Micron
Protozoi : Micron
Elminti :mm, cm, metri
( Angstrom: 1/10 di nanometri 1 picometro : 1/1000 di
nanometri)
Classificazione dei batteri
• A seconda delle differenze tra ceppi della
stessa specie si possono distinguere :
• Biotipi (Differenze biochimiche)
• Sierotipi (Differenze antigeniche)
• Fagotipi (Differenze di sensibilità ai
batteriofagi)
• Resistotipi (Differenze di resistenza agli
antibiotici)
TASSONOMIA
Come si chiamano i batteri:
Genere specie
Staphylococcys aureus
Staphylococcus epidermidis
Streptococcus pneumoniae
Sreptococcus pyogenes
Escherichia coli
CLASSIFICAZIONE IN BASE ALLA FORMA
COCCHI
BACILLI
SPIRILLI
CLASSIFICAZIONE IN BASE ALLA DISPOSIZIONE NELLO SPAZIO
• Paia:
diplococchi,
diplobacilli
• Catene:
streptococchi,
streptobacillli
• Ammassi:
stafilococchi
Saprofita cavità orale
Treponema
Forma e disposizione dei
batteri
• Cocchi (diplococchi,
streptococchi,
stafilococchi, tetradi)
• Bacilli (coccobacilli,
diplobacilli,
streptobacilli vibrioni)
• Spirilli (spirochete,
leptospire,spiraliformi).
Grandezze dei microrganismi
• Batteri : Micron (1/1000
di mm)
• Virus : Nanometri (
1/1000 di micron)
• Funghi : Micron ( lieviti
3-5 micron Ife 15-30
micron).
• Protozoi : Micron
• Elminti :mm, cm, metri
• (Angstrom: 1/10 di nanometri
• 1 picometro : 1/1000 di
nanometri)
Coloranti
• Coloranti basici (blu di metilene, fucsina
basica, safranina hanno affinità per le
molecole caricate negativamente)
• Coloranti acidi ( fucsina acida, eosina ,
possiedono elevata affinità per le strutture
cellulari a carica positiva)
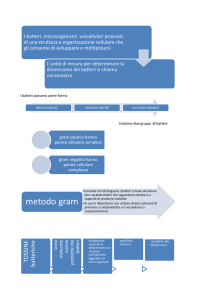
Le Colorazioni
• Si dividono in
• SEMPLICI ( un solo colorante)
• DIFFERENZIALI ( vengono usati piu’
coloranti)
CLASSIFICAZIONE IN BASE AL COMPORTAMENTO
ALLA COLORAZIONE DI GRAM
GRAM POSITIVI
blu
GRAM NEGATIVI
rossi
A Danish doctor working in Berlin, accidentally
stumbled on a method which still forms the basis
for the identification of bacteria.
Colorazione di GRAM
GRAM +
GRAM -
Colorazione di Gram
Diplococchi Gram positivi
(Streptococcus pneumoniae?)
Bacilli Gram positivi ramificati con
colorazione frammentaria (Actinomyces ?)
(ascessi a livello della bocca)
Bacilli Gram positivi ramificati con colorazione
Frammentaria (Nocardia ?)( polmoniti negli immunodepressi)
Bacilli Gram positivi corti con una estremità
Arrotondata (Propionibacterium ?)(patologie della cute
–acne)
Le differenze tra batteri GRAM positivi e
GRAM negativi sono fondamentali in termini di:
VIRULENZA
PATOGENICITÀ
MANIFESTAZIONI CLINICHE
TERAPIA
1-Carattestiche della cellula
batterica
Sruttura – componenti essenziali ( nucleo citoplasma ,
membrana citoplasmatica parete cellulare ) e facoltativi ( pili
,fagelli capsula ,spora )
Caratteristiche dei Gram+ e Gram-
2-Come crescono i batteri
di quali omponenti hanno bisogno per crescere
e come li possiamo identificare
3-Come possono scambiarsi
materiale genetico (coniugazione,
trasformazione , trasduzione)
4-Quali sono i fattori di virulenza
Le strutture della cellula
procariotica
• Strutture fondamentali:
•
•
•
•
•
Parete cellulare
Nucleo
Citoplasma
Membrana citoplasmatica
Mesosomi
• Strutture facoltative:
•
•
•
•
Capsula
Pili
Flagelli
Spora
La membrana esterna
• La membrana esterna è come un rigido
sacco intorno alla cellula. Essa mantiene la
struttura batterica ed è una barriera
impermeabile a grosse molecole e molecole
idrofobiche.
• Protezione dalle condizioni ambientali
avverse
Funzioni della parete cellulare
•
•
•
•
•
Protezione meccanica
Conferimento della forma
Funzione immunitaria
Funzione di virulenza
Responsabile della reazione di Gram
Parete cellulare batterica
• Lo spessore della parete cellulare:
• Il peptidoglicano nei Gram+ varia dai
200-800 A°
• Nei Gram- varia dai 20-30 A°
Parete cellulare
• Il peptidoglicano
nei Gram+ varia
dai 200-800 A°
• Nei Gram- varia dai
20-30 A°
Parete cellulare
• Sulla parete agisce
il Lisozima e la
Penicillina
• Protoplasti ( Gram+
senza parete)
• Sferoplasti ( Gramsenza parete)
Struttura della Parete cellulare
Struttura del peptidoglicano (enorme
polimero)
• a) scheletro portante di natura
polisaccaridica
• b) corte catene peptidiche
• c) legami crociati che si stabiliscono tra
le corte catene peptidiche
Struttura del peptidoglicano
• A) lo scheletro portante contiene 2
carboidrati azotati:
• N-acetylglucosamina e l’acido Nacetylmuramico in sequenza alternata
uniti da legami beta glicosidici.
PEPTIDOGLICANO
Componente fondamentale della parete cellulare dei batteri
Polimero formato dalla ripetizione di una unità strutturale
costituita da 2 carboidrati azotati:
N-acetilglucosamina e Acido N-acetilmuramico legati da un
legame b, 1-6
b,1-6
NAM
NAG
L’acido N-acetilmuramico è a sua volta legato alla
N-acetilglucosamina della subunità successiva da un
legame b, 1-4
b,1-4
b,1-4
Al gruppo carbossilico dell’ac.N-acetilmuramico è inoltre legato
un tetrapeptide (L-alanina, ac. D-glutammico, L-lisina o ac.
Mesodiaminopimelico, D-alanina)
I diversi polimeri lineari sono a loro volta legati trasversalmente
in corrispondenza delle catene tetrapeptidiche da
legami peptidici
Parete cellulare
Diversa nei batteri GRAM positivi o GRAM negativi
GRAM +
GRAM -
GRAM POSITIVI
Ponte pentaglicinico
PARETE DEI BATTERI GRAM +
Acidi tecoici e lipoteicoici
• Sono presenti nei Gram+.
• Sono catene di glicerolo o
ribitolo con legami
fosfodiesterici legati alla
parete (peptidoglicano ).
• Hanno funzione antigenica.
• Hanno funzione di adesività
N-acetylglucosamina (NAG) e acido N-acetylmuramico (NAM).
In E. coli, il pentapeptide consiste degli aminoacidi L-alanina, acido Dglutamico, acido meso diaminopimelico, e due D-alanine.
• Il Monomero Peptidoglicano dello Staphylococcus
aureus
• Nello S. aureus, il pentapeptide consiste degli
aminoacidi L-alanina, D-glutamina, L-lysina, e due Dalanine.
Sintesi del Peptidoglicano, Step 1
I monomeri del peptidoglicano vengono sintetizzati nel citosol
del batterio dove si attaccano ad una molecola trasportatrice di
membrana chiamata bactoprenolo. I bactoprenoli trasportano
i monomeri del peptidoglicano attraverso la membrana
citoplasmatica
Primo step : N-acetylglucosamina (NAG) si congiunge al uridin
difosfato per formare UDP-NAG. Parte del NAG viene
enzimaticamente convertito in acido N-acetylmuramico
(NAM) formando UDP-NAM.
Sintesi del peptidoglicano
Bactoprenolo:
• molecola lipidica con funzioni di trasporto
• È un alcol a 55 atomi di carbonio fortemente
idrofobico che porta legato un precursore
peptidoglicanico
• Ha la funzione di rendere gli intermedi
poisaccaridici sufficientemente idrofobici da
poter passare attraverso la membrana
citoplasmatica
Sintesi del Peptidoglicano, Step 2
Cinque aminoacidi vengono sequenzialmente aggiunte al
UDP- NAM formando un pentapeptide.
Gli ultimi due sono molecole D-alanine enzimaticamente
prodotte da L-alanina, la forma consueta dell’aminoacido.
Il NAM-pentapeptide è attaccato alla molecola portatrice di
bactoprenolo nella membrana citoplasmatica,
L’energia è fornita da uno dei gruppi fosfati ad alta energia
dell’ UDP.
Sintesi del Peptidoglicano, Step 3
A Autolisina
Un gruppo di enzimi AUTOLISINE rompono i legami glicosidici
tra i monomeri di peptidoglicano
a livello del punto di accrescimento della parete e
inoltre rompono i legami che intercorrono tra le catene peptidiche
.
Sintesi del Peptidoglicano, Step 4
Bactoprenoli ed enzimi della transglicosidase (non raffigurati qui)
inseriscono i monomeri del peptidoglicano
nelle rotture del peptidoglicano nel punto di crescita della parete cellulare.
Sintesi del Peptidoglicano, Step 5
Bactoprenoli ed enzimi transglicosidasi (non raffigurati qui)
inseriscono i monomeri del peptidoglicano
nelle rotture del peptidoglicano nel punto di crescita della parete
cellulare.
Sintesi del Peptidoglicano, Step 6
Enzimi transglicosidasi catalizzano la formazione di legami
glicosidoci tra NAM e NAG dei momomeri del peptidoglicano
e NAG e NAM del peptidoglicano esisitente.
Sintesi del Peptidoglicano, Step 7
Infine, enzimi della transpeptidasi riformano i cross-links
del peptide tra le file e gli strati del peptidoglicano
per rendere spessa la parete.
The Role of Penicillins in Blocking Transpeptidase
Enzymes
from Assembling the Peptide Cross-Links in
Peptidoglycan
Penicillins and cephalosporins bind to the transpeptidase enzyme and block the
formation of the peptide cross-links. This results in a weak cell wall and osmotic
lysis of the bacterium.
Batteri Gram A partire dall’esterno all’interno, i Gram
negativi presentano:
a) La membrana esterna
b) Lo spazio periplasmico
c) Il peptidoglicano (sottile).
La Lipoproteina di Braun unisce la
membrana esterna al peptidoglicano
Parete cellulare dei Gram negativi
• Lipide A: funzione tossica ( endotossina)
• Core polisaccaridico
• Antigene O: è costituito da zuccheri che
caratterizzano la specificità antigenica
• Sulla membrana esterna sono presenti le
porine ( trasporto di molecole) e le Omp
(proteine della membrana esterna)
• Lipide A: disaccaride
(glucosamina) con attaccati 3
acidi grassi
• Core polisaccaridico: 10
zuccheri ketodeossioctonato,
fosforiletanolamina. eptosio,
glucosio,galattosio, Nacetylglucosamina.
• Antigene O: catene
polisaccaridiche(galattosio,ramn
osio,mannosio).
LPS
Lipopolisaccaride formato da
Lipide A
(si lega al core polisaccaridico) endotossina
Polisaccaride
core-nelle salmonelle 5 zuccheri(è la
stessa per ogni specie
.
Catena laterale O La catena si attacca al core con
sierotipi
un legame glicosidico distingue i
• Il contenuto proteico nella membrana esterna è
costituito dalle porine e dalle proteine della
Membrana esterna (OMP).
• La membrana esterna e il canale delle porine
permettono il passaggio di metaboliti e di piccoli
antibiotici idrofili, ma la membrana esterna è
una barriera per antibiotici di grandi dimensioni
e proteine come il lisozima.
Membrana esterna
•
•
•
•
Peptidoglicano (sottile)
Spazio periplasmico
Membrana esterna
Lo spazio periplasmico
è unito alla membrana
esterna al
peptidoglicano grazie
alla Lipoproteina di
Braun.
• Spazio periplasmico:
E’ lo spazio tra l’interno della
membrana esterna e l’esterno
della membrana citoplasmatica.
• Contiene:
• Enzimi idrolitici ( proteasi,
fosfatasi, lipasi, nucleasi ed
enzimi degradanti i carboidrati).
• Esoenzimi come collagenasi,
ialuronidasi, proteasi e beta
lattamasi.
• Proteine di trasporto delle
sostanze nutritive e proteine
costituenti il sistema di
chemiotassi.
Di
Brown
Endotossine The presence of endotoxins in the blood is
•
•
•
•
•
•
called endotoxemia
Pirogenicità
Attivazione del complemento
Ipotensione
Ipoglicemia
CID
Collasso cardiocircolatorio
•
•
•
result in systemic vasodilation (hypotension),
diminished myocardial contractility,
endothelial injury
activation of the coagulation system, culminating
in disseminated intravacsular coagulation (DIC)
•
•
This causes multiorgan system failure that affects
the liver, kidneys, and central nervous system,
among others.
Unless the underlying infection (and LPS
overload) is rapidly brought under control, the
patient usually dies)
:
Harmful Effects of Lipopolysaccharide (LPS; Endotoxin)
Released from the Gram-Negative Cell Wall
The LPS binds to a LPS-binding protein circulating
in the blood and this complex, in turn, binds to a
receptor molecule (CD14) found on the surface of
body defense cells called macrophages. This
triggers the macrophages to release various
defense regulatory chemicals called cytokines,
including IL-1, IL-6, IL-8, TNF-alpha, and PAF. The
cytokines then bind to cytokine receptors on target
cells stimulating the production of inflammatory
mediators such as prostaglandins and leukotrienes
as well as activating both the complement
pathways and the coagulation pathway.
Excessive production of clotting factors may lead to
ARDS( acute respiratory distress syndrome) and
DIC(disseminated intravascular coagulation) while
an overproduction of prostaglandins, leukotrienes, and
complement proteins can damage the vascular
endothelium resulting in shock and MOSF(multiple
organ system failure).
Coagulación Intravascular Diseminada
Disseminated intravascular coagulation, or DIC, is a serious disruption in the
body’s clotting mechanism.
Normally, the body forms a blood clot in reaction to an injury.
With DIC, the body overproduces many small blood clots throughout the
body, depleting the body of clotting factors and platelets.
These small clots are dangerous and can interfere with the blood supply to
organs, causing dysfunction and failure. Massive bleeding can occur due to
the body’s lack of clotting factor and platelets.
DIC is life-threatening and needs to be treated promptly.
Disseminated Intravascular Coagulation
Causes
There are many causes of DIC. The disorder is usually caused by a release of
chemicals into the bloodstream from one of the following conditions:
SEPSIS (a system-wide infection), especially with gram-negative bacteria
Strutture di una cellula procariotica
•
•
•
•
•
•
•
•
•
•
•
Strutture fondamentali:
Parete cellulare
Nucleo
Citoplasma
Membrana citoplasmatica
Mesosomi
Strutture facoltative:
Capsula
Pili
Flagelli
Spore
• NUCLEO
• Non è delimitato da membrana nucleare
• Un solo cromosoma, circolare a doppia
elica
Si divide per replica semiconservativa
• PLASMIDI
• Molecole circolari di DNA bicatenario,
replica autonoma, liberi o integrati nel
cromosoma, 2 tipi coniugativi e metabolici
(
metabolici codificano per prodotti utili al batterio)
C itoplasma
• Acqua per il 70%
• presenta corpi inclusi ( granuli di
polifosfato, glicogeno)
• questi granuli sono serbatoi di
carbonio e forniscono materiale
energetico e di biosintesi.
• Ribosomi batterici ( 70S: 50S e 30S)
Membrana citoplasmatica
• Funzioni:
•
•
•
•
Barriera permeabile selettiva
Barriera meccanica
Trasporto di sostanze selettive
Sede di processi metabolici (respirazione,
fotosintesi, biosintesi)
• Separa l’interno della cellula con l’ambiente
cellulare
• Presenza di chemiorecettori
composizione: Come tutte le membrane biologiche in natura la
membrana batterica citoplasmatica è composta di molecole
fosfolipidiche e proteiche.
In realtà è un bilayer fluido fosfolipidico intessuto di proteine. E’ vero
tuttavia che molti batteri contengono molecole simili agli steroli
chiamati opanoidi.
Come gli steroli trovati nelle membrane delle cellule eucariotiche, gli
opanoidi probabilmente stabilizzano la membrana citoplasmatica
batterica.
Funzione principale: La membrana citoplasmatica è una membrana
selettivamente permeabile
Mesosomi
• I mesosomi sono
invaginazioni della
membrana plasmatica
• Forma vescicolare,
tubulare, lamellare.
• I mesosomi settali:
aiutano al replica del
cromosoma batterico.
• I mesosomi lamellari
sono implicati nel
processo di
secrezione.
Pili
• I Gram- hanno strutture proteiche esterne dette pili o
fimbrie.
• Lunghezza di 9-10nm di diametro
• 2 tipi ( sessuali, comuni)
• I sessuali partecipano nel processo di trasferimento
genetico detto Coniugazione)
• I pili comuni aiutano l’adesione batterica
• Sono codificati da plasmidi
Flagelli
• La sintesi dei flagelli è regolata da 2030 geni
• Movimento rotazionale
• Nei Gram- 4 anelli, nei Gram+ 2 anelli
• L’energia è fornita dalla forza motrice
dei protoni, negli eucarioti l’energia è
fornita dall’ATP.
Flagelli
• Organi di locomozione
• Lunghi 15-20 micron
• In base al numero e
disposizione dei
flagelli i batteri sono
monotrichi, lofotrichi,
amfitrichi, peritrichi.
• Struttura: 3 parti:
Filamento,
• Corpo basale,
• Uncino
Flagello :un filamento cavo di lunghezza variabile
composto dalla proteina flagellina è collegato ad una
struttura di raccordo detta uncino
Figura 3.34 Ultrastruttura dei flagelli batterici. Struttura
dei corpi basali e dei ganci nei batteri Gram-negativi (a) e
Gram-positivi (b).
Microbiologia 6/ed
L. M. Prescott, J. P. Harley, D. A. Klein
Copyright © 2006 - The McGraw-Hill Companies, srl
Flagelli
• La sintesi dei flagelli è
regolata da 20-30 geni
• Movimento rotazionale,
a capriola.
• Nei Gram- 4 anelli, nei
Gram+ 2 anelli.
Flagelli
• I batteri grazie ai flagelli si muovono
• Chemiotassi positiva: verso fonti nutritive
• Chemiotassi negativa : si allontanano da
antibiotici, disinfettanti
• Presenza di chemiorecettori sullo spazio
periplasmico o sulla membrana
citoplasmatica
CAPSULA
• Glicocalice o capsula.
Composta da
polisaccaridi, proteine
(B.anthracis).
• Proteggono il batterio
dalla fagocitosi.
• I batteri capsulati si
colorano con inchiostro
di china.
• Lo strato di slime ha
funzione d’adesività,
rigidità e virulenza.
Streptococcus pyogenes
Acido D glutammico
Spora
• Quando le condizioni ambientali
diventano sfavorevoli avviene la
• Sporulazione: formazione della spora
• Forma di resistenza alla T°, radiazioni,
Essiccamento, Disinfettanti
• Generi Bacillus e Clostridium
Formazione della spora
• Cellula batterica madre in cui si forma la
spora si chiama sporangio
• Nello sporangio la spora si localizza o a livello
centrale o ad una estremità
Spora
Forma di resistenza alla T°,
Rapporto sporangio-spora :
Battridio, Plettridio, Clostridio.
Plettridio
Clostridio
Battridio,
Composizione della spora
• Composizione della spora dall’esterno
verso l’interno (al m.e): Esosporio, tunica
esterna, tunica interna, corteccia.
• La spora è composta da acido dipicolinico
complessato agli ioni calcio.
• Povera di acqua
• Ricca di proteine solforate.
Sporulazione
La sporulazione avviene in
10 ore circa e comprende
7stadi
1. formazione del filamento
assiale
2. formazione del setto
sporale
3. formazione di membrana
che avvolge parte del
DNA
4. formazione della
corteccia
5. formazione delle tuniche
6. formazione dell’esosporio
7. maturazione , enzimi litici
che distruggono lo
sporangio e rilasciano la
spora libera.
2 Setto sporale
3 Membrana
che avvolge
il DNA
7 enzimi litici
4Corteccia
5 Tuniche
6 esosporio
La spora batterica:
attività metaboliche di interesse durante la sporulazione
Stadio 0
Cellula
vegetativa
Stadio II Stadio III Stadio IV
Setto della protoplasto corteccia
spora
Enzimi e
sostanze
con attiv
antibiotica
Antibiotici
Proteasi
Amilasi
Fosfat.
alcalina
Aconitasi
Catalasi
Stadio V
tuniche
Stadio VI
maturazione
Acido
Incorpora Rsistenza al
dipicolinico zione di
calore
cisteina
Incorporaz
di Calcio
•Termoresistente
• Priva di attività metabolica
• Resistente a molti agenti chimici e fisici, antibiotici,
disinfettanti, enzimi idrolitici, solventi, radiazioni
ionizzanti e U.V.
La spora batterica: esocrescita
Assorbimento d’acqua significativo
grande aumento di dimensioni
Fase principalmente BIOSINTETICA
Esempi di termoresistenza nelle spore:
Clostridium botulinum 330 minuti a 100°C
Clostridium tetani 90minuti a 100°C
(Cellule vegetative : 80°C per 5-10min)
Spora
• Trasformazione di spora dormiente in cellula
vegetativa permette la sporogenesi:
• Attivazione, germinazione, esocrescita in cellula
vegetativa.
• Le spore vengono uccise a 121°C, 15’, 1 atm
• Le cellule vegetative a 100°C
• trasmettono malattie
• servono per il controllo di qualità delle
autoclavi.
CRESCITA BATTERICA
La coltivazione dei batteri in laboratorio
richiede l'impiego dei cosiddetti
"terreni" o "mezzi di coltura", con i
quali si cerca di riprodurre
artificialmente un ambiente in grado di
soddisfare le esigenze metaboliche del
microrganismo che si desidera
coltivare.
Gli scopi principali sono:
1 identificazione del microorganismo
responsabile di infezione e malattia(
scopo diagnostico).
2 studiare le caratteristiche biologiche
(fenotipo , genotipo etc)
I terreni possono essere
acquistati già pronti oppure
la preparazione può
avvenire in laboratorio con
polveri che si trovano in
commercio.
Le istruzioni per la
preparazione sono
riportate sulla confezione
o su appositi manuali per
terreni particolari e più
complessi.
• Sciogliere i costituenti in acqua distillata
(scaldando leggermente).
• Sterilizzare in autoclave a 121° per 15-20
minuti.
• Versare in appositi contenitori (piastre
petri, provette).
• Conservare a 4°C o a temperatura
ambiente a seconda del tipo di terreno.
Terreni di coltura per batteri
Terreni di coltura per i batteri:
• Sono substrati inerti dove
sono contemplate tutte le
necessità metaboliche di cui
ha bisogno il microrganismo
che si vuole isolare.
• Importanti per l’isolamento
dei batteri e quindi per la
cura, diagnosi e e profilassi di
una malattia infettiva.
Elementi essenziali per una
corretta crescita batterica :
• I terreni di coltura devono
essere sterili
• Nel terreno devono essere
presenti sostanze nutritive
• Nel terreno ci deve essere una
giusta concentrazione di sali
minerali
• Nel terreno ci deve essere una
giusta concentrazione di ioni
H+
• La coltura batterica deve
essere incubata a una giusta
temperatura e a una giusta
tensione parziale di ossigeno e
di anidride carbonica
• Nel terreno possono essere
aggiunti fattori di crescita
CRESCITA BATTERICA
ESTRATTI. Tessuti eucariotici (lievito, fegato, cervello,
cuore, muscolo bovino etc.) vengono estratti tramite
ebollizione e poi ridotti ad una pasta concentrata o in
polvere. Questi estratti vengono frequentemente
usati come risorsa di aminoacidi, vitamine e
coenzimi, inclusi molti di quelli necessari come
fattori di crescita. Sono anche presenti
microelementi e altri minerali e solitamente dello
zucchero.
CRESCITA BATTERICA
BUFFER. Questi composti vengono incorporati
per mantenere il range ottimale di pH.
Sostanze come i fosfati di sodio e di potassio
e il carbonato di calcio prevengono
cambiamenti marcati nel pH che altrimenti
risulterebbero dalla produzione microbica di
acidi o basi organici.
CRESCITA BATTERICA
BODY FLUIDS. Sangue, siero, plasma o altri fluidi
biologici sono frequentemente aggiunti alle
colture per l’isolamento e la coltivazione di
molti patogeni.
• I fluidi biologici contribuiscono a fornire fattori
di crescita e/o sostanze che detossificano certi
inibitori.
CRESCITA BATTERICA
INDICATORI di pH. Un indicatore acido-base
viene spesso aggiunto a terreni differenziali
per rilevare i cambiamenti nella
concentrazioni di ioni idrogeno durante la
crescita di un oragnismo come accade in, Mac
Conkey Agar (lactose and Neutral Red that acts as a pH indicator,
changing from red to yellow - Lac+ and Lac-)
• Medium: soluzione di nutrienti che
permettono la crescita dei batteri.
• Coltura pura : popolazione di cellule
geneticamente omogenea
• Colonie: crescita di un clone di cellule
sulla superficie dei terreni solidi che
porta ad una visibile massa batterica.
• Clone: cellule di una colonia che
discendono da una singola cellula
originale.
Nutrizione
• Classificazione dei
terreni di coltura per i
batteri:
• Stato fisico:
• Liquidi e
• Solidi
Nutrizione
Terreni liquidi:
• Brodo di carne
•
Acqua peptonata
•
Bile
•
Siero di latte
Terreni solidi:
• Brodo di carne+ Agar nutriente (1,5%)
• gelatina
• patata
CRESCITA BATTERICA
AGAR.
• Agar è usato per solidificare i terreni di
coltura.
• E’ un polisaccaride ottenuto da certe alghe
marine.
• Agar fonde intorno a 100°C e solidifica
intorno 43°C.
• L’agar non è una sostanza nutriente per i
microrganismi
In base alla composizione i terreni di coltura
possono essere divisi in
• Minimi
• Semplici
• Complessi
• Di arricchimento
• Selettivi
• Differenziali
Nutrizione
• Terreni minimi: sono
costituiti da soli
composti inorganici
• Terreni semplici: Si
conosce l’esatta
proporzione dei singoli
costituenti.
• Terreni complessi: Sono
terreni dei quali l’esatta
composizione non si
conosce.
Nutrizione
Terreni d’arrichimento :
Sono terreni preparati
aggiungendo al Nutrient
agar altri nutrienti
biologici complessi
Terreni selettivi
• Sono terreni che consentono di aumentare la
carica della specie batterica che ci interessa
isolare, grazie alla presenza di fattori che
inibiscono la crescita di specie batteriche
contaminanti presenti nel campione in
esame.
Terreni selettivi: Sono terreni che
permettono l’accrescimento
preferenziale di certe specie patogene
attraverso l’azione d’inibitori capaci di
ritardare ed impedire la
moltiplicazione di specie batteriche
contaminanti (Lowenstein Jensen,
Mannitol Salt Agar, Sabouraud)
Sodio biselenito
Terreni differenziali :
terreni che presentano oltre ai
fattori inibenti, indicatori che ci
consentono d’individuare in
maniera orientativa i batteri
capaci di moltiplicarsi in base
all’aspetto delle colonie ( Mac
Conkey che contiene il lattosio e
il rosso neutro. Le colonie che
fermentano il lattosio si colorano
di rosso)
Selettivo/differenziale. Agar sale-mannitolo
Contiene NaCl, mannitolo, rosso fenolo.
Utilizzato per isolare stafilococchi e
streptococchi, inibisce la crescita della
maggiorparte dei batteri.
MAC KONKEY AGAR
(medium che include il lattosio come unico zucchero fermentante)
esempio
Coliformi
Salmonella
Shigella
Citrobacter (tipico)
Lattosio
fermentante
(acido forte)
+
–
Reazione netta pH
acido
(colonia rossa)
alkalino
(colonia bianca)
.
Culture on Lowenstein-Jensen medium revealed typical
dry,heaped (cumulo)-up yellow to buff -colored colonies
of Mycobacterium tuberculosis.
A) Misura della massa cellulare:
B) determinazione della concentrazione
cellulare:
A) Misura della massa
cellulare:
•
•
•
•
•
misura del peso secco
misura del volume della massa
cellulare
determinazione dell’azoto totale
misura dell’attività metaboliche
Colorimetria
B) Determinazione della
concentrazione cellulare
•
•
•
•
A1) misura del peso secco:
Prelievo della coltura
Raccolta mediante centrifugazione o filtrazione
Seccate alla stufa a secco a 100°C, o sottovuoto a
40°C.
• Il peso secco mg/ml si aggira sul 20-25% del peso
umido.
• A2) Misura del volume della
massa cellulare:
• una aliquota della coltura si
centrifuga in provette
calibrate e si valuta il volume
del materiale sedimentato.
• Viene espresso come % del
volume della coltura.
• Questo metodo trova
applicazione per i
microrganismi a crescita
miceliale.
• A3) Determinazione dell’azoto totale:
• La valutazione dell’azoto totale dà una stima della
massa cellulare. Questa tecnica ha il difetto di
richiedere una quantità di cellule che sta
nell’ordine di milligrammi .
• Altre metodiche sono: la determinazione del
fosforo, proteine, DNA.
• A4) Misura dell’attività metabolica:
• Su questo principio si basa la misura del consumo di
ossigeno da parte di germi aerobi o della produzione
di CO2 da parte degli anaerobi. Mediante l’uso di
precursori radioattivi, sulla base della quantità di
radioattività incorporata, si può valutare la quantità
dei microorganismi
• A5) Colorimetria:
• E’ il metodo più comune sia
per seguire la crescita che
per valutare la massa di una
coltura di germi che non
siano filamentosi.
• La valutazione della
quantità d luce trasmessa
prende il nome di
Turbidimetria, mentre la
valutazione della quantità
della luce riflessa si chiama
Nefelometria( per basse
concentrazioni).
• la Torbidità si misura come
densità ottica D.O. che è
proporzionale alla massa
cellulare.
• Lo strumento utilizzato per
misurare il numero dei
batteri è lo
Spettrofotometro che
fornisce direttamente il
valore della densità ottica
della sospensione.
• La lunghezza d’onda della
luce utilizzata è di 520680nm(riduce
l’assorbimento del mezzo di
coltura)
• B) determinazione
della concentrazione
cellulare:
• Conteggio totale al
microscopio(camere
contacellule)
• Conteggio delle unità
vitali (Diluizione e
piastramento)
. B1)
Conteggio totale al microscopio: camera
contacellule:
•
vetrino con reticolo formato da quadranti e rettangoli di area nota. Un Vetrino
coprioggetti crea una intercapedine di spessore noto, in cui s’introduce una
aliquota della sospensione da contare.
SVANTAGGI:
1 - SI CONTANO SIA I
BATTERI VIVI
CHE QUELLI MORTI
2 - METODO
SOGGETTIVO
• Si contano le piastre con 20-200/30-300
colonie
• Si moltiplica il numero delle colonie contate
per l’inverso del fattore di diluizione
• Si riporta tutto al ml o g di campione
• È preferibile operare la semina in doppio o in
• triplo per aumentare la precisione
Tempo di generazione : il
tempo richiesto per la divisione
cellulare.
Varia con la specie e con le condizioni
di crescita.
Curva di crescita di una coltura
batterica:
a) fase di latenza
b) fase di accelerazione positiva
c) fase di crescita esponenziale
( trofofase )
d) fase di accelerazione negativa
e) fase stazionaria ( idiofase)
f) fase di declino
A) Fase di latenza : detta anche di
ringiovanimento o fase di
adattamento metabolico .
Non si hanno atti moltiplicativi.
La durata della fase di latenza
dipende: dal tipo di batterio,
dall’età dell’inoculo, dallo
stato fisiologico delle cellule e
dal terreno di coltura.
B) Fase di accelerazione positiva :
fase in cui i batteri iniziano a
dividersi, ma solo il 20% si
divide con un tempo di
generazione più lungo rispetto
al suo standard.
• C) Fase esponenziale: o
trofofase o fase logaritmica:
fase in cui il 100% dei batteri si
divide , in maniera asincrona.
• Il batterio in questa fase
produce metaboliti primari.
• D) fase di accelerazione
negativa: Aumentano i
cataboliti tossici e le sostanze
nutritive si riducono. In questa
fase si dividono l’80% dei
batteri, mentre il 20% inizia a
morire.
E) Fase stazionaria o
idiofase: Questa è una fase
dove il 50% si divide
mentre il resto muore. In
questa fase i batteri
producono i metaboliti
secondari ( antibiotici,
tossine, pigmenti,).
I batteri sporigeni durante
la fase stazionaria danno
origine alle spore, per cui il
titolo vitale può restare
costante o diminuire di
poco.
• F) Fase di declino:
La condizione stazionaria è
seguita dalla fase di morte.
Questa si deve alla forte
riduzione di sostanze nutritive
ed all’aumento di sostanze
tossiche. I batteri sporigeni
non raggiungono il declino.
•
•
Crescita asincrona
Crescita sincrona: i metodi di
sincronizzazione possono
essere divisi in 2 categorie:
a) metodi che agiscono sul
metabolismo cellulare
b) metodi fisici che separano le
cellule
Crescita sincrona e metodi di
sincronizzazione
a) Metodi che agiscono sul metabolismo
cellulare portando tutte le cellule della
popolazione allo stesso punto.
b) Metodi fisici che permettono di separare
dalla popolazione la frazione di cellule che
sono nello stesso punto del ciclo cellulare.
Metodi a):
sincronizzazione per sbalzi termici;
sincronizzazione per affamamento;
sincronizzazione mediante illuminazione.
Metodi b):
sincronizzazione per centrifugazione;
sincronizzazione per filtrazione.
• Quando, come in molti studi, si desidera mantenere le colture
in un ambiente costante per lunghi periodi di tempo, possono
essere impiegate colture continue.
• Un sistema di coltura continua è costituito da una camera di
crescita in cui viene continuamente aggiunto terreno fresco e
da cui viene contemporaneamente allontanato un uguale
volume di terreno esaurito.
•
Una volta che il sistema ha raggiunto l’equilibrio ,il numero
delle cellule e la concentrazione dei nutrienti rimane costante.
• Un vantaggio pratico del chemostato è che esso
consente di mantenere una popolazione in fase di
crescita esponenziale per lunghi periodi, anche per
giorni e per settimane.
• Poiché le cellule in fase esponenziale sono
generalmente le più adatte per lo studio fisiologico
dei microorganismi, l’impiego del chemostato
consente ai ricercatori di averne sempre a
disposizione.
• Il chemostato è uno strumento che consente
di controllare sia la densità di popolazione che
la velocità di crescita di una coltura.
Crescita batterica
Colture continue si ottengono in un
Sistema aperto con il controllo di
• Composizione del terreno
• pH (acidofili, neutrofili, basofili),.
• Ossigenazione (aerobi obligati,
anaerobi obbligati, anaerobi
facoltativi),
• Temperatura (psicrofili, mesofili,
termofili)
• particolare tipo di chemostato fornito di una
fotocellula che controlla la torbidità della
coltura, regolando di conseguenza il flusso del
terreno fresco e l'allontanamento di cellule e
cataboliti
• Questi sistemi consentono di effettuare studi
sulle popolazioni microbiche
• Opportunamente modificati vengono utilizzati
per la produzione industriale di prodotti
microbici, quali:
• -Antibiotici -Enzimi
In senso elementare, gli esseri viventi possono
essere classificati secondo il loro “rapporto
con l’ossigeno” in:
• Aerobi stretti (o obbligati) – quelli che
richiedono O2;
• Anaerobi stretti (o obbligati) – quelli che
cresono solo in assenza di ossigeno
• Anaerobi facoltativi – quelli che possono
crescere in presenza o assenza di O2.
coltura in sospensione:
a) I batteri aerobi obbligati si raccolgono in testa alla provetta, in modo da assorbire
la maggior quantità possibile di ossigeno.
b) I batteri anaerobi obbligati si raccolgono sul fondo, per evitare l'ossigeno.
c) I batteri anaerobi facoltativi possono crescere sia in presenza che in assenza di
ossigeno, per cui si distribuiscono lungo tutta la provetta concentrandosi in maniera
maggiore in prossimità della superficie in quanto crescono meglio in presenza di
ossigeno.
:d)Il metabolismo dei batteri aerotolleranti non è influenzato dalla presenza di
ossigeno e, per tale motivo, sono diffusi lungo tutta la provetta.
1- Caratteristiche della cellula batterica
Sruttura – componenti essenziali ( nucleo citoplasma , membrana
citoplasmatica parete cellulare ) e facoltativi ( pili ,fagelli ,capsula e spora)
Caratteristiche dei Gram+ e Gram-
2-Come crescono i batteri
di quali componenti hanno bisogno per crescere come si contano e come
li possiamo identificare
3-Come possono scambiarsi materiale genetico
(coniugazione, trasformazione , trasduzione)
4-Quali sono i fattori di virulenza



![5\) batteri [modalità compatibilità]](http://s1.studylibit.com/store/data/000928299_1-28a224c15810efb654d8d9e4b207aa31-300x300.png)