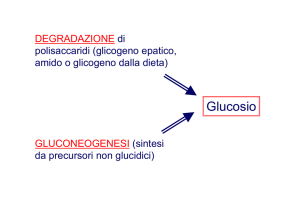
DIVISIONE DEL LAVORO METABOLICO
• MUSCOLO SCHELETRICO
è predisposto a produrre ATP che sarà utilizzato per generare lavoro
meccanico
• TESSUTO ADIPOSO conserva e distribuisce energia sotto
forma di triacilgliceroli, utilizzati come combustibile per tutto il corpo
ma anche come isolante termico
• CERVELLO I neuroni ricavano l’ATP per il trasporto attivo degli ioni
Na+ e K+ dal glucosio ed in condizioni di digiuno dal β-idrossibutirrato.
• FEGATO distribuisce e modifica le sostanze nutrienti rifornendo
tutti gli organi e tessuti attraverso il sangue.
• La sua funzione è correlata alla DIETA o all’intervallo tra i pasti
FUNZIONI DEL FEGATO
• organo intermediario tra l’assorbimento intestinale ed i processi
metabolici che coinvolgono i diversi organi e tessuti
• E’ irrorato da due grossi vasi: la vena porta e l’arteria epatica:
• RICEVE dalla arteria epatica il sangue arterioso proveniente dal cuore.
RICEVE dalla vena porta il sangue venoso refluo dal canale digerente
Contribuisce per il 2-3% alla massa corporea
Consuma circa il 25-30% dell’ossigeno
utilizzato dall’organismo
LOBULI EPATICI
• cellule parenchimatose: epatociti (60-70%)
• cellule non parenchimatose, rivestono i sinusoidi:
Cellule endoteliali, cellule di Kupffer, cellule stellate (30-40%), linfociti “natural killer”
Rappresentazione schematica di un lobulo epatico in sezione
longitudinale: in evidenza i rapporti tra Epatociti vasi ematici e
linfatici
Compartimentazione metabolica conseguente la diversa vascolarizzazione
degli epatociti
FUNZIONI DEGLI EPATOCITI
• ESCLUSIVE
•
•
•
•
Chetogenesi
Detossificazione
Biosintesi di proteine e lipoproteine ematiche
Sintesi di sali biliari
• PREVALENTI
•
•
•
•
Sintesi e catabolismo del glicogeno
Gluconeogenesi
Ureogenesi
Uricogenesi
FUNZIONI delle cellule non parenchimatose
Riconoscimento e degradazione di
macromolecole estranee che arrivano
al fegato
Funzioni
Degradazione delle lipoproteine
plasmatiche che ritornano al fegato;
Idrolisi degli esteri del colesterolo trasportati dalle HDL
REGOLAZIONE del TURNOVER delle lipoproteine circolanti (e del colesterolo)
Cellule di Kupffer (macrofagi specializzati)
Grande capacità fagocitica: Elevato numero di lisosomi
Cellule endoteliali: rivestono i sinusoidi epatici, efficiente diffusione dei metaboliti
dal sangue alle cellule epatiche
Cellule stellate (tra sinusoidi ed epatociti) ricche di lipidi. Immagazzinare vitamina
A e produrre componenti della matrice cellulare
Linfociti natural killer o Pit cells : citotossici nei confronti di linee cellulari
tumorali e di cellule infettate da virus e batteri
FUNZIONI DEL FEGATO
ASSORBIMENTO di componenti dell’alimentazione che vengono
trasportati dall’intestino al fegato attraverso la vena porta
METABOLISMO biosintesi, immagazzinamento, trasformazione o
degradazione a molecole eliminabili
RIFORNIMENTO costante a tutto l’organismo di metaboliti
energetici e materiale strutturale
DISINTOSSICAZIONE, elaborazione di sostanze tossiche
mediante biotrasformazioni
ESCREZIONE attraverso la BILE, formazione e degradazione di
molti componenti del plasma del sangue
Il fegato come organo di raccolta e riciclo…..
RICEVE
le sostanze prodotte dal metabolismo
degli altri organi e tessuti
tutte le molecole assorbite a livello del tratto digerente
DECIDE il loro destino metabolico
RIMUOVE le sostanze tossiche
E’ la CENTRALE DI SMALTIMENTO METABOLICO:
rifornisce tutti gli altri organi e tessuti di sostanze nutrienti
INTERVIENE NEL METABOLISMO DI QUASI TUTTI I METABOLITI
Ha la funzione di mantenere costanti le concentrazioni plasmatiche
di queste sostanze - OMEOSTASI
FASE DI ASSORBIMENTO
• inizia con l’assunzione di cibo, dura da 2 a 4 ore circa
•
• I tessuti utilizzano prevalentemente glucosio
•
• Il FEGATO forma glicogeno e lipidi
Il FEGATO COME ORGANO DI RISERVA E TAMPONE
Principali carboidrati alimentari e loro prodotti di idrolisi
Mais,riso
patate
Grano
Polisaccaride
Zucchero di canna
latte
amido
Disaccaride
Maltosio
Saccarosio
Lattosio
Monosaccaride
Glucosio
Fruttosio e
Glucosio
Galattosio
Glucosio
METABOLISMO DEI CARBOIDRATI
FASE DI ASSORBIMENTO
• Il fegato trattiene 60gr di glucosio ogni 100gr di
zucchero presenti nel sistema portale
•
risponde ad un livello ematico del glucosio:
• AUMENTO della fosforilazione del glucosio
• (GLUCOCHINASI con Km elevato)
• ABBONDANZA di trasportatori GLUT-2
La famiglia dei trasportatori di glucosio
Nome
Localizzazione cellulare
GLUT1
Tutti i tessuti dei mammiferi
GLUT2 Fegato e cellule β del pancreas
Km
1mM
1515-20mM
Commenti
Captazione basale del glucosio
Nel Pancreas svolge un ruolo di
regolazione dell’
dell’insulina
nel Fegato rimuove dal sangue
il glucosio in eccesso
GLUT3
Tutti i tessuti dei mammiferi
5 mM
GLUT5
Intestino tenue
1mM
GLUT4
Tessuto muscolare e cellule adipose
muscolo sotto sforzo
- Principalmente un trasportatore di
Fruttosio. Presenza sulla
membrana indotta dall’
dall’insulina
GLUT2 funziona in modo che la quantità di glucosio all’interno della
cellula è la stessa di quella nel sangue
GLUT sono proteine transmembrana disposte in maniera
asimmetrica
Assumono due conformazioni che
si escludono l’una con l’altra
• Km elevato: 10mM
• Enzima inducibile dall’insulina
• Non viene inibito da un eccesso
di glucosio-6-P
• È regolato da GKRP, proteina
regolatrice della glucochinasi
presente nel nucleo
• Il fruttosio-1-P favorisce il
legame con GKRP
GLUCOSIO e FRUTTOSIO-1-P
SENSORI della
disponibilità degli
zuccheri
GLUCOCHINASI (GK)
Proteina regolatrice della glucochinasi: GKRP o esochinasi IV
GLUCOSIO: favorisce la dissociazione del complesso GK-GKRP
FRUTTOSIO 1-P: favorisce il legame tra glucochinasi e GKRP
SENSORI DELLA DISPONIBILIA’ DEGLI ZUCCHERI
Il ruolo metabolico di questi due isoenzimi è diverso :
Esochinasi
livelli glucosio entro 5mM/L, principale
responsabile della fosforilazione del
glucosio
Glucochinasi
nel fegato è regolata dai livelli di glucosio
nel sangue (>10mM/L) l’eccesso di glucosio è
convertito in G6P
• Esochinasi
– Poco specifica
– Inibita dal glucosio-6P
– Enzima allosterico
• Glucochinasi
– Specifica per il glucosio
– Presente nel fegato
– Non inibita dal glucosio-6P
METABOLISMO DEI CARBOIDRATI
•
•
•
•
•
•
•
GLUCOSIO
GALATTOSIO
FRUTTOSIO
PENTOSIO
LATTATO
GLICEROLO
GLICOGENO
BDT
T
T
BT
T
BT
BDT
•
•
•
•
Biosintesi
Deposito
Escrezione
Trasformazione o
degradazione
Il fegato converte i monosaccaridi l’uno nell’altro……
GLUT2
glucochinasi
METABOLISMO DEL FRUTTOSIO
Molto attivo nel fegato
glucochinasi
VIE METABOLICHE CHE UTILIZZANO IL
GLUCOSIO-6-FOSFATO NEL FEGATO
FASE DI ASSORBIMENTO: elevate concentrazioni di glucosio
LA GLICOGENO FOSFORILASI EPATICA
é inibita da elevate concentrazioni di glucosio
Nel fegato la glicogeno fosforilasi è un sensore per il glucosio
Modificazione allosterica nel fegato
Il GLUCOSIO provoca una Modificazione conformazionale
Che espone i gruppi fosforici della serina-14 all’azione
della FOSFORILASI FOSFATASI I
INSULINA attiva la fosforilasi fosfatasi I (PP1)
Glicogeno fosforilasi a e b nel fegato
Fosfoproteina
Fosfatasi I
Il rilascio della fosfoproteina fosfatasi I (PP1) ATTIVA la Glicogeno sintasi
Benchè l’insulina sia il principale segnale per la sintesi di glicogeno,
il Fegato è sensibile alla concentrazione di glucosio nel sangue e capta
o rilascia glucosio a seconda delle necessità.
AUMENTO DI ATP e G 6-fosfato
E’ FAVORITA LA SINTESI DEL GLICOGENO
METABOLISMO EPATICO DEI CARBOIDRATI
NELLA FASE DI ASSORBIMENTO
• Il trasportatore di glucosio presente negli epatociti è GLUT2
• Il glucosio nel fegato viene fosforilato dalla GLUCOCHINASI
(Km elevato: 10mM), non è inibita dal suo prodotto
1) la glicolisi è accellerata dall’attivazione degli enzimi
chiave quali fosfofruttochinasi e piruvato chinasi. L’acetilCoA viene consumato nella sintesi degli acidi grassi
2) la via del pentoso fosfato decorre più rapidamente
3) Favorita la sintesi del glicogeno
4) La gluconeogenesi è rallentata
La via del pentoso fosfato decorre più rapidamente……….
Fornisce equivalenti riducenti NADPH
Sintesi di acidi grassi
Sintesi di colesterolo e acidi biliari
Reazioni di detossificazione via citocromo p450
Riduzione del glutatione catalizzata dalla
glutatione reduttasi per la rimozione di radicali
liberi dall’organismo
DIFESA DAL DANNO OSSIDATIVO
Glutatione perossidasi
2G-SH + H2O2
Glutatione ridotto
→
GS-SG + H2O
Glutatione ossidato
Glutatione ossidato (GS-SG), viene poi ridotto dalla glutatione reduttasi (NADPH-dipendente)
NADPH + GS-SG ↔ NADP+ + 2G-SH
DEFICIENZA di G-SH comporta un maggiore azione dei processi ossidativi
•
•
•
•
•
METABOLISMO
Acidi grassi
Corpi chetonici
Colesterolo
Acidi biliari
DEL LIPIDI
BT
B
BTE
BE
• METABOLISMO degli Aa.
• Amminoacidi
BT
• Urea
B
Biosintesi
Deposito
Escrezione
Trasformazione o degradazione
VLDL
albumina
METABOLISMO DEGLI ACIDI GRASSI NEL FEGATO
METABOLISMO DEI GRASSI NELLA FASE DI
ASSORBIMENTO
• Il fegato è la sede della sintesi de novo degli acidi
grassi (attivazione della acetil CoA carbossilasi)
• I substrati per questa sintesi: acetil-CoA e NADPH
vengono forniti dal catabolismo dei carboidrati
• I lipidi formati vengono associati a proteine:
• Si formano le lipoproteine a bassa densità VLDL poi
cedute al sangue
• I MAGGIORI CONSUMATORI DI LIPIDI SONO IL
TESSUTO ADIPOSO ED I MUSCOLI
Sintesi delle lipoproteine plasmatiche
VLDL
Trigliceridi e colesterolo dal fegato ai tessuti extraepatici
(muscolo e miocardio)
HDL
Colesterolo, colesterolo esterificato e Fosfolipidi
dai tessuti extraepatici al fegato
Reticolo endoplasmatico rugoso: si sintetizzano le apolipoproteine
Reticolo endoplasmatico liscio: si aggregano le frazioni lipidiche
Apparato del Golgi: componente glucidica, necessaria per la secrezione
Il fegato possiede il più elevato “turnover” proteico e
flusso ematico
PROTEINE PLASMATICHE
LIPOPROTEINE
BT
ALBUMINA
BT
FATTORI DELLA COAGULAZIONE
ORMONI
BT
ENZIMI
BT
BT
METABOLISMO DEGLI AMMINOACIDI NELLA FASE
DI ASSORBIMENTO
• La disponibilità di Aa. é più elevata del fabbisogno del
fegato. In misura limitata aumenta la sintesi proteica
• Una parte viene perciò degradata cioè DEAMINATA
• Lo scheletro carbonioso degli Aa. GLUCOGENICI viene
introdotta nel metabolismo intermedio ( ciclo di Krebs)
• Lo scheletro carbonioso degli Aa.CHETOGENICI
è utilizzato per la sintesi dei lipidi
Assorbimento intestinale
Idrolisi proteica dai tessuti extraepatici
(muscolo)
Principali proteine circolanti prodotte dal fegato
• Albumina
• Proteine di trasporto (transferrina, aptoglobina,
ceruloplasmina, etc…)
• Proteine della coagulazione (fibrinogeno, protrombina,
fattori V, VII, IX, X)
• Apoproteine (apo-B-100, apoA1)
• Inibitori delle proteasi
• Fattori del complemento
• Proteine della fase acuta
METABOLISMO DEGLI AMMINOACIDI NEL FEGATO
FASE DI ASSORBIMENTO
•
•
•
•
•
inizia con l’assunzione di cibo, dura da 2 a 4 ore circa.
I tessuti utilizzano prevalentemente glucosio
Il FEGATO forma glicogeno e lipidi
Aa GLUCOGENICI
ciclo di Krebs
Aa.CHETOGENICI
sintesi dei lipidi
FASE DI POST-ASSORBIMENTO
• risulta prolungata in condizioni di fame o digiuno
• I tessuti consumano prevalentemente acidi grassi,
• amminoacidi e corpi chetonici.
• IL CAMBIAMENTO TRA LE DUE FASI DIPENDE DAL LIVELLO
PLASMATICO DEI METABOLITI E DALL’AZIONE CONCERTATA
DEGLI ORMONI (insulina, glucagone)
Il FEGATO COME ORGANO DI RISERVA E TAMPONE
METABOLISMO DEI CARBOIDRATI NELLA FASE
DI POST-ASSORBIMENTO
(interruzione di apporto di alimenti)
produzione di glucagone (cellule α del pancreas)
insulina inibita (cellule β)
• 1) mobilitate le riserve di glicogeno
• 2) il glucosio-1-P viene trasformato in glucosio-6-P e
dopo distacco del gruppo P (glucosio 6-fosfatasi)
rilasciato nel sangue
• 3) il glicogeno epatico ha una riserva solo di 150gr di
glucosio e si esaurisce dopo 6-12 ore
• 4) si attiva la gluconeogenesi
• 5) si utilizzano gli scheletri carboniosi degli aa.
Glucogenici
Si attiva la GLUCONEOGENESI………..
Consente di mantenere la glicemia nei limiti fisiologici nei periodi di digiuno
Assicura il rifornimento di glucosio al tessuto nervoso,
agli eritrociti, al rene, alla midollare del surrene
Utilizza:
1) Piruvato
2) acido lattico
3) amminoacidi glucogenici
4) glicerolo
Precursori del glucosio e relativa via
metabolica di provenienza
Precursori del glucosio e loro ingresso nella gluconeogenesi
CICLO DI CORI muscolo sotto sforzo
CICLO GLUCOSIO-ALANINA
GLUTAMMATO
α -CHETOGLUTARATO
Gluconeogenesi
da glicerolo
METABOLISMO DEI GRASSI NELLA FASE DI
POST-ASSORBIMENTO
• 1) nel digiuno prolungato la principale fonte di energia
sono gli acidi grassi forniti dal tessuto adiposo
(LIPOLISI)
• 2) gli ac. Grassi sono degradati ad acetil-CoA e
trasformati in corpi chetonici
• (acetoacetato e β-idrossibutirrato)
• 3) la formazione di corpi chetonici aumenta nei primi
giorni di digiuno e rimane costante per settimane
Degradazione e mobilitazione dei trigliceridi
Trigliceride lipasi
Ormone sensibile
Monogliceride lipasi
Digliceride lipasi
Forma fosforilata attiva: indotta dal
glucagone e catecolammine
Forma defosforilata inattiva: indotta
dall’insulina
Acidi grasso e glicerolo
Azione anti-lipolitica
Degradazione e mobilitazione dei trigliceridi
• Una concentrazione bassa di glucosio nel sangue provoca rilascio
di glucagone o adrenalina.
• Il legame al recettore dell'ormone provoca attivazione, tramite
le proteine Gs, dell'adenilato ciclasi che produce cAMP
• La proteina chinasi A (PKA) cAMP-dipendente fosforila le
molecole di perilipina presenti sulla gocciolina lipidica e la
trigliceride lipasi.
• La fosforilazione della peripilina consente l'accesso della
trigliceride lipasi alla goccia lipidica.
• Gli acidi grassi rilasciati viaggiano in circolo legati all'albumina
• Sintesi di VLDL
Mobilizzazione dei triacilgliceroli depositati nel tessuto adiposo
PERILIPINE:
Famiglia di proteine
che limitano l’accesso
alle Gocce lipidiche
FOSFORILAZIONE cAMP/PKA
PERILIPINA-P
Lipasi ormone-sensibile può
degradare il trigliceride
METABOLISMO ENERGETICO NEL FEGATO DURANTE
UN DIGIUNO PROLUNGATO
Come avviene il controllo
della glicemia ?
CARBOIDRATI, INSULINA e GLUCAGONE
SUBITO DOPO I PASTI
TRA I PASTI
Il bilancio netto tra la sintesi del glicogeno e la sua
demolizione è SOTTO IL CONTROLLO DEI LIVELLI
ORMONALI di insulina e glucagone
regolando i livelli di cAMP, determinano i rapporti tra
le forma attive di glicogeno sintasi e glicogeno
fosforilasi.
Gli stessi ormoni regolano anche i livelli di F2,6BP e
dunque il bilancio tra glicolisi e gluconeogenesi.
GLUCAGONE agisce essenzialmente a livello del
fegato mentre L’ADRENALINA o epinefrina ha COME
tessuto bersaglio il muscolo