Università degli Studi di Modena e Reggio Emilia
Corso di Risonanza Magnetica
Nucleare
Parte 1
Cinzia Restani
[email protected]
CIGS
Centro Interdipartimentale
Grandi Strumenti
NMR
Un campione immerso in un forte
campo magnetico può assorbire l’energia di
quelle radiazioni che cadono nella regione
delle radiofrequenze. Di conseguenza le
energie in gioco in questo tipo d’eccitazione
sono molto piccole, meno di 0,1 cal/mole per
un nucleo come il protone (1H )
Un grafico delle intensità dei picchi contro le rispettive frequenze di
assorbimento costituisce uno spettro NMR
FID
Spettro 1H NMR
Se l’assorbimento energetico e’ determinato dalla presenza di certi
nuclei nella molecola …
Le frequenze assorbite sono conseguenza delle caratteristiche del
campione
La spettroscopia NMR fornisce infatti
informazioni sul numero e la posizione di vari atomi in
una molecola. Nel caso del protone, il nucleo d’altra parte
a cui più frequentemente la tecnica è applicata, ci
permette di determinare il numero degli atomi di 1H più
vicini a un altro 1H; così come dà informazioni sulla
presenza nelle immediate vicinanze dell’atomo osservato
di vari gruppi funzionali,come doppi legami C=C, gruppi
carbonilici ecc…
1H
Dipolo nucleare
magnetico
Il 1H ruota intorno al proprio
asse e genera un piccolo
campo elettromagnetico
Rotazione
del nucleo
Il momento angolare P della particella in
movimento è quantizzato e dipende dallo spin nucleare I.
Questo significa che il numero di stati discreti che un nucleo
può assumere dipendono da I secondo la relazione :
2I + 1
Il campo magnetico è caratterizzato da un
momento magnetico nucleare di spin :
= yP= yI h/2
y = rapporto giromagnetico
h = costante di Plank
Il
momento
magnetico
è
proporzionale al momento angolare. Se il
momento angolare è quantizzato, anche il
momento magnetico sarà quantizzato
Momento Magnetico
Nucleare di Spin
Sono osservabili in NMR solo i nuclei che hanno
un momento magnetico nucleare di spin. Essi si comportano
come l'
ago di una bussola che si può orientare in un campo
magnetico applicato
Lo spin nucleare viene prodotto da protoni e neutroni, ed è la
somma degli spin delle singole particelle che compongono il nucleo e che
per ciascuna ha valore di ½
Regole per determinare lo
Spin Nucleare
se i protoni e i neutroni sono entrambi pari, il
nucleo ha spin zero
12C e 16O che hanno I = 0
non hanno momento magnetico di spin
non sono osservabili in NMR
se protoni e neutroni sono entrambi dispari, il
nucleo ha spin intero (1, 2, 3…)
2H e 14N che hanno I = 1, presentano una
distribuzione della carica non sferica, il che
influenza il tempo di rilassamento e di conseguenza
la larghezza dei segnali e l’accoppiamento con i
nuclei vicini, ma sono osservabili in NMR
se i protoni e i neutroni sono gli uni pari e gli altri dispari, il
nucleo ha spin semi intero (1/2, 3/2, 5/2…)
1H, 19F, 13C, 31P, 15N che hanno I = ½ , una distribuzione
sferica ed uniforme della carica e sono osservabili in NMR
Il numero di spin determina il numero
delle orientazioni che un nucleo può assumere in
un campo magnetico esterno uniforme, in accordo
con la formula 2I + 1. Se I = ½ , come nel caso
del 1H, gli stati di spin associati sono due:
α = +1/2 e = -1/2 corrispondenti a due diversi
livelli di energia
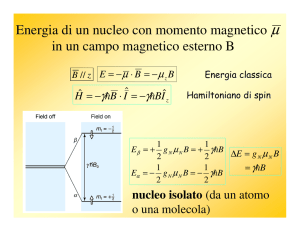
In assenza di campo magnetico
esterno i due stati di spin sono praticamente
equivalenti
- sono isoenergetici Eα = E
- hanno la stessa probabilità di esistere …
- con la stessa densità di popolazione n α = n
In assenza di un campo
magnetico esterno, gli spin sono
casualmente orientati
Un nucleo dotato di spin
immerso in un campo magnetico Bo è
sottoposto, come l'
ago di una bussola, ad
una coppia di forze che lo fa ruotare, per
allinearlo con Bo. Per un nucleo con
spin 1/2, ci sono due orientamenti
permessi:
- parallelo al campo (bassa energia)
- contro il campo (alta energia)
Bo
E =E
Poiché la differenza di energia
tra i due stati di spin è piccolissima,
dell'
ordine di 9.10-6 kcal/mole, si
raggiunge rapidamente l'
equilibrio e in
media solo il 50% dei nuclei assume
l'
orientamento allineato con Bo, mentre il
restante 50% assume l'
orientamento
opposto
Il momento magnetico nucleare non è perfettamente allineato con Bo,
ma continua ad oscillare attorno al campo stesso, compiendo un moto di precessione
simile a quello di una trottola. I due stati possibili del nucleo non hanno la stessa
energia, ma lo stato con m = +1/2 (allineato con il campo) si trova ad energia
leggermente più bassa di quello con m = - 1/2 (opposto al campo)
I nuclei sono soggetti a due forze,
- una che tende ad allinearli al campo
magnetico Bo
- una che li fa ruotare
Come risultato si ha un moto di
precessione
Il momento angolare P della particella in
movimento è quantizzato e dipende dallo spin nucleare I.
Questo significa che il numero di stati discreti che un nucleo
può assumere dipendono da I secondo la relazione :
2I + 1
Il campo magnetico è caratterizzato da un
momento magnetico nucleare di spin :
= yP= yI h/2
y = rapporto giromagnetico
h = costante di Plank
Il
momento
magnetico
è
proporzionale al momento angolare. Se il
momento angolare è quantizzato, anche il
momento magnetico sarà quantizzato
Moto di Precessione
L’interazione tra il momento magnetico del nucleo ed il campo esterno Bo
è il momento torcente
= B0
Questa relazione rappresenta il moto di precessione del momento magnetico del
nucleo intorno alla direzione del campo magnetico Bo
Poiché il momento torcente è definito anche come = dP/dt e poiché per un moto
angolare a velocità 0 si ha che dP/dt = P 0, la velocità angolare del moto di
precessione è espressa dalla ….
Equazione di Larmor:
Frequenza di Larmor:
= yBo radianti/sec
ovvero
= yBo /2 Hz
0
Il moto di precessione dei momenti magnetici
nucleari avviene con una frequenza proporzionale alla differenza di energia
aumentare del
tra i due livelli di spin, detta Frequenza di Larmor: all'
campo applicato aumenta il E tra i livelli energetici e , quindi aumenta
la frequenza di Larmor
Equazione di Plank
Equazione di Plank:
E = h = hyBo /2
L’equazione di Plank è l’equazione NMR fondamentale
correla la radiofrequenza con l’intensità del campo magnetico applicato
Tanto più il campo Bo è forte, tanto maggiore sarà la separazione tra i
livelli energetici, tanto più lo strumento si dimostra sensibile
Abbondanza Naturale
La spettrometria NMR è una tecnica intrinsecamente poco
sensibile
distribuzione degli spin nucleari in presenza di un campo
magnetico Bo
Aumentando il campo magnetico, aumenta il E,
quindi la differenza di popolazione tra livelli di spin e
conseguentemente l’intensità del segnale
L’intensità di un segnale di un isotopo è
proporzionale alla recettività del nucleo stesso:
y3NI(I+1)
N = abbondanza naturale
dell’isotopo considerato
L’abbondanza naturale influisce pesantemente sull’intensità del segnale
I
Abbondanza naturale
%
Y
107 rad T-1s-1
Frequenza di
risonanza
MHz
1H
1/2
99,98
26,7519
100
2H
1
0,016
4,106
11B
1/2
81,17
8,583
12C
0
98,89
----
---
13C
1/2
1,11
6,726
25
14N
1
99,64
1,933
15N
1/2
0,36
-2,711
10
19F
1/2
100
25,167
94
31P
1/2
100
10,829
40
Isotopo
Assorbimento di Energia
Movimento di precessione del 1H
Se il campione viene irradiato con una
radiazione elettromagnetica di frequenza uguale alla
frequenza di Larmor, ci sarà una interazione della
componente magnetica della radiazione (B1) con i
momenti magnetici nucleari oscillanti alla frequenza di
Larmor. L’energia della radiazione potrà così essere
trasferita ai nuclei
Ogni assorbimento di radiazione
comporta un cambiamento di orientazione dello spin
nucleare che ruoterà da allineato con il campo, ad
opposto al campo. Quando si verifica questa
transizione di spin, si dice che i nuclei sono in
risonanza con la radiazione applicata, da qui il nome
di Risonanza Magnetica Nucleare
Segnale NMR
Per esempio per promuovere
una transizione tra i due livelli energetici
del 1H è necessaria una frequenza di
100MHz in presenza di un campo
magnetico di 2,35T, o qualsiasi altra
combinazione /Bo che soddisfi il criterio
di risonanza
A questo punto l’impulso rf cessa ed
entra in funzione un circuito ricevente, in quanto il
ritorno all'
equilibrio di un sistema di spin che ha
assorbito un impulso rf, genera un segnale che può
essere rivelato
FID
I segnali raccolti dal rivelatore vengono rappresentati in un
interferogramma, il cosiddetto FID (free induction decay), in
cui l’intensità del segnale tende esponenzialmente a zero al
passare del tempo (decadimento nel dominio del tempo)
Spettro
Con la trasformata di Fourier il grafico nel dominio del tempo viene
convertito in un grafico nel dominio delle frequenze, cioè si passa dal
FID ad un classico spettro NMR
Campo basso
Intensità del segnale
Campo alto
Scala delle Ascisse in ppm
A
seconda
del
tipo
di
spettrometro varie scale possono essere
utilizzate per definire la localizzazione dei
picchi, relativamente a un composto di
riferimento che in genere é il tetrametilsilano
(TMS)
Il TMS è un liquido volatile, simmetrico, solubile nella maggior parte dei
solventi organici, non reagisce con la maggior parte dei composti organici, ha un atomo di
Si debolmente elettronegativo e può essere aggiunto direttamente alla soluzione del
campione come standard interno (zero della scala). Gli spettri riportano generalmente la
scala sull’asse delle ascisse. Questa scala è in unità di parti per milione (ppm)
La scala è calcolata secondo l’equazione
= chemical shift (Hz) x 106/frequenza portante del nucleo (Hz)
ed é definita in modo tale che la posizione dei segnali (chemical shift) sia
indipendente dalla frequenza portante a cui oscilla il protone. Il segno dello
shift rispetto il TMS (0 ppm) per convenzione é preso come positivo, per
segnali che appaiono a campi più bassi del TMS e negativo se é a campi più
alti. Nel caso di una scala in Hz lo stesso segnale avrebbe shift differenti in
relazione al campo magnetico utilizzato, al contrario se usiamo la scala in
ppm. Esempio: un segnale a 300 Hz in un apparecchio a 300 MHz lo si
ritrova a 600 Hz nel caso di un apparecchio a 600 MHZ
Chemical Shift
Nuclei della stessa specie non sono tutti magneticamente
equivalenti, perché la presenza di e- facenti parte della struttura
tridimensionale della molecola, produce variazioni nell’ambiente
magnetico intorno ad ogni atomo.
1H magneticamente non equivalenti “sentono” campi magnetici
diversi (anche se di poco) e quindi risuonano a frequenze diverse
La differenza nella posizione di
risonanza di un particolare protone rispetto a
quella di un protone di riferimento (TMS) viene
detta spostamento chimico-chemical shift. La
grandezza del chemical shift dipende
principalmente dall’elettronegatività dei gruppi
funzionali che sono vicini ai protoni osservati e
la natura dei campi magnetici indotti Bi in
molecole che hanno legami
Entrambi gli effetti sono associati con la
circolazione degli e- nella molecola e con le interazioni dei
campi magnetici indotti con il campo B0 applicato
Anisotropia
diamagnetica la schermatura e la
deschermatura di un nucleo dipendono dall’orientazione della
correnti
molecola rispetto a
B0 presenza di eindotte campi indotti orientazione dei campi indotti
rispetto il campo applicato
Beff = B0+Bi deschermatura
Beff = B0-Bi schermatura
Elettronegatività
La schermatura subita da un nucleo
dipende direttamente dalla densità e- che lo
circonda, pertanto, in assenza di altre perturbazioni,
ci si dovrebbe aspettare che diminuisca con
l’aumentare dell’elettronegatività dei gruppi
adiacenti. L’influenza dell’elettronegatività è
evidente quando si fa un confronto tra i chimical
shift degli alogenuri di metile, CH3-X
Ibridazione e Anisotropia magnetica
L’influenza degli ela si vede quando si
confronta il chemical shift dei protoni alifatici di un alcano
con quello dei protoni vinilici di un alchene ad esempio
etano (CH3-CH3 =0.9 ppm) ed etilene (CH2=CH2 =5.25
ppm)
I nuclei di H dell’etilene sono deschermati in parte perché un atomo di C ibridato sp2
è più elettronegativo di un C ibridato sp3, in parte perché i protoni vinilici si trovano in una
regione di campo in cui Bi si somma a B0: Beff = B0+ Bi
La molecola dell’acetilene è
lineare, ed il triplo legame è simmetrico
rispetto all’asse della molecola. Se tale asse
si trova allineato con B0 gli elettroni del
legame acquistano un movimento circolare
perpendicolare al campo B0, generando un
Bi che si oppone a B0. Poiché i protoni
giacciono lungo l’asse magnetico, le linee
di forza del campo indotto dal movimento
circolare degli e- agiscono da schermo nei
confronti dei protoni.
I protoni dei composti aromatici, come nel benzene ( =7.27 ppm),
risuonano a campi più bassi di quelli dei protoni vinilici degli alcheni perché c’è una
ibridazione sp2 in entrambe le molecole, ma il Bi è maggiore nell’anello benzenico per
via della natura ciclica della circolazione degli e- . Questo effetto prende il nome di
“corrente ad anello”.
Gli
effetti
notevoli che alcuni gruppi
hanno sul chemical shift
hanno portato alla stesura
di tabelle in cui si correla
lo spostamento chimico
con
le
caratteristiche
strutturali che lo hanno
provocato
Molteplicità dei Segnali
La spettroscopia NMR, tramite la molteplicità dei segnali, ci fornisce
informazioni relativamente al numero di vicini immediati che un particolare tipo di
idrogeno possiede. Vicini immediati sono definiti quegli atomi che hanno un momento di
spin >0, solitamente ½ e si trovano in molti casi a non più di tre legami o di due atomi di
distanza dall’atomo in esame
L’accoppiamento di spin, come
viene definito il fenomeno, può essere
descritto come un accoppiamento indiretto
degli spin protonici mediante gli e- di
legame. Lo spin di un
e- di legame
influenzerà un altro e- di legame e così via.
Nel caso di un accoppiamento H-H, come in
CHA-CHX, il protone HA “sentirà” due campi
magnetici diversi a seconda dello stato di
spin di HB e darà origine a due segnali nello
spettro NMR (doppietto)
L’accoppiamento tramite due legami viene detto geminale, l’accoppiamento
tramite tre legami viene detto vicinale. Generalmente l’accoppiamento perde di importanza
oltre il terzo legame a meno che non sia presente una tensione ad anello, come nel caso di
piccoli sistemi ciclici, una delocalizzazione, come nel caso degli anelli aromatici ecc …
La differenza di frequenza in Hz tra i picchi che costituiscono il segnale è
proporzionale all’efficacia dell’accoppiamento e viene indicata mediante una costante
d’accoppiamento J che è indipendente dal campo magnetico B0. Le costanti
d’accoppiamento tra i protoni raramente superano i 20 Hz
E’ possibile prevedere la molteplicità del sistema di ogni
tipo di nucleo chimicamente distinto secondo le regole generali:
- nel caso di un nucleo A con momento di spin Iz che si accoppia
con un atomo X, il segnale dell’atomo X viene suddiviso in un numero
di picchi dato dall’equazione
N =2nIz + 1
N = numero di picchi osservabili per X
n = numero di atomi A magneticamente
equivalenti e vicini a X
Iz = spin nucleare dell’atomo A
- Se Iz = ½ l’equazione viene semplificata
N=n+1
Queste regole valgono nel caso di analisi del I ordine
quando /J > di circa 9,10 e le costanti di accoppiamento di tutti i
nuclei di idrogeno accoppiati con il nucleo in esame assumono lo stesso
valore
Le intensità dei picchi di un multipletto dipendono, a loro volta, da n.
Nel caso di un doppietto le intensità dei picchi si trovano in rapporto di 1:1: in un tripletto
sono in rapporto 1:2:1; in un quartetto 1:3:3:1. La formula generale è
(a + b)n
Quando questo binomio viene sviluppato per il valore desiderato di n, i coefficienti
forniscono le intensità relative. La molteplicità e le intensità relative possono essere ricavate
dal triangolo di Pascal in cui n è il numero di protoni equivalenti. La rispondenza tra le
intensità calcolate e quelle osservate è tanto migliore quanto più il rapporto /J è grande
Nel caso in cui non siano rispettati i criteri riassunti in tabella si
osservano dei sistemi di spin la cui molteplicità non può essere descritta in
base alla regola n+1
Integrazione
Le aree dei picchi in uno spettro 1H NMR sono un’importante misura del numero
relativo dei nuclei di idrogeno presenti in una molecola perché queste aree sono una funzione
lineare del numero dei nuclei che hanno generato il picco
L’altezza
dei
singoli
scalini
è
proporzionale all’area dei
picchi sottostanti e quindi
al numero di protoni che ha
generato quel certo segnale.
Le misure di integrazione sono affette da un 5-10% di errore