Chimica Organica
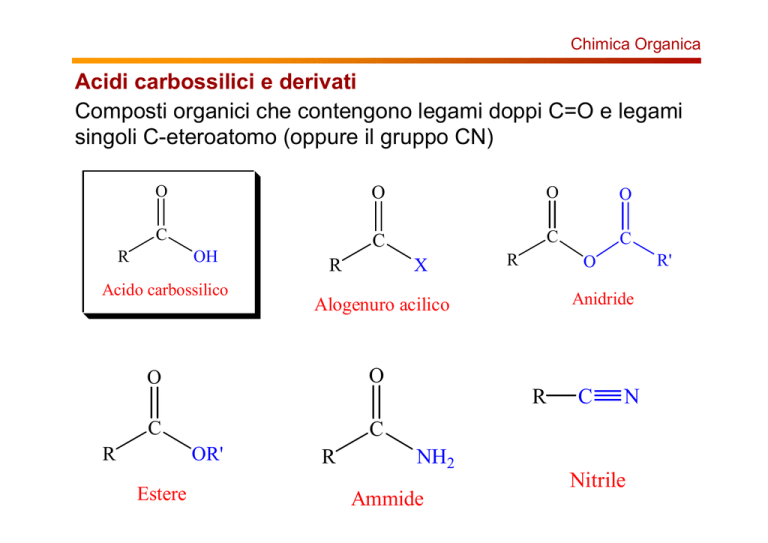
Acidi carbossilici e derivati
Composti organici che contengono legami doppi C=O e legami
singoli C-eteroatomo (oppure il gruppo CN)
O
O
O
O
C
C
C
C
R
OH
Acido carbossilico
R
X
R
Anidride
Alogenuro acilico
O
O
R
C
R
C
N
C
OR'
Estere
R'
O
R
NH2
Ammide
Nitrile
Chimica Organica
Nomenclatura degli acidi
Si individua la catena di atomi di carbonio più lunga contenente il gruppo
carbonilico e si cambia la desinenza in –oico premettendo il suffisso acido.
Si numerano i carboni partendo dal gruppo carbossilico. Si assegnano
numero e nome a ciascun sostituente che vengano riportati in ordine
alfabetico
Per i composti che hanno il gruppo –CO2H direttamente legato a un anello
si usa il suffisso –carbossilico (sempre premettendo la parola acido)
Chimica Organica
Nomi comuni degli acidi carbossilici
Formula
Nome
Comune
Origine
Nome IUPAC
Punto di
Eboll.
HCO2H
Acido Formico
Formiche
(L. formica)
Acido Metanoico
101° C
CH3CO2H
Acido Acetico
Aceto (L. acetum)
Acido Etanoico
118° C
CH3CH2CO2H
Acido
Propionico
Latte
(Gk. protus prion)
Acido
Propanoico
141° C
CH3(CH2)2CO2H
Acido Butirrico
Burro (L. butyrum)
Acido Butanoico
164° C
CH3(CH2)3CO2H
Acido
Valerianico
Radice della
valeriana
Acido
Pentanoico
186° C
CH3(CH2)4CO2H
Acido
Capronico
Capra (L. caper)
Acido Esanoico
205° C
CH3(CH2)5CO2H
Acido Enantico
Vite
(Gk. oenanthe)
Acido Eptanoico
223° C
Chimica Organica
Proprietà degli acidi carbossilici
δO
H
H
C
C δ+ O
δ+
H
δ-
H
Acido acetico
La presenza di un sito donatore ed uno accettore di legami ad idrogeno consente la
formazione di dimeri. Le temperature di ebollizione degli acidi carbossilici sono molto
elevate.
Chimica Organica
Proprietà degli acidi carbossilici
Chimica Organica
Proprietà degli acidi carbossilici
La maggior stabilità dell’anione carbossilato (per risonanza) giustifica la maggior
acidità degli acidi carbossilici rispetto agli alcoli.
Chimica Organica
Proprietà degli acidi carbossilici
Chimica Organica
Proprietà degli acidi carbossilici
Chimica Organica
Proprietà degli acidi carbossilici
Chimica Organica
Nomenclatura degli alogenuri acilici
Gli alogenuri acilici prendono il nome identificando l’alogeno e poi il gruppo
acile a esso legato. Il nome del gruppo acile si fa derivare da quello
dell’acido corrispondente togliendo la parola acido e cambiando la
desinenza –ico in –ile, oppure –carbossilico in –carbonile.
Chimica Organica
Nomenclatura degli esteri
Il nome degli esteri si ricavano identificando prima l’acido carbossilico da
cui derivano, togliendo la parola acido e cambiando la desinenza –ico in –
ato e poi aggiungendo il nome del gruppo alchilico legato all’ossigeno.
Chimica Organica
Nomenclatura delle anidridi
Le anidride simmetriche derivanti da acidi monocarbossilici, e quelli cicliche
derivanti da acidi dicarbossilici vengono denominate semplicemente
sostituendo la parola acido con la parola anidride.
Chimica Organica
Nomenclatura delle ammidi
Le ammidi che non hanno alcun sostituente sull’azoto vengono denominato
sostituendo la desinenza –ico o –oico dell’acido con quella –ammide,
oppure quella –carbossilico con -carbossammide.
Se l’atomo di azoto è legato a sostituenti alchilici, il nome dell’ammide si fa
precedere dalla maiuscola corsiva N, per indicare la sostituzione sull’azoto,
seguito dai nomi dei gruppi alchilici sostituenti.
Chimica Organica
Nomenclatura dei nitrili
I nomi dei nitrili semplici aciclici si ricavano aggiungendo il suffisso –nitrile
al nome dell’alcano corrispondente, considerando l’atomo di carbonio
nitrilico come C1.
CH3
CH3CN
CH3CHCH2CH2CN
5
4
3
2
1
4-Metilpentanonitrile
Etanonitrile
(Acetonitrile: dall'acido acetico)
CN
6
1
5
CN
CH3
4
Benzonitrile
(dall'acido benzoico)
2
3
CH3
2,2-Dimetilcicloesancarbonitrile
(dall'acido 2,2-Dimetilcicloesancarbossilico
Chimica Organica
Sostituzione nucleofilica acilica
Addizione nucleofilica (aldeidi e chetoni)
δO
R
C
δ+
_
O
_
R
Nu
H3O
C
C
R
OH
+
Nu
R
R
Nu
R
Sostituzione nucleofilica acilica (derivati degli acidi)
δO
C
R δ+
_
_
X
Nu
R
O
O
C
C
X
Nu
R
Nu
Chimica Organica
Sostituzione nucleofilica acilica
Chimica Organica
Sostituzione nucleofilica acilica
Chimica Organica
Reazioni degli acidi carbossilici
1. Riduzione ad alcoli
2. Conversione a cloruri acilici
Chimica Organica
Reazioni degli acidi carbossilici
3. Esterificazione di Fischer
O
R
COH
Acido carbossilico
O
+
R'
OH
Alcol
H2SO4
R
COR'
Estere
+ H2O
Chimica Organica
Reazioni degli alogenuri acilici
Chimica Organica
Reazioni delle anidridi
Chimica Organica
Reazioni degli esteri
Chimica Organica
Reazioni dei nitrili
H2O
R
H3O+ o OH-
C
N
Nitrile
O
C
R
LiAlH4
H
H
OH
C
+ NH3
R'MgX
R
NH2
Ammina
Acido carbossilico
O
C
R
Chetone
R'
Chimica Organica
Meccanismo dell’addizione acilica di reattivi di
Grignard a gruppi ciano.
_
R
C
+ R' MgX
N
R
C
N
MgX+
R'
H3O+
OH
R'
R
R'
C
R'
MgX
R
C O
R'
+ MgXOH + NH3