AGGIORNAMENTI
Bif XIV N. 3
103
2007
Terapia della degenerazione maculare
correlata all’età
La registrazione di due nuovi farmaci, da parte dell’Agenzia Europea dei Medicinali (EMEA), per la terapia della degenerazione maculare umida, prevede che le ditte definiscano un piano educazionale (educational plan) per gli operatori sanitari e per i pazienti al fine di informarli sul corretto impiego del farmaco e sugli eventuali rischi di utilizzo1,2. Il Bif, con
questo articolo, vuole contribuire con una valutazione critica delle due nuove entità terapeutiche.
Riassunto
dei trattamenti oggi disponibili, in confronto al ruolo
clinico delle due nuove entità terapeutiche (pegaptanib e ranibizumab, rispettivamente principi
attivi di Macugen® e Lucentis®).
Due nuovi farmaci stanno facendo la loro
comparsa nel panorama delle terapie oggi disponibili
per rallentare la progressione di una patologia diffusa
tra la popolazione anziana: la degenerazione maculare
correlata all’età (age-related macular degeneration,
ARMD). Questa malattia ad eziologia sconosciuta, con
carattere progressivamente degenerativo, provoca la riduzione della capacità visiva e costituisce una delle
principali cause di cecità nei soggetti anziani.
Il pegaptanib è stato immesso in commercio in
Italia nell’ottobre 2006 e recentemente (30 gennaio
2007) l’EMEA ha approvato la commercializzazione
anche del ranibizumab, un anticorpo anti-VEGF,
proteina con attività angiogenetica fortemente espressa
nei pazienti affetti da ARMD.
Alla luce dei dati oggi disponibili, emerge che questi
due farmaci possono avere un ruolo nel rallentare la
progressione della patologia, anche se al momento gli
studi sono ancora limitati per chiarire se questo effetto
si mantenga per periodi superiori ai due anni, ma soprattutto se il rapporto beneficio-rischio rimanga favorevole nel lungo periodo.
Inoltre, i diversi approcci terapeutici, come la
terapia fotodinamica, la terapia laser e la supplementazione con antiossidanti più zinco, assumono un
grado di utilità terapeutica variabile, in funzione dell’estensione e della localizzazione delle lesioni (se
subfoveale o generalizzata) e del tipo di degenerazione (se essudativa o atrofica). La forma più rara è
quella essudativa o “umida” ed è proprio su questa
che si concentra la terapia con i nuovi farmaci e con
gli altri interventi non farmacologici. Per la forma più
comune, quella secca, sono invece disponibili poche
opzioni terapeutiche.
Attualmente il costo elevato del trattamento con i
nuovi farmaci antiangiogenetici rappresenta sicuramente un limite a fronte di benefici modesti (rallentamento della progressione degenerativa).
Questo articolo presenta una sintetica panoramica
Abstract
Two new drugs are now marketed to treat a widespread
disease among the elderly population: age-related macular
degeneration (ARMD). This disease is progressively degenerative and of unknown etiology. It may lead to a loss of
vision in both eyes (blindness) in the elderly.
Pegaptanib has been marketed in Italy since October
2006 and recently (30th January 2007) the EMEA has approved also the marketing of ranibizumab, an anti-VEGF –
a protein having angiogenic activity expressed in patients
affect of ARMD.
According to available data, these two drugs may slow
down disease progression. Nevertheless, studies are not
enough to make clear if the drug effect may last more
than 2 years, and the long-term safety profile of the drug
is still unknown.
Moreover, the different therapeutic strategies such as
photodynamic therapy, laser therapy and supplementation with antioxidants plus zinc present unpredictable
therapeutic usefulness, depending on the extension and
localization of lesions (subfoveal or generalized) and on
the type of degeneration (exudative or atrophic). The
rarest form is the exudative or humid. These new therapies, as well as the majority of drugs, focus mainly on
the treatment of this form, whereas few therapies are at
the moment available to treat the most common form,
the dry one.
The cost of the new antiangionetic treatments is a
strong limit compared to the modest benefit they produce
(slowing down of degenerative progression).
This article presents the different therapies now available to treat the disease and compared them to the clinical relevance of the new therapeutic options (pegaptanib for Macugen® and ranibizumab for Lucentis®).
!
Agenzia Italiana del Farmaco
104
Bif XIV N. 3
AGGIORNAMENTI
2007
Introduzione
ossido e 2 mg di ossido di rame; antiossidanti più
zinco; o placebo. Dopo un periodo di follow-up
medio di 6,3 anni, sono stati osservati i seguenti
risultati: i pazienti senza o con ARMD
media/borderline non hanno avuto benefici dal
trattamento antiossidante e/o della supplementazione di zinco, i pazienti con ARMD moderata e avanzata presentavano una diminuzione del
rischio di progressione della malattia e della perdita di acuità visiva se avevano assunto antiossidanti e zinco rispetto al placebo per sette anni
(35,7% vs 26,7%, OR 0,66, IC 0,47-0,91). Inoltre, questi due gruppi hanno evidenziato una riduzione del rischio anche quando veniva assunto soltanto lo zinco (OR 0,71, IC 0,52-0,91).
In particolare i pazienti affetti da ARMD secca
generalizzata o con atrofia non centrale in uno
o entrambi gli occhi hanno beneficiato del trattamento.
In base ai dati dello studio AREDS sarebbe necessario trattare 11 pazienti per sette anni con la
supplementazione di antiossidanti e zinco per
prevenire la progressione della malattia in uno
di loro.
A fronte di questi dati di efficacia, va sottolineato che la supplementazione di antiossidanti
ad alti dosaggi sembra associata ad un significativo aumento del profilo di rischio: la terapia
con beta-carotene, secondo diversi studi, può
essere associata ad aumento dei tumori al
polmone e ad un possibile aumento del rischio di
malattie cardiovascolari, mentre la vitamina E ad
un aumento del rischio di mortalità cardiovascolare e di attacco cardiaco.
Non ci sono farmaci autorizzati per quest’impiego che è quindi limitato ad alcuni supplementi dietetici.
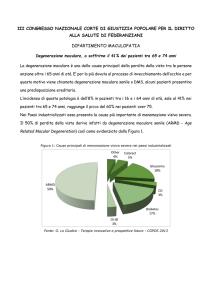
L’
angiogenesi patologica rappresenta la più
diffusa causa di cecità nel mondo industrializzato. Tra le malattie con eziologia angiogenetica della retina le più diffuse nei paesi occidentali sono la retinopatia diabetica e la
degenerazione maculare correlata all’età (agerelated macular degeneration, ARMD). In quest’ultima condizione patologica, la neovascolarizzazione avviene nella coroide e nelle forme più
gravi, che sono causa maggiore di cecità nei
soggetti sopra i 64 anni3, si sviluppano microemorragie derivate dalla formazione di nuovi vasi
sanguigni che portano alla perdita della vista. La
proteina angiogenetica VEGF (Vascular Endothelial Growth Factor) è marcatamente aumentata nella ARMD e può essere uno dei principali mediatori della malattia.
La ARMD ha due caratteristiche morfologiche
diverse: la forma secca (atrofica), che è la più
comune, e la forma umida (neovascolare o essudativa), che è quella più rara, ma con la maggiore
incidenza di cecità3. È proprio su quest’ultima che
si concentrano le terapie con i nuovi farmaci e
con gli altri interventi non farmacologici. Per la
forma più comune, invece, sono disponibili
poche opzioni terapeutiche.
Le terapie
Terapia della forma secca di ARMD
• Antiossidanti e zinco
Lo studio AREDS4 ha coinvolto 3640 soggetti, tra
i 55 e gli 80 anni, i quali sono stati suddivisi
in 4 gruppi: pazienti
Il costo elevato senza ARMD, con
ARMD media o bordel trattamento
derline, con ARMD
con i nuovi
moderata e con ARMD
avanzata. I pazienti
farmaci
stati assegnati in
antiangiogenetici sono
modo random ad alrappresenta
trettanti gruppi di trattamento: antiossidanti
sicuramente
(500 mg di vitamina
un limite a fronte C, 400 UI vitamina E,
15 mg di beta carotedi benefici
ne); 80 mg di zinco
modesti
sotto forma di zinco
• Laser
Alcuni studi5,6 hanno valutato l’efficacia della
terapia laser in persone con alto rischio di ARMD
secca allo scopo di prevenirne la progressione. I
primi studi randomizzati hanno osservato che la
terapia con il laser producesse piccoli miglioramenti nell’acuità visiva5; tuttavia uno di questi
trial ha evidenziato un aumento del rischio di
neovascolarizzazione negli occhi trattati6. Due
recenti studi randomizzati sono stati interrotti a
causa di un aumento del grado di neovascolarizzazione7,8.
Un ulteriore studio 9 ha dimostrato che la
terapia laser non determina alcun beneficio in
pazienti con ARMD.
“
”
!
Agenzia Italiana del Farmaco
bollettino d’informazione sui farmaci
Bif XIV N. 3
Terapia della forma umida di ARMD
105
2007
teporfina. Il 94,3% dei pazienti trattati con 0,3 mg
di ranibizumab ed il 96,4% di quelli con dosaggio
da 0,5 mg hanno perso meno di 15 lettere verso il
64,3% di quelli trattati con verteporfina (p < 0,001
per entrambi i confronti). L’acuità visiva è migliorata di 15 lettere o più nel 35,7% del gruppo con
0,3 mg di farmaco e nel 40,3% del gruppo con dosaggio pari a 0,5 mg verso il 5,6% del gruppo trattato con verteporfina (p < 0,001 per entrambi i confronti). In media, l’acuità visiva è aumentata di 8,5
lettere nel gruppo con 0,3 mg di ranibizumab e di
11,3 lettere in quello con 0,5 mg verso una perdita
di 9,5 lettere per il gruppo trattato con verteporfina
(p < 0,001 per entrambi i confronti)12.
L’Agenzia Italiana del Farmaco (AIFA) ha approvato la commercializzazione di questo
farmaco in classe C/OSP1 a causa del rapporto sfavorevole costo/beneficio13.
• Inibitori della proteina VEGF
Il VEGF è un potente fattore mitogeno e di permeabilità vascolare, e gioca un ruolo importante
nella neovascolarizzazione. Per questo sono stati
studiati diversi farmaci con attività anti-VEGF al
fine di contrastare gli effetti negativi di neovascolarizzazione nelle membrane coroidali.
• Ranibizumab (Lucentis®)
In uno studio multicentrico denominato
MARINA10, della durata di 2 anni, 716 pazienti
con ARMD con neovascolarizzazione coroidale
classica o occulta sono stati assegnati a ricevere in
modo randomizzato 24 iniezioni intravitreali con
cadenza mensile di ranibizumab (a dosaggi di 0,3
mg oppure 0,5 mg ) verso placebo.
L’end point primario era rappresentato dalla
minore perdita di acuità visiva (meno di 15 lettere
di acuità visiva nel periodo compreso tra il basale
e 12 mesi).
Dopo 1 anno, il 94,5% dei pazienti ai quali
erano stati somministrati 0,3 mg di ranibizumab
e il 94,6% di quelli trattati con 0,5 mg avevano
perso meno di 15 lettere, rispetto al 62,2% dei pazienti che avevano ricevuto placebo (p < 0,001 per
entrambi i confronti).
L’acuità visiva risultava migliorata di 15 o più
lettere nel 24,8% del gruppo trattato con 0,3 mg
di ranibizumab, e nel 33,8% del gruppo in trattamento con 0,5 mg di farmaco, contro il 5% del
gruppo placebo (p < 0,001 per entrambi i dosaggi).
Gli aumenti medi nell’acuità visiva sono stati
di 6,5 lettere nel gruppo ranibizumab a 0,3 mg, di
7,2 lettere nel gruppo a 0,5 mg, contro una riduzione di 10,4 lettere nel gruppo placebo (p <
0,001 per entrambi i confronti). I benefici nell’acuità visiva sono stati mantenuti a 24 mesi.
Per quanto riguarda il profilo di sicurezza, nel
corso dello studio ci sono stati 5 casi (1%) di
presunta endoftalmite e 6 casi (1,3%) di uveite, tra
i pazienti trattati con ranibizumab.
I risultati dello studio hanno mostrato che la
somministrazione intravitreale di ranibizumab
per 2 anni previene la perdita della visione e migliora l’acuità visiva media nei pazienti con neovascolarizzazione coroidale classica o occulta, associata alla ARMD.
Nello studio ANCHOR11, 423 pazienti con
ARMD umida sono stati randomizzati al trattamento con ranibizumab nella dose di 0,3 mg o 0,5
mg verso placebo, più terapia fotodimanica con ver-
• Bevacizumab (Avastin®)
Nonostante non ci siano ancora studi clinici randomizzati sull’uso del bevacizumab in questa patologia, esiste una documentata esperienza clinica del
farmaco in regime off-label sotto forma di iniezioni
intravitreali14. Il bevacizumab, un anticorpo direttamente correlato al ranibizumab, è commercializzato anche in Italia ed è autorizzato per il trattamento del cancro colorettale e del carcinoma mammario metastatico. Il ranibizumab, più precisamente, è un frammento anticorpale del bevacizumab,
con alcune modifiche nella sequenza aminoacidica
che ne aumentano il legame al VEGF15. In uno studio prospettico condotto su 17 pazienti con ARMD
umida è stato utilizzato il trattamento con bevacizumab (2,5 mg in 0,1 ml di bevacizumab intravitreale ogni 4 settimane per un totale di 3 iniezioni)
ed è stato osservato un miglioramento dell’acuità
visiva nella maggior
parte dei pazienti16.
Il trattamento
La
con bevacizumab insupplementazione travitreale è decisadi antiossidanti
mente meno costoso
(20-25 euro a iniead alti dosaggi
in confronto
sembra associata zione)
al trattamento con
ad un
ranibizumab (2019
euro a iniezione) e in
significativo
confronto a pegaptaaumento
nib (550 euro a iniezione).
del profilo
La Commissione
di rischio
Tecnico-Scientifica
“
”
!
Agenzia Italiana del Farmaco
106
Bif XIV N. 3
AGGIORNAMENTI
2007
tecnica di fotocoagulazione. Essi hanno mostrato
un rallentamento della diminuzione dell’acuità
visiva e il mantenimento della sensibilità al contrasto in pazienti con membrane neovascolarizzate a livello coroidale iuxtafoveale.
Non mancano però gli effetti collaterali; tra i
più frequenti va ricordata la presenza di scotomi
nell’area d’intervento. Inoltre, in alcuni studi
sono stati registrati alcuni casi di anopsia acuta.
Oltre al discutibile profilo di tollerabilità, il limite
maggiore dell’utilizzo di tale intervento è rappresentato dalla sua applicabilità, limitata ai pazienti
con una ben definita neovascolarizzazione.
Questa condizione si osserva infatti in solo il 15%
dei pazienti affetti da ARMD umida19,20.
(CTS) dell’AIFA, con determinazione del 23 maggio 2007, su richiesta della Società Oftalmologica
Italiana, ha inserito il bevacizumab (Avastin®) nella legge 648/9617 per l’indicazione “Trattamento
delle maculopatie essudative e del glaucoma neovascolare”. In questo modo l’impiego del bevacizumab è a totale carico del Servizio Sanitario Nazionale per quest’indicazione, con monitoraggio
sia a livello clinico che di spesa.
• Pegaptanib (Macugen®)
Il pegaptanib è un aptamero, vale a dire una
piccola porzione di RNA sintetico, con affinità
specifica per alcune porzioni della proteina angiogenetica VEGF.
Il pegaptanib sembra rallentare la progressione
di ARMD. In un’analisi combinata di due studi
paralleli 18 , randomizzati, controllati, multicentrici, che hanno usato gli stessi criteri di inclusione (per un totale di 1186 pazienti,
realmente valutati), è stata osservata una risposta
clinica favorevole, ma non correlata alla dose. Lo
studio ha valutato l’efficacia del pegaptanib a
diversi dosaggi (0,3 mg, 1 mg e 3 mg) verso
iniezioni simulate. I risultati più significativi si
sono osservati con le dosi più basse di pegaptanib
intravitreale. Nel gruppo a cui è stato somministrato pegaptanib al dosaggio di 0,3 mg, il 70% dei
pazienti ha perso meno di 15 lettere di acuità
visiva, confrontato con il 55% dei controlli, (p <
0,001). Molti pazienti che hanno ricevuto la dose
più bassa di pegaptanib confrontanti con
iniezioni simulate hanno conservato o migliorato
l’acuità visiva (33% verso 23%; p = 0,003). Dopo
sei settimane di trattamento, la media di acuità
visiva nei pazienti trattati con 0,3 mg di pegaptanib era migliorata rispetto ai pazienti trattati
con le simulazioni (p < 0,002).
Durante lo studio si sono osservate reazioni
avverse quali: endoftalmiti (in 1,3 % dei pazienti),
danno traumatico della cornea (0,7 %), distacco
di retina (0,6 %). Queste reazioni hanno causato
perdita dell’acuità visiva.
Il pegaptanib sembra una terapia efficace nel
ridurre la progressione della ARMD, ma la sua sicurezza d’uso nel lungo periodo non è ancora definita. L’AIFA ha approvato la commercializzazione del pegaptanib in Italia in classe C/OSP1
per sfavorevole rapporto costo/beneficio.
• Terapia fotodinamica con verteporfina
(Visudyne®)
Un’altra tecnica usata è la terapia fotodinamica
che si associa alle iniezioni di verteporfina (un
sensibilizzatore alla luce laser).
In un’analisi ad interim di due trial clinici controllati e randomizzati con 609 pazienti21, l’uso di
questa tecnica ha comportato una riduzione significativa del valore di perdita della vista dopo un
anno di follow-up rispetto al placebo. L’analisi per
sottogruppi ha evidenziato che la significatività
dell’effetto era limitata ai pazienti con neovascolarizzazione ben definita; effetti non statisticamente
significativi sono, invece, stati osservati in pazienti
affetti da neovascolarizzazione occulta. La verteporfina in Italia è registrata in Italia in classe H.
• Terapia radiante
Una metanalisi 22 degli studi clinici randomizzati dell’efficacia di questo intervento ha
concluso che non ci sono benefici e che gli effetti
a lungo termine di questa terapia sono sconosciuti.
• Triamcinolone acetato e anecortave
Uno studio non controllato con iniezioni intravitreali di triamcinolone acetonide (25 mg) ha
evidenziato miglioramenti visivi a breve termine
in 2/3 degli occhi trattati 23 . Questi risultati
devono però essere confermati da studi clinici
randomizzati e controllati. Uno studio randomizzato e controllato di 530 pazienti con neovascolarizzazione subfoveale coroidale classica24 ha
valutato l’effetto di anecortave acetato, un cortisone angiogenetico, versus la terapia fotodinamica. Lo studio ha evidenziato percentuali
simili nel mantenimento dell’acuità visiva (45
versus 49%).
• Fotocoagulazione termica con laser
Numerosi ed ampi studi randomizzati e controllati19,20 sono stati condotti per studiare questa
!
Agenzia Italiana del Farmaco
bollettino d’informazione sui farmaci
Bif XIV N. 3
Nel marzo del 2006 la domanda di autorizzazione all’immissione in commercio in Europa,
della specialità contenente anecortave, è stata volontariamente ritirata dalla ditta. Il comitato
europeo per la valutazione dei medicinali per uso
umano (CHMP), al momento del ritiro, ha
espresso alcune perplessità sui benefici apportati
dal farmaco e sui rischi identificati25.
7.
8.
9.
Conclusioni
Considerando i diversi approcci terapeutici alla
ARMD, emerge che i trattamenti con gli inibitori
di VEGF hanno fornito dati di efficacia solo in
parte promettenti: sono necessari ulteriori studi
che ne confermino il reale valore e soprattutto, ad
oggi, è quasi sconosciuto il loro profilo di sicurezza nel lungo periodo. Un forte limite per
l’uso degli inibitori di VEGF è costituito dal loro
elevato costo. Relativamente a questo aspetto è
auspicabile pianificare studi clinici randomizzati
e controllati, ad oggi non disponibili, che confermino il profilo di efficacia del bevacizumab, il
cui costo è nettamente inferiore rispetto a pegaptanib e ranibizumab.
È importante sottolineare che i diversi approcci
terapeutici possono variabilmente essere considerati di prima scelta in funzione del tipo di
lesione e delle caratteristiche della ARMD.
La supplementazione di antiossidanti e zinco
a dosaggi piuttosto elevati ha evidenziato buoni
risultati nel prevenire la progressione della patologia, ma le alti dosi pongono alcuni limiti in
riferimento all’aumento del rischio di tumore al
polmone e di malattie cardiovascolari.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
Bibliografia
1. www.emea.europa.eu/humandocs/PDFs/EPAR/macugen/
H-620-en6.pdf (accesso verificato in data 11/07/07).
2. www.emea.europa.eu/humandocs/PDFs/EPAR/lucentis/
H-715-en6.pdf (accesso verificato in data 11/07/07).
3. Stone RM. Harrison - Principi di medicina interna. Milano:
McGraw-Hill, 2002 (1ª ed. Italiana della 15ª originale).
4. Age-Related Disease Study Group (AREDS). A
Randomised, placebo-controlled, clinical trial of high-dose
supplementation with vitamins C and E, beta carotene,
and zinc for age-related macular degeneration and vision
loss: AREDS report n.8. Arch Ophthamol 2001; 119: 6-60.
5. Ho AC, Maguire MG, Joken J, et al. Laser-induced drusen
reduction improves visual function at 1 year.
Ophthalmology 1999; 106: 1367-73.
6. Laser treatment in eyes with large drusen. Short-term
effects seen in a pilot randomised clinical trial. Choroidal
22.
23.
24.
25.
!
107
2007
Neovascolarization Prevention Trial Research Group.
Ophthalmology 1998; 105: 11-23.
Owens SL, Bunce C, Brannon AJ, et al. Prophylactic laser
treatment hastens choroidal neovascularization in unilateral age-related maculopaty: final results of the drusen
laser study. Am J Ophthalmol 2006; 141: 276-81.
Friberg TR, Musch DC, Lim JI, Morse L, Freeman W,
Sinclair S. Prophylactic treatment of age-related macular
degeneration report number 1: 810-nanometer laser to
eyes with drusen. Unilaterally eligible patients.
Ophthalmology 2006; 113: 622.e1.
Complications of age-related macular degeneration.
Prevention Trial Research Group. Laser treatment in
patients with bilateral large drusen: the complications of
age-related macular degeneration prevention trial.
Ophthalmology 2006; 113: 1974-86.
Rosenfeld PJ, Brown DM, Heier JS, et al. Ranibizumab for
neovascular age-related macular degeneration. N Engl J
Med 2006; 355: 1419-31.
Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N Engl J Med 2006; 355: 1432-44.
Anonimous. A view on new drugs for macular degeneration. Drug Ther Bull 2007; 45: 49-52.
G.U. n.130 del 7/6/2007.
Rosenfeld PJ. Intravitreal avastin: the low cost alternative
to lucentis? Am J Ophthalmol 2006; 142: 141-3.
Steinbrook R. The price of sight-ranibizumab, bevacizumab, and the treatment of macular degeneration. N Engl
J Med 2006; 355: 1409-12.
Bashshur ZF, Bazarbachi A, Schakal A, Haddad ZA, El
Haibi CP, Noureddin BN. Intravitreal bevacizumab for the
management of choroidal neovascularization in agerelated macular degeneration. Am J Ophthalmol 2006;
142: 1-9.
G.U. n. 122 del 28 maggio 2007 (serie generale),
Determinazione AIFA del 23 maggio 2007.
Gragoudas ES, Adamis AP, Cunningham ET Jr, et al.
Pegaptanib for neovascular age-related macular degeneration. N Engl J Med 2004; 351: 2805-16.
Macular Photocoagulation Study Group. Laser coagulation for juxtafoveal choroidal neovascolarization. Five-year
results from randomized clinical trials. Arch Ophthalmol
1994; 112: 500-9.
Macular Photocoagulation Study Group. Occult choroidal
neovascularization. Influence on visual outcome in
patients with age-related macular degeneration. Arch
Ophthalmol 1996; 114: 400-12.
Photodynamic therapy of subfoveal choroidal neovascularization in age-related macular degeneration with verteporfin: one-year results of 2 randomized clinical trials –
TAP report. Treatment of age-related macular degeneration with photodynamic therapy (TAP) Study Group. Arch
Ophthalmol 1999; 117: 1329-45.
Sivagnanavel V, Evans JR, Ockrim Z, Chong V.
Radiotherapy for neovascular age-related macular degeneration. Chocrane Database Syst Rev 2004; 4:
CD004004.
Jonas JB, Kreissig I, Hugger P, Sauder G, Panda-Jonas S,
Degenring R. Intravitreal triamcinolone acetonide for exudative age related macular degeneration. Br J Ophthalmol
2003; 87: 462-8.
Slakter JS, Bochow T, D’Amico DJ, et al. Anecortan acetate (15 milligrams) versus photodynamic therapy for treatment of subfoveal neovascularization in age-related
macular degeneration. Ophthalmology 2006; 113: 3-13.
www.emea.europa.eu/humandocs/PDFs/EPAR/retaane/
9871206en.pdf (accesso verificato in data 11/07/07).
Agenzia Italiana del Farmaco