Determinazione della carica microbica
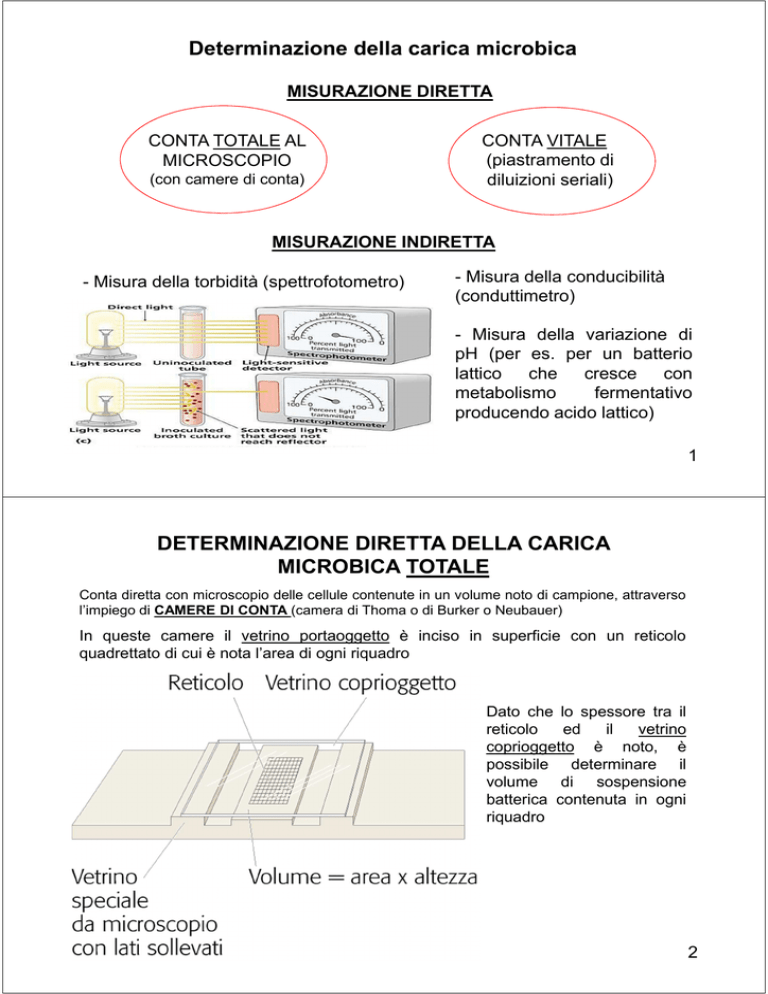
MISURAZIONE DIRETTA
CONTA TOTALE AL
MICROSCOPIO
(con camere di conta)
CONTA VITALE
(piastramento di
diluizioni seriali)
MISURAZIONE INDIRETTA
- Misura della torbidità (spettrofotometro)
- Misura della conducibilità
(conduttimetro)
- Misura della variazione di
pH (per es. per un batterio
lattico
che
cresce
con
metabolismo
fermentativo
producendo acido lattico)
1
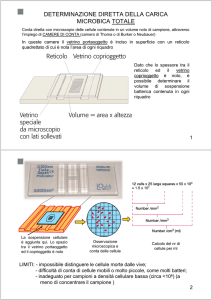
DETERMINAZIONE DIRETTA DELLA CARICA
MICROBICA TOTALE
Conta diretta con microscopio delle cellule contenute in un volume noto di campione, attraverso
l’impiego di CAMERE DI CONTA (camera di Thoma o di Burker o Neubauer)
In queste camere il vetrino portaoggetto è inciso in superficie con un reticolo
quadrettato di cui è nota l’area di ogni riquadro
Dato che lo spessore tra il
reticolo
ed
il
vetrino
coprioggetto è noto, è
possibile determinare il
volume di sospensione
batterica contenuta in ogni
riquadro
2
La sospensione cellulare
è aggiunta qui. Lo spazio
tra il vetrino portaoggetto
ed il coprioggetto è noto
Osservazione
microscopica e
conta delle cellule
Calcolo del nr di
cellule per ml
LIMITI: - impossibile distinguere le cellule morte dalle vive;
- difficoltà di conta di cellule mobili o molto piccole, come molti batteri;
- inadeguato per campioni a densità cellulare bassa (circa <106) (a
meno di concentrare il campione )
3
Determinazione della carica microbica VITALE
DILUIZIONI SERIALI DECIMALI
1 ml
1 ml
1 ml
1 ml
1 ml
1 ml
soluzione fisiologica
o una soluzione
tampone adatta a
preservare la
sopravvivenza dei
microrganismi
Campione
da
analizzare
9 ml
Diluizione
9 ml
9 ml
9 ml
1:10
1:100
1:1000
10-1
10-2
10-3
9 ml
9 ml
1:10000
1:100000
1:1000000
10-4
10-5
10-6
Semina per
spatolamento
(0,1
*
ml)
NON CONTABILI
159
o inclusione (1
ml)
159 x 103 = 1,6 x
Fattore di
diluizione
https://www.youtube.com/watch?v=teV7rlBkpQU
2
0
colonie
colonie
*, le colonie sono visibili
ESCLUSIVAMENTE
105 ufc / ml
DOPO INCUBAZIONE
Unità Formanti Colonia delle piastre all’adeguata
temperatura
4
colonie
Semina per inglobamento
17
colonie
Capsule Petri di terreno colturale agarizzato dopo semina
delle diluizioni seriali e incubazione
5
Determinazione della carica microbica VITALE
attraverso il piastramento di diluizioni seriali
Permette di ottenere i migliori risultati possibili circa il numero di cellule vitali in un campione
ed è perciò ampiamente utilizzata
Permette di contare solo le cellule vive, dove per viva si intende una cellula capace di
dividersi e di dare origine a una progenie
È adatta ad individuare anche un numero molto ridotto di cellule in un campione
Con l’uso di opportune condizioni o opportuni terreni selettivi è possibile ottenere la conta
vitale di specifici gruppi microbici
Talvolta non è facile trovare condizioni di crescita (terreno, temperatura, tempo di
incubazione) adatti a tutti i microrganismi di un campione microbiologicamente complesso.
Inoltre, certi microrganismi crescono più rapidamente di altri
Questa tecnica si basa sul PRESUPPOSTO che ogni colonia sia originata da una
singola cellula vitale. Sorgono pertanto problemi per cellule legate fra loro, ad
esempio in catenelle come gli streptococchi. Per questo, il risultato di questo
analisi di conta microbica non è indicato come numero di cellule, ma come UNITÀ
FORMANTI COLONIA (UFC) per unità di peso o di volume
6
7
8
N.B.: al fine di stabilire nel modo più corretto possibile la carica microbica vitale di
un campione, non si considerano solo le colonie di una singola piastra ad una
singola diluizione, ma si considerano congiuntamente tutte le piastre aventi un
numero di colonie accettabile (cioè compreso tra circa 10/20 a circa 200/300). Ciò
deve essere ad esempio fatto nelle analisi di conta microbica vitale per i controlli
sanitari (o per una qualsiasi analisi che abbia valore legale). Vediamo, ad esempio,
cosa vi è scritto nel documento ISTISAN 08/36 dell’Istituto Superiore di Sanità
(«Metodi microbiologici tradizionali e metodi molecolari per l’analisi degli integratori
alimentari a base di o con probiotici per uso umano»).
:
9
Esempio: Diluizione
-6
197 colonie
,
,
-7
108
,
-6
106
/
19 colonie
10
Conta vitale per diluzioni seriali e semina in pastra
RICAPITOLANDO:
- permette di contare solo le cellule vive, dove per viva si intende una cellula capace
di dividersi e di dare origine a progenie.
Il PRESUPPOSTO è che OGNI colonia sia originata da una singola cellula vitale.
Problema per cellule legate fra loro in catenelle (vedi streptococchi). Per questo non
si parla di cellule per unità di peso o di volume, ma di UNITA’ FORMANTI
COLONIA!!!
Non è talvolta facile trovare condizioni di crescita (terreno, temperatura, tempo di
incubazione) adatti a tutti i microrganismi di un campione microbiologicamente
complesso. Inoltre certi microrganismi crescono più rapidamente di altri.
Per ovviare a questi problemi e anche ad altri, è importante preparare diverse
repliche!
Questa metodica permette di ottenere i migliori risultati possibili circa il numero di
cellule vitali in un campione ed è perciò ampiamente utilizzata!!!
È adatta a trovare anche un numero molto piccolo di cellule!!!
Con l’uso di opportune condizioni o terreni selettivi è possibile ottenere la conta
11
vitale di specifici gruppi microbici.
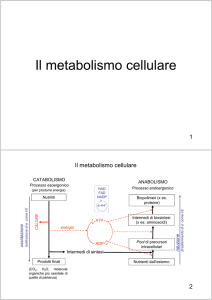
Il metabolismo cellulare
12
Il metabolismo cellulare
CATABOLISMO
ANABOLISMO
NAD
FAD
NADP
(per produrre energia)
Nutriliti
Biopolimeri (x es.
proteine)
ATP
Intermedi di biosintesi
(x es. aminoacidi)
ADP
Pool di precursori
intracellulari
energia
Intermedi di sintesi
Prodotti finali
riduzione
CALORE
(sottrazione di e- come H)
ossidazione
e-+H+
Processo endoergonico
(trasferimento di e- come H)
Processo esoergonico
Nutrienti dall’esterno
(CO2, H2O, molecole
organiche più ossidate di
quelle di partenza)
13
RUOLO DELL’ ATP NEL METABOLISMO
È un derivato dell’AMP (adenosin monofosfato) al quale sono
legati altri 2 gruppi fosforici per mezzo di legami anidride
( ADP + Pi + energia = ATP )
fosfato inorganico
I legami anidride sono legami ricchi di
energia e quindi sono particolarmente reattivi
- L’ATP è in grado di cedere gruppi fosforici a numerosi intermedi
metabolici, convertendoli nella forma attivata con livelli di energia libera tali
da consentire a questi intermedi fosforilati di partecipare alle reazioni
biosintetiche, che sono termodinamicamente favorevoli (∆G°<0)
- Una analoga reazione con un reagente in forma non fosforilata sarebbe
termodinamicamente sfavorevole (∆G°>0)
La generazione di ATP è quindi necessaria per il
funzionamento dei processi biosintetici
14
Come ottengono ATP i microrganismi?
Lettera O, non
numero “zero”!
RESPIRAZIONE: sintesi di ATP attraverso il
sistema enzimatico della Fo-F1 ATP sintasi (o
Fo-F1 ATPasi), al termine della catena di
trasporto degli elettroni
FOTOFOSFORILAZIONE: sintesi di ATP attraverso l’impiego
di energia luminosa per creare una separazione di cariche
FOSFORILAZIONE A LIVELLO DI SUBSTRATO: consiste nel
diretto trasferimento di un fosfato ad alto contenuto energetico
da un composto fosforilato ad ADP per formare ATP
15
REAZIONI di OSSIDO-RIDUZIONE
donatore di e- (agente riducente… che si ossida!)
- accettore di e (agente ossidante… che si riduce!)
-
il valore del potenziale di RIDUZIONE è un indice di quanto la molecola in
oggetto sia un buon donatore o un buon accettore di e2H+/H2
O2/H2O
- 0.42 V (infatti H2 è un ottimo donatore di elettroni)
+ 0.82 V (infatti O2 è un ottimo accettore di elettroni)
per OGNI composto che si OSSIDA in una semireazione DEVE esserci un
composto che si RIDUCE in un’altra semireazione ad essa accoppiata
H2
½ O2 + 2H+ + 2 e-
2H+ + 2 e- (semireazione 1)
H2O (semireazione 1)
REAZIONE NETTA
H2 + ½ O2
H2O
16
REAZIONI di OSSIDO-RIDUZIONE
-
donatore di e- (agente riducente… che si ossida!)
-
accettore di e- (agente ossidante… che si riduce!)
il valore del potenziale di RIDUZIONE è un indice di quanto la molecola in
oggetto sia un buon donatore o un buon accettore di e2H+/H2
O2/H2O
- 0.42 V (infatti H2 è un ottimo donatore di elettroni)
+ 0.82 V (infatti O2 è un ottimo accettore di elettroni)
per OGNI composto che si OSSIDA in una semireazione DEVE esserci un
composto che si RIDUCE in un’altra semireazione ad essa accoppiata
H2
½ O2 + 2H+ + 2 e-
2H+ + 2 e- (semireazione 1)
H2O (semireazione 1)
REAZIONE NETTA
H2 + ½ O2
H2O
17
Nei sistemi biologici le reazioni di ossido-riduzione UTILI ai fini energetici avvengono quando
l’ e- e il protone (H+) che lo segue sono rimossi da un substrato (per azione di un enzima) per
essere trasferiti ad un TRASPORTATORE che agirà come intermedio di trasporto tra un
donatore e un accettore
associati ai protoni!!!
Gli e- non esistono allo stato libero nei sistemi biologici MA SI SPOSTANO DA
DONATORI AD ACCETTORI ATTRAVERSO LA MEDIAZIONE DI TRASPORTATORI
FISSI
LIBERI
Associati alla
membrana
NAD+
reazioni CATABOLICHE
NADP+
reazioni ANABOLICHE
cofattori di enzimi responsabili
delle deidrogenazioni
per esempio
lattato deidrogenasi
riduzione
del NAD
+
NAD+
NADH + H+
+
ossidazione
del NAD
Lattato
Piruvato
18
NICOTINAMIDE ADENIN DINUCLEOTIDE
FORMA OSSIDATA (NAD+)
NICOTINAMIDE ADENIN DINUCLEOTIDE
FORMA RIDOTTA (NADH + H+)
NICOTINAMIDE
NICOTINAMIDE
ADENINA
RIBOSIO
2 FOSFATI
RIBOSIO
ADENINA
RIBOSIO
2 FOSFATI
RIBOSIO
Quando il NAD in forma ossidata (NAD+) acquista 2 elettroni, cioè si
riduce, acquista anche un H+ e un H+ viene rilasciato nel citoplasma… per
questo il NAD in forma ridotta deve essere indicato come NADH + H+
19
Che bisogno c’è, da un punto di vista metabolico, di due
piridinnucleotidi (NAD e NADP) così simili a livello funzionale?
RISPOSTA: i piridinnucleotidi ossidati entrano come reagenti nei processi
catabolici, mentre quelli in forma ridotta partecipano ai processi biosintetici
Ciò significa che:
- i piridinnucleotidi si devono trovare per lo più in forma ossidata perché i processi
catabolici possano funzionare
- per le reazioni biosintetiche si devono trovare in gran parte in forma ridotta
SONO QUINDI NECESSARI DUE TIPI DI piridin-nucleotidi
Il NAD è mantenuto largamente nello stato ossidato → interviene quindi
nelle reazioni cataboliche (è importante ricordarlo per quando parleremo
della fermentazione)
Il NADP è mantenuto largamente nello stato ridotto → interviene quindi nelle
reazioni anaboliche
20