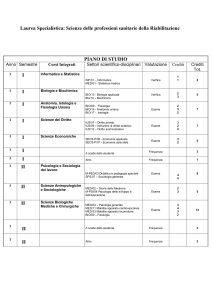
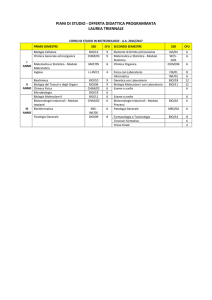
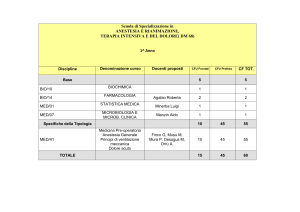
Hyalistil BIO
Soluzione oftalmica umettante
e lubrificante a base di
SODIO IALURONATO 0,2%
HYALISTIL BIO per le sue proprietà umettanti e visco-elastiche va utilizzato per la lubrificazione e
l’idratazione della superficie oculare, in tutti i casi di irritazione e/o secchezza dovuti ad alterazioni
del film lacrimale.
HYALISTIL BIO procura un sollievo istantaneo ed una sensazione di benessere duratura.
Composizione:
1 ml di soluzione contiene sodio ialuronato 0,2%, benzalconio cloruro, sodio cloruro, sodio fosfato
monobasico monoidrato, sodio fosfato bibasico dodecaidrato, acqua purificata.
Presentazioni:
Flacone da 5 ml.
Flacone da 10 ml.
Indicazioni:
HYALISTIL BIO è indicato in tutti i casi di discomfort oculare; in particolare, allevia irritazione e secchezza dovuta ad alterazioni quali-quantitative del film lacrimale o a fattori ambientali come polline,
polvere, abbagliamento, inquinamento e uso di videoterminali. Assicura la protezione della superficie oculare durante i processi di riparazione delle abrasioni.
Caratteristiche e meccanismo d’azione:
HYALISTIL BIO contiene sodio ialuronato, un polimero naturale presente in diversi distretti del
corpo umano. Le particolari caratteristiche fisiche del sodio ialuronato conferiscono alla soluzione
importanti proprietà viscoelastiche.
HYALISTIL BIO riveste la superficie dell’occhio e, per le sue caratteristiche lubrificanti e idratanti, riduce la frizione causata da movimenti quali l’ammiccamento e assicura protezione durante i processi di riparazione dell’epitelio corneale. Pertanto, HYALISTIL BIO, garantisce contemporaneamente
una sensazione di benessere duraturo e di massimo comfort.
Dosaggio e somministrazione:
Instillare 1-2 gocce di HYALISTIL BIO, quattro volte al dì nel fornice congiuntivale, secondo necessità.
Istruzioni per l’uso:
Avvitare il tappo fino in
fondo per perforare il
flacone.
Svitare il tappo.
Capovolgere il flacone
ed instillare la soluzione
oftalmica esercitando
una lieve pressione sul
flacone stesso.
Richiudere il flacone
avvitando il tappo fino
in fondo.
1G104520G2
Controindicazioni:
Ipersensibilità verso uno dei componenti.
Precauzioni e avvertenze:
Evitare il contatto con lenti a contatto morbide.
Rimuovere le lenti a contatto prima della somministrazione di HYALISTIL BIO
ARTWORK
THIS ARTWORK IS PROPERTY OF:
SIFI SpA
PRODUCT NAME:
INS-Hyalistil Bio Multidose
PRODUCT CODE:
1G104520G2
COUNTRY: Italia
ELABORATO: Leaflet
FORMULAZIONE: Eye drops
SEPARATIONS: ( BLACK )
BARCODE TYPE: Laetus (IXXIIIIXX) 706
CUTTING PROFILE: T13
MEASURES (mm): 122 x 220
FOLDED (mm): L 122 x H 25
MATERIAL: Carta
g/sq.mt: 50
PDF 1.5
Realized by:
QUALITY SYSTEM - ISO 9001:2008
ISSUE DATE
OPERATOR
05-08-13
RE004
DRAFT
03
EURPACK Grafiarma Grafiflex - Aprilia (LT) tel. +39 06 92732420 [email protected] - Robecco s/N (MI) tel. +39 02 94974002 [email protected]
mm 10
20
30
40
50
60
70
80
90
Ricordiamo che il risultato cromatico delle stampe potrà essere diverso in funzione del supporto e della tecnica utilizzata. We remind you that
prints chromatic results could be different depending on support and used technique. - La responsabilità della EURPACK GRAFIFARMA GRAFIFLEX
Srl, termina con l’approvazione del seguente documento. EURPACK GRAFIFARMA GRAFIFLEX’s responsability ends with the approval of the present
document. - Vietato l’utilizzo del presente tassello di informazioni se non espressamente autorizzato dalla EURPACK GRAFIFARMA GRAFIFLEX Srl.
It is forbidden the use of the present information if not officially allowed from EURPACK GRAFIFARMA GRAFIFLEX Srl.
V.01-2013
CLIENT APPROVAL
DATE
SIGNATURE
FRONT
ed attendere almeno 15 minuti prima di indossare nuovamente le lenti.
Non toccare l’estremità del flacone aperto e non metterla a diretto contatto con l’occhio. Non utilizzare HYALISTIL BIO se il contenitore è danneggiato.
Conservare a temperatura inferiore a 25° C. Non utilizzare HYALISTIL BIO dopo la data di scadenza.
Il prodotto deve essere usato entro 28 giorni dalla prima apertura.
La somministrazione di HYALISTIL BIO a bambini o persone con abilità limitata deve essere effettuata da parte di un adulto responsabile.
Interazioni con farmaci o altri dispositivi medici per uso
oftalmico:
Non sono note interazioni del prodotto con la somministrazione
di farmaci per uso oftalmico.
Tuttavia, si consiglia di non somministrare HYALISTIL BIO contemporaneamente o comunque entro 10 minuti dalla somministrazione di farmaci o altri dispositivi medici per uso oftalmico.
Effetti indesiderati:
L’uso del prodotto può causare occasionalmente intolleranza (lieve bruciore o irritazione).
PER ESCLUSIVO USO TOPICO OCULARE
TENERE FUORI DALLA PORTATA DEI BAMBINI
Fabbricante:
S.I.F.I. S.p.A. – Via Ercole Patti, 36 – 95025
Aci S. Antonio (CT) – ITALIA
Ultima revisione del testo: Agosto 2013
1G104520G2
0546
ARTWORK
THIS ARTWORK IS PROPERTY OF:
SIFI SpA
PRODUCT NAME:
INS-Hyalistil Bio Multidose
PRODUCT CODE:
1G104520G2
COUNTRY: Italia
ELABORATO: Leaflet
FORMULAZIONE: Eye drops
SEPARATIONS: ( BLACK )
BARCODE TYPE: Laetus (IXXIIIIXX) 706
CUTTING PROFILE: T13
MEASURES (mm): 122 x 220
FOLDED (mm): L 122 x H 25
MATERIAL: Carta
g/sq.mt: 50
PDF 1.5
Realized by:
QUALITY SYSTEM - ISO 9001:2008
ISSUE DATE
OPERATOR
05-08-13
RE004
DRAFT
03
EURPACK Grafiarma Grafiflex - Aprilia (LT) tel. +39 06 92732420 [email protected] - Robecco s/N (MI) tel. +39 02 94974002 [email protected]
mm 10
20
30
40
50
60
70
80
90
Ricordiamo che il risultato cromatico delle stampe potrà essere diverso in funzione del supporto e della tecnica utilizzata. We remind you that
prints chromatic results could be different depending on support and used technique. - La responsabilità della EURPACK GRAFIFARMA GRAFIFLEX
Srl, termina con l’approvazione del seguente documento. EURPACK GRAFIFARMA GRAFIFLEX’s responsability ends with the approval of the present
document. - Vietato l’utilizzo del presente tassello di informazioni se non espressamente autorizzato dalla EURPACK GRAFIFARMA GRAFIFLEX Srl.
It is forbidden the use of the present information if not officially allowed from EURPACK GRAFIFARMA GRAFIFLEX Srl.
V.01-2013
CLIENT APPROVAL
DATE
SIGNATURE
BACK