PR.FO.01
Gestione dei farmaci in ospedale
Azienda USL 3
Rev. 1: 20/05/2013
Pag.: 1/4
Documenti di
Registrazione
Responsabili
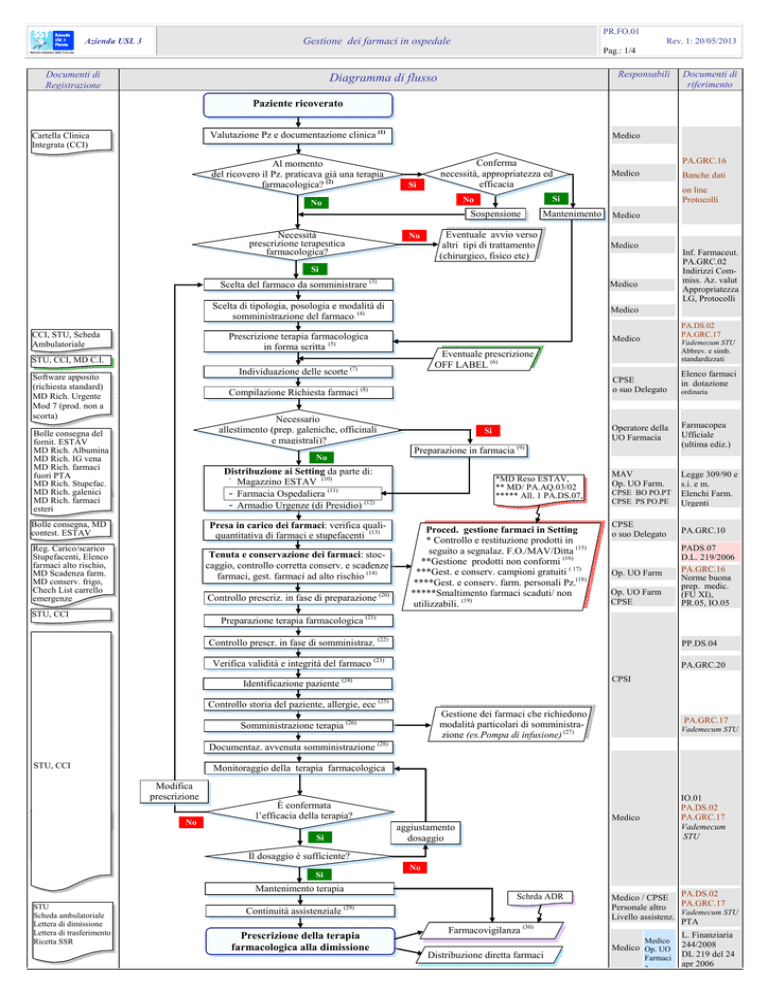
Diagramma di flusso
Documenti di
riferimento
Paziente ricoverato
Valutazione Pz e documentazione clinica (1)
Cartella Clinica
Integrata (CCI)
Al momento
del ricovero il Pz. praticava già una terapia
farmacologica? (2)
Medico
Si
Conferma
necessità, appropriatezza ed
efficacia
Sospensione
Necessità
prescrizione terapeutica
farmacologica?
No
Medico
Mantenimento
Eventuale avvio verso
altri tipi di trattamento
(chirurgico, fisico etc)
Medico
Medico
Si
CCI, STU, Scheda
Ambulatoriale
Scelta del farmaco da somministrare (3)
Medico
Scelta di tipologia, posologia e modalità di
somministrazione del farmaco (4)
Medico
Prescrizione terapia farmacologica
in forma scritta (5)
Medico
Eventuale prescrizione
OFF LABEL (6)
STU, CCI, MD C.I.
Individuazione delle scorte (7)
Software apposito
(richiesta standard)
MD Rich. Urgente
Mod 7 (prod. non a
scorta)
CPSE
o suo Delegato
Compilazione Richiesta farmaci (8)
Necessario
allestimento (prep. galeniche, officinali
e magistrali)?
Bolle consegna del
fornit. ESTAV
MD Rich. Albumina
MD Rich. IG vena
MD Rich. farmaci
fuori PTA
MD Rich. Stupefac.
MD Rich. galenici
MD Rich. farmaci
esteri
Si
Distribuzione ai Setting da parte di:
Magazzino ESTAV (10)
- Farmacia Ospedaliera (11)
- Armadio Urgenze (di Presidio) (12)
Bolle consegna, MD
contest. ESTAV
Presa in carico dei farmaci: verifica qualiquantitativa di farmaci e stupefacenti (13)
Reg. Carico/scarico
Stupefacenti, Elenco
farmaci alto rischio,
MD Scadenza farm.
MD conserv. frigo,
Chech List carrello
emergenze
Tenuta e conservazione dei farmaci: stoccaggio, controllo corretta conserv. e scadenze
farmaci, gest. farmaci ad alto rischio (14)
Controllo prescriz. in fase di preparazione (20)
STU, CCI
*MD Reso ESTAV,
** MD/ PA.AQ.03/02
***** All. 1 PA.DS.07,
Proced. gestione farmaci in Setting
* Controllo e restituzione prodotti in
seguito a segnalaz. F.O./MAV/Ditta (15)
**Gestione prodotti non conformi (16)
***Gest. e conserv. campioni gratuiti ( 17)
****Gest. e conserv. farm. personali Pz.(18)
*****Smaltimento farmaci scaduti/ non
utilizzabili. (19)
Inf. Farmaceut.
PA.GRC.02
Indirizzi Commiss. Az. valut
Appropriatezza
LG, Protocolli
PA.DS.02
PA.GRC.17
Vademecum STU
Abbrev. e simb.
standardizzati
Elenco farmaci
in dotazione
ordinaria
Operatore della
UO Farmacia
Farmacopea
Ufficiale
(ultima ediz.)
MAV
Op. UO Farm.
CPSE BO PO.PT
CPSE PS PO.PE
Legge 309/90 e
s.i. e m.
Elenchi Farm.
Urgenti
CPSE
o suo Delegato
PA.GRC.10
Op. UO Farm
PADS.07
D.L. 219/2006
PA.GRC.16
Norme buona
prep. medic.
(FU XI),
PR.05, IO.05
Preparazione in farmacia (9)
No
Banche dati
on line
Protocolli
Si
No
No
PA.GRC.16
Op. UO Farm
CPSE
Preparazione terapia farmacologica (21)
Controllo prescr. in fase di somministraz. (22)
PP.DS.04
Verifica validità e integrità del farmaco (23)
PA.GRC.20
CPSI
Identificazione paziente (24)
Controllo storia del paziente, allergie, ecc (25)
Somministrazione terapia
Gestione dei farmaci che richiedono
modalità particolari di somministrazione (es.Pompa di infusione) (27)
(26)
PA.GRC.17
Vademecum STU
Documentaz. avvenuta somministrazione (28)
STU, CCI
Monitoraggio della terapia farmacologica
Modifica
prescrizione
No
È confermata
l’efficacia della terapia?
Si
Medico
aggiustamento
dosaggio
IO.01
PA.DS.02
PA.GRC.17
Vademecum
STU
Il dosaggio è sufficiente?
Si
No
Mantenimento terapia
Schrda ADR
STU
Scheda ambulatoriale
Lettera di dimissione
Lettera di trasferimento
Ricetta SSR
Continuità assistenziale (29)
Prescrizione della terapia
farmacologica alla dimissione
Farmacovigilanza (30)
Distribuzione diretta farmaci
Medico / CPSE PA.DS.02
PA.GRC.17
Personale altro
Vademecum STU
Livello assistenz.
PTA
Medico
Medico Op. UO
Farmaci
a
L. Finanziaria
244/2008
DL 219 del 24
apr 2006
Note
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10)
(11)
(12)
(13)
I medici valutano, al momento della prescrizione, tutte le informazioni cliniche disponibili sul paziente. La documentazione clinica deve essere accurata e
completa contenere un’attenta anamnesi farmacologica nell’ottica di rilevare allergie, intolleranze, interazioni con altri farmaci o con erbe medicinali,
consumo di prodotti da banco, di alcool ed abitudini alimentari del paziente, condizioni cliniche che sconsigliano l’uso di determinati farmaci o
impongono modificazioni di dosaggio.
In caso di pazienti che praticano già una terapia farmacologica al momento del ricovero sarà necessario valutarne l’importanza, l’appropriatezza e
l’efficacia sulla base delle condizioni cliniche del Pz. e della documentazione disponibile, di eventuali consulenze specialistiche e decidere se continuare
il trattamento, sospenderlo o sostituirlo.
Il medico decide il farmaco da somministrare in base alla diagnosi, efficacia terapeutica, interazioni farmacologiche, controindicazioni, allergie, ecc. E’
reso disponibile l’accesso alle informazioni (accesso on line a linee guida, PTA, procedure, protocolli, informatore farmaceutico, banche dati ed altri
strumenti informativi); É obiettivo della Sez. Farmaceutica Ospedaliera rendere disponibili in tutti i reparti, possibilmente elettronicamente, tutte le
informazioni sui farmaci relativamente a: indicazioni terapeutiche, effetti collaterali, reazioni avverse, controindicazioni, precauzioni di impiego,
interazioni con altri medicinali e/o con cibo, azioni da adottare in caso di reazioni avverse o interazioni, requisiti per la conservazione.
Nome commerciale e/o principio attivo, dose, forma farmaceutica, posologia, via e modalità di somministrazione con indicazione temporale. Riportare
l’esatta concentrazione, il dosaggio, la posologia e in alcuni casi l’età e il peso del paziente. La prescrizione deve essere effettuata te-nendo conto dei
prodotti inseriti nel PTA. Le eccezioni vanno notificate alla Direzione Sanitaria accompagnate da re-lazione dettagliata sul singolo caso vista-ta dal Resp.
di Struttura.
Il medico prescrive la terapia sulla STU. Le prescrizioni devono essere chiaramente leggibili (SCRIVERE IN STAMPATELLO) e non devono dare adito
a confusione: chiarezza grafica, chiarezza di contenuto, completezza, tracciabilità. Deve essere evitato al massimo l’uso di numeri decimali (per esempio,
scrivere 500 mg invece di 0,5 g); in caso di utilizzo di numeri decimali, usare sempre uno “zero” iniziale prima di un numero decimale in-feriore ad uno
(per esempio 0,5 ml); per contro, evitare l’uso di uno “zero” terminale dopo un numero uni-tario (per esempio 5,0 ml) poiché tale scritta potrebbe
prestarsi ad erronea lettura con somministrazione di dosaggio 10 volte più elevato. Evitare le abbreviazioni dei nomi dei farmaci o la terminologia latina
per l’uso. Per le terapie che necessitano di unità standard le unità devono essere espresse per esteso piuttosto che con abbreviazione. Evitare nelle
prescrizioni la frase “al bisogno”, ma, qualora riportata, deve essere specificata la posologia, la dose massima giornaliera e l’eventuale intervallo di tempo
fra le somministrazioni.
N.B.: la prescrizione della terapia farmacologica in forma verbale di regola NON E’ AMMESSA, tuttavia in situazioni di emergenza/urgenza si
può procedere al trattamento anche in assenza di prescrizione scritta. Tale prescrizione, comunque, appena possibile, deve essere convalidata in
forma scritta dal prescrittore, con annotazione – nella documentazione di competenza – della pregressa prescrizione verbale, affinché sia rintracciabile
la reale sequenza degli atti.
Prescrizione “OFF-LABEL” Il medico prescrive farmaci già registrati, ma usati in modalità diversa da quanto indicato nella scheda tecnica di
autorizzazione all'immissione in commercio. Tale uso si configura come SPERIMENTALE. La responsabilità per even-tuali conseguenze negative
derivanti dall’utilizzo dei farmaci off-label ricade in capo al Medico e non all’Azienda Sanitaria. La normativa impone al medico di valu-tare l’assenza di
valida alternativa tera-peutica e un utilizzo ponderato sulla base della documentazione scientifica che ne attesti l’efficacia e la sicurezza e impone
l’acquisizione del consenso informato scritto. Il medico prescrittore ha l’obbli-go di stilare una relazione che giustifichi l’utilizzo del farmaco “off label”
con riferimenti alla letteratura internazionale. La relazione deve essere inviata alla Direzione Sanitaria Aziendale e in copia alla farmacia ospedaliera.
Il responsabile di ogni Struttura Organizzativa definisce un elenco quali-quantitativo dei medicinali che devono costituire la dotazione ordinaria. Tale
elenco deve essere redatto sulla base dei consumi storici annuali dei Setting prodotti dal Responsabile della Farmacia ospedaliera.L’elenco deve essere
disponibile per la consultazione presso la stessa Articola-zione Organizzativa. L’entità delle scorte presenti deve essere correlata alle esi-genze e agli
effettivi consumi della strut-tura per far fronte al fabbisogno di una settimana e comprendere farmaci inseriti nel PTA. Eventuali prodotti gestiti “a scorta”
non utilizzati, ma ancora in confezione integra e non scaduti, devono essere restituiti al magazzino ESTAV entro cinque mesi dal giorno della scadenza
L’Inf. Coordinatore (o suo delegato) controlla le scorte ipotizzando il fabbisogno dei farmaci di largo consumo ed inserisce l’ordine nel programma
informatico utilizzando la richiesta standard. Per richiedere un farmaco in urgenza deve essere compilato un apposito modulo cartaceo ESTAV. Il modulo
deve essere inviato alla Farmacia per la convalida. La Farmacia invierà il modulo al magazzino ESTAV via fax. Durante le ore di chiusura della Farmacia
detto modulo deve essere inviato direttamente al magazzino ESTAV dal Setting. La richiesta dei prodotti non a scorta ed in economia deve essere
compilata sul registro cartaceo (modello 7) ed inviata in farmacia. Gli ordini di prodotti farmaceutici per il reintegro delle scorte dei setting sono eseguite
- di norma - dal personale infermieristico. Il prodotto ordinato in urgenza viene inviato dal magazzino ESTAV entro due ore, con un costo aggiuntivo di
52 € per urgenza. Scopo della richiesta standard è quello di selezionare i reparti a seconda dei prodotti che questi stessi possono liberamente ordinare.
Le preparazioni galeniche sono allestite dai farmacisti in farmacia, su prescrizione medica personalizzata, per preparazioni non codificate in nessuna
farmacopea (es: dosaggi orfani) e dietro ri-hiesta informatizzata del reparto per preparati officinale la cui formulazione è prevista dalle farmacopee. Per
preparazioni non allestite in farmacia (es: chemioterapici) è in fase di completamento ed attivazione una procedura condivisa tra le farmacie ospedaliere di
PT e PE e i DH dei due ospedali. In ogni tappa del processo di allestimento deve essere rintracciabile l’operatore, il materiale usato ed i controlli di qualità
effettuati.
Distribuzione ai reparti da Estav: I FARMACI A SCORTA vengono distribuiti dal MAV (MAGAZZINO AREA VASTA) a setting e servizi.Oltre al
controllo della precisa corrispondenza tra la prescrizione medica e il medicinale prelevato per l’impiego, il personale addetto deve comunque sempre
verificare la scadenza ed integrità dei farmaci e di tutti gli altri prodotti farmaceutici interessati alla terapia.
Distribuzione ai setting da Farmacia interna: la Farmacia gestisce alcuni prodotti come da accordo Azienda USL3 con ESTAV ed alcune urgenze
(farmaci esteri, stupefacenti, emoderi-vati CRS, farmaci extra PTA). I farmaci non in commercio in Italia devono essere richiesti su opportuna modulistica
diret-tamente alla Farmacia ospedaliera (F.O.). I farmaci devono essere richiesti direttamente alla F.O. secondo le modalità di legge vigenti. Le
preparazioni galeniche officinali e magistrali devono essere richieste alla F.O. con procedura informatizzata. I farmaci fuori prontuario necessario alla
conti-nuità assistenziale del Pz. devono essere richiesti alla Farmacia con opportuna modulistica entro le ore 11 della mattina dal lunedì al venerdì Per le
soluzioni concentrate di K sono indivi-duati determinati Setting autorizzati all’utilizzo per i quali il prodotto è inserito nelle richieste standard. In caso di
urgenza o casi particolari (integrazione per NPT) le soluzioni conc. di K sono custodite in farmacia o nell’armadio delle urgenze per i Setting.
Distribuzione ai Setting da armadio urgenze. Presso la Sala Operativa 118 di PT ed il P.S. di Pescia sono allestiti due armadi per farmaci urgenti
stabiliti da un elenco di prodotti ritenuti importanti dal punto di vista clinico
Verifica qualitativa e quantitativa dei farmaci: i giorni in cui vengono consegnati i farmaci da parte del personale addetto, il delegato verifica e
controlla:
- la congruità quali-quantitativa tra quanto consegnato e quanto scritto sia sul modulo di richiesta che sulla bolla di consegna;
- il ricevimento dei prodotti nei tempi previsti;
- le modalità di conservazione e stato del materiale inviato (es. mantenimento della catena del freddo, integrità delle confezio-ni, corretta etichettatura,
consegna dei prodotti nelle confezioni originali, .ecc.);
- predisposizione del reso o di eventuale contestazione qualora vengano riscontrate difformità tra richiesta e consegna;
- i farmaci in consegna dai magazzini ai Setting relativamente alla loro scadenza devono avere almeno i 2/3 della validità..
Per le soluzioni conc. di K ed altri farma-ci ad alto rischio attenersi alle disposiziozioni e raccomandazioni Ministeriali specifiche
Il RA sistema i farmaci nell’armadio anteponendo le confezioni che riportano la data di scadenza più prossima, controfirma la ricevuta e ne invia copia al
GREF. In caso di consegna di farmaco difforme in qualità e/o in quantità rispetto alla richiesta, l’infermiere attiva la procedura del reso. In ogni in caso chi
ha effettuato il controllo appone timbro, firma, nome e cognome.
(14) Tenuta e conservazione dei farmaci:
a. Stoccaggio dei farmaci: il CPSE è responsabile in reparto della gestione dell’armadio farmaceutico, tale funzione può essere formalmente delegata. E’
comunque fondamentale che tutto il personale di assistenza venga portato a conoscenza delle regole generali per un corretto stoccaggio ed una buona
conservazione. Per i prodotti per i quali deve essere prevista la conservazione in armadi chiusi a chiave (es. stupefacenti, veleni) o in contenitori/ armadi
con opportune caratteristiche (infiammabili) attenersi alla normativa vigente. Se si ritiene che, per alcuni farmaci, non siano state rispettate le condizioni
di conservazione, deve essere interpellato, prima dell’utilizzo, il Servizio di Farmacia. Nota Bene: Lo stoccaggio deve avvenire in locali opportunamente
custoditi. In particolare devono essere regolate e diffuse a tutti gli operatori coinvolti le corrette modalità per quanto riguarda: temperatura e condizioni di
conservazione, così come precisate dalla F.O., in conformità a quanto indicato su confezioni e foglietto illustrativo. Devono essere definite modalità di
conservazione che facilitino la corretta identificazione delle confezioni e riducano la possibilità di scambio di farmaco. Le confezioni possono essere
riposte in ordine alfabetico (per nome commerciale o per principio attivo) e/o suddivisi per categoria terapeutica e/o per via di somministrazione.
Garantire la rotazione delle scorte (regola “FIRST IN FIRST OUT”), in modo da rendere più accessibile, e quindi utilizzare per primo il prodotto con scadenza
più ravvicinata.
b. Controllo della corretta conservazione dei farmaci: controllare temperatura, caratteristiche strutturali degli spazi, armadi, carrelli e contenitori.
Contrassegnare la data di apertura sulle confezioni multìdose di farmaci (gocce, sol os/nas, colliri, dermatologici locali specialmente se applicati su cute
lesa). Per farmaci da conservare a temperature controllate attenersi alle disposizioni indicate sui farmaci stessi. Nota Bene: porre attenzione riguardo ai
locali dedicati allo stoccaggio dei farmaci, in particolare controllare che le temperatura non sia superiore ai 25°, per i farmaci a conservazione ambiente. I
frigoriferi devono essere dotati di display per la temperatura e rilevamento grafico della stessa. Ogni armadio, contenitore, carrello e tutto ciò che è
predisposto alla conservazione farmaci deve essere tenuto lontano da fonti di calore.
c. Gestione farmaci ad alto rischio: per farmaci a particolare rischio terapeutico (es: soluzioni concentrate di K, chemioterapici, anestetici, farmaci con
basso I.T.) è opportuno prevedere particolari attività volte a limitare il più possibile eventuali errori. Ad es. disporre i vari dosaggi di una stessa specialità
farmacologica interponendo specialità diverse. Per quanto riguarda le soluzioni di K concentrato queste vanno tenute separate dagli altri farmaci per una
loro corretta identificazione e deve essere presente contrassegno di pericolosità. Esempi di farmaci particolarmente a rischio: Agonisti adrenergici,
anestetici generali endovena e locali iniettabili, bloccanti neuromuscolari, anticoagulanti esclusa eparina, antiaritmici, benzodiazepine, digitalici, sodio
nitro prussiato, antineoplastici, soluzione di potassio concentrato, ecc
d. Controllo delle scadenze: le Strutture Organizzative devono controllare periodicamente le date di scadenza e lo stato di conservazione dei prodotti
farmaceutici secondo un piano specifico, di cui è responsabile il Coordinatore assistenziale. Compilare lo scadenziario dei farmaci evidenziando quelli a
scadenza ravvicinata senza ritrascrivere sulla confezione la data di scadenza. Si devono verificare le scadenze e la corretta conservazione (ad es. verificare
l’apposizione della data di apertura e/o ricostituzione, nei prodotti che lo richiedono), analogamente, devono essere controllati tutti i luoghi/contenitori
dove sono presenti i prodotti farmaceutici (carrelli della terapia, carrelli delle emergenze, ecc.)NB: la data di scadenza indicata si riferisce al prodotto in
confezionamento integro, correttamente conservato.
(15) Controllo e restituzione di prodotti a seguito di segnalazione dalla farmacia/MAV/Ditta: il Coordinatore infermieristico in caso di segnalazioni
provenienti dalla farmacia/ MAV prende visione della segnalazione/circolare, provvede a ricercare il farmaco interessato nella sede di deposito ed
eventuali altre sedi (es: carrelli) e a restituirlo alla farmacia/MAV. Nota Bene: la segnalazione dei farmaci in ritiro o in sequestro avviene tramite mail
inviata da UO farmaceutica ospedaliera o da altre strutture ospedaliere e/o aziendali (direzione sanitaria, GRC, protocollo aziendale)Si deve mantenere la
refrigerazione per i farmaci da frigo anche se in ritiro o in sequestro e devono essere accompagnati dall’apposito modulo di conservazione correttamente
compilato. Se non diversamente comunicato i resi vanno inviati al MAV.
(16) Gestione prodotti non conformi: i prodotti farmaceutici scaduti, alterati o difettosi, in attesa dello smaltimento, devono essere separati dai prodotti in
corso di validità, racchiusi in un contenitore recante la dicitura: “FARMACI SCADUTI DA SMALTIRE”.
(17) I campioni gratuiti di farmaci devono essere conservati dal medico sotto la sua responsabilità, in luoghi ad accesso personale e assolutamente separati
dagli altri farmaci. Eventuali scaduti devono essere gestiti esclusivamente dal medico. La prescrizione di utilizzo dei campioni, può avvenire pertanto
unicamente da parte del medico proprietario e responsabile dei campioni, nel rispetto degli indirizzi terapeutici definiti dal responsabile della
Struttura/Azienda sanitaria. Se è necessaria la conservazione in frigorifero, i campioni possono essere tenuti in un contenitore con indicato esternamente il
nome del medico proprietario.
(18) Gestione e conservazione dei farmaci personali del paziente ricoverato: al momento della dimissione, i farmaci personali devono essere restituiti
all’assistito o, se ciò non fosse possibile, eliminati secondo le regole che presiedono allo smaltimento dei prodotti farmaceutici. Di norma non è previsto
l’utilizzo di farmaci personali del paziente durante la degenza almeno che il medico non disponga diversamente. Solo in casi eccezionali e al fine di non
interrompere la terapia, potranno essere utilizzati farmaci di proprietà del degente fino al ricevimento di quelli richiesti al MAV o alla Farmacia.
(19) Invio dei farmaci scaduti/non utilizzabili alla farmacia per lo smaltimento: I prodotti scaduti/non utilizzabili devono essere smaltiti secondo la normativa
vigente e secondo lo specifico “Protocollo Operativo Aziendale per la gestione dei rifiuti sanitari”. Gli stupefacenti scaduti devono essere smaltiti
secondo le norme vigenti che prevedono segnalazione da parte del Setting alla farmacia della giacenza dei farmaci scaduti e la successiva comunicazione
della Farmacia, che individua la data di invio dei farmaci dal setting in farmacia. Il setting deve restituire il farmaco stupefacente scaduto, utilizzando
modulistica ministeriale
(20) Controllo della prescrizione in fase di preparazione: oltre al controllo della precisa corrispondenza tra la prescrizione medica e il medicinale prelevato
per l’impiego, il personale addetto deve comunque sempre verificare la scadenza ed integrità dei farmaci. Controllare le diverse prescrizioni per lo stesso
paziente. Effettuare sempre il controllo della prescrizione: in caso di informazione mancante o dubbia l’infermiere non deve procedere alla
somministrazione della terapia ma chiedere immediatamente chiarimenti al medico.
(21) La preparazione della terapia deve essere effettuata subito prima della somministrazione, per evitare il deterioramento dei componenti del prodotto.
Evitare durante la preparazione le frequenti interruzioni. Attenersi alla specifica procedura per l’allestimento farmaci chemioterapici. Per la diluizione
delle soluzioni conc4entrate di K , in genere, per tutti i farmaci ad alto livello di attenzione, attenersi alle raccomandazioni Ministeriali dove si prevede il
controllo della procedura di diluizione da parte di un secondo operatore. Nota Bene: nella preparazione della terapia farmacologica vengono considerati il
contesto ambientale in cui si opera, la tipologia di farmaco, le caratteristiche dello stesso, le modalità di ricostituzione e di diluizione, la stabilità
chimicofisica, eventuali incompatibilità con altri farmaci. Particolare attenzione deve essere poi posta nell’effettuazione di calcoli per la trasformazione in
unità di misura diverse (es.: da unità di peso ad unità di volume) e per le diluizioni di farmaci concentrati. Particolari cautele potranno essere adottate per
la preparazione di specifici farmaci, con il ricorso a modalità ausiliarie (tabelle di diluizione, calcolatrici, ecc). Per evitare errori di terapia qualora il
farmaco venga diluito, applicare un etichetta con il nome del paziente, farmaco, diluizione, data, ed eventuali condizioni ambientali se richiesto.
(22) Controllo della prescrizione in fase di somministrazione: la somministrazione non deve essere mai effettuata nel caso in cui la prescrizione risultasse
non chiara o incompleta. Nel dubbio è necessario contattare il prescrivente. Deve essere verificata la corrispondenza tra il farmaco prescritto e quello
effettivamente prelevato per la somministrazione al paziente. Nota Bene: In caso di mancata corrispondenza tra i nomi delle due specialità, fare
riferimento al principio attivo e ai dosaggi.
(23) Verifica della validità e integrità del farmaco: in caso di dubbi riguardo all'integrità del prodotto, il farmaco non deve essere somministrato
(24) Identificazione paziente: prima di ogni somministrazione, colui che somministra deve identificare la donna controllandone nome e cognome riportati
sulla scheda di terapia e chiedendo conferma delle generalità al paziente (se è in grado di rispondere) e consultando la documentazione sanitaria.
Informare la paziente, se possibile, circa la terapia che gli è stata prescritta inclusi gli effetti collaterali ed incoraggiarla a fare domande relativamente alla
terapia somministrata: la corretta informazione aumenta la compliance. È auspicabile, quando possibile, la verifica e il controllo da parte di un altro
operatore circa l’identità della donna a cui si deve somministrare la terapia, al fine di evitare un qualsiasi errore di somministrazione.
(25) Controllo allergie: l’addetto alla somministrazione deve controllare, attraverso la STU la presenza di eventuali allergie. È auspicabile che le STU siano
complete anche dei dati di anamnesi allergologica, intol-leranze, consumo di prodotti da banco, alcool ed abitudini alimentari del paziente, al fine di non
utilizzare farmaci potenzialmente dannosi.
(26) Verificare la corrispondenza fra quanto indicato nella scheda di terapia e quanto preparato. Leggere attentamente al momento della somministrazione: il
dosaggio, la concentrazione, la via di somministrazione, la scadenza, l’etichetta del farmaco. Verificare che l’assunzione del farmaco sia avvenuta
correttamente. Evitare assolutamente di lasciare farmaci sul comodino sia in presenza che durante l’assenza momentanea del Pz. Le unità posologiche del
Pediatra
farmaco non devono essere rimosse dalla loro confezione originale, fino al momento della loro preparazione o somministrazione
Nota Bene: la
somministrazione della terapia farmacologica deve essere un atto unitario, sequenziale e cronologico. Atto unitario in quanto deve essere compiuto da una
sola persona. Il principio dell’unitarietà dell’azione (colui che preleva il farmaco e prepara eventuali diluizioni è colui che lo somministra) riconosce delle
eccezioni; esse sono date da: situazioni di emergenza, attività di insegnamento agli studenti, preparazione centralizzata in Farmacia, ecc.
(27) Somministrazione di farmaci in pompa Verificare ed impostare la velocità della pompa di infusione e controllare le linee di raccordo. Sostituire i kit di
infusione ogni 24 ore o secondo indicazione del produttore. La somministrazione di terapia in pompa presuppone una prescrizione completa dei parametri
da impostare per l’infusione. Verificare che sia stato seguito un breve corso di formazione al momento dell’acquisizione di nuove pompe e che tutto il
personale sia formato.
(28) Documentazione dell’avvenuta somministrazione: si appone la sigla dell’avvenuta somministrazione sulla STU. In caso di variazioni rispetto al piano
terapeutico, incluso il rifiuto della te-rapia da parte del Pz., occorre regi-strare l’accaduto sulla documentazio-ne sanitaria, informandone il medico
responsabile. Nel caso di somministrazioni di solu-zioni concentrate di K è da utilizzare una check list che indichi in ogni mo-mento l’esatta procedura da
seguire.
(29) Al momento della dimissione o della visita ambulatoriale vengono consegnati i farmaci per proseguire la terapia a domicilio. Controllare la
corrispondenza tra prescrizione e farmaco consegnato e apporre i fustelli sulle ricette. È ammessa solo l’erogazione di farmaci di classe A o particolari
farmaci elencati in delibere regionali o nazionali per partico-lare patologia. Per i farmaci al di fuori delle fattispecie sopra indicate deve essere redatta e
consegnata al Pz. la ricetta per l’approvvigionamento del farmaco all’esterno. In caso di chiusura della farmacia o in base a particolari accordi di
distribuzione da parte di ambulatori e servizi, i farmaci saranno consegnati direttamente in reparto e le ricette, debitamente compilate, dovranno essere
fatte pervenire in farmacia per i successivi atti amministrativi. Al fine di non interrompere la continuità terapeutica i farmaci devono essere consegnati
anche in caso di chiusura della farmacia ospedaliera. Si raccomanda comunque di consegnare la terapia sufficiente fino alla prescrizione del MMG.
(30) Dopo la somministrazione di un farmaco, tutti gli operatori sanitari che sono a contatto col Pz. hanno l’obbligo di sorveglianza sulle eventuali possibili
reazione avverse da farmaco. In caso di reazione avversa hanno l’obbligo di segnalazione sulla scheda mi-nisteriale ADR dopo avere attuato tutte le
iniziative cliniche del caso.

![Convenzione Farmacia di Castione Andeven[...]](http://s1.studylibit.com/store/data/000549370_1-32c309aae628fa144ca6b56b922fd7f6-300x300.png)










