ELETTROSTATICA:
ELETTRIZZAZIONE
ELETTRIZZARE = SEPARARE CARICHE ELETTRICHE GIÀ
PRESENTI NELLA MATERIA (la carica totale dell’universo, non varia)
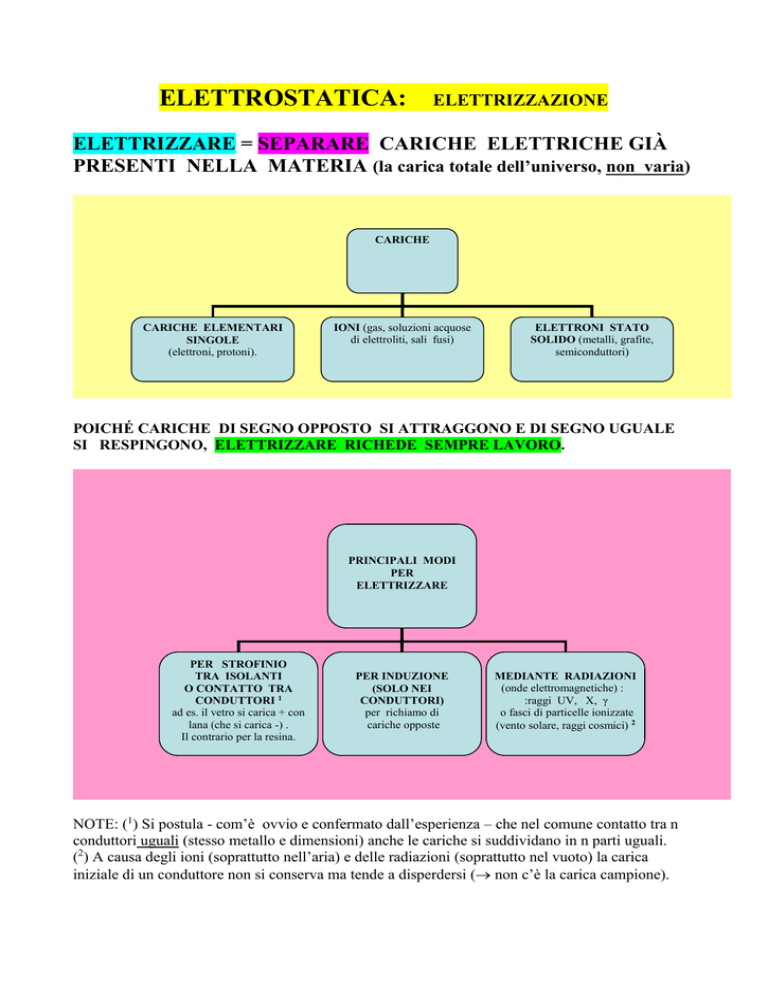
CARICHE
CARICHE ELEMENTARI
SINGOLE
(elettroni, protoni).
IONI (gas, soluzioni acquose
di elettroliti, sali fusi)
ELETTRONI STATO
SOLIDO (metalli, grafite,
semiconduttori)
POICHÉ CARICHE DI SEGNO OPPOSTO SI ATTRAGGONO E DI SEGNO UGUALE
SI RESPINGONO, ELETTRIZZARE RICHEDE SEMPRE LAVORO.
PRINCIPALI MODI
PER
ELETTRIZZARE
PER STROFINIO
TRA ISOLANTI
O CONTATTO TRA
CONDUTTORI 1
ad es. il vetro si carica + con
lana (che si carica -) .
Il contrario per la resina.
PER INDUZIONE
(SOLO NEI
CONDUTTORI)
per richiamo di
cariche opposte
MEDIANTE RADIAZIONI
(onde elettromagnetiche) :
:raggi UV, X, γ
o fasci di particelle ionizzate
(vento solare, raggi cosmici) 2
NOTE: (1) Si postula - com’è ovvio e confermato dall’esperienza – che nel comune contatto tra n
conduttori uguali (stesso metallo e dimensioni) anche le cariche si suddividano in n parti uguali.
(2) A causa degli ioni (soprattutto nell’aria) e delle radiazioni (soprattutto nel vuoto) la carica
iniziale di un conduttore non si conserva ma tende a disperdersi ( non c’è la carica campione).
8
L’ INDUZIONE ELE TTROSTATICA
La figura a fianco illustra il fenomeno dell’induzione
sul conduttore B isolato (sostegno giallo) e scarico per
effetto della vicinanza delle carica A, ad es. quella
positiva di un altro conduttore isolato – si noti che
essendo sferico le sue cariche sono disposte in modo
uniforme sulla sua superficie, e mai al suo interno,
come vedremo – richiama su B in prossimità di A
cariche negative (elettroni di conduzione) che creano
a loro volta cariche positive nei punti di B più lontani
(per l’eccesso di carica positiva degli ioni + rimasti).
B, per ipotesi inizialmente scarico, rimane tale.
Suddividendo poi B in due parti (ad es. tagliandolo o
rompendolo) si possono pertanto ottenere altri due corpi carichi di segno opposto oppure uno solo
“mettendo a terra” B (anche solo toccandolo dietro), in modo che le sue positive si disperdano.
LEGGE DI COULOMB E COSTANTE DIELETTRICA (ASSOLUTA O RELATIVA)
PER
DUE CARICHE (PICCOLE DA POTERSI CONSIDERARE PUNTIFORMI) Q1 E Q2 > 0 A DISTANZA r
TRA LORO VALE NEL VUOTO LA LEGGE DI COULOMB DEL TUTTO SIMILE A QUELLA GRAVITAZIONALE:
Q1 Q2
|F | = KC ---------- , dove KC = 8,9876 10 9 N m2 / C-2 ( C = Coulomb. Unità di carica elettrica)
r2
1
o anche, ponendo (per motivi che vedremo) KC = -------- essendo allora 0 = 8,8542 10 -12 F / m:
40
Q1 Q2
|F | = -------------- 0 E’ LA COSTANTE DIELETTRICA ASSOLUTA DEL VUOTO
2
40 r
Q1 Q2
PER OGNI MEZZO (OMOGENEO) DIVERSO DAL VUOTO RISULTA INVECE: |F | = --------------4 r2
AVENDO POSTO: = R 0 . R (NUMERO PURO SEMPRE > 1) È LA COSTANTE DIEL. RELATIVA
CHE SI DETERMINA SPERIMENTALMENTE.
ECCO
ALCUNI LORO VALORI (A
t = 20° C):
Vuoto: 1
plexiglas: 3
polistirolo: 2,5 – 2,7
terra (secca): 3
Na Cl :
Vetro : 3-12
carta (secca): 3
polivinile: 3 – 5
terra (umida): 10
diamante: 5,7
Mica : 7 – 8
cartone: 5
nylon: 3,7 – 5,5
ghiaccio: 3,1
Ambra: 2,8
gomma: 3 - 4
marmo: 8
alcool: 25,7
Porcellana: 6
paraffina: 2 – 2,5 zolfo: 3,8 – 4,4
Acqua (0°C): 87,7
5,9
quarzo: 4,5
aria (secca): 1,000513
benzene: 2,3
acqua (20°C): 80,1 acqua (50°C): 69,9 acqua (90°C): 58,3
H2 : 1,000253
He: 1,0000548
r È SEMPRE > 1 PER EFFETTO DELLA POLARIZZAZIONE DEI DIELETTRICI
LA POLARIZZAZIONE
La polarizzazione è presente in tutta la materia ma
si manifesta solo nei dielettrici in quanto nei
conduttori viene mascherata dall’induzione.
Essa è dovuta a spostamenti microscopici delle
cariche elettriche degli atomi e delle molecole
mentre nell’induzione dei conduttori sono sempre
macroscopici). Ogni atomo, elettricamente neutro, in
prossimità di cariche elettriche si deforma infatti sia
pure impercettibilmente - il nucleo positivo si sposta
da una parte, la nuvola elettronica dall’altra - dando
luogo alla polarizzazione (sempre presente, ma con
effetti molto lievi, quindi R 1 ad es. elio o aria)
per deformazione. Nei composti che presentano
invece molecole (o ioni) con cariche non distribuite
uniformemente – presentanti cioè dipoli dovuti a
legami chimici di tipo ionico, almeno in parte, l’es.
tipico (e quasi unico per la sua rilevanza) è l’acqua –
le cariche tendono ad orientarsi nel campo elettrico
creando così un ordine che si oppone ad disordine
dovuto all’agitazione termica (polarizzazione per
orientamento che si aggiunge alla precedente).
Nel caso dell’acqua –alla cui alta polarizzazione è
dovuto la dissociazione elettrolitica dei sali, acidi,
basi (sostanze polari, mentre non lo è ad es. lo
zucchero) si spiegano quindi facilmente i suoi
diversi valori di R al variare della temperatura e il
basso valore del ghiaccio (ioni quasi bloccati).
MA PERCHÉ LA POLARIZZAZIONE MODIFICA r ?
Come risulta chiaramente dalla 1° figura, mentre all’interno del dielettrico si alternano cariche di
segno opposto (gialli negativi e grigi positivi) così
vicine da far apparire il dielettrico al suo interno
macroscopicamente privo di carica , sulle sue due
superfici esterne esse costituiscono a tutti gli effetti
due strati di cariche di segno contrario a quello delle
armature la cui azione risulta così indebolita. La
forza ora attrattiva che si esercita tra le due armature
in presenza del dielettrico interno risulta pertanto
attenuata - rispetto a quella che avrebbe se in mezzo
ci fosse il vuoto - di un fattore che globalmente si
quantifica mediante il valore della costante
dielettrica relativa, sempre quindi maggiore di 1.
Resta così pienamente spiegata l’attrazione che la carica Q - positiva o negativa che sia – esercita
sempre inizialmente sulla pallina S scarica (o su piccoli pezzetti di carta ecc.). Essa è dovuta
all’attrazione che Q esercita sulle cariche di S ad essa più prossime (quindi di segno opposto) che
per polarizzazione su S si sono formate. Venuta poi S a contatto con Q, S si carica (per contatto)
dello stesso segno di Q e viene quindi respinta.