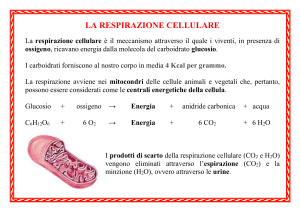
I gas respiratori O2 e CO2 sono scambiati per
diffusione semplice sia a livello dell’interfaccia
alveoli-capillari polmonari sia a livello
dell’interfaccia capillari sistemici-cellule. La
diffusione obbedisce alla legge di Fick:
Permeabilità della
Gradiente di concentrazione
membrana
A (c 2 c1) P
J
d
Area di scambio
Flusso
Spessore
Negli organismi biologici in genere il fattore
determinante è il gradiente di concentrazione
perché A, d e P sono massimizzate per favorire il
processo.
In fisiologia respiratoria ci si riferisce alle pressioni
parziali dei gas in soluzione. Un gas si sposta da
regioni a maggior pressione parziale verso regioni
a minor pressione parziale
Prima di descrivere lo scambio dei gas vale la pena
ricordare che il passaggio di gas da ambiente gassoso
ad ambiente liquido è condizionato da alcuni fattori:
• Temperatura
• Pressione parziale del gas all’interfaccia aria-liquido
• Proprietà chimiche del gas e del liquido
La concentrazione di un gas in un liquido a
temperatura costante è regolata dalla legge di Henry:
C gas in soluzione = k · P
L’anidride carbonica è
circa 20 volte più
solubile dell’ossigeno in
acqua. Quindi anche a
uguali pressioni parziali
la quantità di gas
N.B.: All’equilibrio la pressione parziale
di ossigeno
èè
disciolta
in acqua
uguale nella fase gassosa e in soluzione.
Questo
però
maggiore
per la
CO2
NON SIGNIFICA CHE LE CONCENTRAZIONI
rispetto a ODI
2
OSSIGENO SIANO UGUALI!!! Infatti la concentrazione di
ossigeno disciolta dipende anche dalla SOLUBILITÁ
dell’ossigeno (che in acqua è poco solubile)
Come avviene lo scambio dei
gas respiratori nei polmoni e nei
tessuti?
Le pressioni parziali dei gas alveolari differiscono
da quelle atmosferiche
per tre motivi: Sangue
Sangue
Fra aria e sanguearterioso
avvengono continuamente
venoso
scambi
L’aria
satura di vapor acqueo
PO alveolare è100mmHg
40mmHg
2
In seguito ad un’inspirazione aria atmosferica
fresca si mescola con quella ricca di CO2 dello
P
40mmHg
CO2
spazio morto di conduzione
pH
7.40
46mmHg
7.37
A cosa può essere dovuto un
basso contenuto arterioso di
ossigeno?
1.
La riduzione della PO2 alveolare
diminuisce l’assunzione di ossigeno
dai polmoni
Esistono due cause possibili di una ridotta PO2
alveolare:
i.
L’aria inspirata ha un basso contenuto di
ossigeno (vedi altitudine)
ii. La ventilazione alveolare è inadeguata
(ipoventilazione)
2. Le alterazioni della membrana alveolare
modificano lo scambio di gas fra alveoli e
capillari polmonari
Lo scambio di ossigeno dagli alveoli al sangue richiede il
passaggio attraverso la barriera formata da cellule
alveolari e endotelio capillare. Questa diffusione può
essere alterata per:
i. Diminuzione dell’area disponibile per lo scambio
gassoso
ii. Aumento dello spessore della membrana
alveolare
iii. Aumento della distanza di diffusione
L’ossigeno è trasportato nel sangue con due
meccanismi:
in soluzione nel sangue (meno del
10% dell’ossigeno consumato che è ca
250ml/min a riposo)
legato all’emoglobina a cui si lega
secondo la reazione reversibile
Hb + O2 ↔ HbO2
E’ possibile respirare senza emoglobina?
La richiesta di O2 in condizioni normali è di:
250 ml/min
Con una G.C. di 5 l/min ed una quantità di O2
sciolto sotto forma di gas di 3 ml/l, avremmo una
disponibilità di O2 di:
3 ml/l x 5 l/min = 15 ml/min
Per far fronte a una richiesta di 250 ml/min la G.C.
dovrebbe aumentare 16 volte mentre può al
massimo crescere 9 volte
Respirazione con emoglobina
L’emoglobina lega 20 ml di O2 ogni 100 ml di
sangue (cioè per esattezza 19.7 ml/100ml che
equivalgono a 197 ml/l di sangue). Di questi ne
scambia 5 ml/100 ml con i tessuti.
5
ml/100
ml scambiato
equivalgono
a 50 ml/l
che
1gr
Hb trasporta
ca 1.35ml
O2 (numero
di Hüfner)
moltiplicati
per/ lladiG.C.
(5 l/min) danno:
ca 146gr Hb
sangue
ca 197ml O50
l di sangue
2 / ml/l
x 5 l/min = 250 ml/min
che rappresenta la quantità di O2 al minuto di cui
abbiamo bisogno in condizioni normali
A
M
Emoglobina =
proteina con elevatissima
capacità di trasporto per O2
Proteina con struttura quaternaria (M.W.= 68kDa)
Ossigenazione
formata da
4 sub-unità ciascuna
avvolta attorno ad
dell’emoglobina
e non
un gruppo emeossidazione!!!
(fra loro identici) contenente un
atomo di Fe che lega una molecola di ossigeno:
pertanto la molecola di emoglobina può trasportare
fino a 4 molecole di ossigeno
Adulto (HbA) α2 β2
Adulto (2%) (HbA2) α2δ2
Feto (HbF) α2γ2
Il legame fra ossigeno ed emoglobina segue
la legge dell’azione di massa
Hb + O2 ↔ HbO2
Verso sx se la
concentrazione di
ossigeno diminuisce
Verso dx se aumenta
la concentrazione di
ossigeno
cambia colore se legata a O2
HbO2 (rosso vivo; ossiemoglobina)
Hb
(rosso bruno; deossiemoglobina)
l’O2 si lega al Fe2+ del gruppo eme ma non lo
ossida: forma un legame reversibile ad alta
affinità.
se il Fe2+ diventa Fe3+, l’Hb diventa
metaemoglobina (composto stabile con l’O2,
cessa di trasportare O2).
la metaemoglobina-reduttasi ripristina i livelli di
Hb.
Ingresso dell’ossigeno
disciolto nel plasma
Diffusione all’interno
delle cellule
dell’ossigeno disciolto
nel plasma; questo
riduce la Po2 nel
plasma e tende a far
spostare la reazione
verso dx con
liberazione di O2
dall’Hb
Rilascio di
ossigeno da
Hb
Il legame di ossigeno all’emoglobina si
esprime in percentuale. Per un certo
valore di PO2 vale:
Quantità di O2 legata
Quantità max che
può essere legata
Saturazione %
X 100 =
dell’emoglobina
Che relazione esiste fra PO2 e quantità
di ossigeno legata all’emoglobina?
98%
75%
In un muscolo
in forte
esercizio PO2
scende a
20mmHg e la
saturazione di
Hb al 35% ca
In questo
range la
saturazione di
Hb non scende
troppo
L’andamento sigmoide della
A livello tissutale
PO2 =40mmHg
Hb cede il 25%
dell’ossigeno
trasportato,
restando satura
al 75%
curva sta ad indicare una
cooperazione positiva fra le
quattro subunità
della molecola
26.8
di Hb
la quantità di O2 legata all’Hb è proporzionale
alla PO2
legame reversibile
100% di saturazione (raggiungibile solo per PO2
pari a 600mmHg!!) equivale alla capacità
massima del sangue di legare l’O2
la [Hb] nel sangue è 15gr/100ml
1 gr di Hb lega 1.35 ml di O2
l’Hb lega: 15gr/100 ml x 1.35 ml O2 = 20 ml O2
/100 ml sangue
la mioglobina è formata da una sola subunità di
globina
possiede alta affinità per l’O2. E’ contenuta nel
m. scheletrico ed è saturata a PO2 = 40 mmHg
(sangue venoso)
è una riserva di O2 muscolare, che viene ceduto
quando l’O2 diminuisce
l’Hb ha una affinità 250 volte maggiore per il
CO
il CO sposta la curva di saturazione verso
sinistra (maggiore affinità)
PCO molto basse saturano l’Hb
lo scambio di O2 in presenza di 50% HbCO è
fortemente sfavorito
Effetti di pH, T e PCO2
N.B.: Variazioni molto pronunciate nella parte ripida
della curva. Questo significa che le variazioni hanno
molto effetto a livello tissutale (PO2 fra 20 e 40mmHg)
più che a livello polmonare (PO2 fra 90 e 100mmHg)
Variazione di pH = effetto Bohr
Forte esercizio fisico
75%
Anaerobiosi
57%
Produzione di ac. lattico
Rilascio di H+ nel LEC
Questo significa che in
condizioni di acidosi il sangue
rilascia più O2 ai tessuti che in
quel momento ne hanno
bisogno
Effetto del 2,3-DPG
DPG deriva da un intermedio
della glicolisi. Una ipossia ne
aumenta i livelli riducendo
l’affinità di legame di Hb e
ossigeno. Altitudine e
anemia sono le cause più
frequenti
HbA e HbF
Migliore capacità di
legare O2 in ambiente
placentare dove il
tenore di ossigeno è
basso
Riassumendo
Trasporto di CO2
Prodotto di scarto della respirazione cellulare
che determina acidosi, alterazioni del SNC fino
alla morte
Più solubile dell’ossigeno nei liquidi corporei
Prodotta in quantità notevoli rispetto a quella
trasportata nel plasma
*Questa quota ha due scopi:
• Fornire un meccanismo per il
trasporto di CO2
•
Rendere
il
bicarbonato
Il trasporto di CO2 nel sangue segue tre vie
disponibile
come
tampone
- disciolta nel sangue 7%
- diffusione nei globuli rossi 93% di cui
70% convertita in bicarbonato*
23% legata a Hb
diffusione
HCO3- scambiato con
Cl- in antiporto
Scambio dei cloruri
Per mantenere la reazione
(elettroneutro)
spostata verso dx e
neutralizzare così la CO2 che
*
si formaFormazione
in continuazione,
di carbaminoemoglobina.
vengono sottratti i prodotti
La sua formazioneEffetto
è facilitata
tampone dianche
Hb
della reazione.
*Si può
scrivere
perché
H+ e
CO
l’affinitàdadiHb.
HbQuando
2 riducono
Gli ioni
H+semplicemente
sono bufferati
O2 troppo la Hb non riesce
la COper
come:
2 aumenta
gli idrogenioni
che si
CO2 + Ha2neutralizzare
O ↔ H+tutti
+ HCO
3 acidosi
accumulano determinando
Reazione reversibilerespiratoria
che
obbedisce alla legge dell’azione
di massa
Al diminuire della PCO2
plasmatica la CO2 disciolta
nell’eritrocita diminuisce
spostando la reazione verso
dx.
Lo scambio dei cloruri si
inverte e gli idrogenioni
lasciano l’Hb
Scambio dei cloruri e legame di H+ con Hb
forniscono due sistemi volti a sottrarre CO2 e
garantire così il gradiente necessario al suo
ingresso nell’eritrocita.
Nei casi di eccessiva produzione di CO2 la Hb
non riesce a tamponare tutti i protoni prodotti
che passano quindi nel plasma causando
ACIDOSI RESPIRATORIA
Abbiamo visto che circa il 23% di CO2 si lega a
Hb e in particolare sui gruppi NH2 esposti
formando così carbaminoemoglobina. Tale
legame è facilitato dalla presenza di CO2 e H+ i
quali riducono entrambi l’affinità di Hb per
l’ossigeno.
CO2 + Hb
HbCO2
TRASPORTO AI POLMONI DI CO2
PCO2alv < PCO2venoso
Effetto Haldane
La rimozione di ossigeno dall’emoglobina (a
livello tessutale) aumenta l’affinità
dell’emoglobina per l’anidride carbonica. Questo
permette alla CO2 di essere “caricata” sull’Hb
vuota
A livello dei tessuti:
l’Hb deossigenata lega meglio la CO2
formando composti carbamminoemoglobinici (effetto Haldane).
l’effetto Haldane è responsabile di circa la
metà della CO2 che viene scambiata e
trasportata a livello dei tessuti.
A livello alveolare:
la formazione di HbO2 riduce il legame di
CO2 e H+ con l’Hb
la maggiore CO2 disponibile viene
scambiata con l’alveolo ed espulsa
C
Trasporto di ossigeno nel sangue
1,5%
Disciolto
98,5%
Legato a Hb
Trasporto di anidride carbonica nel sangue
23%
7%
Disciolto
70%
Bicarbonato
Legata a Hb
Processo ritmico, non cosciente
A differenza del battito cardiaco però il
muscolo scheletrico non è dotato di
automaticità ma riceve innervazione da
motoneuroni somatici che a loro volta
prendono ordini dal SNC
Meccanismo altamente regolato
GVD
GVV
I centri di controllo respiratori sono localizzati a
livello del ponte e del bulbo. I neuroni formano
un generatore centrale di rimo respiratorio. Tale
rete è difficile da studiare per la complessità e la
localizzazione. La maggior parte di informazioni
derivano da pazienti con lesioni cerebrali. Esiste
un modello atto a spiegare il meccanismo, i cui
punti fondamentali sono i seguenti
Neuroni respiratori bulbari controllano
inspirazione (GVD) ed espirazione (GVV)
Neuroni del ponte modulano la ventilazione
La ritmicità deriva da un insieme di neuroni
che scaricano spontaneamente
La ventilazione è soggetta a modulazione da
parte di vari fattori chimici e dei centri
cerebrali superiori
Il centro respiratorio bulbare è controllato
continuamente nel suo funzionamento dai livelli
plasmatici di CO2, O2 e H+. I neuroni bulbari sono
raggruppati in due importanti nuclei che sono:
• gruppo ventilatorio dorsale, INSPIRATORIO
• gruppo ventilatorio ventrale, ESPIRATORIO
e controllo dei muscoli inspiratori implicati
nell’inspirazione profonda
CO2, O2 e pH
La CO2 è lo stimolo principale per modificare la
ventilazione. I chemocettori per ossigeno e
anidride carbonica sono associati alla
circolazione arteriosa. Quando O2 diminuisce
troppo o la CO2 aumenta, il centro inspiratorio
viene stimolato ad aumentare la ventilazione. I
chemocettori comprendono chemocettori
periferici (glomi aortici e carotidei) e
chemocettori centrali (superficie ventrale del
bulbo)
L’ossigeno non è
comunque un fattore
importante nel determinare
la ventilazione perché PO2
* Condizione compatibile
deve scendere sotto a con un’altitudine di 3000m
60mmHg prima di stimolare
la ventilazione*. I
chemocettori periferici
quindi non svolgono un
ruolo quotidiano nel
controllo della ventilazione
Va notato che gli H+ presenti nel
plasma passano male attraverso la
BEE e hanno quindi scarso effetto
sui chemocettori centrali
Il fattore fondamentale nel controllo della ventilazione
è la CO2 che agisce sui chemocettori centrali
Quando PCO2 aumenta, la CO2 passa
rapidamente la barriera emato-encefalica
andando ad attivare i chemocettori centrali che
segnalano al generatore centrale di ritmo
respiratorio di aumentare la frequenza e la
profondità degli atti respiratori. In realtà il
parametro che i chemocettori valutano è il valore
di pH in base alla seguente reazione
CO2 + H2O
↔ H2CO3
↔ H+ + HCO3-
Questi chemocettori centrali si adattano
all’ipercapnia cronica, mentre i chemocettori
periferici non si adattano all’ipossia cronica: in
questi casi, come ad esempio nell’enfisema, la
bassa PO2 rimane l’unico stimolo alla
ventilazione
Accanto a quanto visto esistono anche
riflessi protettivi che difendono il polmone
(riflesso di distensione di Hering-Breuer)
La ventilazione è inoltre modulata da
centri superiori come ipotalamo e sistema
limbico. Va però detto che non esiste
modo per bloccare i riflessi mediati da
chemocettori
Per chi fosse interessato
http://www.ismmed.org/np_altitude_tutorial.htm
http://www.high-altitude-medicine.com/