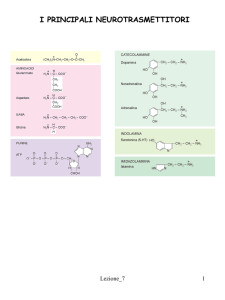
TRASMISSIONE CATECOLAMINERGICA
Le catecolamine (CA) vengono riilasciate da:
- Terminali delle fibre post-gangliari del sistema nervoso simpatico
- Midollare del surrene
- Neuroni CA-ergici del SNC (popolazione minoritaria)
Coinvolta in: depressione, schizofrenia,
Parkinson, tossicodipendenze, etc.
Le catecolamine del sistema nervoso autonomo
Noradrenalina (NA): principale nt rilasciato dalle fibre simpatiche
Adrenalina (Adr): prodotta dalla midollare del surrene (Adr:NA = 4:1)
Le fibre (pregangliari) del SN simpatico originano dai segmenti toracici (T1T12) e lombari (L1-L3) del midollo spinale
I principali effettori viscerali innervati dalle fibre post-gangliari del simpatico
sono: muscolo dell’iride e muscolo ciliare, ghiandole lacrimali e sublinguali,
cuore, bronchi, vasi, fegato, pancreas, tratto GI, etc.
DA: viene rilasciata dagli interneuroni DA-ergici presenti a livello gangliare
Neurone
pre-gangliare
ACh
DA
NA
Neurone
post-gangliare
Principali funzioni delle catecolamine del SN simpatico:
↑ frequenza cardiaca (effetto cronotropo positivo) – b1
↑ velocità di conduzione atrio-ventricolare (effetto dromotropo positivo) – b1
↑ forza di contrazione (effetto inotropo positivo) – b1
Vasocostrizione – a1
Sistema renina-angiotensina – b1 juxtaglomerulari
↑ Part
Rilasciamento muscolatura liscia GI e musc detrusore della vescica – b2
Contrazione musc sfinteri – a1
Broncodilatazione – b2
Glicogenolisi epatica => iperglicemia – b2
Lipolisi – b3
Effetti periferici della DA:
A basse concentrazioni (attivazione D1):
Vasodilatazione (per azione diretta sui vasi o per inibizione del rilascio delle CA)
↑ filtrazione glomerulare, flusso ematico renale e natriuresi
A concentrazioni relativamente alte:
Effetto inotropo positivo (per b1 del miocardio e > rilascio di NA dai terminali
nervosi)
A concentrazioni piuttosto alte:
Vasocostrizione (per a1)
La trasmissione NA-ergica nel sistema nervoso centrale
La maggior parte delle vie NA-ergiche ha origine dal LOCUS COERULEUS e
dal SISTEMA TEGMENTALE LATERALE
Il locus coeruleus contiene ~ 43% dei neuroni NA-ergici cerebrali che
proiettano a: corteccia cerebrale, ippocampo, talamo, ipotalamo, midollo
spinale (corna ventrali), tronco encefalico, cervelletto
Nel sistema tegmentale laterale si distinuguono tre nuclei:
- nucleo motorio dorsale del vago
- nucleo del tratto solitario (NTS, controllo dei neuroni pregangliari del midollo
spinale e della catena laterale del simpatico)
- nucleo tegmentale laterale (proietta ad ipotalamo, bulbo olfattorio e amigdala)
Funzioni dei sistemi NA-ergici del SNC
• Controllo della pressione arteriosa:
Baro- e chemocettori
aortici e carotidei
Nuclei tegmentali laterali (NTS)
↓ Part => ↓ firing barocettori => disinibizione NTS => tono simpatico
↑ resistenze vascolari
↑ gittata cardiaca
• Depressione:
Le sindromi depressive sono spesso caratterizzate da un’alterata regolazione
dei sistemi NA-ergici centrali (es: alterazioni a2 e b2 nella cx frontale e nel
sistema limbico)
• Stimolazione dello stato di veglia:
L’attività dei neuroni NA-ergici che originano nel locus coeruleus è aumentata
nello stato di veglia, mentre è ridotta durante il sonno
Locus coeruleus
a1 post-sinaptici
NA
Recettori a2
(sedazione)
(promuovono lo
stato di veglia)
• Regolazione del comportamento alimentare:
IPOTALAMO
n. paraventricolare ( a2 => ↑ ingestione di cibo/carboidrati)
n. perifornicale ( b2 e D2 => ↓ assunzione alimenti)
• Effetti endocrini:
Controllo del rilascio di ACTH, GH, TSH, LHRH
La trasmissione DA-ergica nel sistema nervoso centrale
SISTEMA NIGRO-STRIATALE:
SNc
DA
SNR
Striato (caudato + putamen)
GABA
SNc: gruppo A9 dei neuroni DAergici del mesencefalo. I dendriti liberano DA
nella SNR => regolazione dell’attività dei terminali afferenti dai gangli della base
SISTEMI MESOLIMBICO E MESOLIMBOCORTICALE:
Nucleo accumbens
VTA
(A10)
DA
Corteccia prefrontale
SISTEMA MESOTALAMICO:
VTA
(A10)
DA
Abenula
SISTEMI TUBEROINFUNDIBOLARE E TUBEROIPOFISARIO:
Ipotalamo
(n.arcuato e periarcuato)
(A12)
DA
Ipofisi intermedia (⊝ secrezione
a-MSH e bEnd)
Ipofisi posteriore (⊝ secrezione
ossitocina e vasopressina)
Eminenza mediana (la DA può
essere liberata nel circolo portale
ipofisario => raggiunge l’ipofisi
=> ⊝ secrezione prolattina)
Rappresentazione schematica dei sistemi mesolimbico e mesocorticale:
Ruoli fisiopatologici della DA del SNC
• Controllo del tono muscolare e della coordinazione motoria:
Autorecettori DAergici
SNc
DA
Terminazioni neuroni Glu-ergici corticali
Striato
Neuroni post-sinaptici intrastriatali colinergici
Neuroni GABAergici (dal GB o SN)
In condizioni di ridotto tono DAergico (es. morbo di Parkinson o trattamento con
neurolettici) si manifestano: fini tremori a riposo, acinesia, rigidità muscolare
• Contollo delle funzioni psichiche (schizofrenia):
Antipsicotici (neurolettici) => AT-D2 (la potenza clinica si correla con l’affinità
per i recettori D2)
L-DOPA
Cocaina
Amfetamine
↑ DA => psicosi simile alla forma paranoide della schizofrenia
Pazienti schizofrenici ----(PET)---> ↑ D2 (striato e tubercolo olfattorio)
causa o conseguenza della schizofrenia???
“IPOTESI” DOPAMINERGICA DELLA SCHIZOFRENIA:
↓ Attività DAergica nell’area
prefrontale => mancanza di
feedback inibitorio sul sistema
mesolimbico
Sintomi “negativi”: isolamento dalla vita
sociale, appiattimento delle risposte
emotive (demenza)
↑ Attività DAergica nel sistema
mesolimbico (mediata da D2, D3 e D4)
Sintomi “positivi”: deliri, allucinazioni,
disordini del pensiero
• Tossicodipendenza:
Il sistema mesolimbocorticale è responsabile delle proprietà di gratificazione
e di rinforzo caratteristiche delle sostanze d’abuso
Psicostimolanti (cocaina, nicotina, etc.), morfina e EtOH => ↑ DA nel NAc
• Controllo del vomito:
D2 nella CTZ => vomito (AT D2=antiemetici)
D2 nella parete gastrica => ⊝ motilità gastrica (AT D2=procinetici)
METOCLOPRAMIDE: sedazione + Parkinsonismo x uso cronico
AT-D2
DOMPERIDONE: poco liposolubile => passa difficilmente la BEE, ma
raggiunge la CTZ! => scarsi effetti centrali => utile nel
controllo del vomito da farmaci anti-Parkinson
NB: anti-M, anti-H1, e AG 5-HT3 => antiemetici per azione sulla CTZ
• Diminuzione dell’assunzione di cibo:
D2 nel n. perifornicale ipotalamico (=> aumento ponderale con antipsicotici)
• Ipotermia:
D2 ipotalamici (=> ipertermia marcata => “sindrome maligna” da neurolettici)
• ↓ secrezione di prolattina:
D2 ipofisari (=> iperprolattinemia da neurolettici)
Sintesi delle catecolamine
dieta
FENILALANINA
Phe-idrossilasi
Reazione lenta
Enzima limitante
Associato al RE
Scarsa specificità di substrato
(decarbossila DOPA, ma anche
gli altri aa aromatici levogiri)
La velocità di sintesi delle CA dipende dall’attività dell’enzima Tyr-idrossilasi:
- ↑ in condizioni di elevata attività neuronale (x ↑ del numero di molecole di
enzima presenti nel neurone)
- ↓ per inibizione dell’enzima dovuta ad accumulo dei prodotti finali della
sintesi delle CA (feedback inhibition)
- ↑ a seguito di fosforilazione dell’enzima (PKA, PKC e PK-Ca2+-CaM-dip. =>
↑ attività idrossilasica)
Immagazzinamento vescicolare delle catecolamine
ADP
H+
ATP
H+
NA
ATP
ATP NA ATP
2+
ATP
Mg
Cromogranine
DA-b-idrossilasi
Inibito da RESERPINA => ↑ [CA]citoplasmatica
=> >degradazione CA => effetti antiipertensivi,
extrapiramidali, depressione, sedazione
Le cromogranine sono proteine acide idrosolubili, presenti in elevate conc nelle
vescicole sinaptiche dei terminali CAergici e nei granuli delle cellule cromaffini
CROMOGRANINE + ATP + Ca2+ + Mg2+ => complesso macromolecolare che
lega le CA nelle vescicole => bassa [CA] libera
SIMPATICOMIMETICI INDIRETTI:
Derivati feniletilaminici che competono con le CA per il legame con le
cromogranine => ↑ [CA] libera intravescicolare => e citoplasmatica => rilascio
di CA con meccanismo non vescicolare dal terminale nervoso (inversione
NET/DAT) [es: b-OH-feniletilamina, amfetamine]
Le amine simpaticomimetiche indirette possono indurre un rapido esaurimento
delle riserve del neurotrasmettitore => TACHIFILASSI
Degradazione metabolica delle catecolamine
Degradazione metabolica delle catecolamine
Le principali vie di degradazione delle CA sono:
- deamminazione ossidativa (MAO) [-NH2/NHCH3 -CHO]
- O-metilazione (COMT) [catecolo-OH -CH3]
MAO:
Le MAO neuronali sono localizzate sulla membrana esterna dei mitocondri
nella terminazione CA-ergica
Se ne conoscono 2 sottotipi prodotti da 2 geni diversi:
MAO-A: deamminazione di a-NA e indol-etilamine (es 5-HT)
presenti nei terminali adrenergici e serotoninergici
MAO-B: deamminazione fenil-etilamine (DA, tiramina)
ubiquitarie (alte conc in fegato e reni)
inibite dalla selegilina (F per il morbo di Parkinson)
INIBITORI delle MAO: iproniazide, fenelzina e tranilcipromina. Sono inibitori
poco selettivi e irreversibili delle MAO con azione antidepressiva. Determinano
gravi crisi ipertensive per associazione con cibi contenenti tiramina (vino,
formaggi, etc.).
COMT:
Sono localizzate prevalentemente in sede post-sinaptica, nel citoplasma (++) e
nella membrana (-)
Donatore di gruppi metilici: S-adenosil metionina
Ubiquitarie (alte conc in fegato e reni)
Selettive per il catecolo
Attivate da Mg2+ e altri cationi bivalenti
NB: la rimozione delle CA ad opera delle MAO e delle COMT è meno efficiente
rispetto all’uptake neuronale!!
Solo nel fegato la funzione di questi enzimi è più importante
Recettori per le catecolamine
Sono recettori accoppiati alle proteine G
Il legame con le CA avviene a livello delle 7 regioni transmembrana (altamente
conservate)
Famiglia
a1
a2
Sottotipi
Meccanismi di trasduzione
a1A
↑IP3/DAG
a1B
↑IP3/DAG
a1C
↑IP3/DAG
a1D
?
a2A
AG: fenilefrina
AT: prazosina
↓ cAMP
↑permeabilità al K+
↓permeabilità al Ca2+
↓ cAMP
↓permeabilità al Ca2+
↓ cAMP
a2B
a2C
b
b1
b2
b3
↑cAMP
Ordine di potenza degli agonisti:
a: Adr ≥ NA >> isoproterenolo
b: isoporterenolo > Adr > NA
b1: Adr ~ NA
b2: Adr 10-50 x NA
b3: NA 10 x Adr
AG: clonidina
AT: yohimbina
Recettori a-adrenergici
Localizzazione cellulare
a1:
Recettori giunzionali post-sinaptici presenti sulla muscolatura liscia dei vasi (VC),
nel tratto GI e nel cuore
Nel SNC abbondano in corteccia, ippocampo e ipotalamo
AG: fenilefrina, metossamina; AT: fenossibenzamina
a2:
- Presinaptici (inibiscono la liberazione di NA e ACh)
- Extragiunzionali (sulla muscolatura liscia dei vasi mediano VC interagendo con
le CA circolanti e non con quelle provenienti dalle terminazioni simpatiche).
Presenti anche su piastrine e leucociti
Struttura e sistemi di trasduzione dei recettori a1
- 7 TM
- Siti di N-glicosilazione sul N-terminale
- Lunga coda C-terminale
Gq
a1 => PLCb
IP3: mobilizzazione del Ca2+ dai depositi intracellulari
DAG: PKC => fosforilazione canali e pompe =>
regolazione conduttanze ioniche
⊝ glicogeno sintasi
↑ [Ca2+]i => PK Ca2+-CaM-dipendente (es: fosforilasi chinasi => ↑ glicogenolisi
epatica)
PK Ca2+-dipendenti (es: chinasi della catena leggera della miosina
=> contrazione della muscolatura liscia vasale)
Canali al K+ Ca2+-dipendenti (iperpolarizzazione => rilassamento
della muscolatura liscia gastro-intestinale)
Altri meccanismi derivanti dall’attivazione di Gq:
PLA2 => AA PGs e LTs
PLD
Fosfatidilcolina
Liberazione di Ca2+ dai depositi intracellulari
Acido fosfatidico
Metabolizzato a DAG
Stimolazione diretta dei canali al Ca2+ (?)
Struttura e sistemi di trasduzione dei recettori a2
- 7 TM
- 2 siti di N-glicosilazione sul N-terminale (a2A e a2C)
- Lungo dominio intracellulare fra TM5 e TM6
- Breve regione C-terminale (siti di tio-acilazione)
a2A:
Gia => ⊝ AC
Gibg => Canali al K+ accoppiati a proteine G (=> iperpolarizzazione => rilassamento musc liscia GI)
Go => ⊝ VOCCs di tipo L ed N (=> ⊝ liberazione NA e ACh)
a2B
Go/i (?) => PLA2 (AA TXA2 => ↑ aggregazione piastrinica)
↑ [Ca2+]i (=> contrazione muscolatura liscia dei vasi)
La stimolazione dei recettori a2 porta a ↓ Part per:
⊝ rilascio di CA dai terminali sinaptici dell’ortosimpatico (autorecettori inibitori)
⊝ dell’attività dei centri vasomotori centrali
Struttura e funzioni dei recettori b-adrenergici
- 7 TM
- 60% identità di sequenza nelle regioni TM (binding site)
- il gruppo NH+ di Adr e NA interagisce con l’Asp113 del dominio TM3
- siti di N-glicosilazione sul N-terminale (1 su b1, 2 su b2 e b3)
- lunga coda C-terminale (in b1 e b2)
- siti di tioacilazione sul C-terminale (di b2)
Localizzazione:
b1: cuore ()
apparato juxtaglomerulare renale ( secrezione di renina)
SNC (post-sinaptici)
b2: muscolatura liscia (rilassamento – es: bronchi)
muscolatura scheletrica (↑ forza di contrazione)
fegato ( glicogenolisi)
SNC (prevalentemente pre-sinaptici)
b3: tessuto adiposo (↑ lipolisi)
Meccanismi di trasduzione del segnale:
b Gs ↑ cAMP PKA
Fosforilasi K glicogeno fosforilasi =>
↑ glicogenolisi
⊝ glicogeno sintasi
triglicerido-lipasi
b1 Gs VOCCs (L) nel muscolo cardiaco e scheletrico
RECETTORI DOPAMINERGICI
Famiglia
D1-like
D2-like
Sottotipi
D1
Meccanismi di
trasduzione
AC
PLC
D5
=
D2*
⊝ AC
↑ perm K+
↓ perm Ca2+
D3
?
D4
⊝ AC
AG
selettivi
AT
selettivi
Fenoldopam
Apomorfina
SCH-39930
=
=
Bromocriptina
=
Quinpirolo (>)
=
Sulpiride
Aloperidolo
=
=
Clozapina (>)
* 2 isoforme che originano per splicing alternaltivo di uno stesso gene e che
differiscono per la presenza (long isoform) o l’assenza (short isoform) di una
sequenza di 39aa corrispondenti alla terza regione intracellulare
Struttura dei recettori DAergici
Le porzioni TM presentano sequenze aa-cidiche altamente conservate
I segmenti citoplasmatici di D1-like e D2-like presentano una bassa omologia
(< 40%) => diversa capacità di interagire con proteine intracellulari (=>
meccanismi di trasduzione del segnale differenti)
DRIPs (DA receptor-interacting proteins): proteine del citoscheletro adattatrici
o del segnale che regolano la trasmissione DAergica mediante una
modulazione di biosintesi e localizzazione dei recettori, trasduzione del
segnale, internalizzazione dei recettori D1 e D2
Localizzazione dei recettori DAergici
Nel SNC:
D1: sottotipo più diffuso
D1-like
D5: ippocampo e talamo
D2-like
D2 (85-95% di tutti i D2-like): espressi in tutte le aree ad
innervazione DAergica
D3: aree limbiche (tubercolo olfattorio, SNc, ippocampo, NAc, VTA)
D4: cx, ippocampo, ipotalamo
I recettori D2 sono anche presenti nei gangli del SN simpatico dove mediano
l’inibizione del rilascio di NA e Adr