28 aprile 2003
prof. Romagnoli
Riprendiamo il discorso del tessuto muscolare. Avevamo lasciato da completare il discorso sul
tessuto muscolare striato scheletrico. Vi ricordate? Abbiamo visto queste fibre e le loro
caratteristiche microscopiche. Abbiamo visto l’apparato contrattile, le miofibrille. E abbiamo anche
visto come avviene l’interazione tra actina e miosina… come questa, consumando ATP, permette la
contrazione… come l’ATP sia anche il fattore di rilasciamento che permette poi il distacco fra
l’actina e la miosina alla fine di ogni ciclo di contrazione. Abbiamo visto il sistema che garantisce il
controllo della contrazione… quindi il reticolo endoplasmatico liscio, fonte endocellulare di calcio,
i tubuli trasversali che permettono che il segnale elettrico di membrana giunga a ridosso delle
cisterne terminali del reticolo endoplasmatico liscio, determinando l’apertura dei canali del calcio.
Avevamo anche fatto un rapido accenno ai sistemi che garantiscono in fondo l’approvvigionamento
energetico ai mitocondri, riserve di glicogeno per il metabolismo glicidico, e la presenza anche di
una proteina colorata, la mioglobina, che è distribuita dentro la sostanza (??) fondamentale e che
rappresenta una riserva di ossigeno. Vi ho già rammentato che esistono delle fibre rosse e delle fibre
bianche, anche a guardarle. Il tacchino è un buon esempio perché i muscoli dalla coscia sono rossi e
quelli delle ali sono bianchi. Vi ricordate? Vi ho detto che nella nostra muscolatura in realtà in ogni
muscolo fibre rosse e fibre bianche si mescolano. Quelle rosse, già così visibilmente più ricche di
mioglobina, si intuisce che sono meglio predisposte per un’ attività non necessariamente,
estremamente potente e rapida, ma protratta nel tempo, resistente alla fatica, capace di lavorare a
lungo in regime aerobico. Mentre le fibre bianche sono più ricche, in proporzione, di miofibrille che
non di sarcoplasma, e sono capaci di attività più intensa e breve ma più facilmente esauribile.
Tenete presente che poi ci sono ulteriori suddivisioni che si possono fare delle fibre muscolari: cioè
le fibre rosse e bianche possono ulteriormente venire suddivise in base alle caratteristiche della
miosina. Ci sono diverse isoforme di miosina: non è tutta uguale, quella che si trova nella fibra
muscolare striata… ci sono diverse isoforme, legate a prestazioni un po’ diverse. Sappiate che
esiste, volendo, una complicazione della classificazione delle fibre muscolari, che va al di là delle
fibre bianche e delle fibre rosse. Una volta saputo che questo problema è aperto, io credo non sia di
estremo interesse per voi andare troppo più a fondo.
L’impalcatura generale della fibra l’abbiamo esaminata.
Cosa rimane da vedere? Intanto, come finisce la fibra muscolare, e che cosa c’ha intorno la fibra
muscolare. Che cosa ha intorno ve lo potete facilmente aspettare: c’avrà una membrana basale!
Perchè essendo una struttura non connettiva ed essendo immersa, in fondo, in uno stroma
connettivale, è chiaro che intorno ad ogni singola fibra si organizza una membrana basale: è quella
1
che poi fa parte, è la parte prevalente del cosiddetto endomisio (vi ricordate? il connettivo stromale
che sta tra le singole fibre, e che in fondo consiste, di fatto, di queste membrane basali). Qui in
questo schemino vedete accennato la rete di fibre reticolari e la lamina basale che delimita queste
fibre muscolari. Tenete presente – io non mi ci dilungo, pure può darsi che troviate questo tema
sviluppato sui libri, ma in ogni caso ve ne riparleranno quando farete la patologia del tessuto
muscolare – che esistono tutte una serie di proteine che, attraverso la membrana, garantiscono
l’aggancio alla membrana basale. Noi abbiamo parlato di questo più a fondo a proposito dei tessuti
epiteliali: vi ho detto che delle proteine di membrana, nella loro parte extracellulare, vengono a
costituire la lamina rara che garantisce l’adesione, sia generica ( perchè tra glicoproteine c’è una
adesività) sia specifica ( perchè alcune delle molecole di membrana riconoscono esattamente
alcune delle molecole della lamina densa e garantiscono adesività). Questo succede anche nel
tessuto muscolare striato, e sappiamo anche che sulla faccia interna della membrana esistono delle
proteine che in qualche modo collegano il citoscheletro di queste fibre alla membrana e, attraverso
la membrana, alla membrana basale, che è all’esterno. Il citoscheletro… le miofibrille, certo, fanno
parte del citoscheletro, anche loro… ma le fibre muscolari striate hanno anche dei filamenti
intermedi, fatti da una particolare proteina che si chiama desmina, hanno un sistema anche
contrattile ubiquitario, quindi con filamenti sottili costituiti da quelle isoforme di actina che sono
tipiche di tutte le cellule e non solo caratteristiche del sistema muscolare. Ecco: componenti
citoscheletriche sono sotto studio sempre più attento, garantiscono la solidarietà tra l’interno della
fibra… Queste componenti citoscheletriche contribuiscono a garantire l’ordine delle miofibrille,
quella che è la regolare organizzazione del sarcomero. E il regolare allineamento delle miofibrille,
con tutte le linee Z tutte alla stessa altezza, tutti i dischi A tutti alla stessa altezza, e così via, è
garantito da componenti citoscheletriche che, agganciandosi alle linee Z, e poi collegando tra loro le
miofibrille, e poi andandosi ad agganciare alla membrana, garantiscono che tutte le varie miofibrille
stesse siano ognuna al loro posto alla giusta altezza. Perché vi sottolineo questo aspetto dell’ordine
interno garantito dal citoscheletro, e dell’aggancio tra questo e la membrana, e attraverso la
membrana plasmatica alla membrana basale? Vedrete: esistono delle patologie in cui sono alterate
alcune delle molecole, in particolar modo quelle che mediano l’aggancio tra il citoscheletro e la
membrana (oltre a queste, la membrana basale, meno frequentemente)… e il risultato è che tutte le
volte che la fibra si contrae, in qualche modo diventa un trauma per questa fibra, perché non riesce a
mantenere le sue parti ben coese tra loro. Possiamo fare un esempio abbastanza banale. Avete visto
che quando succedono gli incidenti di Formula 1, uno rimane stupito che gente che va a finire sul
bordo della pista a 200 km/h, non si fa niente! Perchè? Perchè rimane come ingessata dentro
l’abitacolo, e quindi fa corpo con l’abitacolo, non ha traumatismi nello sbatacchiare contro
l’abitacolo. Incidenti anche a velocità più bassa… Perché il problema della cintura di sicurezza?
2
Noi sappiamo, oggi, che sbattere la testa contro il vetro della macchina a 50 km/h può essere
mortale, per il percorso fatto e la botta repentina contro la parete dell’abitacolo. Nella stessa
maniera, di fatto succede che, se la fibra muscolare non riesce a garantire bene il collegamento tra
l’interno e l’esterno, tutte le volte che si contrae va incontro ad una sorta di traumatismo, che pian
piano la fa degenerare, e vedrete che ci sono delle malattie gravi, delle distrofie muscolari, che
comportano, alla lunga, un danno delle fibre muscolari che un po’ è riparabile, e insorgono grossi
problemi, fino anche a morti premature. Ecco, quindi, l’importanza di questa membrana basale, e
della solidarietà che si garantisce attraverso appropriate molecole - i nomi di queste molecole per
ora li lasciamo da parte, altri ve li spiegheranno, ma sappiate che ci sono, sono specifiche, quindi
sono oggetto di patologie da mutazione e così via, molto ben caratterizzate -, molecole tali che
garantiscono la solidarietà tra l’interno della fibra e l’esterno.
Arrivati alla fine della fibra, la fibra non finisce tronca, ma finisce con una serie come di
estroflessioni digitiformi, e al termine poi, le miofibrille, e precisamente sono i filamenti sottili (la
fine è sempre a livello di dove ci aspetteremmo una linea Z), i filamenti sottili vanno ad inserirsi
alla membrana cellulare: ci sono delle proteine di aggancio, come quelle che avevamo visto in tutte
le giunzioni (pensate alle giunzioni intermedie, o fasce aderenti, delle cellule epiteliali, in cui vi
sono filamenti sottili del citoscheletro ubiquitario, mentre qui sono filamenti sottili delle
miofibrille), che ugualmente vanno a finire a ridosso della membrana plasmatica, e poi c’è una
placca di adesione, ci sono delle proteine intermedie che agganciano poi alla membrana plasmatica,
e questa a sua volta fino alla membrana basale che circonda la struttura (?).
Le fibre reticolari che formano la parte reticolare della membrana basale… Qualcuno lo chiama
sarcolemma, la membrana basale della fibra muscolare. A me non piace perché il termine
sarcolemma, nel corso delle generazioni di studiosi, ha assunto significati diversi. C’è stato un
periodo in cui sarcolemma era tutto ciò che si otteneva sbucciando la fibra muscolare: sappiamo che
questo corrisponde alla membrana plasmatica + la membrana basale. Poi c’è stato un periodo in cui
il termine sarcolemma era usato per indicare il plasmalemma della fibra muscolare. Poi qualcuno
usa il termine sarcolemma per la membrana basale della fibra muscolare. Secondo me, quando un
termine si usa troppo, come in questo caso, finisce che non si capisce più cosa si sta indicando. Il
termine endomisio, invece, può essere appropriato, perché, di fatto, anche se i due termini nascono
attraverso percorsi culturali diversi, però, di fatto, l’endomisio corrisponde alla membrana basale.
Allora, vi dicevo… La componente reticolare di questa struttura si continua poi con le fibre
collagene del tendine (?), che dall’estremità delle fibre muscolari, prosegue per andare a trasferire
fine al punto di applicazione della forza, la forza sviluppata dal muscolo. Quindi, di fatto… Tenete
presente che non è solo all’estremità: certo ci deve essere un buon aggancio, sì! Se no, cosa
succede? Succede che se il piede non sta attaccato per bene alla calza, quando io tiro su la gamba la
3
calza mi rimane giù a sbrendoloni. È chiaro che ci deve essere un sistema che garantisce che quando
la fibra si accorcia tutto il connettivo con cui è agganciata si accorcia con lei. Ma l’aggancio non è
mediato solo all’estremità della fibra: tutta l’adesione che si crea tra questa sottile membrana basale
(ma estesa in superficie) e la superficie della fibra è importante per garantire poi il trasferimento
della forza alle componenti connettivali del tendine. Ecco perchè succede che, se qualcosa va storto
nell’aggancio tra fibra e membrana basale, poi praticamente tutti i movimenti del muscolo
diventano un traumatismo per la fibra stessa, perchè non è più solidale con questa specie di rete, che
garantisce il trasferimento della azione muscolare. Ripeto: la fine è interdigitata. Abbiamo già detto
che la interdigitazione, in questo caso, è un sistema che garantisce al meglio la adesione, proprio tra
la fine della fibra e la componente connettivale che deve proseguire il lavoro della fibra stessa.
Vi faccio vedere un po’ di immagini proprio per sottolineare qualche altra caratteristica delle fibre
muscolari.
Immagini:
Questo è un esempio di una fibra ricca di mitocondri, non soltanto abbondanti sotto la
membrana plasmatica, ma abbondanti anche in colonne tra le miofibrille (i mitocondri delle
fibre muscolari sono trai più grossi che abbiamo, e particolarmente ricchi di creste laminari).
Vedete le miofibrille, vedete i nuclei disposti alla periferia, vedete i vasi che stanno tra le
fibre. E sempre c’è questa membrana basale, e questi sono indicati, gli orifici dei tubuli (il
sistema dei tubuli longitudinali, il reticolo endoplasmatico liscio, le cisterne terminali). A
ogni livello del tubulo T, si crea un sistema in cui al centro c’è un tubulo T e ai lati due
cisterne terminali: è la così detta triade: ci sono tre elementi che si ripetono.
Rappresenta una fibra più povera di mitocondri, quindi sarà una fibra bianca. Vedete i
mitocondri più piccoli, più radi; in proporzione, più territorio occupato da miofibrille,
grosse; meno mitocondri sia in superficie, sia dentro. L’organizzazione del reticolo
endoplasmatico è sempre la solita. Qui per ricordare che vicino ai nuclei c’è un piccolo
apparato del Golgi; ci saranno anche delle cisternine di reticolo endoplasmatico, ma proprio
poca cosa, perchè una volta che la fibra è arrivata alle sue dimensioni, l’attività di rinnovo,
della struttura stessa, della membrana e così via, avviene, ama avviene ad un ritmo
abbastanza basso. Ricordatevi che le miofibrille non hanno bisogno di reticolo
endoplasmatico ruvido, perché sono proteine e strutture che rimangono nello ialoplasma, e
quindi sono fatte dai ribosomi non legati a membrana. Questo schemino vi fa vedere anche
che a ridosso delle fibre muscolari (qui ve lo fa vedere in una fibra bianca, ma lo stesso
discorso vale anche per le fibre rosse), ci sono delle cellule che occupano una posizione
particolare: sono isolate, sono a contatto con le fibre muscolari, racchiuse dentro la
4
membrana basale (la membrana basale è questa qui, vedete, l’ha come scollata, la lamina e
le fibre reticolari, avvolte anche queste cellule (?). Queste cellule si chiamano cellule
satelliti, precisamente cellule satelliti muscolari (perchè vedrete che esistono anche cellule
satelliti nel tessuto nervoso), cellule satelliti muscolari. Qual è il loro significato? Sono delle
cellule progenitrici del muscolo. Facciamo una parentesi su come si formano le fibre
muscolari. Le fibre muscolari striate, sono dei sincizi, quindi si formano da una serie di
cellule (si chiamano mioblasti) che si costituiscono durante lo sviluppo embrionale, e poi si
saldano tra loro, quindi le membrane vengono a contatto, c’è una riorganizzazione delle
molecole di membrana, e le due cellule si fondono insieme, e poi altre cellule si aggiungono,
si formano dei così detti miotubi, dentro i quali si cominciano a differenziare le miofibrille e
diventano fibre muscolare.
Le cellule satelliti, sono delle cellule come i mioblasti, che rimangono lì tranquille; sono
capaci di dividersi e servono a garantire l’accrescimento delle fibre muscolari; quando siamo
bimbi abbiamo muscoli più corti, e anche le nostre fibre muscolari sono più corte; quando
cresciamo non aumentano le fibre muscolari, tranne nei primissimi anni di vita, ma
aumentano di dimensione. Questo aumento è garantito anche dall’aumento di nuclei, perchè
voi capite che ogni tot di citoplasma ci vuole un nucleo a presiedere alle sintesi proteiche e a
quanto serve in quella zona: quindi se la fibra diventa più lunga, devono anche aumentare i
nuclei, perchè se no sarebbero troppo diradati e confarebbero bene il loro lavoro; questo si
ottiene attraverso l’incorporazione di cellule satellite dentro la compagine delle fibre
muscolari.
Queste cellule satelliti servono anche per garantire la rigenerazione di fibre muscolari che
siano state, in parte, danneggiate. Sembra che queste cellule satelliti non abbiano le
caratteristiche di cellule staminali (cioè di cellule capaci di riproduzione indefinita e di
rigenerazione totale del tessuto); sono piuttosto delle cellule del compartimento di
espansione, quindi sono capaci di espandersi ma un numero limitato di volte: ecco perchè in
quelle patologie che io vi accennavo, in cui la fibra viene danneggiata per scollamenti
continui rispetto alla membrana basale, per un po’ di anni le cellule satelliti ce la fanno a
rigenerare quello che viene danneggiato, e quindi il paziente sta abbastanza bene, ma dopo
un certo periodo la capacità rigenerativa viene superata e il soggetto arriva a stare male.
Quindi la capacità rigenerativa delle cellule satelliti, non è tale da poter garantire
indefinitamente nel tempo la rigenerazione del tessuto, ma solo una capacità di
rigenerazione limitata.
Proseguendo negli schemini, vediamo quello che succede quando una fibra muscolare è
danneggiata: ci sono due possibilità:
5
1. La fibra si difende: questa zona qui viene come annullata via dalla fibra; la
membrana plasmatica si richiude a questo livello; questa zona alterata verrà portata
via dai macrofagi. Dopodiché, ecco che alle estremità ci può essere una certa attività
di riproduzione dei nuclei, che si riallungano guidati, sembra, dalla membrana
basale, e le due estremità della fibra si vengono incontro e fanno quello che sanno
fare le cellule della famiglia del muscolo: si fondono tra loro (è una attività che
sanno fare dal periodo embrionale), e quindi si ricostituiscono. All’inizio i nuclei
sono in posizione centrale, e poi rigenerate le miofibrille e i nuclei si spostano.
2. L’altra possibilità è che questa rigenerazione (non sono antitetiche, possono avvenire
anche tutte e due a seconda dell’entità del danno), ecco che invece, sempre
l’amputazione, sempre l’intervento dei macrofagi e l’attività proliferativa (nella
possibilità di rigenerazione che abbiamo visto prima, non si capisce se questi nuclei
aumentano di numero o si limitano a spostarsi: se il danno è piccolo, probabilmente
sono sempre i soliti che si spostano); qui invece devono aumentare di numero: ecco
che prima si dividono le cellule satelliti, e si dispongono, sempre accolte dentro la
membrana basale che fa da guida per questo processo (se la membrana basale si
interrompe, probabilmente ognuno di questi due monconi si chiude in se stesso e nel
mezzo rimane una cicatrice o un piccolo tendine intermedio; bisogna che sia
mantenuta l’integrità della membrana basale per guidare la rigenerazione delle
cellule che vanno a rioccupare questo spazio), poi si fondono tra loro (ripeto, questa
è una operazione che sano fare; che sanno fare, vuol dire che hanno le molecole di
membrana per riconoscersi e per attivare il processo di fusione), poi loro
ricominciano a dirigere la sintesi di molecole dei miofilamenti, che si organizzano in
filamenti, poi in miofibrille, i nuclei si spostano (non capisco dove!), e la fibra si
rigenera.
Ecco quindi che il tessuto muscolare striato ha la capacità riparativa garantita:
-
per piccoli traumi: dalla capacità di spostarsi dei nuclei, e di diffondersi;
-
per gravi lesioni: dalla capacità di proliferare,
di piazzarsi nella sede
adeguata, di fondersi e rigenerare nuovi tratti di tessuto, da parte delle cellule
satellite. In fondo il lavoro che sanno are durante l’accrescimento, lo
proseguono a saper fare durante la riparazione.
Miofibrille. Richiamo l’attenzione su queste strutture: una piccola formazione cava,
circondata da altre due un po’ più grosse → ecco una triade. Vi accennavo dianzi a questi
dispositivi dove il tubulo T (ecco il tubulo T preso di traverso), viene portato sui due lati
6
dalle cisterne terminali dei due tratti del tubulo longitudinale, e forma una tripletta di
strutture che prende il nome di triade.
Questo per farvi vedere in sezione la membrana basale; vedete come sono messe vicine tra
loro le fibre muscolari? Questo è l’endomisio; praticamente giusto giusto una lamina basale,
che si vede questo feltro grigio; nel mezzo queste strutture che sono le due lamine reticolari,
fuse insieme (influiscono poco nello spessore). Qui vedete il nucleo, intorno al nucleo una
gocciolina lipidica, un corpo multivescicolare, un endosoma, un piccolissimo apparato del
Golgi.
Con questo il discorso sul tessuto muscolare striato scheletrico è concluso. Passiamo ad esaminare il
tessuto cardiaco.
TESSUTO CARDIACO
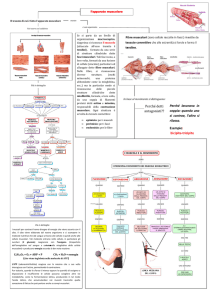
Ci sono diversi modi per raccontare il tessuto muscolare cardiaco.
Il tessuto muscolare cardiaco è fatto di fibre, così come quello scheletrico: entità molto lunghe,
cilindriche, prolungate nello spazio; ci sono dentro le miofibrille e le miofibrille sono
morfologicamente uguali a quelle del muscolare scheletrico; chimicamente no, per es. anche la
troponina, quella molecola regolativi che serve a legare il calcio, ha almeno una subunità, la
subunità I, che è diversa tra il muscolo cardiaco e lo scheletrico. Dice: che ce ne importa? Ce ne
importa perchè oggi come oggi il criterio più sicuro e veloce per la diagnosi di infarto è proprio il
dosaggio in circolo della troponina I cardiaca, che si riesce a riconoscere con appositi anticorpi
rispetto a quella scheletrica, per capire se davvero è morto del tessuto, e quindi delle molecole che
erano dentro sono passate fuori e poi sono andate in circolo. Quindi le differenze molecolari trai tipi
di tessuto, non solo sono interessanti per capire la fisiologia e per capire la fisiologia del tessuto, ma
hanno già, molte di queste, applicazioni pratiche.
Dunque esistono delle differenze molecolari, ma morfologicamente le miofibrille del cuore sono
uguali alle miofibrille dei muscoli scheletrici.
Dov’è il punto fondamentale di differenza? Mentre le fibre muscolari scheletriche sono degli ampi
sincizi strutturati, anatomici, quindi sono delle colonne, ognuna separata dall’altra e ogni colonna è
una massa intera con tanti nuclei (come le colonne nelle chiese romane, che vanno dalla base al
soffitto, un capitello; attraversano tutto lo spazio della chiesa); le fibre del cuore invece, sono fatte
da tante cellule, miocardiociti, ciascuna chiusa in se stessa con la sua membrana, ciascuna con il suo
nucleo, messe in colonna l’una sull’altra. Se voi guardate i templi greci, le colonne sono fatte da
tanti rocchi, messi uno sopra all’altro, a formare una colonna; così sono fatte le fibre del cuore.
7
Quindi voi potete partire dall’idea che esistono delle fibre cardiache, ma che queste fibre sono fatte
da tante cellule separate messe in colonna l’una dietro l’altra; viceversa potete partire a “raccontare”
il cuore, dicendo che il cuore è fatto di cellule che però si organizzano l’una dietro l’altra a formare
colonne. Qual’è una prima conseguenza strutturale importante? Adesso dimentichiamoci le colonne
del tempio greco, dove i rocchi sono sempre dei cilindri: qui queste cellule non necessariamente
sono fatte a cilindro: possono essere fatte a Y, possono essere fatte a X. Quale sarà la conseguenza?
Che una cellula può biforcarsi e a ogni sua estremità, continuarsi con un’altra cellula, e questa a sua
volta può essere biforcata, e a volte anche con più forcazioni, e continuarsi con un’altra e con
un’altra. Qual è il risultato? Che le fibre del cuore si collegano, si anastomizzano. Anastomizzarsi
vuol dire di per sé, congiungersi bocca a bocca (lo stoma e la bocca). Il termine si utilizza in prima
battuta per gli organi cavi (l’intestino viene anastomizzato ad un altro), ma si può usare anche per
strutture di questo tipo per indicare che le fibre si collegano l’una all’altra, attraverso proprio la
forma consentita da queste cellule; il risultato è che le fibre del cuore non stanno belline una
accanto all’altra, ma formano un intreccio, si usa il termine plesso. Il miocardio (il tessuto
muscolare cardiaco) ha una struttura plessiforme.
Abbiamo tante cellule: come fanno a mettersi d’accordo? Non può mica una cellula contrarsi, e
l’altra non contrarsi! Bisognerò che si mettano d’accordo per contrarsi insieme durante la sistole
cardiaca. Ecco che allora nascono due problemi:
a. come fare a far si che le cellule rimangano attaccate, e che quindi le fibre non si disgreghino in
tante unità quando le cellule si contraggono. Come fareste voi a garantire che quando io muovo la
macchina si muova anche il carrello che ho dietro: ci metto un gancio di traino attaccato al telaio. E
così fanno le nostre cellule cardiache: là dove giungono a contatto, mettono in membrana una serie
di molecole che garantiscono una giunzione tra le due strutture. È una giunzione particolare che ha
certe caratteristiche della giunzione intermedia, perchè qui vanno a finire miofibrille e quindi si
inseriscono in particolar modo i filamenti sottili, e certe caratteristiche del desmosoma, perchè
anche dentro il miocardio ci sono filamenti intermedi, e anche i filamenti intermedi vanno a finire a
questo livello e vanno e si inseriscono alla membrana: ci sono dei tratti dove si inseriscono alla
membrana i filamenti sottili, dei tratti dove si inseriscono, con quel gioco a forcina, i filamenti
intermedi; ci sono delle giunzioni aderenti complicate, che garantiscono la solidità meccanica. Ma
se voi avete la roulotte non dovete soltanto garantire che la roulotte si trascina, ma anche che se voi
accendete le luci davanti, si accendano anche quelle di dietro. Ecco quindi il problema del
collegamento elettrico. Ma come mai dà tanta importanza al collegamento elettrico? Dopo tutto non
è una roulotte! Già, ma abbiamo visto che nel tessuto muscolare il segnale che dà l’innesco
all’attività contrattile, è un segnale elettrico, più precisamente una variazione del potenziale di
membrana, che si propaga lungo la superficie cellulare. Ecco che allora a livello di queste superfici
8
di contatto ci sono anche delle giunzioni comunicanti, delle giunzioni gap, che garantiscono che un
segnale elettrico di una cellula, si propaghi alla cellula accanto e poi alla cellula accanto, poi alla
cellula accanto, e così per tutto il percorso. Queste zone in cui finiscono le cellule cardiache, non
sono tagliate proprio di piatto, sono tagliate a zig zag.
9