Respirazione cellulare
Metabolismo dei glucidi
Metabolismo
E’ l’insieme delle reazioni chimiche che avvengono in una
cellula o, più in generale, in qualsiasi organismo.
Le sostanze coinvolte in tali reazioni sono dette
Sintetizzati dagli organismi
Macromolecole organiche:
zuccheri, lipidi, proteine …
metaboliti
Derivati dall’ambiente
Nutrienti, acqua, anidride
carbonica, ossigeno …
Metabolismo
E possibile individuare due gruppi fondamentali di
reazioni chimiche:
Anabolismo
Catabolismo:
fase costruttiva
fase di degradazione
consumo di energia
liberazione energia
Reazioni chimiche
endoergoniche
Reazioni chimiche
esoergoniche
3
Metabolismo = anabolismo + catabolismo
Le diverse vie metaboliche non si svolgono in modo indipendente: spesso
sono collegate in cicli di utilizzo e riclico di sostanze
Proteine,
polisaccaridi,
lipidi…
Zuccheri,
amminoacidi,
acidi grassi…
demolizione
Molecole
organiche di
piccole
dimensioni
Macromolecole
sintesi
+
Metabolismo e energia
•
Gli organismi sono in grado di utilizzare soltanto due tipi di energia :
En. Luminosa
En. Chimica
Autotrofi
Eterotrofi
Fotosintesi
Respirazione cell.
Metabolismo e energia
Reazioni chimiche
endoergoniche
E. prodotti
E. assorbita
E. reagenti
Il contenuto
energetico dei
reagenti è minore di
quello dei prodotti
Reazioni chimiche
esoergoniche
E. reagenti
E. liberata
E. prodotti
Il contenuto
energetico dei
reagenti è maggiore di
quello dei prodotti
l'ATP, il trasportatore universale di energia
• In tutti i viventi esiste una
molecola, chiamata adenosin
trifosfato (ATP) che ha il
compito di assorbire l'energia
prodotta dalle reazioni
esorgoniche di demolizione e
di renderla disponibile per i
lavori cellulari.
base azotata adenina
tre gruppi fosfato
I legami presenti tra questi gruppi fosfato
racchiudono l'energia utilizzabile dalla
cellula.
zucchero a cinque
atomi di carbonio
L’ATP: una molecola “Ricaricabile”
L’ATP: una molecola “Ricaricabile”
L’ATP immagazzina energia chimica nel legame fra due dei
suoi gruppi fosfato.
ADP
ATP
Energia
P
P
adenina
P
Legami ad alta
energia
Quando il legame si rompe,
con una reazione di idrolisi,
l’energia chimica si rende
disponibile per altri processi
biologici.
Ribosio
Le cellule respirano?
• La respirazione cellulare è il
meccanismo che permette alla cellula, in
presenza di ossigeno,di ricavare energia
utilizzabile nei processi vitali dai legami
chimici delle molecole assorbite nella
digestione.
• La respirazione cellulare consta di
diverse reazioni, in cui i prodotti di un
passaggio sono utilizzati come reagenti
per il processo successivo.
• I prodotti di scarto della respirazione
cellulare (come CO2 o H2O) vengono
eliminati dalla cellula e, negli organismi
superiori, escreti attraverso la
respirazione polmonare e le urine.
10
Equazione generale della respirazione cellulare
C6H12O6 + 6O2 à 6CO2 + 6H2O + 36 ATP
Glucosio
Ossigeno
Acqua
Anidride
Carbonica
Respirazione Cellulare: le fasi
Catena di trasporto
degli elettroni
Glicolisi
Ciclo di Krebs
Dove avviene la
respirazione
cellulare ?
13
Fasi della respirazione cellulare
1. Glicolisi: catabolica, degrada sost. organiche
avviene nel citoplasma
2. Ciclo di Krebs: catabolica, completa la
degradazione di sost. org., avviene nella matrice
mitocondriale
3. Catena di trasporto di elettroni e fosforilazione
ossidativa: trasferimento di elettroni dal NADH ,
con formazione finale di acqua e ATP. La
fosforilazione ossidativa avviene sulle creste
mitocondriali, produce il 90% dell’ATP cellulare.
Respirazione cellulare
In alcuni tessuti ed in alcuni tipi di cellule, eritrociti,
midollare del rene, cervello, spermatozoi e cellule
della retina, la demolizione del glucosio attraverso
la glicolisi è la sola o la principale fonte di energia
metabolica
120 grammi di glucosio / giorno = 480 Kilocalorie
C
A
T
A
B
O
L
I
S
M
O
A
N
A
B
O
L
I
S
M
O
Trasporto del glucosio: trasporto mediato
(tramite proteine chiamate GLUT)
Passivo (secondo gradiente)
GLUT
Il glucosio6P non può attraversare la membrana in
quanto non possiede un trasportatore specifico
TRASPORTATORI DI GLUCIDI: bidirezionali
Nome
Tessuto
GLUT 1
Eritrociti, molti tessuti
GLUT 2
Fegato, cellule β del pancreas,
intestino tenue, rene
GLUT 3
Cervello, molti tessuti
GLUT 4
Muscolo scheletrico e cardiaco,
tessuto adiposo
GLUT 5
Intestino tenue
SGLT1
Trasporto attivo
secondario
(unidirezionale)
Intestino tenue, rene
Kt
1-2 mM
15-20 mM
Funzione
Captazione basale del
glucosio
Captazione e rilascio del
glucosio nel fegato
(galattosio e fruttosio) e
nel rene; sensore per il
glucosio delle cellule β
del pancreas
1 mM
Captazione basale del
glucosio
5 mM
Captazione del
glucosio stimolata da
insulina
-
-
Trasporto del fruttosio
Assorbimento del
glucosio e del galattosio
alimentare dall’intestino
tenue; riassorbimento
del glucosio filtrato nel
rene
Trasporto facilitato
passivo del glucosio
attraverso una
membrana cellulare
GLUT4: trasportatore di glucosio insulina-dipendente
presente nel tessuto muscolare scheletrico e cardiaco e
nel tessuto adiposo
L’insulina induce
l’esocitosi dei
trasportatori di
glucosio nei
tessuti con
trasporto
Insulinadipendente
andando ad
incrementare la
capacità delle
cellule di
trasportare
glucosio
Glicolisi
C6H12O6
Glucosio
Questa prima fase avviene nel
citoplasma di tutte le cellule,
procariote od eucariote:
una molecola di glucosio, a sei
atomi di carbonio viene
trasformata, tramite 9
reazioni, in due molecole di
acido piruvico a tre atomi di
carbonio.
2 ADP + 2 Pi
Glicolisi
2 ATP
Queste reazioni sono
accompagnate da una
liberazione di energia (2 ATP).
E una fase anaerobica, non
richiede ossigeno
2 Ac. piruvico
C3H4O3
La Glicolisi
Stadio 1
Stadio 2
Stadio 3
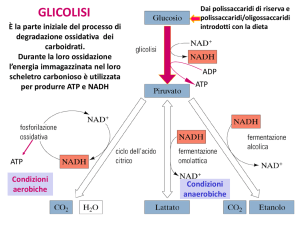
GLICOLISI:
•
•
•
Glucosio--à 2 piruvato + 2 ATP + 2 NADH
avviene nel citosol di tutte le cellule
è costituita da 10 tappe
può essere suddivisa in due fasi
• Investimento energetico
• Produzione energetica
LE TAPPE DELLA GLICOLISI
STEP 1: Fosforilazione del glucosio
ΔG < 0
ESOCHINASI
ΔG’°= -16,7 KJ/mol
STEP 2: Isomerizzazione del glucosio6P in fruttosio6P
E’ una reazione di
isomerizzazione
reversibile
Fosfoglucosio
isomerasi
ΔG’°= 1,7 KJ/mol
STEP 3: Fosforilazione del fruttosio-6-P
ΔGo’ = -14,2 kJ/mol
Reazione irreversibile
Fosfofruttochinasi 1
STEP 4: Demolizione dell’esoso in triosi
Chetoso
ΔGo’ = -23,9 kJ/mol
Aldoso
STEP 5: Isomerizzazione dei triosofosfati
Diidrossiacetone fosfato e gliceraldeide 3 fosfato sono
interconvertibili, in una reazione di isomerizzazione
(chetoso)
96%
(aldoso)
4%
Da 1 molecola di fruttoso1,6 bifosfato, mediante reazioni sequenziali di
Aldolasi e triso fosfato isomerasi, si ottengono 2molecole di G3P
STEP 6: ossidazione della gliceraldeide 3 fosfato
Ossidazione (deidrogenazione) seguita da fosforolisi
ΔGo’ = +6,3 kJ/mol
Legame ad alta energia
tra l’acido fosforico e il
gruppo carbossilico legame
da anidride mista
Acil fosfato
La reazione si dice accoppiata in quanto l’energia
derivante dall’ossidazione dell’aldeide viene
utilizzata per la formazione del leg.fosfo-anidridico
STEP 7: 1° Fosforilazione dell’ADP
Sebbene l’equilibrio sia
termodinamicamente
spostato verso dx, la
reazione è tuttavia
reversibile consentendo la
generazione di ATP nel
processo glicolitico:
tuttavia quando viene
richiesta la sintesi del
glucoso (gluconeogenesi)ha
luogo la formazione del
1-3BPG a spese di ATP
ΔGo’ = -18,9 kJ/mol
Fosforilazione a livello del substrato
1° Reazione di fosforilazione a livello di substrato:
consiste nel trasferimento di un gruppo fosfato da un composto ad
elevato contenuto energetico all’ADP con formazione di ATP
STEP 8: Trasferimento intramolecolare del
radicale fosforico
FOSFOGLICERATO
MUTASI
Scambio reversibile di un
gruppo fosfato tra
il C-2 e il C-3 del
glicerato
Mg++
Mutasi: enzimi che catalizzano il trasferimento di un raggruppamento da una
parte all’altra della molecola che conserva la propria identità
Isomerasi:catalizzano una modificazione di identità del substrato.
STEP 9:Formazione del fosfoenolpiruvato (PEP)
composto ad alta energia
ΔGo’ = 1,8 kJ/mol
STEP 10: 2° Fosforilazione dell’ADP
Piruvico Chinasi
Forma
Enolica
La seconda fosforilazione
dell’ADP a livello del substrato
Forma
chetonica
Consumo
2 ATP
Zucchero 6 C
Si divide in 2x3 C
Produzione
di 4 ATP
La velocità della GLICOLISI è regolato dalle seguenti condizioni:
• disponibilità di GLUCOSIO nella cellula
• attività delle tre tappe irreversibili catalizzate dalla esochinasi
(I tappa), fosfofruttochinasi (III tappa) e della piruvato chinasi
(X tappa)
• disponibilità di ADP e NAD+
Bilancio energetico della GLICOLISI:
Glucosio
FRU6P
1,3BPG
PEP
GLU6P
F1,6BP
3PG
PIR
- 1ATP
- 1ATP
+ 1ATP (x2)
+ 1ATP (x2)
netto 2ATP
GLICOLISI ANAEROBIA
1 Glucosio
2 Ac. Piruvico (ΔG’° = -146 kJ/mole)
GLICOLISI AEROBIA
1 Glucosio
CO2 + H2O
(ΔG’° = -2840 kJ/mole)
La conversione del glucosio
in due molecole di piruvato
ha avuto come risultato la
sintesi netta di 2 molecole
di ATP e 2 di NADH
Dato che la
concentrazione di NAD+
nella maggior parte delle
cellule è bassa,
affinché la glicolisi possa
procedere il NADH
prodotto deve essere
riossidato a NAD+
Regolazione
della via
glicolitica
Esochinasi
Fosfofruttochinasi
+
Insulina
F2,6BP
Glucagone
Piruvato Chinasi
-
Alanina, Acetil CoA, acidi grassi
Esochinasi e glucochinasi
L’ esochinasi è presente in tutte le cellule
La glucochinasi è presente nel fegato
Isozimi: enzimi diversi che
catalizzano la stessa reazione
ESOCHINASI :
• Cinetica iperbolica
• adattamento indotto
• non specifico per il glucosio (fosforila
anche il fruttosio e il mannosio)
• Km = 10-100 µM
• lavora normalmente (in vivo) alla
velocità massima
• inibita allostericamente dal prodotto
G6P
• inibitore irreversibile: 2-desossiglucosio
GLUCOCHINASI (epatociti, cellule β del
pancreas) :
• Cinetica sigmoide (da glucosio)
• specifico per il glucosio
• Km ≅ 10 mM
• enzima inducibile (indotto da insulina)
• non inibito da prodotto
• inibito da FRU6P ed attivato da FRU1P,
intermedio del metabolismo del FRU,
tramite una proteina inibitrice
L‘esochinasi
• L’esochinasi catalizza la fosforilazione del glucosio nella
maggior parte dei tessuti
• Ha un’ampia specificità per il substrato (fosforila anche
altri esosi)
• è inibita dal prodotto della reazione (glucosio 6-fosfato)
• ha una Km bassa per il glucosio (e quindi un’affinità alta)
• ha una Vmax bassa, per cui non possono essere fosforilati più
zuccheri di quanti la cellula non ne possa utilizzare
La glucochinasi
• E’ il principale enzima responsabile della fosforilazione del
glucosio nel fegato e nelle cellule delle isole pancreatiche.
• Nel fegato facilita la fosforilazione del glucosio durante
l’iperglicemia.
• Differisce dalla esochinasi perché:
1) ha una Km >> esochinasi (cioè richiede una
[ glucosio] più elevata per raggiungere 1/2 Vmax) perciò
funziona soltanto quando la [glucosio] negli epatociti è alta
(es. dopo un pasto ricco di carboidrati)
2) ha una Vmax elevata (permette al fegato di eliminare con
efficienza dal sangue portale il glucosio, anche dopo un pasto
ricco di carboidrati, minimizzando l’iperglicemia durante il
periodo dell’assorbimento)
La glucochinasi
(fegato) è
caratterizzata da
un’affinità per il
glucosio molto più
bassa (Km= 10mM) di
quella dell’esochinasi
(Km= 0.010 mM) e non è
soggetta all’inibizione
allosterica da parte del
glucosio 6-fosfato
Destini
alternativi
degli
intermedi
glicolitici nelle
vie
biosintetiche
Vie di
utilizzazione di
substrati diversi
dal glucosio nella
Via Glicolitica
muscolo
fegato
Glicolisi e
metabolismo
ossidativo
Destino del
NADH
glicolitico e
del Piruvato
mitocondrio
citosol
mitocondrio
In anaerobiosi, il
NADH è ri-ossidato
ed il Piruvato
ridotto a lattato nel
citosol dalla lattico
deidrogenasi (LDH)
nel processo di
fermentazione
lattica
Trasporto del piruvato dal citosol
nella matrice mitocondriale
Citosol m.m.e
Matrice
m.m.i.
H+
H+ H+
H+
H+
H+
H+
H+
H+
H+
H+
piruvato
H+
H+
H+
In condizioni di normale apporto di O2 il piruvato entra
nei mitocondri
attraverso un trasportatore di membrana specifico e
viene trasformato
in AcetilCoA
dal complesso enzimatico della
PIRUVATO DEIDROGENASI mitocondriale
La decarbossilazione ossidativa del piruvato è catalizzata
dalla piruvato deidrogenasi
Il complesso della PDH comprende tre enzimi che partecipano alla
conversione del piruvato in acetil coenzima A
Enzima
Coenzima
Vitamina richiesta
Piruvato
decarbossilasi (E1)
Tiamina pirofosfato
(TPP)
Tiamina (vitamina B1)
Diidrolipoil
transacetilasi(E2)
Acido lipoico
Diidrolipoil
deidrogenasi (E3)
PDH-Chinasi
PDH-Fosfatasi
CoA
Acido Pantotenico
(vitamina B5)
FAD
Riboflavina (vitamina B2)
NAD+
Niacina
Ciclo di Krebs
AcetilCoA + 3NAD+ + FAD + GDP + Pi + 2H2O →
2 CO2 + 3 NADH + 3 H+ + FADH2 + GTP + CoA
Ciclo Krebs
Equazione generale:
AcetilCoA + 3NAD+ + FAD + GDP + Pi + 2H2O →
2 CO2 + 3 NADH + 3H+ + FADH2 + GTP + CoA
• L’acetilCoA viene ossidato completamente a 2 molecole di CO2
• 3 molecole di NAD+ e 1 di FAD vengono ridotte, legando gli atomi di H
provenienti dall‘acetilCoA e da 2 molecole di H2O (8 H)
• Una molecola di GTP si forma a partire da GDP e Pi (reazione di
fosforilazione a livello di substrato). Equivale alla formazione di un ATP
secondo la reazione di interconversione dei nucleotidi:
GTP + ADP ↔ GDP + ATP
7.5
1.5
10
30 32
Tre fattori governano la velocità
del ciclo di Krebs:
• disponibilità di unità acetiliche, di
ossalacetato e di coenzimi ossidati
*
• inibizione da accumulo di prodotti
(NADH e ATP)
• inibizione allosterica a feedback
dei primi enzimi del ciclo da parte
degli ultimi intermedi
(diminuisce la KM per
l’isocitrato di 10 volte)
, ATP
(in alcuni tessuti)
Inibizione
Attivazione
REGOLAZIONE DEL
CICLO DI KREBS
Funzioni cataboliche:
ossidare completamente acetil CoA
produrre coenzimi ridotti dalla cui riossidazione
ottenere energia
Funzioni anaboliche:
produrre intermedi per sintesi di molecole
biologiche
CICLO ANFIBOLICO
Ruolo ‘ANABOLICO’ del ciclo di Krebs
La fosforilazione ossidativa ha inizio con
l’ingresso degli elettroni nella catena
respiratoria
Elettroni raccolti dalle deidrogenasi nei processi
catabolici e trasferiti sulle molecole
coenzimatiche (NAD+ e FAD)
La catena respiratoria mitocondriale
NADH
NAD+
in
Membrana
mitocondriale
interna
Complesso I
NADH DH
out
Q10
Complesso III
cit.c reduttasi
Complesso IV
cit.c ossidasi
Cit.c
DEIDROGENASI
Subunità
DNAn
DNAm
Totale
1/2 O2+2H+
Complesso II
Succinico DH
38
7
45
CATENA CITOCROMICA
4
4
10
1
11
10
3
13
H2O
Complessi della catena respiratoria
• L’ordine degli elementi della catena respiratoria è:
complesso I (o complesso II) - CoQ - complesso III citocromo c - complesso IV
• Durante il trasporto degli e-, i 3 complessi I, III e IV
utilizzano l’ energia che si libera dal trasporto degli estessi per trasferire protoni (H+, presenti liberi nella
matrice mitocondriale) dalla matrice allo spazio
intermembrana del mitocondrio.
Agiscono quindi da pompe protoniche
I complessi I, III e IV della catena respiratoria
mitocondriale accoppiano al trasferimento di elettroni una
traslocazione protonica dalla matrice verso lo spazio
intermembrana, formando un gradiente elettrochimico
transmembrana perché la membrana mitocondriale interna
è praticamente impermeabile ai protoni
L’ipotesi chemiosmotica di Mitchell
L’ATPasi (complesso V) utilizza il gradiente protonico in
direzione opposta per sintetizzare ATP nel processo noto
come fosforilazione ossidativa.
REGOLAZIONE
• Catena respiratoria, fosforilazione ossidativa
sono strettamente interdipendenti: se si blocca l’
una si blocca anche l’ altra
• Sono controllate dalla disponibilità dei propri
substrati, cioè:
- coenzimi ridotti NADH e FADH2 (ciclo di Krebs)
- O2
- ADP e Pi
La catena di trasporto mitocondriale degli elettroni (catena respiratoria) catalizza il trasferimento degli
elettroni dal NADH e dal FADH2 sull' ossigeno molecolare
secondo le reazioni globali:
NADH+H++ 1/2 O2----> NAD++H2O ΔG°’ ≃ - 220 kJ/mol : 2,5 ATP
FADH2+ 1/2 O2----> FAD+H2O ΔG°’ ≃ - 160 kJ/mol : 1,5 ATP
• In aerobiosi, il NADH è ri-ossidato a livelli della
catena respiratoria formando ATP nella fosforilazione
ossidativa ed il Piruvato è ossidato ad CO2 ed H2O nel ciclo di
Krebs
(processi mitocondriali)
il NADH glicolitico è ri-ossidato a livelli della
catena respiratoria ma non potendo attraversare la membrana
mitocondriale interna utilizza due sistemi per poter
‘virtualmente’ entrare nel mitocondrio:
• sistema navetta o SHUTTLE del Glicerolo fosfato
(determina la formazione di FADH2 mitocondriale)
• sistema navetta o SHUTTLE del malato-aspartato
(determina la formazione di NADH mitocondriale)
Gli equivalenti riducenti vengono trasportati all’interno
dei mitocondri attraverso dei sistemi navetta (Shuttle)
SHUTTLE del Glicerolo fosfato
SHUTTLE del malato-aspartato