Università degli Studi di Messina
Cattedra di Chirurgia Generale
Titolare: Prof. Salvatore Gorgone
Chirurgia Cardiaca
Prof. Salvatore GORGONE
Anatomia della Parete toracica
n
n
n
n
n
n
n
n
Forma cilindro-conica ad apice superiore tronco
Parete anteriore: dal giugulo all’apofisi xifoidea (~18 cm),
costituita dallo sterno e prime 10 cartilagini costali
Pareti laterali: costituita dalle ultime 10 coste
Parete posteriore: costituta dalle 12 vertebre toraciche con i
loro processi trasversi e dalle 12 coste
L’apertura superiore è delimitata dalle prime coste, dal
manubrio dello sterno e dal corpo della I vertebra toracica
L’apertura inferiore, circoscritta dalla XII vertebra e dalle
coste, anteriormente dalle cartilagini VII e XII costali e dal
processo xifoideo, è obliterata dal diaframma
Muscoli estrinseci (grande e piccolo pettorale, dentato anteriore;
trapezio, gran dorsale, romboide, dentato posteriore, lunghi del dorso) e
muscoli intrinseci (intercostali esterni, medi, interni)
Vasi e nervi intercostali
♂ l’altezza del torace è
maggiore che nella
donna: le coste sono
più oblique in basso e
lo sterno più verticale
♀ il torace è meno alto:
le coste più
orizzontali, lo sterno
più proiettato in
avanti; è più simile
alla gabbia toracica
di età infantile
Mediastino
n
n
Spazio toracico centrale compreso tra le due cavità pleuriche
Mediastino anteriore
»
»
»
»
n
Mediastino posteriore
»
»
»
»
»
n
Timo
Vene brachiocefaliche
Nervi frenici e nervi vaghi
Arco aortico
Esofago
Dotto toracico
Tronchi simpatici
Aorta discendente
Vene azygos ed emiazigos
Mediastino medio
» Trachea
» Ili polmonari
Pericardio
Cuore
n
n
n
n
n
n
n
n
Il cuore è un organo muscolare cavo, che genera un flusso continuo
di sangue per mantenere un livello pressorio nell’albero circolatorio
Si presenta come un cono appiattito antero-posteriormente con
l’asse della punta diretto in basso, indietro ed a sinistra
La faccia anteriore, convessa, corrisponde prevalentemente alla parete libera del
ventricolo destro, al cono d’efflusso polmonare, ad una piccola porzione del ventricolo
sinistro ed all’origine dell’aorta e dell’arteria polmonare. Il solco interventricolare
anteriore divide le superfici dei due ventricoli, mentre il solco atrioventricolare
anteriore divide la superficie ventricolare da quella atriale. Separata dal pericardio,
tale faccia è in rapporto con la parete sternocostale e la porzione mediastinica
pleuropolmonare
La faccia infero-posteriore poggia per buona parte sul diaframma ed è costituita dai
due ventricoli e dai due atri. Il solco interventricolare posteriore divide le superfici dei
ventricoli, il solco atrioventricolare posteriore i ventricoli dagli atri ed il solco
interatriale i due atri. Separata dal pericardio, questa faccia è in stretto rapporto con
alcune strutture del mediastino posteriore: l’esofago e l’aorta discendente toracica
Il margine acuto corrisponde ad una porzione del ventricolo destro; è in rapporto con
la superficie del diaframma
Il margine ottuso, più ampio, costituisce la parete laterale del ventricolo sinistro ed è
in stretto rapporto con la parete mediale del polmone sinistro
La base del cuore è formata dalle pareti atriali, dallo sbocco della vena cava superiore
in atrio destro e dallo sbocco delle quattro vene polmonari in atrio sinistro
L’apice cardiaco appartiene esclusivamente al ventricolo sinistro e corrisponde all’itto
della punta
n
Atrio destro
–
n
n
è tricuspide, ogni cuspide è a forma di coppa che nella porzione libera presenta margine ispessito con un nodulo
Valvola polmonare
–
n
più ampia della mitrale. I tre lembi non sono di uguale dimensione. Corde tendinee più esili
Valvola aortica
–
n
due lembi la cui superficie di collabimento è ampia. Le corde tendinee nascono dai muscoli papillari
Valvola tricuspide
–
n
costituito da una porzione membranosa e da una ampia porzione muscolare. Superiormente esso si continua con lo
scheletro, struttura connettivale che circonda le valvole mitrale, aortica e tricuspide
Valvola mitrale
–
n
comprende una porzione di afflusso ed una di efflusso separate solo dall’ampio lembo anteriore della valvola mitrale. Ha
due muscoli papillari. La struttura muscolare parietale è ben rappresentata. Durante la sistole spinge il sangue nel
circolo generale
Setto interventricolare
–
n
ha una camera di afflusso sotto la tricuspide ben separata dalla camera di efflusso o infundibolo polmonare. Ha diversi
muscoli papillari. La struttura della parete muscolare non è molto sviluppata. Durante la sistole spinge il sangue nel
circolo polmonare
Ventricolo sinistro
–
n
costituito in gran parte dalla struttura costituita dal collabimento dei due foglietti primitivi che in età neonatale
collabiscono ed in seguito chiudono il forame ovale
Ventricolo destro
–
n
riceve le vene polmonari. L’auricola è allungata
Setto interatriale
–
n
riceve le vene cave superiore e inferiore e il seno coronarico. L’auricola è ad ampia base d’impianto
Atrio sinistro
–
n
Anatomia del cuore
Simile all’aortica ma manca lo scheletro fibroso di sostegno e le cuspidi sono più sottili
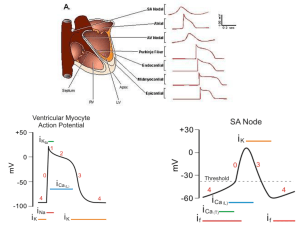
Nodo del seno, Nodo atrio-ventricolare, Fascio di His deputati alla diffusione ritmica e coordinata dell’eccitazione
elettrica del muscolo cardiaco
Coronaria destra, Coronaria sinistra arterie che irrorano la massa muscolare
Il cuore è rivestito da una membrana
fibroelastica il pericardio, tra pericardio
e miocardio vi è una cavità virtuale, la
cavità pericardica, che in condizioni
normali contiene ~50 ml di liquido
pericardico, per permettere al cuore di
muoversi liberamente durante la
contrazione e il rilasciamento
Fisiologia cardiaca
n
n
n
n
n
n
n
Il cuore è una pompa muscolare atta a generare un flusso continuo di sangue ed a
mantenere un livello pressorio nell’albero circolatorio
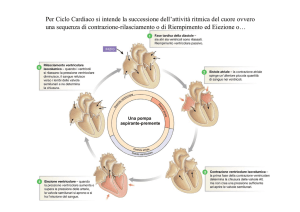
Il ciclo cardiaco presenta la ritmica alternanza da uno stato di contrazione ad uno di
rilasciamento muscolare. Il movimento d’apertura e di chiusura delle valvole segue
passivamente le variazioni pressorie che si determinano all’interno delle cavità cardiache
per effetto del meccanismo contrazione-rilasciamento muscolare, garantendo un flusso
unidirezionale del sangue
Le sezioni del cuore costituiscono due sistemi idraulici posti in serie
– il circolo polmonare (sezione destra) a bassa pressione
– il circolo sistemico (sezione sinistra) ad alta pressione
Il sangue è un fluido incomprimibile circolante all’interno di un sistema idraulico chiuso
(albero circolatorio)
Portata cardiaca: la quantità di sangue espulsa dal ventricolo sinistro in un minuto deve
essere pari a quella che giunge al ventricolo destro nella stessa unità di tempo
Il cuore è quindi in grado di adeguare la portata cardiaca alle esigenze metaboliche dei
tessuti periferici attraverso semplici variazioni dei due parametri: frequenza cardiaca e
gittata sistolica
L’aumento della frequenza non è in grado di migliorare la portata cardiaca in modo
lineare; oltre un limite critico, infatti, la riduzione del riempimento diastolico e della
perfusione coronarica che ne consegue comportano un sensibile calo della portata
Fisiologia cardiaca
n
Dalla ritmica attività delle contrazioni atriale e ventricolare vengono
generati i toni cardiaci provocati dalla rapida accelerazione e
decelerazione che il sangue subisce durante il ciclo cardiaco
n
I tono origina dalla sistole ventricolare segnandone l’inizio; è causato
dall’urto del sangue contro le valvole atrio-ventricolari e all’oscillazione
del sangue tra le valvole e le pareti e dall’oscillazione del sangue che esce
dalla dall’aorta e dall’arteria polmonare
II tono origina dalla fine della sistole ventricolare; è causato dalla
vibrazione della colonna di sangue sui lembi chiusi delle valvole aortica e
polmonare
III tono origina alla fine della fase diastolica di riempimento rapido; è
causato dalla vibrazione di tutto il sistema atrio-ventricolare
IV tono origina a metà della sistole atriale; è causato dalla stessa sistole
n
n
n
Fisiologia cardiaca
n
n
n
Diastole ventricolare: comincia subito dopo l’onda T dell’ECG con il rilasciamento della
muscolatura ventricolare. Le valvole semilunari si chiudono per effetto di un regime
pressorio più elevato in aorta ed in arteria polmonare rispetto alle cavità ventricolari; le
valvole mitrale e tricuspide, al contrario, si aprono in seguito alla caduta delle pressioni
ventricolari al di sotto di quelle atriali ed il sangue fluisce attraverso di esse ad una velocità
che progressivamente si riduce, con il riempimento dei ventricoli, al termine della diastole
Sistole atriale: comincia dopo l’onda P ed attraverso la contrazione della muscolatura
atriale contribuisce ad un 20% del riempimento ventricolare
Sistole ventricolare: ha inizio dopo il complesso QRS dell’ECG con la contrazione del
miocardio e la rapida chiusura delle valvole atrioventricolari per l’improvviso aumento di
pressione all’interno delle cavità ventricolari. Si distingue una fase isometrica della sistole
durante la quale tutte le valvole cardiache risultano chiuse e la tensione sviluppata dalle
pareti muscolari si trasmette alla massa sanguigna contenuta nelle cavità ventricolari
aumentandone la pressione interna; quando quest’ultima supera la pressione diastolica in
aorta ed in arteria polmonare, con l’apertura delle rispettive valvole semilunari, ha inizio la
fase isotonica durante la quale la tensione di parete si trasmette alla massa sanguigna
espulsa nelle arterie ad un determinato regime pressorio
Meccanismi dello scompenso cardiaco
– Perdita di massa contrattile con sostituzione fibrotica per danno cellulare diretto
– Aumento di massa muscolare in risposta ad un sovraccarico di pressione o di volume
Elettrocardiogramma
introdotto alla fine dell’800 da Einthoven
n
n
n
L’ECG è la registrazione superficiale dell'attività elettrica del
cuore
Si ottiene posizionando gli elettrodi sulla cute, sei sul torace
anteriore e quattro sulle estremità degli arti
Si può dividere in cinque parti
– Inizia con un'onda di modeste dimensioni, l'onda P, provocata dalla
sistole atriale, che offre indicazioni del tempo impiegato dall'impulso
per propagarsi a entrambi gli atri
– Segue un tratto piano privo di onde, il segmento PQ, che indica il
passaggio dell'impulso dagli atri ai ventricoli
– Successivamente troviamo il complesso QRS, formato dall'onda Q,
breve e verso il basso, l'alta e stretta onda R e la piccola onda S,
anch'essa verso il basso; il complesso caratterizza la sistole
ventricolare con l'arrivo dell'impulso ai ventricoli (onda Q) e
l'estensione a tutto il tessuto (onde R e S)
– Il lungo intervallo ST che segue l'onda S e comprende l'onda T
rappresenta il periodo in cui i ventricoli si contraggono e poi (con
l'onda T) ritornano a riposo. L’onda U ha significato scarso e incerto
– Esistono anche altre grandezze (come l'intervallo QT), significative
per patologie particolari
Le due derivazioni A e B hanno
differente morfologia ma
registrano gli stessi fenomeni
n
n
n
n
n
Il tracciato elettrocardiografico è costituito da una sequenza di onde che esprimono la
depolarizzazione (attivazione) e la ripolarizzazione (recupero) delle diverse sezioni del
cuore
La medesima sequenza di onde (P,QRS,T,U) si ripete costantemente ad ogni battito
cardiaco, almeno in condizioni normali
Il tracciato elettrocardiografico registrato su carta comprende 12 derivazioni, 6 delle quali
definite periferiche (I, II, III, aVR, aVL, aVF) perché ottenute ponendo gli elettrodi alle
estremità degli arti, mentre le altre 6, denominate precordiali, perché si registrano con
elettrodi posti sul torace, si distinguono con i simboli V1,V2,V3,V4,V5,V6
Tutte le derivazioni registrano la stessa serie di fenomeni, cioè la medesima sequenza di
onde, anche se la forma e l’ampiezza di queste varia da una derivazione all’altra. In realtà
ciascuna derivazione “vede” il cuore da un punto di osservazione diverso, per cui tutte
insieme offrono un panorama completo della realtà
Oltre che registrato sulla carta apposita, l’ECG può essere osservato su un monitor. Nelle
Unita Coronariche, nelle Terapie Intensive, nelle Sale Operatorie la monitorizzazione
dell’ECG fornisce informazioni di grandissima importanza sull’attività cardiaca
Extrasistole
n
n
Extrasistole significa extra contrazione (o sistole) ventricolare, cioè che si è originata nel
ventricolo sinistro. Ma come si può vedere (frecce rosse) la contrazione, come tempo, non arriva
interpolata esattamente tra due contrazioni normali (le punte nere più basse), ma arriva anticipata
(prematura) e con un periodo di pausa più lungo. È proprio questa pausa compensatoria che,
insieme alla extrasistole, fa sentire il sintomo caratteristico di "vuoto alla gola". Anche perché
l'extrasistole ventricolare non esprime una corretta funzione di pompa del cuore. Il cuore infatti,
nella contrazione extra, non ha la capacità di riempirsi come dovrebbe e quindi all'atto della sistole
la funzione di pompa non è efficace
l'extrasistole più prematura è più può essere pericolosa per la possibilità di dar luogo a un
insieme di tante extrasistoli consecutive (run = corsa) che potrebbero portare alla insufficiente
funzione di pompa cardiaca e quindi a perdita di coscienza
Radiografia del torace
Ecocardiogramma
n
n
n
n
n
n
Permette la visualizzazione dell'anatomia cardiaca con ultrasuoni
emessi da una sonda, le immagini ottenute vengono elaborate dalle
onde riflesse raccolte dalla sonda stessa
Evidenzia le varie componenti del cuore ed il movimento delle pareti
cardiache
Tecnica monodimensionale, bidimensionale e tridimensionale
L'ecocardiografia color-doppler è idonea allo studio dei flussi di sangue
nelle cavità cardiache e attraverso le valvole
Indicata nelle valvulopatie, nelle cardiomiopatie di diversa eziologia e
naturalmente nella cardiopatia ischemica. Indispensabile è il contributo
diagnostico che si può ottenere nelle cardiopatie congenite sia del
bambino che dell'adulto, inoltre può fornire indicazioni decisive circa i
tempi e le modalità degli interventi cardiochirurgici correttivi delle
valvulopatie
L'ecocardiografia transesofagea, sfrutta la vicinanza dell'esofago alle
pareti cardiache permettendo una migliore definizione di alcune parti
del cuore. La sonda ad ultrasuoni viene introdotta nell'esofago
endoscopicamente. Trova indicazione nelle cardiopatie congenite,
valvolari e per la visualizzazione di trombi endocavitari
Coronarografia - Scintigrafia
n
n
n
n
n
n
La coronarografia è una metodica diagnostica che prevede l'introduzione di cateteri nelle arterie
dell'inguine per poter iniettare un mezzo di contrasto e visualizzare le arterie coronarie direttamente
all'origine. L'esame viene eseguito mediante la tecnica radiografica tradizionale
La metodica permette di valutare l'anatomia del circolo coronarico. Viene effettuato in anestesia
locale e solitamente è bene accetta dal paziente
Il catetere viene fatto avanzare nelle arterie, in aorta e fino all'imbocco delle arterie coronarie dove
l'iniezione del mezzo di contrasto "colora" e opacizza i vasi rendendoli visibili ai raggi X. È possibile
evidenziare eventuali ostruzioni, come placche aterosclerotiche, all'interno dei vasi coronarici. Si
tratta generalmente di un esame gravato da una bassissima incidenza di complicanze
L'indicazione alla coronarografia, tranne nelle urgenze, viene solitamente posta dopo aver eseguito
gli altri esami diagnostici cardiologici (ECG da sforzo, Ecocardiografia, Scintigrafia miocardica)
e riguarda in particolar modo la cardiopatia ischemica che non risponde convenientemente alle cure
farmacologiche oppure nelle condizioni considerate a maggior pericolo per il paziente
L'esame coronarografico viene generalmente eseguito in previsione di un intervento di
rivascolarizzazione miocardica di angioplastica oppure con by-pass aorto-coronarico
L'esame ha una durata di circa 60 minuti, prevede un breve ricovero di 2-3 giorni anche se in alcuni
ambienti si sono stati ottenuti tempi di ricovero non superiori alle 24 ore, ed è eseguibile presso centri
dotati di laboratori di emodinamica
Cateterismo cardiaco
n
n
È possibile introdurre nel cuore, attraverso vene o arterie periferiche, sottili sonde flessibili (cateteri) a
scopo diagnostico o terapeutico
A scopo diagnostico
– il catetere, spinto sotto controllo radiologico fin dentro le cavit
cavitàà cardiache, può misurare la pressione
intracavitaria o registrare l’
l’elettrocardiogramma direttamente all’
all’interno del cuore
– attraverso il catetere si può effettuare un prelievo di sangue per
per misurare la saturazione d’
d’ossigeno nelle diverse
cavità
cavità cardiache (questa tecnica si impiega per misurare la portata cardiaca
cardiaca o per calcolare l’
l’entità
entità di uno shunt
intracardiaco)
– si può iniettare mezzo di contrasto per opacizzare le cavità
cavità del cuore o i vasi arteriosi (per esempio, le coronarie)
o venosi
n
A scopo terapeutico
– il cateterismo cardiaco può consentire di dilatare vasi stenotici
stenotici (ristretti) od occlusi (tecnica denominata
angioplastica)
)
o
valvole
stenotiche
(valvuloplastica
valvuloplastica)
)
angioplastica
(
– si possono correggere alcune malformazioni congenite del cuore come
come il difetto interatriale o interventricolare e
la pervietà
pervietà del dotto arterioso di Botallo
– numerose aritmie cardiache possono essere curate con una metodica
metodica di stimolazione transcatetere:
transcatetere: per esempio
nel blocco AA-V è possibile introdurre nel cuore un elettrocatetere che, connesso ad uno stimolatore
(pacemaker)
pacemaker) stimola il cuore evitando che insorga l’
l’arresto cardiaco dovuto all’
all’asistolia
– somministrando attraverso la punta del catetere, posta a contatto
contatto con la superficie interna del cuore, energia a
radiofrequenza,
radiofrequenza, è possibile creare piccole lesioni che provocano a carico del tessuto
tessuto un danno termico, il quale
evolve poi in fibrosi; si possono così
così eliminare piccole zone miocardiche dalle quali si origina un’
un’aritmia;
questa metodica prende il nome di ablazione transcatetere
Circolazione extracorporea
Dennis 1951
n Permette di sostituire temporaneamente (ore) la funzione
di pompa del cuore e di scambiatore di gas dei polmoni
n L’ipotermia (moderata 32°C - 25°C, profonda 25°C - 18°C) e la
cardioplegia (uso di soluzioni che arrestano il cuore, riducendo le
richieste metaboliche del miocardio e stabilizzando lo stato fisico-chimico
delle membrane cellulari, proteggendolo dall’insulto ischemico)
permettono di protrarre anche per due – tre ore il tempo
di ischemia miocardica
n Monitoraggio continuo del paziente intra e postoperatorio
n Trattamento intensivo postoperatorio
CEC in cardiochirurgia
» necessità dell’arresto cardiaco controllato
» necessità di disporre di un cuore fermo, esangue
» necessità di sostituire la funzione cardiopolmonare
n
n
n
La circolazione extracorporea può essere definita come un dispositivo per
l’ossigenazione e la propulsione a flusso/pressione controllati del sangue venoso
L’intero flusso ematico venoso refluo in atrio destro viene aspirato e dirottato verso
una macchina esterna ove viene ossigenato e pompato a pressione controllata e
quindi reintrodotto nell’albero arterioso (aorta o arteria femorale)
Ne consegue che:
– il sangue deve passare attraverso condotti non endotelizzati
– gli organi ricevono un flusso non pulsatile ma continuo
n
La specie umana tollera questa condizione, che può essere definita “parafisiologica”
Circuito extracorporeo
n
n
n
n
Il sangue, dopo eparinizzazione del paziente viene raccolto da una cannula
posta in atrio destro o da due cannule inserite nelle vene cave e raggiunge
l’ossigenatore da dove, depurato dalla CO2 e ossigenato, quindi
opportunamente riscaldato o raffreddato, viene pompato nell’albero arterioso
attraverso una cannula inserita nell’aorta ascendente o nell’arteria femorale
In questo modo il sangue del paziente bypassa il cuore e i polmoni rendendo
possibili interventi a cuore aperto con campo esangue e cuore fermo
Circuiti accessori permettono di aspirare il sangue eparinato dal campo
operatorio, che viene raccolto e convogliato in un serbatoio (cardiotomo),
filtrato e fatto defluire nell’ossigenatore. Necessari sono i filtri per fermare
microemboli e piccole bolle d’aria, uno scambiatore di calore e sistemi di
monitoraggio della pressione e della temperatura
Per evitare l’immissione di aria in circolo si adoperano per il priming
soluzioni idroelettrolitiche bilanciate fino ad ottenere un ematocrito del 20%
Metodologia clinica della circolazione extracorporea
n
n
n
n
n
n
n
n
n
n
n
n
n
n
n
n
Monitoraggio dei parametri vitali fondamentali (FC, ECG, P.A., pressione arteriosa polmonare,
diuresi, temperatura nasofaringea e vescicale/rettale, emogasanalisi arteriosa, parametri
ematochimici, ematocrito, emoglobinemia, pH)
Preparazione del campo chirurgico (stermotomia mediana, pericardiotomia longitudinale)
Eparinizzazione (per ottenere la scoagulazione completa)
Incannulazione arteriosa (aorta ascendente)
Incannulazione venosa (vena cava inferiore o inferiore/superiore)
Inizio della circolazione extracorporea
Raffreddamento corporeo (con l’ausilio della heart-lung machine)
Clampaggio dell’aorta
Somministrazione di cardioplegia
“Tempo centrale cardiochirurgico”
Riperfusione cardioplegica
Declampaggio aortico
Ripristino della normotermia
Ripresa dell’attività elettromeccanica del cuore
Sospensione della CEC
Decannulazione dell’aorta e delle vene cave
Metodologia clinica della cardioplegia
n
n
n
n
n
n
n
Dopo il clampaggio aortico, la soluzione cardioplegica viene iniettata
nel bulbo aortico (via anterograda)
La stessa soluzione viene iniettata anche nel seno coronarico (via
retrograda)
Si ottiene l’arresto elettromeccanico del cuore in diastole
Si monitorizza la temperatura del setto interventricolare con apposita
sonda e si provvede al mantenimento di una temperatura settale < 15
°C con regolari somministrazioni di soluzione cardioplegica ogni 20
minuti
La cardioplagia viene mantenuta per tutta la durata del tempo
cardiochirurgico centrale
Al termine del tempo centrale, la fase della riperfusione inizia per via
retrograda fino alla ripresa dell’attività elettromeccanica del cuore
Si procede quindi al declampaggio aortico ed alla perfusione
coronarica ematica fisiologica
n
n
n
n
n
n
n
n
La pressione arteriosa, mediante agocannula in un’arteria periferica,
permette di valutare l’efficacia contrattile del miocardio e di controllare la
volemia del paziente
La pressione venosa centrale si ottiene incannulando una vena centrale
(succlavia, femorale, giugulare interna) e serve a valutare sia l’attività
cardiaca che l’entità della massa circolante
La misurazione della gittata cardiaca serve a valutare la funzione di pompa
del cuore
La diuresi viene monitorata con un catetere vescicale a palloncino
La funzione respiratoria viene controllata con l’esame emogasanalitico
ripetuto a intervalli regolari
A fine intervento vengono posizionati due drenaggi in mediastino sia per
drenare le perdite ematiche sia per misurare le perdite ed effettuare un
adeguato rimpiazzo
Il bilancio idroelettrolitico si calcola comparando le perdite (diuresi,
perdite ematiche, drenaggio dal sondino naso-gastrico, perspiratio
insensibilis) con le entrate (soluzioni somministrate per endovena e per os)
Il tempo di risveglio del paziente, il suo orientamento nel tempo e nello
spazio, la capacità di muovere gli arti su richiesta sono i parametri
neurologici principali che vanno eventualmente completati con l’esame
neurologico e con l’EEG
Trattamento intensivo
n La ridotta riserva cardiaca, l’instabilità circolatoria, le
ripercussioni della circolazione extracorporea sui vari apparati,
l’elevata richiesta metabolica (per lo stato di “infiammazione
generalizzata” e per la necessità di riscaldarsi dall’ipotermia)
impongono il trattamento in Unità di Terapia Intensiva
nell’immediato periodo postoperatorio
n Il paziente ancora sedato e intubato viene collegato ad un
respiratore automatico e monitorizzato. Raggiunta la stabilità
circolatoria e riscaldato l’operato viene gradualmente lasciato
emergere dalla sedazione e quindi estubato
n Sono necessarie 8 - 12 ore postoperatorie per raggiungere una
situazione di equilibrio stabile e 24 ore per recuperare il normale
stato di coscienza
Arresto circolatorio
n
n
Complicanza del decorso postoperatorio, soprattutto delle prime 24 ore postoperatorie
Cause più frequenti
–
–
–
–
–
–
n
infarto postoperatorio
tamponamento cardiaco
ipovolemia acuta da sanguinamento massivo
distacco di protesi valvolare
ipokaliemia o iperkaliemia
pneumotorace ipertensivo
Terapia
– massaggio cardiaco esterno: 80-100 compressioni al minuto che provochino la depressione dello
sterno di 4-5 cm
– ventilazione in ossigeno puro: 12-15 insufflazioni al minuto sincronizzate con le compressioni
toraciche
– defribillazione elettrica: scarica non sincronizzata di corrente continua fino a 360 Joule di energia
– Farmaci: adrenalina in bolo di 0,5-1 mg o in infusione continua nella linea venosa centrale e
cloruro di calcio
– massaggio cardiaco interno: dopo riapertura d’emergenza del torace
– contropulsatore aortico: catetere a palloncino posizionato in aorta discendente collegato ad un
apparecchio esterno che gonfia il palloncino in diastole e bruscamente lo sgonfia all’inizio della
sistole, in questo modo si ha un rialzo pressorio diastolico con aumento della perfusione coronarica
Massaggio cardiaco esterno
Insufficienza renale acuta postoperatoria
n
n
Circa il 4% dei pazienti operati in CEC sviluppa insufficienza renale
oligoanurica, condizione che è gravata da mortalità elevata (60-80%)
Fattori predisponenti
–
–
–
–
–
–
–
n
creatininemia preoperatoria > 1,6 mg/dl
insufficienza cardiaca preoperatoria
età avanzata
durata della CEC
bassa portata postoperatoria
politrasfusione
uso di mezzi di assistenza circolatoria meccanica
Una volta instaurata, l’insufficienza renale acuta oligoanurica
insensibile al trattamento con i diuretici deve essere trattata
aggressivamente con emofiltrazione o dialisi per evitare le
conseguenze dell’uremia, della ritenzione idrica e dell’iperpotassiemia
n European System for Cardiac Operative Risk Evaluation o
EUROSCORE serve a valutare il rischio chirurgico (1999)
n L’end point analizzato è la mortalità entro 30 giorni
– da 0 a 2 punti stima di mortalità 0,8%
– da 3 a 5 punti stima di mortalità 3,0%
– oltre i 5 punti stima di mortalità 11,2%
Le tecniche mininvasive consentono di evitare la
sternotomia, permettendo di diminuire il trauma e di
praticare minitoracotomie, penetrando tra una costa e
l'altra. L'incisione chirurgica varia dai 5 ai 7 cm, contro
i 25 cm della chirurgia tradizionale. I vantaggi sono
evidenti: minore traumatismo osseo, minore incidenza
di infezioni. Attraverso queste mini incisioni, si fanno
penetrare all'interno del torace microtelecamere
orientabili, manuali o computerizzate, con le quali si
può esplorare la cavità e intervenire con la massima
precisione. La durata dell'operazione è più breve di
quella tradizionale
Dolore
n
Compare nella cardiopatia ischemica e nella pericardite acuta
– Nella cardiopatia ischemica si deve quasi sempre a stenosi (restringimento) o occlusione di
un’arteria coronaria o di un suo ramo che determinando l’ischemia causa il dolore
– Nella pericardite si verifica un’infiammazione del pericardio; il dolore si deve in questo caso
proprio al processo infiammatorio che stimola le terminazioni nervose dolorifiche del pericardio
n
Il dolore cardiaco ischemico è molto più comune di quello pericardico, e può essere
localizzato ovunque nel torace, ma più spesso è retrosternale e s’irradia ad entrambe le
braccia e al giugulo. Questo dolore può essere di durata variabile: quando dura da qualche
minuto fino a 20-30 m, la malattia sottostante è l’angina pectoris, mentre durate maggiori
corrispondono di solito all’infarto miocardico. È non di rado difficile precisare l’origine
(cardiaca o no) di un dolore toracico solo in base alle sue caratteristiche (sede, irradiazione,
intensità, durata), ma è spesso necessario ricorrere a indagini strumentali
(elettrocardiogramma, ecocardiogramma) o di laboratorio per escludere o affermare l’origine
cardiaca del dolore di un determinato paziente. Nella diagnosi differenziale del dolore
cardiaco, vanno considerate le seguenti condizioni:
–
–
–
–
–
Nevriti e nevralgie toraciche (p.e. herpes zoster)
Affezioni gastriche o esofagee (p.e. ernia jatale)
Affezioni respiratorie (p.e. pneumotorace, pleurite)
Affezioni cardiovascolari (p.e. aneurisma dissecante dell’aorta)
Embolia polmonare
Dispnea
n
n
n
n
È la sensazione che per respirare si deve fare uno sforzo, come per
vincere un ostacolo. Questo sintomo riconosce numerose cause, ed è
comune sia nelle malattie dell’apparato respiratorio che in quelle
cardiache
La dispnea d’origine cardiaca è solitamente sintomo di scompenso
cardiaco, esprime cioè quella condizione in cui il cuore non riesce a
fornire una portata circolatoria (cioè una quantità di sangue) sufficiente a
soddisfare le richieste dell’organismo
La dispnea interviene dopo sforzo se la compromissione del cuore è lieve
o moderata, mentre quando lo scompenso è d’entità rilevante il sintomo
compare a riposo. Allora il paziente è costretto a dormire con più cuscini
o deve addirittura mettersi seduto o in piedi per respirare
Una dispnea grave e ad insorgenza improvvisa rappresenta un’emergenza,
e richiede un trattamento immediato.
Cianosi
n
n
n
n
Con questo termine s’indica il colorito bluastro che si osserva a carico della
cute e delle mucose quando il sangue è particolarmente povero d’ossigeno
I globuli rossi contengono l’emoglobina, proteina il cui compito è quello di
trasportare O2; l’ossigeno si lega all’emoglobina nei polmoni e viene poi
ceduto dall’emoglobina ai tessuti a livello capillare. L’emoglobina si può
trovare in due differenti stati: può contenere l’ossigeno o non contenerlo (in
questa seconda situazione prende il nome di emoglobina ridotta) perché non
è riuscita a captarlo a livello degli alveoli polmonari oppure perché lo ha già
ceduto ai tessuti. Il contenuto normale di emoglobina nel sangue è pari a 16
g/100 ml. Quando il sangue capillare contiene più di 5 g/100 ml di
emoglobina ridotta compare la cianosi
Questo reperto non è specifico delle malattie di cuore ma compare anche in
alcune malattie respiratorie
Per accertare la presenza della cianosi è necessario valutare il colorito della
cute e delle mucose, osservando particolarmente le guance, le labbra, le dita
delle mani e dei piedi, le unghie, i padiglioni auricolari
Cardiopalmo
n
n
Normalmente il battito cardiaco non viene avvertito dall’individuo, se non
in particolari condizioni (per esempio, dopo una corsa). La sensazione che
deriva dal sentire il battito del proprio cuore viene definita cardiopalmo.
Spesso il cardiopalmo dipende dall’aumento del numero dei battiti
(tachicardia), ma i due fenomeni non sono sempre associati: è possibile,
infatti, non accorgersi del battito cardiaco anche in presenza di una
tachicardia ad elevata frequenza, al contrario si può “sentire” il cuore anche
se questo batte a frequenza normale (60-100 battiti m' nell’adulto)
Davanti ad un paziente che riferisce cardiopalmo, la prima cosa da fare è
palpare il polso. Questa semplice manovra consente di rilevare due dati: la
frequenza (numero di battiti al minuto) e la regolarità o irregolarità del
polso. È così possibile comprendere se alla base del cardiopalmo vi sia
un’alterazione del ritmo cardiaco (aritmia) o della frequenza o se invece
non sia presente alcun’anomalia che spieghi il sintomo
Sincope
n
n
La sincope viene definita come una transitoria perdita della coscienza e del
tono posturale; essa dipende da un’improvvisa alterazione del metabolismo
delle cellule cerebrali, le quali necessitano, per il loro funzionamento, di un
continuo rifornimento di ossigeno e di glucosio
Le cause più comuni della sincope sono:
– Le alterazioni vascolari quali l’occlusione di un’arteria succlavia (Sindrome da furto
della succlavia)
– L’improvvisa caduta della pressione arteriosa, che comunemente consegue a
vasodilatazione arteriolare (sincope da vasodepressione)
– La perdita del tono delle arteriole è, in genere, di natura riflessa, cioè consegue a un
determinato stimolo che eccita (riflesso) il nervo vago, responsabile della
vasodilatazione
– L’improvvisa mancanza del battito cardiaco. Se il cuore non si contrae per 6 secondi o
più l’individuo perde i sensi perché viene meno il flusso di sangue al cervello
– L’alterazione cerebrale che consegue all’occlusione di un’arteria che porta il sangue al
cervello
– Malattie cardiache come la stenosi della valvola aortica o il mixoma atriale,
l’ipersensibilità del seno carotideo (risposta riflessa eccessiva alla compressione
dell’arteria carotide nel punto in cui si biforca) e altre condizioni di minore rilievo
Edema
n
n
n
Si definisce edema la condizione in cui siero fuoriuscito dai capillari si
raccoglie nel sottocutaneo, nel parenchima di un viscere, o in una cavità
(pleura, pericardio, peritoneo)
L’edema sottocutaneo si accumula, a causa della forza gravità, nelle zone
declivi. Il gonfiore si rileva esercitando una pressione, con il polpastrello
del pollice, sul dorso del piede, alla caviglia o sulla faccia anteromediale
della tibia, là dove l’osso non è ricoperto da muscolo: se è presente
edema, la pressione genera un avvallamento (segno della fovea). Nel
caso in cui il malato decomba da tempo a letto bisogna invece metterlo a
sedere e comprimere in corrispondenza del sacro dove si apprezzerà il
segno della fovea
L’edema si può riscontrare in diverse condizioni, soprattutto:
– Scompenso cardiaco
– Malattie del fegato o del rene in cui è alterata la composizione delle proteine
plasmatiche
Circolazione fetale e alla nascita
n
n
n
n
n
n
I due circuiti sono posti in parallelo e non in serie
Solo poco sangue perfonde i polmoni non espansi, che
rappresentano un circolo ad alta resistenza e pressione
Dal ventricolo destro il sangue passa nell’aorta
discendente attraverso il dotto arterioso di Botallo
Dall’atrio destro parte del sangue defluisce attraverso il
forame ovale nel ventricolo sinistro
L’equilibrata distribuzione dei flussi è uno dei principali
fattori che consentono il normale sviluppo di tutte le
camere cardiache
Alla nascita dopo i primi atti respiratori si ha una marcata
vasodilatazione arteriolare polmonare con grande aumento
del flusso; nel contempo aumentano le resistenze
periferiche per la chiusura dei vasi ombelicali.
L’incremeto della pressione nell’atrio sinistro determina la
chiusura del forame ovale. Pochi giorni dopo la nascita si
ha prima la costrizione e quindi la chiusura del dotto
arterioso di Botallo
Diagnostica delle cardiopatie neonatali
n Valutazione clinica
–
–
–
–
–
–
presenza di cianosi
rumori cardiaci aggiunti
difficoltà nell’alimentazione
mancata crescita ponderale
frequenti infezioni respiratorie
facile stancabilità ed irritabilità
n Alterazioni della frequenza cardiaca e respiratoria,
della perfusione periferica, epatomegalia
n Radiografia del torace, ECG, ecocardiografia
bidimensionale e Doppler, cateterismo cardiaco
Cardiopatie congenite
n
Difetto interatriale
– Comunicazione di varia dimensione tra gli atri (7%)
» ostium secundum (aritmie sopraventricolari, dispnea da sforzo,
frequenti bronchiti, scompenso cardiaco)
» ostium primum (forma più
più benigna, spesso asintomatica)
» seno venoso
– Trattamento chirurgico solo nei casi di scompenso refrattario alla
terapia medica
n
Difetto interventricolare
– Comunicazione tra i ventricoli (shunt sinistro-destro con grave
iperafflusso polmonare e scompenso cardiaco. Se lo shunt è
bidirezionale può comparire cianosi)
» Porzione perimembrabnosa (85%)
» Porzione muscolare del setto
– L’85% dei difetti interventricolari si chiude spontaneamente nel
primo anno di vita o subito dopo
– Un terzo dei pazienti è asintomatico. In caso di scompenso
conclamato ed intrattabile intervento di chiusura con patch di
dacron attraverso una ventricolotomia destra
Cardiopatie congenite
n Persistenza del dotto arterioso
di Botallo
– Il dotto arterioso costituisce una
comunicazione tra l’aorta e la parte distale
del tronco dell’arteria polmonare. Nei nati a
termine il dotto arterioso si chiude nei primi
giorni di vita. Se esso rimane pervio si
verifica iperafflusso polmonare con
graduale tendenza allo scompenso cardiaco
– Il 5% muore entro il primo anno di vita per
scompenso cardiaco e complicanze
polmonari. Nella prima infanzia si
osservano frequenti infezioni dell’apparato
broncopolmonare con scompenso cardiaco;
nei bambini più grandi i sintomi sono
sfumati ma è presente un soffio sistodiastolico sul focolaio della polmonare
Cardiopatie congenite
n
Tetralogia di Fallot
– Malformazione caratterizzata da stenosi infundibolare e valvolare
valvolare polmonare,
ampio difetto del setto interventricolare, cavalcamento aortico del setto ed
ipertrofia del ventricolo destro
– Costituisce il 12% delle cardiopatie congenite. È dovuta alla deviazione
anteriore del setto infundibolare male allineato con le restanti porzioni del
setto interventricolare
– Si realizza nelle forme tipiche un quadro di shunt destro - sinistro con ridotta
portata polmonare, elevata portata aortica, cianosi marcata, dispnea
dispnea da sforzo,
ippocratismo digitale, squatting, policitemia
– Se la stenosi polmonare è moderata lo shunt sarà
sarà prevalentemente sinistro –
destro con cianosi modesta
– La gravità
gravità e l’
l’età
età di comparsa della sintomatologia sono in rapporto al grado
di severità
à
della
stenosi polmonare
severit
– La tetralogia di Fallot è spesso associata con difetti di crescita, ma se viene riparata
precocemente, può essere ottenuta a lungo termine una crescita normale.
normale. L'intervento precoce, prima dei 5
anni di età
età, determina un'accelerazione della crescita in altezza e peso, con
con normalizzazione del processo di
crescita a lungo termine. Consiste nella chiusura della comunicazione
comunicazione interventricolare con eventuale
allargamento della via di efflusso del ventricolo destro
– In considerazione della prognosi naturale molto severa (la sopravvivenza
sopravvivenza media spontanea è di 12 anni, con
mortalità
mortalità del 50% nel primo anno) e degli ottimi risultati tecnici raggiunti,
raggiunti, la tetralogia di Fallot rappresenta
una indicazione assoluta all’
all’intervento chirurgico correttivo. Il trattamento medico serve a prevenire le crisi
asfittiche
Cardiopatie congenite
n
Stenosi polmonare
– 10% delle cardiopatie congenite
– Causa un’
un’ostruzione alla fuoriuscita del sangue dal ventricolo destro con conseguente aumento della pressione
intraventricolare
– È sempre presente un soffio sul focolaio polmonare; nei casi gravi
gravi crisi ipossiche e scarsa crescita; dispnea da
sforzo e facile stancabilità
stancabilità; possibilità
possibilità di morte improvvisa
– Il trattamento di scelta consiste nella dilatazione valvolare percutanea
percutanea con catetere a palloncino
(valvuloplastica) oppure nella commissurotomia valvolare
n
Coartazione aortica
– Restringimento dell’
dell’aorta a livello dell’
dell’istmo
– In epoca neonatale provoca scompenso cardiaco con mortalità
mortalità elevata (75% nel primo anno di vita).
Si impone il precoce intervento chirurgico di resezione dell’
dell’istmo aortico stenotico e successiva anastomosi
terminotermino-terminale dell’
dell’aorta. Può rimanere asintomatica fino all’
all’adolescenza quando compaiono i sintomi:
astenia, crampi da sforzo agli arti inferiori, cefalea, epistassi
epistassi
n
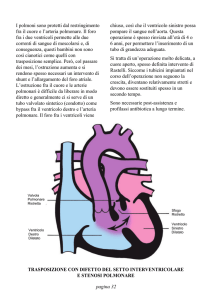
Trasposizione dei grossi vasi
– Frequente cardiopatia cianogena del neonato (30 - 40%)
– È la risultanza di una anomala divisione del tronco bulbare nel corso
corso dello
sviluppo embriologico, così
così che l’
l’aorta origina dal ventricolo destro e
l’arteria polmonare dal ventricolo sinistro
– L’ossigenazione ematica è possibile solo attraverso il mixing delle
due circolazioni per l’
l’esistenza di un difetto interatriale o interventricolare
L’assenza del mescolamento è incompatibile con la vita; mortalità
mortalità 90%
– I sintomi sono precoci: cianosi di vario grado, scompenso cardiaco
cardiaco
– La correzione deve essere precoce ed è gravata di alta mortalità
mortalità
Cardiopatie congenite
n
n
n
n
n
n
n
n
n
n
Stenosi aortica
Ritorno venoso anomalo totale
Anomalia di Ebstein (sviluppo anomalo della tricuspide)
Atresia della tricuspide
Tronco arterioso comune
Cuore sinistro ipoplasico
Cor triatrium
Ventricolo unico
Anomalie coronariche
Malposizione del cuore
Cardiopatie acquisite
n Stenosi aortica
n Insufficienza aortica
n Stenosi mitralica
n Insufficienza mitralica
n Insufficienza tricuspidale
n Stenosi tricuspidale
Valvulopatie cardiache
n
n
n
La stenosi valvolare si crea quando le cuspidi o foglietti valvolari si
inspessiscono e si fondono tra loro negli angoli in cui si toccano
(commissure). Separando le due parti fuse tra di loro si può ridurre la stenosi
e permettere ai foglietti di muoversi più liberamente
L’insufficienza valvolare può essere causata dall’indebolimento o
allungamento dei foglietti valvolari o delle corde tendinee. Il bordo dei lembi
che normalmente devono combaciare viene spostato, la valvola non chiude
più correttamente ed il sangue refluisce indietro. Il rigurgito stesso del
sangue fa ulteriormente progredire la disfunzione valvolare causandone la
dilatazione; diventa quindi necessario restaurare chirurgicamente i corretti
rapporti tra le diverse componenti della valvola. Per far questo può essere
necessario asportare il tessuto in eccesso, oppure accorciare le corde
tendinee, oppure ancora stringere l’anello valvolare rinforzandolo con anelli
di supporto
In alcuni casi le due alterazioni sono presenti contemporaneamente nella
stessa valvola: "steno-insufficienza"
Valvulopatie aortiche
n
Stenosi aortica
– Di origine congenita, degenerativa o reumatica (50% dei casi)
– Inizialmente si ha ispessimento, retrazione e fusione delle cuspidi
cuspidi valvolari che successivamente, a causa della
turbolenza del flusso ematico a livello dell’
dell’ostio valvolare alterato, vanno incontro a calcificazione e/o fusione
fusione di
una o più
più commissure
– L’ostacolo che la valvola aortica stenotica oppone all’
all’uscita del sangue dal ventricolo sinistro determina un
aumento del lavoro necessario per mantenere adeguata la portata cardiaca
– Pazienti portatori di stenosi aortica possono essere asintomatici.
asintomatici. I pazienti sintomatici hanno sincopi,
sincopi, vertigini,
angina pectoris o dispnea durante lo sforzo fisico. Nel 10% si verifica la morte improvvisa.
improvvisa. La sopravvivenza
media senza intervento è di 2 anni
– Bisogna intervenire alla comparsa dei primi sintomi o quando all’
all’esame emodinamico si riscontri un gradiente
pressorio transvalvolare superiore a 75 mmHg
– L’intervento chirurgico correttivo consiste nella sostituzione della
della valvola aortica con una protesi
n
Insufficienza aortica
– Il reflusso di sangue dall’
dall’aorta al ventricolo sinistro durante la diastole determina un aumento
aumento del lavoro del
cuore, il ventricolo sinistro ad ogni sistole deve espellere oltre
oltre alla gittata sistolica anche il sangue refluito
durante la diastole precedente.
– L’etiologia può essere secondaria a malattia reumatica, ad ectasia dell’
dell’anulus aortico, ad endocardite infettiva,
secondaria ad aneurisma aterosclerotico dell’
dell’aorta, essere complicanza della sifilide o di malattie autoimmuni
autoimmuni
– Può essere un vizio valvolare cronico ingravescente, che spesso gode di una lunga fase asintomatica, o avere un
inizio improvviso e acuto
– I sintomi dominanti sono: dispnea da sforzo, angina pectoris,
pectoris, cardiomegalia
– Sostituzione valvolare in tutti i pazienti sintomatici e negli asintomatici
asintomatici con cardiomegalia o con tendenza al
sovraccarico ventricolare in cui non raramente è necessario un intervento d’
d’urgenza
Valvulopatie mitraliche
n
Stenosi mitralica
– Causa più frequente (99%) è la malattia reumatica. Si manifesta con un’incidenza doppia nel sesso
femminile rispetto al maschile
– Il paziente lamenta dispnea da sforzo, ortopnea e dispnea parossistica notturna
– Complicanze della stenosi mitralica sono: la fibrillazione atriale episodica o persistente con
concomitante embolia arteriosa sistemica, l’edema polmonare acuto, l’emottisi, l’ipertensione
polmonare che può determinare scompenso ventricolare destro
– Tre tipi di intervento chirurgico, consigliabile in tutti i pazienti sintomatici a causa del basso rischio
operatorio e della possibilità di episodi embolici cerebrali, possono essere praticati: la
commissurolisi mitralica “a cuore chiuso” mediante un divulsore che forza sui lembi valvolari in
modo da separare le commissure fuse; la commissurotomia in circolazione extracorporea; la
sostituzione della valvola mitralica con protesi
n
Insufficienza mitralica
– Il reflusso di sangue dal ventricolo sinistro all’atrio sinistro può essere ad etiologia cronica dovuto a
malattia reumatica, a mesenchimopatia, a prolasso della mitrale, a lesioni valvolari determinate da
una endocardite infettiva o ad una malformazione della valvola, o acuta per rottura dei muscoli
papillari da ischemia miocardica
– La forma cronica può restare asintomatica per anni. Sintomi caratteristici sono: astenia e ridotta
tolleranza allo sforzo, dispnea da sforzo e parossistica notturna, ortopnea, palpitazioni, cardiopalmo
– Insufficienza mitralica sintomatica refrattaria al trattamento medico o asintomatica con
ingrandimento progressivo del ventricolo sinistro va trattata con riparazione della valvola o con la
sua sostituzione con protesi
Commissurotomia mitralica a cuore
chiuso mediante dilatatore ad
espansione transventricolare
Valvuloplastica mitralica
con catetere a palloncino
Valvulopatie tricuspidali
n
Insufficienza tricuspidale
– É il vizio più frequente a carico della valvola tricuspide. Determina un reflusso di
sangue dal ventricolo destro all’atrio destro durante la sistole
– Riconosce nella maggior parte dei casi una etiologia reumatica. Con l’eccezione delle
forme da endocardite settica, frequenti nei tossicodipendenti, non si presenta in forme
isolate, ma spesso è associata a valvulopatie mitraliche
– Il quadro clinico comprende edemi declivi, turgore giugulare, epatomegalia, frequente è
la fibrillazione atriale
– L’insufficienza tricuspidale isolata lieve o moderata non ha indicazione a correzione
chirurgica perché ben tollerata, quella severa richiede il trattamento chirurgico di
riparazione o di sostituzione quando determina una netta riduzione della capacità
funzionale del paziente
n
Stenosi tricuspidale
– Il quadro anatomico è caratterizzato dalla fusione dei lembi valvolari che delimitano una
piccola apertura centrale di 1 - 1,5 cm di diametro, con alterazioni più o meno gravi
delle corde tendinee
– Per la sua correzione si può procedere alla commissurotomia o alla sostituzione
valvolare, in base alle alterazioni anatomiche dei lembi e delle corde tendinee specie
quando si corregge la concomitante e più importante patologia mitralica
1980
Starr 1960
Non essere ostruttiva
Protesi meccaniche
• a palla
Non essere incontinente
Non provocare emolisi
• a disco oscillante
• a due semidischi
Protesi biologiche
Carpentier
1960
Non essere trombogenica
Essere biologicamente inerte
Essere facile da inserire
Avere lunga durata
Endocardite infettiva
n
Infezione localizzata
–
–
–
n
n
n
n
sulle valvole cardiache (endocardite valvolare da Streptococco)
sulle protesi (endocardite protesica da Stafilococco)
sull’endocardio parietale
Sintomatologia: febbre, segni sistemici di infezione, insorgenza o
aggravamento di un rigurgito valvolare
Frequenti le complicanze emboliche o microemboliche
Trattamento medico mirato, dopo antibiogramma, per via endovenosa
Intervento chirurgico sollecito
– se la sepsi non è controllata rapidamente (10 gg)
dall’antibiotico
– se compare scompenso cardiaco
– se si verificano embolie
Cardiopatia ischemica
n
n
n
n
Squilibrio fra fabbisogno e apporto di O2 che si determina o per aumentato consumo
miocardico o per riduzione del flusso coronarico
La causa più importante è la malattia aterosclerotica
La lesione fondamentale è la placca ateromasica
a sviluppo intraluminale e intraparietale nei vasi arteriosi
Nella genesi dell’ischemia miocardica accanto al fattore organico partecipa quello funzionale:
presenza di spasmo dei vasi coronarici
n
Lo spasmo coronarico in assenza di placca aterosclerotica è possibile ma molto raro. Un tipo del tutto
particolare di malattia coronarica su base non aterosclerotica si manifesta nel trapianto cardiaco (a causa
della denervazione). Si va diffondendo la cardiopatia ischemica da cocaina
n
L’aterosclerosi coronarica può essere asintomatica o può determinare vari gradi di angina per
giungere fino all’infarto, allo scompenso, alle aritmie, alla morte improvvisa
Sintomo principale è il dolore anginoso (improvviso, intenso, di breve durata ~10 m, alla
parete anteriore del torace, si irradia alla spalla e alla faccia ulnare dell’arto superiore sinistro
o alla mandibola). Talora: pallore, sudorazione, senso di angoscia
Nei pazienti con infarto miocardico a breve o lungo termine possono insorgere complicanze
dell’episodio necrotico (perforazione del setto interventricolare, insufficienza mitralica,
aneurisma ventricolare sinistro), che determinano alterazioni dell’emodinamica cardiaca
n
n
Placca che ostruisce il lume
dell’arteria; angiografia
By-pass coronarico
n
n
n
n
n
n
Consiste nella sostituzione del tratto di coronaria compromesso con un
innesto di un segmento di vaso che aggira l'ostruzione
Per l'innesto si possono usare sia segmenti di arterie sia segmenti di vene
Quando si sceglie un segmento di arteria, è possibile suturare le due
estremità una alla aorta e l'altra alla coronaria interessata al di sotto
dell'ostruzione, oppure si può lasciare l'estremità più lontana attaccata
all'arteria "donatrice" e limitarsi a suturare l'estremo libero alla coronaria
(sempre al di sotto dell'ostruzione)
Si preleva l'innesto dall'arteria mammaria interna del torace, dalla vena
safena della gamba, dall'arteria radiale del braccio o anche da altre arterie
più o meno periferiche
Il numero di bypass che si possono effettuare dipende dal numero di
coronarie o di rami delle coronarie ostruiti: uno, tre, cinque, teoricamente
non c'è limite.
Complicanze 5%, Mortalità 2%
Chirurgia coronarica
a cuore battente
n
n
n
n
n
n
La macchina cuorecuore-polmone ha permesso di eseguire con sicurezza molti interventi al
al cuore ma non è esente da
complicanze o ripercussioni sull’
sull’ organismo dovute ad una risposta infiammatoria generalizzata innescata
innescata dal contatto
del sangue con materiale non biologico e all’
all’incisione dell’
dell’aorta e di altre strutture cardiache per l’
l’inserzione di
cannule per il drenaggio e l’
l’iniezione del sangue. Tali complicanze sono probabile danno neurologico
neurologico (ictus, emorragie
cerebrali), insufficienza renale, alterazione dei componenti del sangue con emorragie massive postoperatorie, ischemia
intestinale e danno polmonare
La chirurgia a cuore battente consiste nell’
nell’eseguire l’
l’intervento senza la circolazione extracorporea evitando alcune
complicazioni, utilizzando degli appositi device mentre il cuore continua a muoversi
Viene selezionato un tratto di coronaria a valle dell’
dell’occlusione dove si decide di eseguire il bypass. Vengono applicate
applicate
dei punti di sutura per l’
l’occlusione del vaso stesso, a distanza di circa 2 cm un dall’
dall’altro. Questa zona viene stabilizzata
mediante l’
l’utilizzo dei sistemi a suzione o compressione,
compressione, per renderla immobile il più
più possibile mentre il cuore
continua a battere. Vengono serrati i 2 punti di sutura in maniera
maniera tale da fermare il passaggio di sangue nella zona
prescelta. Viene inciso il vaso coronarico e confezionata l’
l’anastomosi con il condotto prescelto. In questa fase, il
miocardio si trova in una condizione di ischemia e, per tale motivo, si deve eseguire il bypass in circa 7-10 minuti per
evitare un danno irreversibile al cuore. Per ovviare a questa situazione,
situazione, si possono utilizzare dei cosiddetti shunt
intracoronarici,
intracoronarici, che vengono inseriti nel vaso coronarico dopo la sua apertura e che permettono il passaggio del sangue
durante l’
l’esecuzione del bypass
La chirurgia a cuore battente è applicabile nella maggior parte dei pazienti, tranne in quelli con instabilità
instabilità
emodinamica, aritmie pericolose, disfunzione ventricolare sinistra
ra
con
cardiomegalia,
patologia
coronarica
diffusa, in
sinist
presenza di piccoli vasi coronarici calcifici
Vantaggi: possibilità
possibilità di operare pazienti a rischio per circolazione extracorporea, maggiore
maggiore stabilità
stabilità cardiaca
postoperatoria, minore sanguinamento postoperatorio, minori complicanze
complicanze polmonari e renali, riduzione del tempo
medio di degenza ospedaliera postoperatoria
Svantaggi: minore perfezione nella tecnica di confezionamento delle anastomosi,
anastomosi, possibile rivascolarizzazione
incompleta, necessità
à
di
una
maggiore
esperienza
del
chirurgo
necessit
Angioplastica coronarica
percutanea transluminale
n
n
n
n
n
n
L'angioplastica a palloncino diminuisce la
resistenza al flusso ematico del lume coronarico
stirando e lacerando la placca aterosclerotica e la
parete del vaso e ridistribuendo la placca lungo il
diametro longitudinale del vaso
Il meccanismo più importante per il miglioramento del flusso sanguigno
sembra essere la rottura e la frammentazione della placca aterosclerotica che
determina la formazione di numerose fissurazioni e di canali subito riempiti
dal sangue
La frequenza di successo è del 90%
Complicanza immediata è l'occlusione improvvisa del vaso (4-8%)
complicanza a distanza è la ristenosi (30-40%)
Lo stent è il metodo di scelta per trattare la minaccia di chiusura improvvisa
del vaso. In base al loro disegno, rivestimento e composizione, gli stent
differiscono per forze radiali, flessibilità, profilo, rintracciabilità , radio
opacità, biocompatibilità, trombogenicità e rischio di ristenosi intra-stent
La malattia di una singola coronaria è la principale indicazione alla PTCA
Rivascolarizzazione laser transmiocardica in casi di angina pectoris refrattaria non suscettibile di terapia chirurgica o percutanea
Aneurisma dell’aorta toracica
n
L´aneurisma aortico è una dilatazione del vaso in cui le tre tuniche parietali (intima,
(intima, media ed avventizia) sono normalmente
e contemporaneamente presenti
–
n
n
n
n
n
n
n
n
Gli aneurismi dell´
dell´aorta toracica rappresentano il 35% degli aneurismi aortici
» Aneurismi dell´
dell´aorta ascendente (45%)
» Aneurismi dell´
dell´arco aortico (10%)
» Aneurismi dell´
dell´aorta discendente (35%)
Eziologia: patologia aterosclerotica, patologie degenerative, aortiti
aortiti e lesioni congenite. Le lesioni aterosclerotiche danneggiano
danneggiano la
tunica intimale riducendo l´
l´elasticità
elasticità della media. L´
L´ipertensione trova nelle lesioni aneurismatiche un locus minoris resistentiae
determinando un progressivo incremento del diametro aortico. Le lesioni luetiche sono invece tra le cause più
più frequenti di aortite. La
presenza di coartazione aortica, di una persistenza del dotto arterioso
arterioso pervio e di stenosi valvolari aortiche favorisce lo sviluppo
sviluppo di
dilatazioni aneurismatiche
L´evoluzione naturale degli aneurismi vascolari è la progressiva dilatazione sino alla rottura del vaso.
vaso. Al progressivo aumento del
diametro corrisponde un incremento della tensione di parete con conseguente tendenza alla fissurazione
La comparsa di dolore indica una rapida espansione della massa aneurismatica
La radiografia del torace documenta la dilatazione dell´
dell´aorta ascendente ed il tracciato dell´
dell´ECG può evidenziare i segni di
un´
´
ipertrofia
ventricolare
sinistra
da
ipertensione
arteriosa.
L´
´
ecocardiogramma
confermerà
un
L
confermerà la diagnosi fornendo dati sulla
continenza valvolare. La TC spirale con mezzo di contrasto e la RM consentono di definire i rapporti dell´
dell´aneurisma con le strutture
circostanti. Lo studio agiografico è indispensabile per definire l´
l´anatomia delle coronarie
L´intervento chirurgico è indicato in presenza di un aneurisma di diametro superiore ai 5 cm: accesso chirurgico attraverso
sternotomia mediana; sostituzione del tratto aneurismatico dell´
dell´aorta ascendente con una protesi vascolare in circolazione
extracorporea e clampaggio aortico
La patologia aterosclerotica è l´eziologia più
più comune degli aneurismi dell´
dell´aorta toracica discendente. In tale sede, soprattutto a
livello istmico, sono molto frequenti anche gli pseudoaneurismi postpost-traumatici (dilatazione sacciforme dell´
dell´aorta il cui lume è in
diretto contatto con quello aortico ma la cui parete non è composta interamente dalle tre tuniche aortiche)
La sintomatologia è rappresentata dal dolore in regione interscapolare.
interscapolare. L´
L´intervento è indicato se il diametro dell´
dell´aneurisma
supera i 6 cm e consiste nella sostituzione del tratto aortico dilatato con una
na
protesi
vascolare
u
La sintomatologia degli aneurismi toracotoraco-addominali è rappresentata da algie toraciche ed addominali. L´indicazione chirurgica è
definita da un marcato incremento dei diametri aortici (sopra i 6-7 cm). L´
L´accesso chirurgico avviene tramite una toracofrenotoracofrenolaparotomia e l´
l´intervento è condotto con clampaggio dell´
dell´aorta a monte ed a valle del tratto aneurismatico
Tumori del cuore
n Primitivi
– Benigni
»
»
»
5 - 11%
Mixoma
Lipoma
Fibroelastoma papillare
Asintomatici
Riscontro occasionale
– Maligni (sarcomi)
• stenosi mitralica per
ostacolato passaggio del
sangue al ventricolo
sinistro
• embolia arteriosa per
sfaldamento del tumore
• sincope per completo
ostacolo al flusso
transmitralico
n Secondari
21%
» metastasi di carcinoma del polmone,
della mammella, da linfomi e leucemie
» infiltrazione da tumori contigui
affaticamento, dispnea,
edemi, turgore giugulare,
epatomegalia, anemia
Pericarditi
n Pericardite essudativa
– Pericardiocentesi o sternotomia e drenaggio
n Pericardite costrittiva
– Rimozione più ampia possibile del pericardio
(pericardiectomia)
tamponamento
cardiaco
Christian
Barnard
(1922-2001)
3/12/1967
il
Indicazione al trapianto cardiaco
n I pazienti candidati al trapianto sono pazienti
con insufficienza cardiaca avanzata:
– refrattaria alla terapia medica a dosi piene
– con caratteristiche di progressione nel tempo,
nonostante le cure mediche e non migliorabile con
procedure interventistiche o con la cardiochirurgia.
n Sono pazienti con un’importante limitazione
funzionale e una ridotta qualità di vita
Controindicazioni al trapianto cardiaco
n
n
n
n
n
n
n
Età (paziente > 65 anni, con una certa elasticità che tiene
conto dell'integrità biologica più che l'età anagrafica del
paziente)
Ipertensione polmonare con elevate resistenze polmonari
non modificate dal trattamento acuto o prolungato con
farmaci (vasodilatatori e/o inotropi)
Storia di malattia neoplastica che non possa essere
considerata radicalmente curata
Infezioni maggiori in atto da agente sconosciuto
Ulcera peptica attiva sanguinante
Dimostrazione di non-compliance del paziente alle cure
Positività degli anticorpi per HIV
Fattori che aumentano il rischio o riducono il potenziale vantaggio del
trapianto cardiaco
n
n
n
n
n
n
n
n
n
n
n
n
n
n
n
Scompenso congestizio cronico con disfunzione d'organo (specie epatica) persistente
Pregressa cardiochirurgia multipla con esiti che determinano un elevato rischio di sanguinamento
intra - e postoperatorio
Cachessia cardiaca
Grave obesità
Vasculopatia polidistrettuale (specie se con interessamento del circolo cerebrale o aneurisma
dell'aorta)
Diabete mellito insulinodipendente di difficile controllo e/o con danno vascolare e neuropatia
Insufficienza renale
Infezioni maggiori in atto da agente noto
Presenza di foci infettivi non eradicati
Colelitiasi sintomatica
Diverticolosi sintomatica
Epatite da virus B o C
Grave osteoporosi
Grave broncopneumopatia
Embolia polmonare recente (<3 mesi)
Quando possibile queste condizioni devono essere corrette prima dell'ammissione in lista
d’attesa. La coesistenza di più problemi non correggibili, anche se nessuno singolarmente
assolutamente cotroindicante il trapianto, può essere causa d’esclusione
Screening e follow-up dei pazienti in lista d’attesa
n
n
n
Lo screening è la valutazione atta a verificare l’opportunità reale dell’indicazione al
trapianto e ad escludere la presenza di controindicazioni o di condizioni che possono
limitare il successo dell’intervento. Viene eseguito con esami clinico-strumentali, in
parte presso i centri proponenti il trapianto ed in parte presso i centri dove il paziente
viene messo in lista d’attesa per il trapianto
Durante questa fase ed i successivi controlli, viene anche stabilita dal centro trapianti la
priorità o meno di un candidato a ricevere il cuore disponibile. Tale priorità è determinata
dalle condizioni cliniche del paziente, in quanto vengono prediletti a ricevere l’organo
disponibile i pazienti compatibili ed in condizioni cliniche più gravi, purché ancora tali da
non compromettere il successo dell’intervento
Il follow-up dei pazienti in lista d’attesa per trapianto cardiaco è mirato a verificare il
mantenimento delle condizioni di idoneità al trapianto e a verificare nel tempo la
persistenza dell’opportunità dell’indicazione. Viene attuato con visite periodiche
(generalmente mensili) e con aggiornamento periodico (generalmente annuale) degli
esami cardiologici e della situazione infettivologica e immunologica, valutando le diverse
condizioni che possono o meno condizionare la priorità del paziente nella lista d’attesa
Valutazione di idoneità del donatore
n
n
n
n
n
Il numero di interventi di trapianto dipende strettamente dall’identificazione e dal
reperimento di donatori
L’identificazione e la valutazione d’idoneità dei potenziali donatori di organi al
prelievo del cuore è un momento estremamente importante sia per evitare che un cuore
idoneo non venga utilizzato, sia per evitare che un cuore non idoneo (perché a sua
volta malato) venga prelevato e trapiantato con insuccesso (si ricordi che la
disfunzione grave e precoce del cuore trapiantato porta quasi sempre a morte il
ricevente)
Esistono delle controindicazioni assolute all’utilizzo di determinati cuori a scopo di
trapianto
Il donatore deve essere di età inferiore a 60 anni, deceduto per causa naturale o
accidentale, sieronegativo per HBV, HCV, HIV
Una volta stabilità l’idoneità del donatore viene segnalata la disponibilità al Centro di
coordinamento che provvede ad identificare uno o più potenziali riceventi e ad
eseguire le prove di compatibilità immunologica (AB0 e HLA). In tale sede vengono
tenuti in considerazione anche i criteri di priorità dei vari candidati a ricevere il cuore
del donatore
Trapianto cardiaco
n
n
n
n
n
n
n
Il trapianto di cuore è ancora in grande prevalenza ortotopico, per sostituzione del cuore del
ricevente con quello del donatore. Nel trapianto eterotopico il cuore donato viene posizionato
nell’emitorace destro
Alla tecnica tradizionale, nota anche come tecnica biatriale, si è aggiunta di recente la
tecnica bicavale che prevede la resezione della vena cava superiore e inferiore, conservando
l’integrità dell’atrio destro
Appena viene segnalata l’esistenza del potenziale donatore, il primo paziente compatibile in
lista d’attesa deve entrare in ospedale e prepararsi per la possibile operazione, mentre
nell’altro ospedale l’equipe incaricata valuta le caratteristiche dell’organo
Una volta accertata l’idoneità del cuore, l’equipe chirurgica inizia l’asportazione, in stretto
coordinamento con i medici dell’ospedale del ricevente
Il cuore del donatore viene lavato con una soluzione fisiologica salina fredda (4 gradi),
prelevato e immerso in un contenitore con la stessa soluzione, in grado di conservarlo per 4-5
ore
L’intervento poi dura poco più di un’ora, dopodiché il paziente viene portato nell’unità di
terapia intensiva per le cure post-operatorie dove è necessario seguire una terapia con farmaci
che impediscono i fenomeni di rigetto. Altre frequenti complicanze sono le infezioni, la cui
insorgenza viene ridotta da protocolli di farmaci antibiotici, antivirali e antimicotici, e le
coronaropatie
Nel reparto di degenza ordinaria il paziente si ferma per un periodo di circa 3-4 settimane
Rigetto
n Il rigetto può essere:
– Assente
– Lieve caratterizzato da soli infiltrati linfocitari perivasali
– Moderato presenta edema interstiziale, infiltrati pericellulari e
focolai di miocitolisi
– Severo vi è necrosi miocardia diffusa e marcata attivazione dei
linfociti
» Sintomatologia: malessere, febbre, mialgie, linfocitosi;
ipotensione arteriosa
segni di alterata funzionalità cardiaca all’elettrocardiogramma e
all’ecocardiogramma)
n Nel rigetto moderato si impone il trattamento steroideo
n Nel rigetto severo oltre al trattamento medico è
indispensabile il precoce controllo bioptico endomiocardico
per via endoscopica
Ventricular
Artificial
Device