CORSO DI LAUREA MAGISTRALE
SCIENZE DELLA NUTRIZIONE UMANA
ANNO ACCADEMICO 2013-2014
Corso Integrato di Microbiologia Agroalimentare e
Microbiologia Applicata
“Caratteristiche generali dei virus”
Dr.ssa Claudia Matteucci
Dipartimento di Medicina Sperimentale e Chirurgia
Cattedra di Microbiologia
VIROLOGIA GENERALE
-Sono parassiti endocellulari obbligati sia delle cellule
eucariotiche (virus propriamente detti) che delle cellule
procariotiche (batteriofagi)
-Sono quindi capaci di riprodursi esclusivamente
all’interno della cellula parassitata utilizzando i
meccanismi biosintetici cellulari
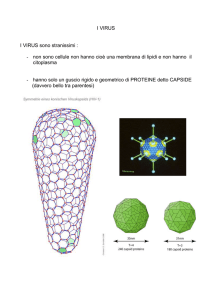
-Sono di piccolissime dimensioni (20-280 nm) e visibili
solo al microscopio elettronico
Dulbecco – Ginsberg “Microbiologia” Ed. Zanichelli
VIROLOGIA GENERALE
• Il genoma protetto da un involucro di
natura proteica (capside).
• Un solo tipo di acido nucleico DNA o RNA
MORFOLOGIA DEI VIRIONI
Virione = particella virale al di fuori della cellula
VIRUS NUDI
Nucleocapside = Genoma + capside
Genoma = Acido nucleico (DNA o RNA)
Capside = involucro proteico intorno all’acido nucleico
VIRUS RIVESTITI
Nucleocapside + Pericapside
Nucleocapside = Genoma + capside
Pericapside = involucro di natura lipoproteica
CAPSIDE
Struttura
• Costituito da capsomeri (subunità proteiche)
Simmetria
• Elicoidale 1 tipo di capsomero
• Icosaedrica 2 tipi
Funzione
• Protezione del genoma e proteine accessorie
• Portatore delle molecole di adesione
• Funzione antigenica
Capside - formato da subunità proteiche ripetute dette
capsomeri che possono essere costituiti da peptidi tutti
identici tra loro (virione a simmetria elicoidale) oppure
diversi (virus a simmetria icosaedrica).
Simmetria cubica o icosaedrica
i protomeri si dispongono in raggruppamenti
simmetrici detti capsomeri.
•
Disposizione spaziale dei protomeri in modo da
formare un solido regolare cavo che più si
avvicini alla sfericità: un icosaedro.
•
•
L’icosaedro è caratterizzato da 12 vertici,
( triangoli equilateri) 20 facce, 30 spigoli.
•
3 assi di simmetria rotazionali passanti al centro
dell’icosaedro.
•
Pentoni ( 5 protomeri) vertici
•
Esoni (6 protomeri) facce
CAPSIDE A STRUTTURA ICOSAEDRICA
Simmetria elicoidale:
•
I protomeri non si raggruppano in complessi ma si
dispongono con un andamento a spirale per
formare il capside.
•
Una specie di cilindro nella cui cavità si trova
l’acido nucleico.
•
Questa simmetria ha un solo asse di simmetria
rotazionale che coincide con l’asse longitudinale
del cilindro.
CAPSIDE A STRUTTURA ELICOIDALE
Pericapside
Alcuni virioni hanno il nucleocapside rivestito da un involucro
(envelope o peplo) detto pericapside di natura lipoproteica
derivato dalla membrana nucleare o citoplasmatica della
cellula parassitata (a seconda che il virus si replichi nel
nucleo o nel citoplasma della cellula ospite).
Pericapside
Stesse funzione del capside
• Portatore delle molecole di adesione del virus
alla cellula ospite
• Funzione antigenica
• Deriva dalla membrana cellulare o nucleare
della cellula ospite
NUDI
RIVESTITI
ICOSADRICI
Genoma
Capside
ELICOIDALI
Genoma
Capside
Pericapside
VIRUS NUDO
Mims et al. “Microbiologia Clinica” Ed. EMSI
VIRUS RIVESTITO
Mims et al. “Microbiologia Clinica” Ed. EMSI
PERICAPSIDE
GENOMA
CAPSIDE
GENOMA VIRALE
I virus possono contenere DNA o RNA
L’ RNA è sempre a catena singola ad eccezione del Rotaviris
(Reovirus) che ha un RNA a catena doppia.
Il DNA è sempre a doppia elica ad eccezione del Parvovirus
L’ RNA può essere a polarità positiva o a polarità negativa
L’RNA a polarità positiva all’interno della cellula può funzionare
direttamente da RNA messaggero.
L’RNA a polarità negativa deve essere trascritto in un elica
complementare che funziona da RNA messaggero: virus con questo
tipo di RNA hanno l’enzima RNA polimerasi RNA dipendente
associata al virione
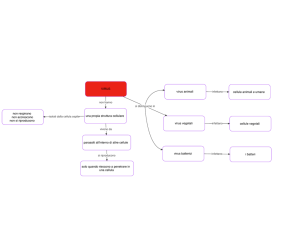
CLASSIFICAZIONE
Caratteristiche dei virus utilizzate nella classificazione:
CARATTERISTICHE DEL GENOMA:
• Tipo di acido nucleico
• Lineare o circolare
• Polarità positiva o negativa
• Presenza di segmenti distinti
• Sequenza nucleotidica
VIRUS A DNA:
• Herpesviridae
• Poxviridae
• Papovaviridae
• Adenoviridae
• Parvoviridae
• Virus dell’ Epatite B
VIRUS A RNA
•
Paramyxoviridae
•
Arenaviridae
•
Bunyaviridae
•
Rhabdoviridae
•
Orthomyxoviridae
•
Retroviridae
•
Caliciviridae
•
Picornaviridae
•
Coronaviridae
•
Togaviridae
•
Reoviridae
•
Filoviridae
INFEZIONE VIRALE
· Adsorbimento = il virus si lega ad uno specifico recettore della
membrana cellulare con un legame chimico-fisico
· Penetrazione = per fagocitosi e nei virus con pericapside per fusione
delle membrane
· Denudamento dell’involucro proteico = digestione dell’involucro
capsidico ad opera degli enzimi idrolitici contenuti nelle vesciche
lisosomiali cellulari
· Replicazione del genoma virale e Traduzione dei messaggeri virali
in PROTEINE VIRALI
· Assemblaggio delle particelle virali
· Liberazione delle particelle virali dalla cellula ed infezione di
altre cellule
FASI INIZIALI DELL’INFEZIONE
Incontro
Passivo, fase aspecifica
Legame
Recettori specifici sulla membrana cellulare
Penetrazione
Virus non rivestiti (NUDI):
viropessia (Endocitosi mediata da recettori)
Virus rivestiti:
scapsidazione
Endocitosi mediata da recettore
Fusione diretta
ATTACCO
• Contatto virus cellula
• Recettori virali sulla cellula
• I recettori per il virus presenti sulla cellula
possono essere proteine o carboidrati su
gp o glicolipidi.
• Antirecettori virali sul virus
RECETTORI PER I VIRUS
• EBV--> C3d presente sui linfociti B
• HAV--> alfa-2 macroglobulina
• HIV--> CD4
• Influenza --> gp contenenti acido
sialico.
• Morbillo --> CD46
• Picornavirus: Un avallamento (canyon)
sulla superficie del Rhinovirus che
s’inserisce sulla molecola di adesione
intercellulare (ICAM-1)
• Rhinovirus --> ICAM-1
ANTIRECETTORI VIRALI PRESENTI SULLA SUPERFICIE DEI VIRUS
• Emoagglutinine (HA)
• Glicoproteine (Gp)
PENETRAZIONE
VIRUS NUDI
a) adsorbimento
b) endocitosi (pH neutro)
c) Fagocitosi
VIRUS CON ENVELOPE
Fusione del pericapside con la membrana cellulare dell’ospite
con il fine di liberare il nucleocapside o il genoma direttamente
nel citoplasma.
DENUDAMENTO
•All’interno della cellula infetta il virione perde l’involucro
esterno, liberando l’acido nucleico e eventuali enzimi virali
che porta con se.
•azione delle proteasi sul capside proteico.
•azione degli enzimi lisosomiali sulle strutture proteiche
SINTESI MACROMOLECOLARE
L’acido nucleico e le proteine strutturali della progenie
virale
vengono
sintetizzate
separatamente
per
poi
riassemblarsi e formare nuovi virioni.
• vengono utilizzati enzimi cellulari
• alcuni virus portano nei virioni peculiari enzimi virali
(RNA polimerasi, DNA polimerasi)
• la replicazione del virus può avvenire nel citoplasma o
nel nucleo secondo il tipo di virus
EVENTI DELLA REPLICAZIONE VIRALE
1)Riconoscimento della cellula bersaglio
2) Adsorbimento
3) Penetrazione
4) Denudamento
5) Sintesi macromolecolari
a) Sintesi degli mRNA precoci e di
proteine non strutturali:geni per enzimi e
proteine leganti acidi nucleici.
b) Replicazione del genoma
c) Sintesi degli mRNA tardivi e di proteine
strutturali.
d) Modificazioni post-traduzionali delle
proteine.
6) Assemblaggio del virus
7) Gemmazione del virus con mantello
8) Rilascio del virus
STRATEGIE REPLICATIVE
A) VIRUS A DNA iniziano la trascrizione nel nucleo della cellula ospite
utilizzando la RNA polimerasi DNA dipendente della cellula ospite. I virus
che replicano nel citoplasma (poxvirus) utilizzano per la trascrizione una
polimerasi veicolata dal virus stesso.
B) VIRUS A RNA a polarità positiva non hanno bisogno di trascrivere il proprio
genoma perché il loro RNA viene tradotto direttamente dai ribosomi della
cellula. I virus ad RNA a polarità negativa possiedono un genoma che non
può essere tradotto e debbono quindi produrre mRNA utilizzando una
trascrittasi virale .
ASSEMBLAGGIO
• L’assemblaggio delle copie del genoma virale con le proteine strutturali
costituiscono nuove particelle virali
• Tutti i VIRUS A RNA si assemblano nel citoplasma delle cellule infettate
• I VIRUS A DNA si assemblano nel nucleo tranne i Poxvirus (citoplasma)
Liberazione
• Lisi cellulare
• Gemmazione
LIBERAZIONE
Acquisizione del mantello e liberazione
• Herpesvirus ( foglietto interno della membrana nucleare)
• Togavirus (reticolo endoplasmatico)
• La liberazione dei virus con pericapside avviene per gemmazione dal
reticolo endoplasmatico e dalle membrane del Golgi
• La liberazione dei virus senza pericapside avviene per lisi cellulare
causata dall’alterata permeabilità della membrana e dal blocco della
sintesi delle macromolecole cellulari
• Nella maggior parte dei virus con pericapside la maturazione del virus
avviene con la liberazione
scapsidazione
Mims et al. “Microbiologia Clinica” Ed. EMSI
Effetti dell’infezione virale sulla cellula ospite
• La moltiplicazione virale produce modifiche nella
cellula ospite. Ne derivano cambiamenti della
morfologia cellulare e alterazioni metaboliche,
genetiche e regolatorie che possono portare alla
morte cellulare o alla sua trasformazione.
Effetti dell’infezione virale sulla cellula ospite
Tipi di infezioni
- Citolitiche acute il virus si replica nella matrice
cellulare, la cellula si lisa liberando le nuove particelle
virali (caratteristica dei virus nudi); causa la morte
della cellula.
- Croniche ad equilibrio intorno al genoma si forma il
capside nel citoplasma cellulare, il nucleocapside si
avvicina alla membrana citoplasmatica e per
gemmazione si matura il virione rivestito
(pericapside); effetto citopatico ridotto.
- Integrate infezione trasformante, il genoma virale si
integra nel genoma della cellula ospite
determinandone una trasformazione permanente.
Infezione virale citolitica
Virus nudo
Virus rivestito
- Infezioni più frequenti
- Morte della cellula
- Virus rivestiti uccidono la cellula più lentamente di quelli nudi
Infezione virale cronica
Virus rivestito
- La cellula ospite non muore
- La cellula produce piccole quantità di virus per periodi di
tempo lunghi senza subire danni evidenti
Infezione virale integrata
- Genoma virale rimane nel nucleo in forma episomiale o
integrata
- Trasformazione neoplastica della cellula
Effetti dell’infezione virale
sulla cellula ospite
EFFETTO CITOPATICO
La moltiplicazione virale produce nella cellula
ospite cambiamenti della morfologia e alterazioni
metaboliche, genetiche e regolatorie che possono
determinare la morte della cellula o la sua
trasformazione
Alterazioni morfologiche
- Degenerazione e lisi della cellula (adenovirus)
- Formazioni di sincizi (fusione di più cellule) (retrovirus,
herpesvirus, paramixovirus)
- Formazioni di inclusioni nella cellula (ammassi di costituenti
virali o di strutture cellulari alterate, citomegalovirus)
- Modificazione dell’espressione delle proteine di membrana
(alterazione importante per il riconoscimento da parte delle
cellule del sistema immunitario)
Alterazioni metaboliche, genetiche
- Alterazione della permeabilità della membrana e dei
meccanismi di trasduzione del segnale intracellulare
- Inibizione della sintesi delle macromolecole cellulari
(DNA, RNA e proteine)
- Alterazioni cromosomiche (modifica stabile del
genoma cellulare)
LE INFEZIONI PERSISTENTI comprendono:
1) CRONICHE
(non litiche, produttive)
2) LATENTI ( sintesi limitata di macromolecole virali
ma senza produzione di virus. il virus
non è rilevabile negli intervalli tra
successive recidive)
3) LENTE (periodo di incubazione lungo)
4) TRASFORMANTI ( immortalizzazione)
VIRUS ONCOGENI
Alcuni virus a DNA ed alcuni Retrovirus stabiliscono infezioni persistenti che
possono anche stimolare una replicazione cellulare incontrollata, causando la
trasformazione o l’immortalizzazione delle cellule
•
Caratteristiche delle cellule trasformate
•
replicazione senza senescenza
•
alterazioni della morfologia
•
alterazioni del metabolismo
•
aumentato tasso di crescita cellulare
•
aumentato trasporto di zuccheri
•
perdita dell’inibizione da contatto
•
acquisizione della capacità di crescita in sospensione o in agar semisolido
QUESTI VIRUS IMMORTALIZZANO LE CELLULE:
1) Attivando o fornendo geni che stimolano la
proliferazione cellulare (oncogeni)
2)Rimuovendo i relativi meccanismi di inibizione che
limitano la sintesi del DNA e la crescita cellulare
(geni oncosoppressori)
PATOGENESI DELLE INFEZIONI VIRALI
PROCESSO ATTRAVERSO
IL QUALE UN’INFEZIONE VIRALE PROVOCA MALATTIA
Comprende cinque eventi principali:
a) Ingresso del virus nell’ospite
b) Replicazione del virus nella sede di primo impianto che può coincidere o
meno con la sede di ingresso
c) Diffusione locale o a distanza
d) Disseminazione agli organi bersaglio
e) Eliminazione del virus dall’organismo
MECCANISMI DI PATOGE\NESI VIRALE
•
La presenza o meno del pericapside è il principale fattore strutturale che
influenza la modalità della trasmissione virale.
VIRUS SENZA PERICAPSIDE:
•
Resistono all’essiccamento, all’azione dei detergenti, a condizioni
estreme di pH, di temperatura, all’ambiente acido dello stomaco,
all’azione della bile nell’intestino (virus trasmessi per via inalatoria, per via
oro-fecale e spesso acquisiti attraverso oggetti contaminati.
VIRUS CON PERICAPSIDE:
•
Labili. Sono trasmessi 1) attraverso goccioline respiratorie, sangue,
muco, saliva o sperma; 2) mediante inoculazione; 3) trapianto d’organo.
Questi virus sono labili in ambiente acido, ed al trattamento con
detergenti, caratteristica che rende impossibile la loro trasmissione per
via oro-fecale. Eccezioni sono l’HBV, e i Coronavirus.
MECCANISMI DI PATOGENESI VIRALE
Infezione del tessuto bersaglio
• Il virus riesce a penetrare nell’organismo attraverso discontinuità della cute
o attraverso le membrane mucoepiteliali che rivestono gli orifizi del corpo
(occhi, tratto respiratorio, bocca, genitali e il tratto gastro enterico)
• Dopo l’entrata il virus si può replicare e rimanere a livello del sito primario,
può diffondersi ad altri tessuti attraverso il circolo ematico ed il sistema
linfatico o può disseminare attraverso i neuroni.
MECCANISMI DI PATOGENESI VIRALE
• VETTORI: sono gli animali che fungono da vettori per
la diffusione della malattia virale ad altri animali,
all’uomo e ad altri ospiti
• SERBATOI: animali che mantengono ed amplificano la
diffusione del virus nell’ambiente
• ZOONOSI: le malattie virali che vengono condivise da
animali (Rabbia) o insetti ( Arbovirus,che includono i
togavirus, flaivirus, bunyavirus, reovirus)
e
dall’uomo.
MECCANISMI DI PATOGENESI VIRALE
•
Il trasporto del virus in circolo viene detto viremia. I virus
possono essere liberi nel sangue o in forma cellulo-associata
all’interno di linfociti e macrofagi
•
I virus che diffondono per via viremica possono raggiungere
organi diversi. Sono definiti organi bersaglio solo quelli in cui la
moltiplicazione virale conferisce all’infezione la sintomatologia
caratteristica
I virus possono raggiungere il SNC attraverso:
1)
il circolo ematico
2) le meningi o il liquido cerebrospinale infettati
3) neuroni periferici e sensoriali.
MECCANISMI DI PATOGENESI VIRALE
Di grande importanza sono anche le vie di
eliminazione del virus non solo per la diffusione
del virus ma anche per le strategie di
prevenzione.
L’eliminazione può avvenire attraverso la via
respiratoria, oro-fecale, urogenitale.
MECCANISMI DI PATOGENESI VIRALE
I virus causano malattia dopo
• Aver superato le barriere di difesa naturali
dell’organismo
• Aver eluso il controllo del sistema immunitario
• Aver distrutto le cellule di un tessuto importante
• Aver attivato una risposta immunitaria ed infiammatoria
distruttiva.
MECCANISMI DI PATOGENESI VIRALE
• La risposta immunitaria può costituire uno dei fattori
maggiormente responsabili della patogenesi di una infezione
virale.
• Il tessuto bersaglio del virus determina la natura della malattia
ed i suoi sintomi, mentre vari fattori virali e dell’ospite
determinano la gravità della malattia.
Questi fattori sono:
• il ceppo virale
• la consistenza dell’inoculo
• le condizioni generali di salute della persona infettata.
• L’efficacia della risposta immune della persona infettata
determina la gravità e la durata della malattia.
MECCANISMI DI PATOGENESI VIRALE
•
Ogni virus ha il suo tropismo tissutale.
•
Molti virus codificano funzioni (fattori di virulenza) che
promuovono l’efficienza di replicazione virale, la trasmissione
virale, l’accesso ed il legame del virus al tessuto bersaglio o
l’elusione da parte delle difese dell’ospite incluse quelle del
sistema immunitario.
Fasi fondamentali nella malattia virale sono:
1) Acquisizione ( ingresso nell’organismo)
2) Iniziazione dell’infezione al sito primario
3) Periodo d’incubazione
MECCANISMI DI PATOGENESI VIRALE
Il periodo d’incubazione può essere:
1) Asintomatico
2) produrre sintomi primari aspecifici
(fase prodromica)
3) fase sintomatica: causati dal danno tissutale e
dagli effetti sistemici causati dal virus e forse
dal sistema immunitario.
MECCANISMI DI PATOGENESI VIRALE
DIFESE DELL’OSPITE CONTRO LE INFEZIONI VIRALI:
•
barriere anatomiche naturali ( cute e mucose integre, muco, ciglia, acido gastrico,
lacrime, bile)
DIFESE IMMUNITARIE ASPECIFICHE (INNATE)
•
febbre, IFN, macrofagi, NK che provano a delimitare e controllare la replicazione
virale locale e la diffusione.
DIFESE IMMUNITARIE SPECIFICHE : RISPOSTA UMORALE E CMI
•
Th1--> CMI, IFN, CTL ( è necessaria per la lisi cellularenel caso d’infezioni non
citolitiche ( HAV) e delle infezioni causate da virus con mantello
•
Th2 --> risposta anticopale ( bloccano il virus durante la viremia)
•
Memoria immunitaria
MECCANISMI DI PATOGENESI VIRALE
INFEZIONE INAPPARENTE O ASINTOMATICA si verifica:
1) quando il tessuto infettato non viene danneggiato;
2) quando l’infezione viene controllata prima che il virus
raggiunga l’organo bersaglio
3) se il tessuto viene rapidamente riparato
4) se l’entità del danno è al di sotto della soglia di disfunzione.
Le infezioni asintomatiche rappresentano la
principale fonte di contagio
Antivirali
• I farmaci antivirali hanno come bersaglio enzimi codificati dal virus
oppure strutture virali importanti per la replicazione.
Virus trattabili con farmaci antivirali:
• Virus dell’Herpes simplex
• Virus della Varicella zooster
• Cytomegalovirus
• HIV
• Virus dell’influenza A
• Virus respiratorio sinciziale
• Virus dell’Epatite A,B e C
• Papillomavirus
• Picornavirus
Antivirali
• Bersagli dei farmaci antivirali:
• In base alle fasi di replica virale i potenziali bersagli dei farmaci
antivirali sono:
• L’adsorbimento
• Penetrazione
• Scapsidazione
• Trascrizione
• Sintesi proteica
• Replicazione del DNA ( polimerasi)
• Biosintesi dei nucleosidi
• Recupero dei nucleotidi ( Timidina chinasi)
• Modificazione delle glicoproteine
• Assemblaggio ( proteasi)
Antivirali
INTERFERONI
• INTERFERONI: Sono costituiti da una
classe di proteine con spiccata attività
antivirale capaci di indurre nelle cellule con
cui vengono a contatto uno stato di
resistenza antivirale legato alla produzione
di proteine dette effettrici.
• La loro azione non è virus-specifica ma
specie-specifica
INTERFERONI
• Tre tipi di interferon vengono indotti da stimoli
diversi:
a)Interferon α indotto da cellule estranee, tumorali,
batteriche o infettate da virus quando queste
vengono a contatto con cellule dendritiche
circolanti.
b)Interferon β indotto in cellule epiteliali, fibroblasti
e macrofagi in risposta ad RNA virale.
c)Interferon γ indotti in linfociti T stimolati da
antigeni ha un’attività essenzialmente
immunomodulante.
CELLULA INFETTA
Blocco della sintesi
proteica
Induzione di morte
(apoptosi)
CELLULA NON INFETTA
Mims et al. “Microbiologia Clinica” Ed. EMSI
INTERFERONI (IFN)
Famiglia di citochine
IFN di tipo I
(IFN-α, IFN-β, IFN-κ, IFN-δ, IFN-ε, IFN-τ, IFN-ζ, IFN-ω)
Si legano ad un singolo recettore IFNAR presente in tutte le
cellule del corpo.
IFN di tipo II
(IFN-γ)
Si lega al recettore IFNGR presente prevalentemente sulle cellule
del sistema immunitario.
IFN di tipo III
(3 sottotipi di IFN-γ)
Si legano al complesso recettoriale IFNLR e IL10R
• Proteine effettrici indotte dagli interferoni:
Oligoadenilato sintetasi che attiva una
ribonucleasi presente in forma inattiva nella
cellula, provocando la depolimerizzazione
dell’RNA virale.
Proteinchinasi che rende inattivo fosforilandolo il
fattore di iniziamento della sintesi proteica IF2.
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI (I)
Mediante il riconoscimento da parte dei recettori di ricognizione
(PRR), molecole PAMPs di origine virale attivano le cellule
dendritiche (fagocitarie).
L’attivazione determina la cascata di eventi intracellulari che
portano alla produzione di citochine proinfiammatorie e
interferoni.
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI (II)
In particolare gli interferoni determinano:
- Effetti sull’immunità innata
• reclutamento e attivazione delle cellule dendritiche
• reclutamento e maturazione di componenti cellulari del sistema
immunitario quali macrofagi (APC), neutrofili e cellule NK
- Effetti sull’immunità adattativa o acquisita
• reclutamento di linfociti T e interazione con le APC
- Effetti su cellule non appartenenti alla risposta immune
• modulazione della sintesi proteica ed induzione e
mantenimento dello stato antivirale
INTERAZIONE PRR-PAMPs
NELLA ATTIVAZIONE DELLA RISPOSTA INNATA DA PATOGENI VIRALI
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI (III)
Il sistema del complemento riconosce antigeni virali e si attiva
generando degli eventi a cascata che determinano:
- Effetti sull’immunità innata
• reclutamento e attivazione delle cellule fagocitarie e dei
granulociti nel sito di infezione.
• la “marcatura” (opsonizzazione) dei patogeni virali in modo da
renderli più aggredibili da parte delle cellule immunitarie.
• distruzione diretta dei patogeni (virus con envelope) attraverso
il complesso di membrana MAC.
• favoriscono la citotossicità verso cellule infettate.
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI
ATTIVAZIONE DELLA RISPOSTA INNATA DA PARTE DI PATOGENI VIRALI
CD = cellula dendritica
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI (IV)
L’attivazione della risposta adattativa nel corso dell’infezione virale:
• previene l’infezione di nuove cellule da parte dei virioni liberi
• elimina selettivamente le cellule già infettate
• linfociti T citotossici (CD8) hanno il ruolo fondamentale di
eliminare le cellule infettate.
Linfociti T citotossici (CD8+)
Dopo essere stati sensibilizzati dalle cellule APC riconoscono le cellule
infettate e le uccidono (effetto citotossico, morte della cellula infettata per
apoptosi).
Durante la replicazione le proteine virali vengono veicolate sulla superficie
della cellula infettata da molecole MHC-I (risposta MHC-I mediata). Questo
complesso viene riconosciuto dai linfociti T citotossici che producono fattori
tossici che uccidono la cellula infettata.
APC
MHC-I
Antigene
MHC-II
CD8+
APC
Cellula
infetta
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI (V)
•La risposta anticorpale previene l’infezione di nuove cellule da
parte del virus libero (neutralizzazione del virus), segnala la
presenza di antigeni virali sulle cellule infettate inducendo la
risposta citotossica NK e CD8 mediata da anticorpi (ADCC),
attivazione del complesso di membrana (lisi cellula infettata).
RISPOSTA DELL’OSPITE ALLE INFEZIONI VIRALI
ATTIVAZIONE DELLA IMMUNITA’ ACQUISITA DA PARTE DI PATOGENI VIRALI
CD = cellula dendritica
STRATEGIE DI ADATTAMENTO DEI VIRUS
Ogni virus mette in atto strategie diverse per replicare
efficacemente, nonostante la presenza dei meccanismi difensivi
dell’ospite.
Infezioni acute: da virus citolitici, ma caratterizzati da una rapida
replicazione nell’ospite e rapido passaggio ad altro ospite prima che
sia completamente attiva la risposta adattativa che rimuove il virus
(es. virus influenzale, virus del morbillo).
Infezioni persistenti: virus che riescono ad eludere le risposte
difensive (es. HIV, HCV) e con esse riescono a convivere. Infezione
lunga con manifestazione clinica nel tempo, dopo anni di
interazione virus-ospite. Anche i virus erpetici (herpesvirus) sono in
grado di persistere nell’ospite entrando in fase di latenza replicativa.
Si riattivano quando le difese dell’ospite diminuiscono.
ELUSIONE DELLA RISPOSTA DA PARTE DEI VIRUS.
Produzione di VIROCHINE, proteine che neutralizzando
l’effetto delle citochine prodotte dall’ospite. Effetto
immunomodulatorio. (es. proteina Tat di HIV).
Virus con envelope portano sulla superficie proteine presenti
sulla membrana dell’ospite (es. HIV, HTLV-1. virus Ebola).
Proteine virali possono bloccare nella cellula infettata la
risposta interferon o la cascata del segnale dei PRR (Toll like
receptor) (es. NS3 di HCV interagisce con la cascata del
TLR3).
Mutazioni del virus durante la replicazione, necessità di
produrre nuovi anticorpi per bloccarlo.