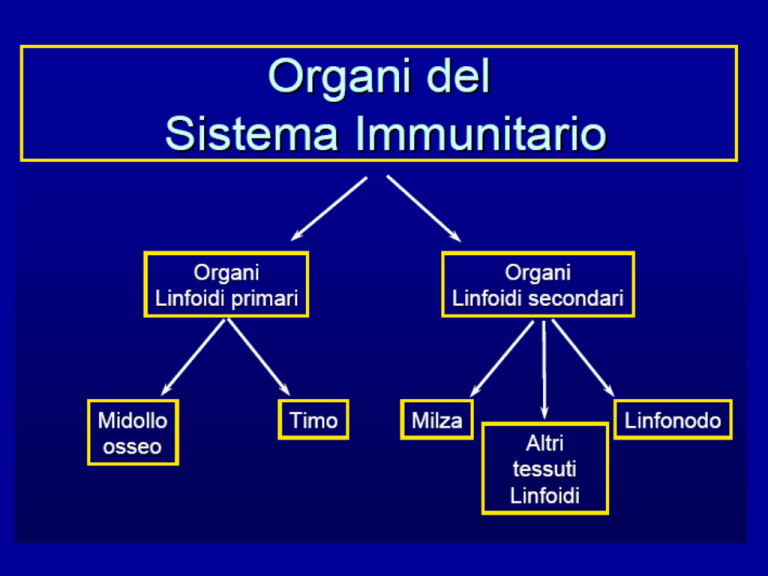
Organi del Sistema immunitario
Tonsille e adenoidi
Linfonodi
Vasi linfatici
Timo
Linfonodi
Milza
Placche di Peyer
Appendicite
Linfo nodi
Midollo osseo
Vasi linfatici
• Gli organi linfatici primari forniscono la sede in cui i linfociti
differenziano e vengono commissionati per l’antigene.
• I linfociti T maturano nel timo
• I linfociti B maturano nel midollo osseo (borsa di Fabrizio negli
uccelli)
• In entrambi i casi un processo selettivo elimina i linfociti immaturi
che riconoscono molecole self oppure riconoscono il MHC autologo
• Gli organi linfatici secondari catturano l’antigene e forniscono la
sede in cui i linfociti possono interagire con esso, andando incontro
alla proliferazione e alla differenziazione in cellule effettrici
• Il tessuto linfatico drena i tessuti e li intereconnette gli uni agli altri
• I linfonodi sono specializzati nel catturare gli Ag presenti nei tessuti
• La milza riceve gli Ag direttamente dal sangue
• Il tessuto meno organizzato si trova nelle membrane delle mucose
(follicoli linfatici dispersi nella lamina dell’intestino e nelle placche di
Peyer, site nella parete intestinale)
• Si possono individuare anche tessuti linfatici terziari: tessuti linfatici
associati alla cute
NEI TESSUTI SECONDARI AVVIENE L’INCONTRO
DEI LINFOCITI CIRCOLANTI CON I PATOGENI
E I LORO PRODOTTI METABOLICI TRASPORTATI
DA UN SITO DI INFEZIONE
Cellule della linea linfatica
• Linfociti sono il 20-40% dei globuli bianchi e
99% delle cellule presenti nella linfa
• Nel corpo umano ci sono circa 1011 linfociti
• Circolano nel sangue e nella linfa e possono
migrare nei diversi tessuti e organI linfatici
• Si dividono in
– Linfociti B
– Linfociti T
– Linfociti null (cellule natural Killer)
• I linfociti B e T quiescenti sono piccoli, mobili, indistinguibili
morfologicamente
• Quelle che non hanno incontrato l’Ag sono vergini (naive) e sono
quiescenti nella fase Go del ciclo cellulare (diametro 6 mm, piccoli
linfociti)
– Citoplasma scarso, cromatina molto addensata, pochi mitocondri
RE e Golgi poco sviluppati
• I linfociti che incontrano l’Ag diventano attivati ed entrano nella fase
G1, S, G2 e M del ciclo cellulare.
– Aumentano di volume (diametro 15 mm cellule blastiche o
linfoblasti) e si sviluppano gli altri organuli cellulari
I linfociti proliferano e differenziano in cellule effettrici e cellule
della memoria
Linfociti B
• Maturano nel midollo osseo
• Esprimono sulla superficie un recettore (Ab) specifico per un
antigene (Ab=antibody anticorpo)
• Dopo l’incontro con l’Ag maturano e si differenziano in Linfociti B
della memoria e linfociti effettori (plasmacellule)
• Linfociti B della memoria esprimono lo stesso Ab delle cellule
progenitrici
• Una plasmacellula sercerne più di 2.000 Ab al secondo
• Le plasmacellule muoiono in 1-2 settimane
Altre molecole di membrana dei
linfociti B
• B220 marcatore della linea linfocitaria B e dei suoi precursori
• Molecole MHC di classe II permette al linfocita B di
comportarsi come cellule presentante l’Ag
• CR1 e C2 recettori per alcuni prodotti del complemento
• Fcg/RII recettore per IgG
• B7-1 e B7-2 interagiscono con CD28 e CTLA-4, importanti
molecole presenti sui linfociti T
• CD40
interagisce con il CD40-ligando sulla superficie del linfocita TH
Cellule T
• Nascono nel midollo osseo e maturano nel timo
• Durante la maturazione esprimono sulla membrana uno
specifico recettore per l’Ag: recettore del linfocita T
(T cell receptor TCR)
• TCR riconosce Ag solo se è legato a proteine MHC,
glicoproteine polimorfiche, presentate da altre cellule
• Ci sono 2 sottopopolazioni di linfociti T:
– T helper (TH)
– Th1 e Th2
– T citotossiche (Tc) o killer
VH
VH
V
CH1 CH1
VL
CH2
CH2
Ig/Ig CH3
CH3
g e
VL
CL
CL
V
e d
C C
z z
Ig/Ig
fyn
lck
Zap 70
Blk, Fyn or Lyn
RECETTORE CELLULE B
RECETTORE CELLULE T
Cellule null
• Non esprimono le molecole caratteristiche dei linfociti T e
B
• Sono prive degli attributi fondamentali dell’immunità: la
specificità e la memoria
• Comprendono i linfociti natural killer (NK)
• Sono di aspetto granulare e rappresentanto il 5-10% dei
linfociti del sangue
• Svolgono un ruolo importante nei confronti delle cellule
tumorali e infettate da virus
Cellule dendritiche
• Le cellule dendritiche sono globuli bianchi che attivano il sistema
immunitario catturando gli antigeni ed esponendoli all’azione delle
cellule 'killer', i linfociti T.
• Queste cellule risiedono principalmente a livello di quei tessuti che
fungono da barriera con l'ambiente esterno e quindi sono più
facilmente raggiungibili da agenti patogeni (mucosa nasale,
polmonare, intestinale, gastrica e cute), dove ricoprono il ruolo di
vere e proprie 'sentinelle'.
• Quando vengono a contatto con agenti estranei
migrano a livello di quei tessuti che
servono da basi al sistema immunitario
(linfonodi), dove allertano le altre cellule
di questa complicata macchina che ci difende
dall'insorgenza di nuove malattie.
Gli strumenti del sistema immunitario
acquisito
• Immunoglobuline o Anticorpi
• Recettore delle cellule T
• Complesso maggiore di istocompatibilità e
proteine MHC su APC
• Cellule che presentano l’antigene (APC)
Antibody Molecule Structure
Ag binding
region
VH
N terminal
end
VL
CH1
disulfide
bonds
Heavy Chain
CH3
CHO
CH2
h
C terminal
end
Ag
CL
=
globular
domains
Y
•
•
•
•
•
•
•
•
•
•
•
2 catene leggere identiche (L, light, 220 aminoacidi)
2 catene pesanti identiche (H, heavy, 440 aminoacidi)
A forma di Y rovesciata
Ponti S-S fra le catene
2 siti di legame per Ag (bivalenti)
Zona di riconoscimento per Ag o Fab (Fragment Antigen
Binding) con sequenza di aminoacidi relativamente variabile
Zona costante o Fc (Fragment cristallizzabile) con sequenza
di aminoacidi relativamente costante
REGIONI IPER VARIABILI
La variabilità della sequenza di aminoacidi è confinata in 3
regioni ipervariabili (5-7 aminoacidi per L, 6-17 aminoacidi
per H)
Il sito antigenico è composto dalle regioni ipervariabili della
catena L e dalle regione ipervariabili della catena H
Alta costante di affinità Ig-Ag (104-1011 l/mole)
Papain Cleavage
Papain Cleavage
2 Fab
Fc
Pepsin Cleavage
Pepsin Cleavage
F(ab’)2
Enzymatic degradation
of Fc fragment.
Funzione effettrice
Legame a C4b
C fissazione
(legame a C1q )
Si lega a FcR
(Mac, Mono)
Si lega a FcR
(neutrofili; NK cells)
Come agiscono gli anticorpi
• Gli Ab eliminano gli Ag e uccidono i patogeni
utilizzando 3 funzioni effettrici principali:
– Opsonizzazione (fagocitosi dell’Ag da parte dei macrofagi e
neutrofili)
– Attivazione del complemento (IgM e sottoclassi di IgG)
– Interazione con i recettori Fc delle cellule NK
Classi di anticorpi
Esistono 2 tipi di catene leggere
– K (uomo 60%)
l (uomo 40%)
Esistono 5 classi di catene pesanti:
m, g, , d, e
Ognuna di queste diverse catene pesanti è chiamata
ISOTIPO
Ogni Ab è formato da 2 catene pesanti e 2 catene leggere
identiche H2L2, oppure è un multimero di questa struttura
base a 4 catene (H2L2)n
5 Classi di anticorpi nell’uomo
• Classe
catena
pesante
sottoclassi
catena
leggera
formula
molecolare
IgG
g
g1g2g3g4
K, l
g2K2, g2 l2
IgM
m
nessuna
K, l
(m2K2)n
(m2l2)n n=1 o 5
IgA
1, 2
K, l
(2K2)n
(2l2)n n=1,2,3,4
IgE
e
nessuna
K, l
(e2K2) (e2l2)
IgD
d
nessuna
K, l
(d2K2) (d2l2)
Immunoglobuline: struttura
IgG, IgD, IgE, and IgA
IgA
IgM
Funzione degli anticorpi
•
•
•
•
IgG:
Coinvolte nella risposta umorale
70% delle Ig sieriche
Azioni:
–
–
–
–
•
•
•
•
•
Opsonizzazione
Neutralizzazione di microbi e tossine
Attivazione del complemento per via classica
Attraversare la placenta
IgM:
Primi a comparire nel sangue in risposta ad antigeni
Potere agglutinante a causa dei molteplici siti disponibili
Attivatori del Complemento
Non attraversano la placenta
•
•
•
•
IgA:
Ig dimeriche
Sintetizzate da linfociti B dei tessuti linfoidi associati alle mucose
Presenti nelle secrezioni, latte, saliva, lacrime, etc.
– Impediscono l’aderenza di microrganismi.
– Scarsa attività opsonizzante
– Attivazione del complemento per via alternativa
• IgE:
• Reazioni di ipersensibilità di Tipo I (asma, febbre da fieno)
provocando il rilascio di citochine e mediatori infiammatori.
• Attivi nelle infezioni da parassiti favorendo l’attività citotossica degli
eosinofili.
• IgD:
• Ig di membrana espresse sulla superficie dei linfociti.
• Ruolo non chiarito, ma sono importanti drante la differenziazione dei
linfociti B.
Il sistema del Complemento
Sistema di Proteine attivate enzimaticamente dal legame di
un anticorpo ad un antigene che portano alla formazione di
un complesso terminale capace di attaccare e dissolvere la
parete batterica o la membrana di cellule tissutali.
Vie di Attivazione:
•Classica - In cui sono presenti tutti i componenti
attivata dal complesso antigene-anticorpo
•Alternativa – Innescata da membrane microbiche e
molecole non anticorpali. Assenza di alcuni componenti.
•Lectinica – Attivata da lectine plasmatiche che si
legano ai microrganismi.
Funzioni:
• Interazione con i recettori della superficie
cellulare per indurre la fagocitosi
– Molecole recettrici su polimorfonucleati, macrofagi e
frammento Fc degli anticorpi
• Produzione di componenti biologicamente attivi.
– Tramite proteolisi il complemento si attiva liberando
un frammento b che prende parte ad ulteriori reazioni
ed un frammento a che si comporta come mediatore
flogistico.
• Danno della membrana tramite il complesso
d’attacco
Complement
C2
C3
C3a
C5a
C1
C7
C6
C8
C5b
IgG
C5b
Antigen
C4
Enzyme
C3b
C5
C9
Complesso di attacco alla
membrana
C5a
C5
70-100 Å
C8
C9C9
C9
C9
C9
C9
C9
C9 C9
C9C9
C6 C5b C7
• Gli anticorpi vengono prodotti da tre distinte famiglie
geniche localizzate su cromosomi diversi:
per le catene leggere K
per le catene leggere l
per le catene pesanti
• Ogni famiglia genica contiene numerosi segmenti genici:
• Regione variabile V e J nella catena leggera
• Regione variabile V, D, J nella catena pesante
• Regione costante
Segmenti genici separati codificanti parti diverse delle
regioni variabili delle catene leggere e delle catene pesanti
vengono unite mediante fenomeni di ricombinazione nel
corso del differenziamento della cellule B
• I riarrangiamenti avvengono in ordine
sequenziale: prima quelli della catena pesante
poi quelli della catena leggera
• Sono finemente regolati, in modo tale che il DNA
di un solo cromosoma parentale venga
riarrangiato a formare un gene funzionale per la
catena leggera o pesante.
• Questa esclusione allelica assicura che Ab
maturo abbia la specificità antigenica singola
Cellule T
• Nascono nel midollo osseo e maturano nel timo
• Durante la maturazione esprimono sulla membrana uno
specifico recettore per l’Ag: recettore del linfocita T
(T cell receptor TCR)
• TCR riconosce Ag solo se è legato a proteine MHC,
glicoproteine polimorfiche
• Ci sono 2 sottopopolazioni di linfociti T:
– T helper (TH)
– T citotossiche (Tc)
• Il TCR riconosce solo Ag processati e associati a una
molecola MHC espressa da una cellula APC o da una
cellula bersaglio
• Il DNA del TCR è organizzato in domini variabili codificati
da diverse regioni geniche e costanti (come Ig)
• Meccanismi di ricombinazione simili a quelli delle Ig
• Cellule T presentano altre molecole accessorie di
interazione con le APC (cellule che presentano
l’antigene)
– CD40, CD2, CD28, CTLA-4
• Il TCR è associato al CD3, un complesso molecolare
Interazione APC e Linfocita T
CTLA-4
B7 (CD80/86)
B7 (CD80/86)
CD28
APC
CD58 (LFA-3)
Attivazione
CD154
(CD40L)
Attivazione
Riconoscimento
TCR
MHC II
Attivazione
CD2
CD4+
Adesione T Cell
CD40
2HN
T
Variabile
costante
NH2
T
V
V
Ogni catena è lunga 280 aa.
Omologia strutturale e di
Sequenza con gli Ab
Circa 100 geni V
50 geni J
Circa 30 geni V
Circa 12 geni J
C
C
membrana
COOH
COOH
Recettore cellule T
Memoria immunologica
• Le risposte immunitarie acquisite danno luogo alla
memoria immunologica di lunga durata e a una
immunità protettiva
• La risposta immunitaria primaria è sviluppata da un
numero limitato di linfociti
• L’intervallo necessario per la loro espansione numerica
fornisce al patogeno l’opportunità di avviare un processo
infettivo fino alla comparsa della malattia
• Il cloni della risposta primaria comprendono anche le
cellule della memoria di lunga durata, che rendono la
risposta più veloce e più intensa a una successiva
esposizione allo stesso patogeno
• L’intensità delle risposte secondarie può essere
sufficiente a respingere la malattia
• Tutte le specie di mammiferi possiedono un gruppo di
geni strettamente associati, il complesso maggiore di
Istocompatibilità (MHC), i cui prodotti proteici sono
coinvolti nel riconoscimento cellulare e nelle discriminazione
self e non-self.
Svolge un ruolo fondamentale nel determinare se un tessuto
trapiantato può essere accettato come self (istocompatibile) o
rigettato (istoincompatibile)
• MHC è fondamentale nello sviluppo delle risposte sia umorali che di
tipo cellulare
• I linfociti T riconoscono gli antigeni solo se associati a molecole MHC
• MHC è un gruppo di geni localizzato su un
ampio tratto del Cromosoma 6 (uomo) e
cromosoma 17 (topo)
• Viene denominato HLA (human leukocytes
antigen nell’uomo)
• I geni sono localizzati in regioni che
codificano 3 classi di proteine:
geni MHC di classe I codificate nelle regioni A, B, C
geni MHC di classe II codificati nelle regioni DP, DQ, DR
geni MHC di classe III
Le molecole MHC espresse da un individuo non si modificano
nel tempo e possono differire da quelle espresse da un altro
individuo della stessa specie
POLIMORFISMO
MHC è uno dei complessi genetici più polimorfici dei
vertebrati più evoluti e possiede un numero straordinariamente
elevato di alleli diversi per ciascun locus
Gli alleli differiscono del 5%-10% nella sequenza del DNA da un
individuo all’altro
Proteine MHC sulle cellule che
Presentano l’antigene
Antigen presenting cells (APC)
• Le molecole MHC di classe I e classe II legano il peptide derivante
dal processamento dell’Ag
• Gli Ag di classe I si associano a molecole derivanti da antigeni
endogeni
• Gli Ag di classe II legano molecole derivate da antigeni esogeni
• MHC di classe I sono su tutte le cellule (non specializzate)
– Fibroblasti, cellule gliali (cervello), cellule endoteliali, epiteliali,
ecc.
• MHC di classe II solo su cellule specializzate:
– Linfociti B
– Cellule dendritiche
– Macrofagi
LE MOLECOLE DI CLASSE I e II appartengono alla
superfamiglia delle immunoglobuline
Entrambe presentano l’antigene ai linfociti T
Le molecole di classe I sono espresse in tutte le
cellule nucleate che presentano gli antigeni endogeni
processati ai linfociti CD8+
Le molecole di classe II sono espresse solo in numero
limitato di cellule presentanti l’antigene (macrofagi,
cellule dendritiche, linfociti B) che presentano gli
antigeni esogeni processati ai linfociti CD4+
Restrizione immunitaria per le molecole MHC:
I linfociti T citotossici CD8 sono ristretti alla classe MHC I
I linfociti TH CD4 alle molecole di classe MHC II
A seconda della provenienza dell’antigene, intracellulare (endogeno)
o extracellulare (esogeno), il sistema immunitario viene attivato
in modo diverso
Antigeni esogeni: ciclo endocitico
Antigeni endogeni: ciclo citosolico
Trasportatore associato alla processazione dell’Ag
ubiquitina7ATP
Ag endogeni
complesso
proteasoma
peptidi
Endocitosi/
fagocitosi
Via endocitica
RE
esopeptidasi
Via citosolica
Ag esogeni
TAP
compartimenti
endocitari
peptidi
Complesso
MHCI/peptide
Aminoacidi
semplici
complesso
MHCII/peptide
SCHEMA GENERICO
Complesso
APC/MHC-pep/CellulaT
recettore
Cellula T
recettore
Peptide estraneo
Complesso peptide
estraneo/recettore/
MHC
MHC (I o II)
Cellula che presenta Ag
CD4/8
MHC
Peptide estraneo
Come viene
innescato
l’intero sistema
Linfociti T helper:
secernono citochine che favoriscono la risposta
umorale e cellulo-mediata.
Si attivano a contatto con uno specifico antigene
presentato da una molecola MHC di classe II (sulla
membrana di un macrofago o su un linfocita B).
Allo stesso tempo si generano linfociti T di memoria a
lunga vita.
Le risposte combinate dei linfociti T helper, dei linfociti
T citotossici e dei linfociti B controllano la specifica
rimozione di antigeni dannosi e forniscono l’immunità
permanente verso di essi.
La risposta immunitaria cellulo-mediata
si verifica quando i linfociti T citotossici
riconoscono uno specifico antigene presentato da
una molecola del complesso maggiore di
istocompatibilità MHC di classe I sulla
membrana di una cellula infettata da un virus o su
una cellula tumorale.
Si differenziano quindi in cellule (killer) assassine.
I linfociti T citotossici rilasciano perforine (
formano dei pori nella membrana della cellula
colpita) e frammentine (entrano nella cellula e
determinano la sua morte, apoptosi).
La risposta immunitaria umorale deriva
dall’attivazione dei linfociti B.
In seguito al contatto con specifici antigeni sulla
membrana del batterio, i linfociti B proliferano e si
differenziano in linfociti B di memoria a lunga vita e
plasma-cellule a vita breve.
Mentre i linfociti B di memoria sono responsabili
dell’immunità permanente ad un antigene, le
plasmacellule secernono anticorpi che si uniscono
ad un antigene bersaglio e quindi reclutano atri
fattori di difesa (per esempio cellule fagocitarie)
per distruggerlo.
Attivazione delle cellule T
• L’attivazione di una cellula T citotossica o helper
a proliferare e differenziarsi in cellula effettrice
avviene per interazione con la cellula che
presenta l’antigene, la quale deve trasmettere
alcuni segnali:
– 1° segnale: peptide estraneo legato alla proteina
MHC.
– 2° segnale: proteine stimolatrici, come le proteine B7
(CD80 e CD86) che sono riconosciute dal corecettore
CD28 sulle superficie della cellula T. Se le cellule T
helper ricevono entrambi i segnali, si attivano,
proliferano e secernono una citochina, chiamata
interluchina-2.
– 3° segnale: secrezione di interleuchine diverse
Le cellule T helper assumono il comando della risposta
immunitaria attivano tutte le altre cellule a proliferare
Attivazione di Cellule T da APC attivato
IL-1
IL-6
IL-12
IL-12 Recettore
CD28
“segnale 3”
B7
“Segnale 2”
CD4+
T cell
CD4
Recettore
Linf. T
LPS
TLR4
“Segnale 1”
Peptide
MHC II
Signal 1: Specificità
Signal 2: Attivazione
Signal 3: Differenziamento
Antigen Presenting Cell (APC)
• I meccanismi con cui le cellule T citotossiche
uccidono le cellule bersaglio infettate sono due:
– 1- rilascio di una proteina, la perforina, in grado di
formare pori sulla membrana della cellula infettata.
Questa proteina, dapprima conservata in vescicole
secretorie, viene rilasciata per esocitosi locale nel
punto di contatto con la cellula bersaglio. Da queste
vescicole sono rilasciate anche alcune proteasi, in
particolare la granzyme B, che attiva alcune caspasi,
innescando il processo apoptotico della cellula
– 2- Una proteina trimerica sulla superficie delle cellula
T citotossica , si lega e attiva la proteina Fas sulla
superficie della cellula bersaglio. La coda citosolica
della Fas contiene un dominio che, quando è attivato,
si lega a una proteina adattatrice e recluta la
procaspasi-8. La successiva attivazione della caspasi 8
da inizio alla cascata proteolitica che porta al
processo apoptotico.
Schema della risposta immunitaria
Ingestione patogeni (Macrofagi)
Digestione Patogeni
Frammenti di antigeni proteici del Patogeno vengolo legati al
MHC aulla membrana dei Macrofagi
I Macrofagi presentano l’antigene ai Linfociti T
Cellule T con recettori per l’antigene vengono sensibilizzate
Cellule T sensibilizzate si dividono
Cellule T helper
Stimolano le cellule
B esprimenti lo
stesso recettore
Cellule T Suppressor
Cellule T citotossiche
Distruggono
l’antigene
Inibiscono le Cellule B
con lo stesso recettore
antigenico
Cellule T helper
Cellule T suppressor
Stimolano le cellule
B esprimenti lo
stesso recettore
Inibiscono le Cellule B
aventi lo stesso recettore
Termine della
risposta
immunitaria
Divisione Cellule B
Plasmacellule
Cellule B di Memoria
Cellule B producono Ab
Anticorpi legano l’antigene
Attivano il Complemento
Aiutano I Fagociti a trovare gli antigeni
Distruggono l’antigene