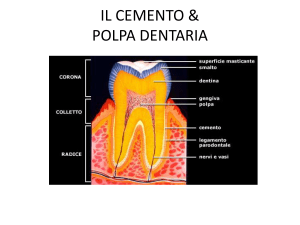
CAPITOLO 1
I LEGANTI
Inquadramento Normativo
Italia: Legge 1086 e successivi aggiornamenti quali D.M: 14/9/2005 «Norme
tecniche per le costruzioni»
Direttiva comunitaria: 89/106/EEC sui Prodotti della Costruzione del 1988.
Norme volontarie degli Enti di normazione UNI, ASTM, DIN, BS
EN, CEN
Vengono citate nelle leggi e capitolati appalti:
UNI EN 206-1 Calcestruzzo
UNI 11104 istruzioni per applicazione di UNI EN 206-1 in Italia
Uni EN 13670-1 Esecuzione di strutture di calcestruzzo- requisiti comini
LEGANTI E MISCELE LEGANTI
COSTRUIRE - Conglomerati: malte e calcestruzzi = materiale inerte tenuto insieme da
leganti
Il legante dà impasto plastico che solidifica facendo presa. E’ resistente. Mostra buona
adesione a pietre e laterizi.
Natura del legante: minerale, naturale (Conglomerati bituminosi), di sintesi
(calcestruzzi e malte di resina)
MISCELE LEGANTI:
• PASTA cemento + acqua
• MALTA cemento + acqua + sabbia
• CALCESTRUZZO cemnto + acqua + sabbia + ghiaia
Stagionatura o maturazione
Presa: fino a che l’impasto non è più sufficientemente plastico da essere
manipolato
-da qualche minuto a qualche giornoIndurimento: l’impasto già rappreso acquista resistenza meccanica –da qualch
eora a qualche meseAEREI, meno resistenti, ne fanno parte le calci UNI EN 459-1 (calci
vive, calci spente, calci idrate e grasselli)
Leganti
IDRAULICI cementi e cementi speciali, calci idrauliche ed
agglomerati cementizi (UNI EN 197-1), cementi da muratura (UNI EN
413-1
CEMENTO PORTLAND (miscela di clinker di Portland e gesso biidrato)
Argilla (silicati idrati di Al Fe, Mg)+
quarzo e calcare)
450-750°C
ossidi
Tabella 1.1 Denominazione, formula e formula nella notazione abbreviata dei composti
del clinker
Tabella 1.2 Componenti del cemento: formula e formula abbreviata
Tabella 1.3 Analisi chimica elementare di un cemento, percentuali in peso
TGA
Da questa composizione, mediante un metodo di calcolo proposto da Bogue, si può risalire al contenuto
percentuale dei composti mediante le seguenti equazioni in cui le formule rappresentano le percentuali dei vari
ossidi e dei composti sul peso del cemento.
C3S = 4,07.CaO – 7,6.SiO2 – 6,72.Al2O3 – 1,43.Fe2O3 – 2,85.SO3
C2S = 2,87.SiO2 – 0,754.C3S
C3A = 2.65.Al2O3 – 1,69.Fe2O3
C4AF = 3,04.Fe2O3
CaSO4.2H2O (gesso) = 2,15.SO3
Tabella 1.4 Analisi dei composti di un cemento Portland, percentuali in peso
Tabella 1.5 Limiti di composizione del cemento Portland
Fig.1.1 Schema del processo di fabbricazione del cemento
argilla
calcare
Cenere di pirite
Sabbia silicea
bauxite
Dispositivo preriscaldatore
Forno rotativo
mulino
Fino 1450 gradi
mulini
Altri additivi:
pozzolana, loppa,
ceneri, calcare
raffreddatore
Aggiunta di gesso biidrato
Figura 1.2 Sezione del clinker al microscopio
Silicato Tricalcico C3S
Tabella 1.6 Relazione tra le percentuali in peso degli ossidi e quelle dei
composti nel clinker del cemento Portland
Reagisce rapidamente con acqua conferendo agli impasti induriti elevata resistenza
meccanica
Se la cottura avviene a temperatura troppo bassa, nel prodotto ottenuto sarà presente,
anziché C3S, una miscela di C2S e CaO che, oltre ad avere scarse capacità leganti,
possiede un elevato tenore di CaO espansivo. Inoltre il C3S è stabile solo al di sopra di
1250 °C mentre sotto tale temperatura si decompone in silicato bicalcico e calce:
Si decompone sotto 700°C: si raffredda bruscamente il clinker per evitarlo!
C2S: forma polimorfa di tipo beta. Si idrata lentamente e quindi contribuisce alla
resistenza solo in tempi lunghi
C3A: si idrata rapidamente ma non contribuisce alla resistenza meccanica. Allumina ed
ossido di ferro sono necessarie per abbassare la T e formare fase liquida nella quale la
calce si scioglie dando C3S.
C4AF: si idrata rapidamente dando modesto contributo alla resistenza. Ha come sopra
funzione di fondente
COMPOSTI MINORI:
• CaO libero: se è >1% espansione e fessuratura
• MgO (non deve superare 2-2,5%) periclasio (no calcari dolomitici!)
• Fosfati e fluoruri
• Alcali (Na2O, K2O)
IDRATAZIONE
Fig .1.3 Idratazione di un granulo di cemento e formazione di uno strato continuo di prodotti di idratazione
Più finemente è macinato il clinker, maggiore è la velocità di idratazione.
Ponendo uguale a 1 la velocità di idratazione del cemento a 20°C, la velocità relativa Vi
a temperatura T da - 10 a 95 °C può essere calcolata con l’equazione seguente in cui R è
la costante dei gas (R = 8,314 J/mole) ed E (T) è un valore empirico dell’energia di
attivazione, pari a 33.500 per valori di T > 20 °C e pari a 34.970 × (20 – T) per valori di T
< 20 °C. Con questa equazione si ricava, ad esempio, che la velocità di idratazione a 60
°C è circa 5 volte quella a 20°, mentre a – 10 °C tale velocità risulta pari a circa il 2% di
quella a 20°
Fig. 1.4 a) Andamento dell’idratazione nel tempo del C3S; b) sviluppo di calore nelle
varie fasi; c) formazione di una pellicola continua di idrato; d) rottura della pellicola,
proiezione di soluzione e formazione di tubuli (fibre) di silicato idrato
Periodo di accelerazione
Fase dormiente
inizio
Periodo di rallentamento
La stechiometria dell’idratazione del silicato tricalcico può essere rappresentata nel modo di seguito indicato, in
cui x + z = 3 e x, y e z non sono generalmente numeri interi
La formula C3S2H3 indica una composizione media del prodotto di idratazione e sono riportati anche i pesi dei
prodotti reagenti e formati; infine, dato che il rapporto fra i vari componenti non è costante , per il silicato idrato
si può utilizzare più semplicemente la formula CSH
Fig. 1.5 Valori analitici di concentrazione di Ca e Si sul raggio di un granulo sferico di C3S sezionato
dopo un’idratazione parziale; la curva che dà il rapporto molare CaO/SiO2 che ne deriva evidenzia un
valore dello strato esterno dei prodotti di idratazione di circa 1,6
Fig. 1.6 Granuli di C3S idratati a vapore, a 2 ore, a 7500 ingrandimenti; si riconoscono il gel in forma di
fibre ad accrescimento radiale, tra di esse la porosità del gelo ed inoltre una porosità di maggiore
dimensione, la porosità capillare. Le fibre di granuli adiacenti stanno formando punti di contatto e
saldatura
0,1 micron
1 micron
Il prodotto di idratazione è ancora un gelo del tipo formato per idratazione del C3S, frammisto a cristalli di
idrossido di calcio
Rapporto CH/CSH favorevole per ottenere maggiore resistenza rispetto a C3S
a lungo termine
Fig. 1.7 Andamento dell’idratazione del silicato bicalcico nel tempo
Se il C3A reagisce con solo acqua forma degli alluminati idrati cristallini che si possono
rappresentare mediante la formula C3AH6. Se la reazione ha luogo in presenza di
idrossido di calcio, allora si forma, con velocità elevata, un alluminato dalla formula
C4AH13; questa reazione ha luogo con notevole sviluppo di calore e rapido
rapprendimento dell’impasto
Quando tutto il solfato di calcio scompare dalla fase acquosa, in conseguenza della reazione di formazione
dell’ettringite, quest’ultima, a contatto con H2O non più satura di CaSO4, diventa instabile e si trasforma in
monosolfalluminato di calcio idrato, designato anche monosolfato, secondo la reazione:
Fig. 1.8 Idratazione dei composti del cemento nel tempo
Fig. 1.9 Sviluppo della resistenza dei composti del cemento nel tempo, secondo Bogue
Falsa presa: dovuta a lavorazione sbagliata in produzione del gesso che non è biidrato e
quindi assorbe acqua.
Calore di idratazione
Il calore di idratazione Cidr del cemento si ricava per differenza applicando la
legge di Hess:
Tabella 1.7 Calore di idratazione (calorie per grammo)
Assumendo che in media la pressione parziale della CO2 sia pari a: pCO2 = 4,10-4 atm alla
temperatura di 25 °C, nell’acqua a contatto con l’aria si scioglie una quantità di CO2
ricavabile dall’espressione (legge di Henry)
La presenza di acido carbonico nell’acqua fa sì che essa reagisca con la pasta di cemento; la
reazione che avviene in due tempi: nel primo la calce idrolisi si trasforma in carbonato di
calcio insolubile:
La reazione precedente non è pericolosa e rende il calcestruzzo meno permeabile; in secondo tempo il CaCO3 è
trasformato in bicarbonato di calcio solubile. In definitiva, per azione dell’acqua aggressiva l’idrossido di calcio
delle paste di cemento è disciolto e asportato come bicarbonato solubile; la porosità aumenta e il pH della pasta
stessa, inizialmente di circa 13, scende a valori più bassi, cosicché anche il silicato di calcio idrato viene
aggredito.
In presenza di CaCO3 si può stabilire nell’acqua il seguente equilibrio che ad ogni temperatura possiede un ben
determinata costante di equilibrio e un rapporto di equilibrio fra la concentrazione di CO2 e quella di Ca(HCO3)2
CO2 dell’aria carbonatazione
Solfati
Ettringite espansione (ROTTURA)
VOLUME MOLARE DELL’ETINGITE Più DEL DOPPIO DEL VOLUME MOLARE DEL MONOSOLFATO
Pressione di cristallizzazione esercitata sui pori
𝑅𝑇
𝐶
P = 𝑉𝑠 log 𝐶
𝑠
R = costante gas
T = temperatura assoluta
Vs= volume molare del sale
C= concentrazione sovrasatura
Cs= concentrazione di saturazione
Per gesso biidrato se rapporto è 2 p= 30 MPa
R è la costante dei gas, T la temperatura assoluta, Vs il volume molare del sale; per la cristallizzazione del gesso
biidrato, con un rapporto C/Cs, pari a 2, la pressione così calcolata è di circa 30 MPa; se il suddetto rapporto sale
a 10, la pressione sale a circa 100 MPa
I solfati alcalini possono formare con l’idrossido di calcio, qualora la loro concentrazione sia così elevata da
superare il prodotto di solubilità del solfato di calcio, quest’ultimo sale. Ad esempio si avrà:
che produce effetti espansivi (Lea). In modo analogo si comporta il solfato di magnesio
PH si alza disgregazione ettringite
Azione aggressiva delle acque di mare in cui il solfato di Mg è di 3 g/l circa.
A temperature inferiori a 6°C, in presenza di carbonato di calcio, l’interazione dei solfati con la pasta
di cemento può portare alla formazione di un altro sale complesso, la thaumasite. Il carbonato di
calcio può essere presente come aggregato o nel terreno a contatto.
Cloruri
Attacco del calcestruzzo con meccanismo non ben definito
Pori del gelo
Porosità capillare
porosità
Fig.1.10 Ritiro della pasta di cemento al variare dell’umidità e della temperatura e
relativa perdita d’acqua
Tabella 1.8 Caratteristiche di vari tipi di porosità della pasta di cemento
Se si fanno reagire 100 g di cemento con 42 g d’acqua, la somma dei volumi di cemento
(Vc) e dell’acqua (Va) mescolati, pari al volume apparente della pasta (Vp) che non
cambia durante l’idratazione a meno di evaporazione verso l’esterno, è maggiore del
volume gelo di cemento (Vg) che è comprensivo sia dei prodotti solidi di reazione e del
cemento non ancora idratato (Vs) sia della porosità del gelo (Pg)
Questa disuguaglianza è spiegabile considernado Pc
Pc =Porosità capillare
Fig. 1.11 Modello di sviluppo di porosità della pasta di cemento
Fig.1.12 Variazione dei volumi in gioco durante l’idratazione del cemento. a) a/c = 0,42; b) a/c = 0,36
POWERS Vpc =(a/c - 0,36h)
h= grado di idratazione
Vpc è espresso in litri/Kg di cemento
Fig. 1.13 Porosità in funzione del grado di idratazione e del rapporto a/c
Fig. 1.14 Influenza della porosità sulla resistenza meccanica della posta di cemento.
POWERS
R = Kx3 =k(1-Ppc)3
R = k(1-(Vpc/(Vs+Vpc)))3
Fig. 1.15 Permeabilità della pasta di cemento in funzione della porosità capillare
TIPI DI CEMENTO PORTLAND E DERIVATI
Tabella 1.9 Limiti di composizione dei cementi Portland ASTM
Cemento Portland bianco
Ossido ferrico < 0,5%
Aggiunta di fondenti (CaF2 o NaAlF4)
Cemento portland ferrico o cemento Ferrari
Cemento resistente ai solfati, con tebnori più elevati di ossido ferrico e quindi con
poco C3A e molyop C4AF. Il rapporto tra Al2O3 e Fe2O3 deve esere prossimo a 0,64.
Cemento Portland al calcare
Al clinker viene aggiunta polvere di calcarae (CaCO3). Formazione di carboalluminati
migliore chiusura degli impasti cementizi (effetto tipico dei filler)
Cemento pozzolanico
Si può definire pozzolana ogni sostanza silicea o silico-aluminosa che, in forma
finemente suddivisa e in presenza d’acqua, sia capace di reagire a temperatura
ambiente con Ca(OH)2 per formare dei composti cementanti.
• alato contenuto di Silice
• Silice reattiva (non cristallina)
• Alta superficie per reagire con acqua e Ca(OH)2.
Pozzolane naturali
Materiali vulcanici incoerenti, la cui parte attiva è una fase vetrosa, costituita in
prevalenza (dal 50 al 100%) da silice e da allumina, contenent un gran numero di
canalicoli e bolle microscopiche.
Da reazioni vulcaniche esplosive –no etnaZone vulcaniche Lazio e Campania.
Anche i tufi pozzolanici ci sono in Italia, Grecia, Germania, usa urss
Terra di diatomee (scheletri di alghe microscopiche) (california, Canada, Algeria,
Danimarca e Germania)
Pozzolane artificiali
Cenere volante (fly ash) centrali a carbone (separatori elettrostatici)
60-90% di silice e allumina
Tabella 1.10 Analisi chimiche dei materiali pozzolanici naturali e artificiali
Cemento pozzolanico : Clinker + materiale pozzolanico + gesso biidrato
Il Ca(OH)2 ( circa 20% del Portland) reagisce con pozzolana e forma nuovo CSH. Le ceneri
danno anche C4AH13
Fig.1.16 Effetto della sostituzione del cemento con pozzolana sullo sviluppo di
resistenza del calcestruzzo
Calore di idratazione
inferiore a Portland ed
evoluzione più lenta.
Resistenza all’attacco acido, resistenza ad acqua di mare (formazione ettringite
grossolana, meno espansiva)
CEMENTO D’ALTOFORNO
Loppa da altoforno getti d’acqua fredda materiale granulare simile alla sabbia
Clinker + loppa + gesso
Il campo di variabilità delle concentrazioni degli ossidi principali, che
costituiscono le loppe basiche utilizzate per la produzione del cemento,
è riportato nella tabella seguente.
La loppa acquista proprietà leganti quando è mescolata con soluzioni di idrossido o solfato di
calcio (attivatori). Fungono dunque da attivatori il CH del Portland.
Forma CSH e CH.
Notevole sviluppo delle resistenza nel tempo ( più di portland e pozzolanico)
Bassi calori di idratazione (costruzioni massicce). Resistenza chimica migliorata rispetto al
Portland
CEMENTI NON PORTLAND
Cemento alluminoso
Privo di C3S e C2S. Bauxite rossa e calcare, 1500-1600°C. Costutuente principale CA ( > 60%
in peso)
Indurimento rapido, conversione soprà 30°c da alluminati idrati esagonali a cubici con
diminuzione di volume e sviluppo di porosità
Vantaggi: refrattario, , resistente ad acque solfatiche e aggressive
Fig. 1.17 Tempo di presa di miscela di cemento Portland e alluminoso
Riparazioni rapide
NORME sui cementi
NORMA UNI EN 197 sui cementi comuni
Tabella 1.11 Prospetto 1 – Tipi di
cemento e composizione. Percentuali
in massa 1)
Tabella 1.12 Prospetto II – requisiti chimici
Tabella 1.13 Prospetto III – requisiti meccanici e fisici
Fig. 1.18 Ago di Vicat per la misura dei tempi di presa
Tempo di inizio presa
Tempo di fine presa
Fig. 1.19 Permeametro di Blaine (per la misura delle superfici)
Superficie
specifica del
cemento
m2/Kg
S = c (t) 1/2
Fig. 1.20 Pinza di Le Chatelier
stabilità
Fig.1.21 Prove di flessione
40x40x160 mm
Carico che produce rottura
Resistenza a flessione
Rc = Pr/1600 N/mm2
Carico che produce rottura
Fig.1.22 Prova di compressione
Resistenza a compressione
Rc = Pr/1600 N/mm2
Dal carico che produce la rottura, Pr, si ricava la resistenza a compressione Rc con
l’equazione seguente, in cui 16 è la superficie delle piastre, in cm2. 16 è la superficie delle
piastre, in cm2.
Prove chimiche
Perdita al fuoco (950°C)
Residuo insolubile (HCl poi Na2CO3)
Contenuto di SO3
Contenuto di MgO
Cloruri
Pozzolanicità
Fig. 1.23 Grafico del saggio di Pozzolanicità
40 gradi. 8 giorni (saggio Fratini)
1. Determinazione alcalinità
2. Da grafico solubilità CaO
3. Dosare Ca(OH)2 in soluzione
Ca(OH)2 Ca2+ + 2 OH-
FORMALISMO reazioni
Trasporre le seguenti reazioni in notazione abbreviata:
Trasporre la notazione abbreviata in notazione estesa
Velocità di idratazione
Calcolare il rapporto tra la velocità di idratazione a 60°C rispetto a quella a 20°C di un
cemento (R = 8,314 J/mole).
Ponendo uguale a 1 la velocità di idratazione del cemento a 20°C, la velocità relativa Vi a temperatura T da
- 10 a 95 °C può essere calcolata con l’equazione seguente in cui R è la costante dei gas (R = 8,314 J/mole)
ed E (T) è un valore empirico dell’energia di attivazione, pari a 33.500 per valori di T > 20 °C e pari a
34.970 × (20 – T) per valori di T < 20 °C. Con questa equazione si ricava, ad esempio, che la velocità di
idratazione a 60 °C è circa 5 volte quella a 20°, mentre a – 10 °C tale velocità risulta pari a circa il 2% di
quella a 20°
V20 = 1
V60 = 5,2
Rapporto 5,2
Capitolo 2
Altri ingredienti del calcestruzzo
Fig. 2.1 Effetto della sostituzione del cemento con fumo di silice sulla resistenza a
compressione del calcestruzzo
Tabella 2.1 Caratteristiche e limiti di accettazione per le ceneri volanti impiegate come
aggiunta nel calcestruzzo secondo EN 450
Omogeneità e pozzolanicità
Fig. 2.2 Cenere volante al microscopio elettronico
Fig. 2.3 Influenza di aggiunte diverse e di diversa finezza di cenere volante sulla richiesta
d’acqua in calcestruzzo.
Si può ridurre dosaggio acqua
Tabella 2.2 Resistenza a compressione (Rc) a 2 giorni di calcestruzzi a slump = 80 mm,
cemento Cem I 32,5
Una possibilità migliore di tenere conto dell’aggiunta di cenere al calcestruzzo è quella di
applicare il coefficiente di equivalenza nel calcolo del rapporto a/c, per verificarne la
rispondenza al requisito del massimo valore richiesto ai fini della durabilità. A tale fine il
rapporto a/c si può valutare in base all’espressione seguente in cui f è il dosaggio di cenere
volante nel calcestruzzo
I limiti di composizione, oltre le quali le resistenze meccaniche
possono essere influenzate (considerando solo calcestruzzo non
armato)
Tabella 2.3 Limiti di composizione per acque di origine industriale