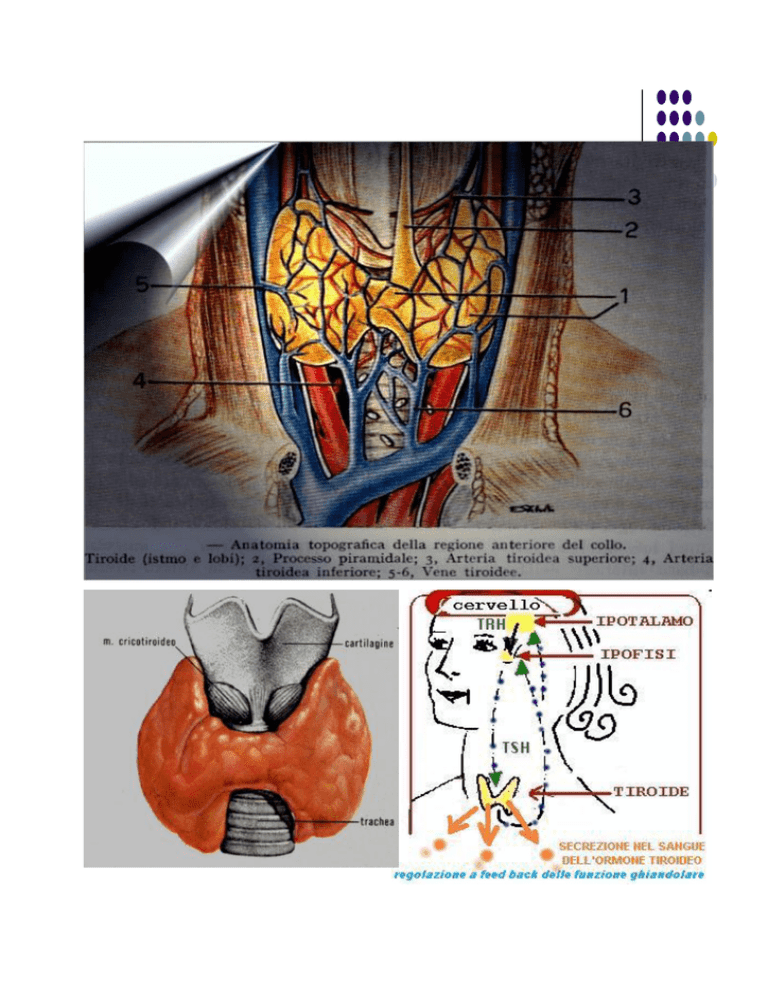
1
La tiroide inizia il suo sviluppo a 4 settimane dal concepimento,
originando come una struttura tubolare endodermica tra la prima e la
seconda tasca brachiale. Il diverticolo tiroideo si allunga lungo la linea
mediana del collo davanti all’osso ioide e alla laringe quindi si biforca e si
unisce agli elementi della quarta tasca brachiale formando la tiroide. La
struttura presente lungo il tragitto diventa il dotto tireoglosso che scompare
lasciando in genere la parte iniziale sotto forma di forame cieco della lingua
e la parte distale che forma il lobo piramidale. Nel contesto del parenchima
si trovano le cellule C che derivano dalla cresta neurale.
Nell’adulto la tiroide rappresenta la più voluminosa ghiandola a
secrezione interna, pesa circa 20 g è costituita da 2 lobi laterali, da un istmo
mediano e nell’80% dei casi dal lobo piramidale.
Essa avvolge le porzioni antero laterali della trachea e del laringe,
occupando con ogni lobo un’area tra trachea ed esofago medialmente,
carotide e muscolo sternocleidomastoideo lateralmente.
La ghiandola è rivestita da una capsula connettivale, da cui originano
setti fibrosi che penetrando nella ghiandola formano numerosi lobi e lobuli.
Ciascun lobulo è costituito da 20-40 follicoli tenuti assieme da una
sottile guaina connettivale, ogni lobulo è irrorato da una propria arteria e
drenato da una propria vena e costituisce l’unità di base anatomica e
funzionale della tiroide.
Al microscopio il follicolo si presenta come una struttura sferica sulle
cui pareti sono allineati, in unico strato, elementi cellulari cuboidali che
circondano il secreto chiamato colloide; esso contiene la tireoglobulina, un
precursore a basso peso molecolare degli ormoni attivi circolanti (T3 e T4).
Tra i follicoli sono disseminate le cellule C che secernono la calcitonina,
ormone ad influenza elettiva sul ricambio osseo e sul metabolismo calciofosforo.
Un’altra fascia connettivale circonda tutta la ghiandola la fascia
pretracheale o capsula chirurgica, anteriormente e lateralmente essa è
sottile e facilmente dissociabile, posteriormente è ispessita ed ha lo scopo di
fissare la ghiandola alle strutture posteriori (cartilagini tiroidea, cricoidea,
primi anelli tracheali) consentendole di muoversi durante la deglutizione.
2
3
4
La tiroide è riccamente vascolarizzata, essa è irrorata da due arterie pari, la
tiroidea superiore e la tiroidea inferiore, talvolta è presente un’arteria
mediana la tiroidea ima.
L’arteria tiroidea superiore è il primo ramo dell’arteria carotide esterna e
giunge alla tiroide nel suo polo superiore insieme alla vena tiroidea superiore
che drena il sangue nella vena giugulare interna.
L’arteria tiroidea inferiore è un ramo del tronco tireocervicale e giunge alla
tiroide nel suo polo inferiore insieme alla vena tiroidea inferiore, che drena
nella vena succlavia.
L’arteria tiroidea ima, quando è presente, origina dall’arco aortico.
Grosse vene a parete sottile si anastomizzano sulla capsula formando una
caratteristica rete superficiale, questo plesso venoso superiormente drena
attraverso la vena tiroidea superiore, inferiormente attraverso la vena tiroidea
inferiore e nella porzione mediana della ghiandola attraverso la vena tiroidea
media direttamente nella vena giugulare.
La prima zona di drenaggio linfatico è costituita dai linfonodi della linea
mediana (comparto centrale) al di sopra dell’istmo (linfonodi di Delphian) e
dai linfonodi mediastinici superiori, la zona successiva è quella dei linfonodi
laterali del collo lungo le vene giugulari interne.
Il nervo laringeo inferiore o ricorrente contrae intimi rapporti in profondità
con le pareti posteriori dei lobi poiché è situato nel solco tracheo-esofageo; a
sinistra, dovendo fare un’ansa attorno all’arco aortico, è situato più
profondamente che a destra.
La branca esterna del nervo laringeo superiore è collocata a destra vicino
all’arteria tiroidea superiore al di sopra del polo superiore della tiroide.
L’increzione di T3 e T4 è regolata dal TSH (Thyroid Stimulating Hormone)
ipofisario mediante un meccanismo a “feedback negativo” per cui all’aumento
degli ormoni tiroidei circolanti si ha un blocco della sintesi di TSH e viceversa;
la secrezione del TSH viene controllata anche dal TRH (Thyrotropin
Releasing Hormone), un neuropeptide sintetizzato dall’ipotalamo.
Gli ormoni tiroidei esercitano molteplici azioni metaboliche e non esiste
5
tessuto, organo o sistema che non sia influenzato dalla carenza o dall’eccesso
di questi ormoni.
6
Vie di migrazione della tiroide
dall’abbozzo primitivo
Principali sedi di ectopia vera
Gozzo plongeant retrosternale
7
Adenoma follicolare
Ø L’adenoma follicolare è una neoplasia
tiroidea benigna capsulata, con evidenza di
differenziazione cellulare follicolare. È la
neoplasia tiroidea più frequente, rilevata in una
percentuale variabile fra il 4% ed il 20% delle
tiroidi esaminate in corso di autopsia
ØSi osserva di preferenza nel sesso femminile e
in età media, ma frequente è l’insorgenza in età
puberale
Ø Usualmente solitario, possiede una capsula
fibrosa che risulta microscopicamente completa,
con una evidente differenza fra la struttura
tumorale ed il parenchima circostante che risulta
compresso dalla neoplasia. Possono esservi
numerosi noduli nel contesto di un gozzo
multinodulare
Ø Il diametro della lesione è variabile ma
compreso, mediamente, fra 10 e 30 mm
Ø I fenomeni di degenerazione intranodulare
risultano relativamente frequenti, ma meno che
nei noduli di gozzo iperplastico e colloidocistico, e possono includere emorragie, edema, 8
fibrosi, calcificazioni e degenerazione cistica
Adenoma follicolare
Anatomia patologica
l
l
l
Fattori predisponenti: carenza iodica, turbe
endocrine puberali, gravidanza, allattamento,
menopausa, ereditarietà
Presenza di numerosi piccoli follicoli che
contengono modesta quantità di colloide. Al
centro zone di fibrosi e focolai emorragici.
Istologicamente l’adenoma follicolare può
essere classificato in sottotipi, in relazione alle
dimensioni, alla presenza di follicoli ed al
grado di cellularità
l
Convenzionali
l
l
l
l
l
Trabecolare/solido (adenoma embrionale)
Microfollicolare (adenoma fetale)
Normofollicolare (adenoma semplice)
Macrofollicolare (adenoma colloidale)
Varianti
l
l
l
l
l
Adenoma trabecolare ialinizzante
Adenoma a cellule ossifile (o a cellule di Hürtle
o oncocitario)
Adenoma con iperplasia papillare
Adenoma tossico iperfunzionante
Adenoma ipercellulare atipico
9
l L’adenoma trabecolare ialinizzante rappresenta
una variante caratterizzata dall’aspetto ialino sia a
livello citoplasmatico che negli spazi extracellulari: può
richiamare la struttura del carcinoma papillare e
midollare ma è benigno
l Alcuni adenomi normofollicolari contengono
strutture pseudo-papillari che possono ingenerare
confusione con il carcinoma papillare: queste strutture
sono verosimilmente espressione morfologica di una
iperattività metabolica localizzata come dimostra la loro
preferenziale espressione in noduli dotati di autonomia
funzionale
l Questi tumori producono ormoni tiroidei in eccesso
indipendentemente dal TSH ed hanno una elevata
captazione dei radiofarmaci tireotropi rispetto al
rimanente parenchima ghiandolare. Quando queste
neoplasie sono associate ad ipertiroidismo vengono
definite come adenomi “tossici” di Plummer: le
cellule raggruppate in pseudo-papille tendono ad
assumere morfologia secretoria, simile a quella
osservabile in corso di morbo di Graves-Basedow
l Gli adenomi tiroidei clinicamente si manifestano come
noduli tiroidei solitari, indolenti spontaneamente ed alla
palpazione, di consistenza variabile, a superficie liscia,
mobili sui piani circostanti, ad accrescimento lento o
assente. Se sono di dimensioni notevoli possono dare
dispnea per compressione tracheale o disfagia per
compressione esofagea. Un improvviso aumento di
volume di un nodulo si accompagna a dolore intenso
ma transitorio alla regione cervicale
l La scintigrafia può rilevare sia noduli freddi (nei quali si
sono formate cospicue aree infartuali, emorragiche o
fibrotiche) che caldi (iperfunzionanti)
l L’emitiroidectomia rappresenta la terapia più efficace
nei noduli caldi solitari della tiroide perché intervento a
bassa morbilità. La strategia sarà diversa nei noduli
solitari freddi. Oggi a scopo preventivo è preferibile 10
eseguire una tiroidectomia totale
Scintigrafie
nodulo caldo
e freddo
Ecografia
nodulo
tiroideo
11
Adenomi a cellule di
Hürtle e atipici
l La variante citologica più importante e relativamente
rara dell’adenoma follicolare è rappresentata
dall’adenoma a cellule ossifile o a cellule di
Hürtle che risulta prevalentemente composto da
grandi cellule con citoplasma eosinofilo e granulare.
L’ultrastruttura di tali cellule dimostra numerosi
mitocondri ed esibisce pleiomorfismo nucleare con
presenza di nucleoli distinti. Le cellule si ammassano
tra loro formando una struttura colonnare. Queste
neoplasie sono tutte potenzialmente maligne anche se
il decorso clinico risulta strettamente correlato con
l’aspetto istologico iniziale e l’assenza di invasività
predice un andamento benigno; alcuni li definiscono
carcinoma a bassa malignità (low grade carcinoma)
l Gli adenomi atipici sono lesioni ipercellulate con
aspetti istologici suggestivi per una evoluzione
maligna ma che non presentano segni di invasività.
Rappresentano il 3% circa degli adenomi follicolari ed
il monitoraggio dei pazienti nel tempo indica una
evoluzione generalmente benigna anche se alcuni
Autori preferiscono classificare queste lesioni come
adenocarcinomi pre-invasivi o carcinomi follicolari in
situ. Il fatto che la neoplasia non vada incontro a
recidiva o metastatizzazione dopo exeresi chirurgica
non prova in via definitiva la benignità della lesione: in
effetti l’escissione potrebbe interrompere l’evoluzione
naturale della lesione verso la diffusione
12
Interventi chirurgici
13
14
15
16
Gozzo immerso con
versamento pleurico
17
Complicanze della
chirurgia tiroidea
l
Acute (insorgono rapidamente, mettono in
pericolo la vita del paziente, richiedono un
trattamento immediato)
l
l
l
l
l
l
l
l
Emorragia
Insufficienza respiratoria acuta
Lesione bilaterale dei nervi ricorrenti
Ipoparatiroidismo acuto
Crisi tireotossica
Pneumotorace
Perforazione della trachea o dell’esofago
Croniche
l
l
l
l
l
Lesione unilaterale del nervo ricorrente
Lesione del nervo laringeo superiore
Ipoparatiroidismo postoperatorio
(permanente, transitorio, subclinico)
Ipotiroidismo postoperatorio e mixedema
Coma mixedematoso
18
Tumori della tiroide
Prof. Salvatore Gorgone
1
Tumori differenziati
della Tiroide
Epidemiologia
w All’esame autoptico incidenza dell’1,7% in una
popolazione non selezionata
w Tale percentuale aumenta nelle Hawaii, in Cina e
Giappone, nell’area di Hiroshima e Nagasaki
raggiunge il 20%
w Rari nei bambini, aumentano di frequenza con l’età
w Maggiore incidenza tra i 25 e i 65 anni
w Tre volte più frequenti nelle donne che nell’uomo
w Più frequenti in aree di endemia gozzigena
w La mortalità annua negli Stati Uniti è di
4/milione/anno per gli uomini e di 5/milione/anno
per le donne
w La bassa mortalità rispetto alla incidenza è dovuta
alla scarsa malignità dei carcinomi differenziati
della tiroide
w La sopravvivenza a 20 anni raggiunge il 95% per i
pazienti con adenocarcinoma papillare e l’80%
per quelli con adenocarcinoma follicolare
Prof. Salvatore Gorgone
2
Fattori predisponenti
w L’irradiazione del collo in età infantile o
nell’adolescenza è un fattore certo ed è in
rapporto alla dose ricevuta e alla particolare
radiosensibilità della tiroide in età pediatrica
w L’80% dei giovani con carcinoma tiroideo
hanno subito irradiazione per iperplasia
timica o tonsillare, acne
w Tra gli anni ‘30 e ‘50 numerosi adulti furono
irradiati per malattia di Basedow, tuttavia in
questa popolazione non si è avuto un
significativo aumento di carcinomi tiroidei
w Dopo Tchernobyl si è avuto un modico
aumento delle neoplasie tiroidee in Europa,
mentre in Ucraina e Bielorussia nei bambini
c’è stato un notevole incremento di
carcinomi tiroidei papillari plurifocali
particolarmente aggressivi e metastatizzanti
Prof. Salvatore Gorgone
3
Fattori predisponenti
vL’esposizione alle radiazioni ionizzanti per irradiazione
esterna del collo aumenta l’incidenza di noduli tiroidei, sia
benigni che maligni: noduli palpabili sono rilevabili nel 20-30%
di popolazioni esposte a radiazioni
vIl periodo di latenza fra esposizione ed evidenza clinica di
malattia è di almeno 4-5 anni e diviene massimale a circa 20
anni all’esposizione per decrescere successivamente
vIl rischio aumenta a partire da dosi medie superiori a 10 cGy e
per dosi fino a 1500 cGy è osservabile una relazione lineare
dose-rischio di carcinoma. Per dosi superiori il rischio decresce
probabilmente in relazione alla necrosi cellulare radioindotta
vIl fattore di rischio principale è rappresentato dall’età del
paziente al momento della irradiazione e dopo i 15-20 anni non
si osserva più incremento del rischio
vL’incidenza del carcinoma tiroideo è in incremento in molte
aree del mondo, soprattutto nelle fasce di età inferiori ai 55 anni,
ed è dimostrata una importante variabilità dell’epidemiologia
delle neoplasie tiroidee nelle varie aree geografiche
Prof. Salvatore Gorgone
4
Adenocarcinoma
papillare
w È il tumore maligno più frequente,
(85% di tutti i tumori tiroidei)
w Colpisce prevalentemente tra i 30 e i
40 anni
w Ha tendenza a rimanere localizzato
nella ghiandola e quando metastatizza
diffonde alle stazioni linfonodali del
mediastino superiore e cervicali
w Può localizzarsi ovunque nella
ghiandola tiroidea e si presenta come
una lesione nodulare di diametro
superiore a 15 mm adesa alla struttura
ghiandolare parzialmente capsulato
“un tumore epiteliale maligno che dimostra evidenza di
differenziazione cellulare follicolare, caratterizzato dalla
formazione di papille e/o da una varietà di alterazioni nucleari”
Prof. Salvatore Gorgone
5
Storia Naturale
w L’80% dei bambini ed il 20% degli adulti
presentano all’esame clinico linfonodi
palpabili; spesso i linfonodi sono di
dimensioni molto superiori allo stesso tumore
primitivo, che può non essere rilevato alla
palpazione
w Più grave ai fini prognostici è il superamento
della capsula tiroidea che può giungere fino
all’invasione di importanti strutture adiacenti
(trachea, esofago, nervo ricorrente)
w Per via ematogena il tumore metastatizza ai
polmoni ed alle ossa (2%)
w L’adenocarcinoma papillare può presentarsi
come nodulo solitario o frequentemente essere
multicentrico. Il nodulo piccolo o piccolissimo
(4 mm) è di colorito bianco grigiastro, con
superficie irregolare, di consistenza solida o
cistica
Prof. Salvatore Gorgone
6
Anatomia patologica
w La superficie di taglio è ruvida per la presenza di minute
deposizioni di calcio; se esistono formazioni cistiche il
contenuto è di tipo acquoso e di colorito bruno
w Al microscopio strati singoli o multipli di cellule di tipo
cuboidale, con nuclei voluminosi che presentano modeste
atipie e scarse mitosi. Queste cellule rivestono formazioni
che si aggettano nel lume di cisti
w La papilla neoplastica contiene generalmente un “core”
centrale di tessuto fibro-vascolare che non è rilevabile
nell’ipertrofia follicolare
Prof. Salvatore Gorgone
7
Anatomia Patologica
w Nello stroma delle formazioni papillari si
trovano patognomoniche formazioni
rotondeggianti che vanno incontro a
calcificazione “corpi psammomatosi”
(rappresentano cellule necrotizzate), visibili
anche all’esame radiologico
w La presenza di formazioni follicolari, nel
16% dei casi, consente di identificare il
carcinoma misto o variante follicolare
dell’adenocarcinoma papillare
w Una diversa variante è rappresentata dalla
forma sclerosante, caratterizzata dalla
diffuso interessamento linfatico e fibrotico
w Le varianti a cellule colonnari o quella
“tall-cell” sono costituite da nuclei
prominenti o da papille ricoperte da cellule
circa due volte più alte che nell’istotipo
tipico
Prof. Salvatore Gorgone
8
Pazienti ad “alto rischio”
Un paziente con patologia nodulare è
considerato “ad alto rischio” nei seguenti casi:
n
n
n
n
n
n
n
n
n
n
nodulo singolo;
TSH normale;
età < 20 anni o >45 anni;
sesso maschile;
pregressa RT in età infantile;
dato anamnestico di recente evolutività o di
aumento dimensionale dopo terapia soppressiva;
dimensioni del nodulo (o di quello dominante in
caso di multinodularità) > 3 cm;
caratteristiche fisiche (durezza);
presenza di linfonodi cervicali;
vascolarizzazione interna e/o anarchica all’EcoDoppler e presenza di microcalcificazioni
Prof. Salvatore Gorgone
9
Sintomatologia e
Diagnosi
w L’adenocarcinoma papillare è un tumore che cresce molto
lentamente
w La sintomatologia soggettiva è molto tardiva ed è riferibile
solo alla invasione locale. Consiste nel dolore alla regione
anteriore del collo, nella voce bitonale o nella disfonia per
infiltrazione dei nervi ricorrenti con paresi o paralisi delle
corde vocali, nella disfagia, nella dispnea
w L’indagine clinica è rivolta alla ricerca di una tumefazione
palpabile e di eventuali tumefazioni cervicali
w Il semplice esame clinico non consente di differenziare
con certezza, specie nelle fasi iniziali, un adenoma da un
adenocarcinoma
w Il 3% dei noduli con caratteristiche cliniche di benignità
all’esame istologico si rivelano essere carcinomi
differenziati
w La malattia risulta confinata in ambito cervicale nel 9399% dei casi alla diagnosi e la diffusione in ambito
linfonodale mediastinico è generalmente associata e
preceduta da un diffuso coinvolgimento linfonodale
cervicale; solo una minima parte di pazienti (1-7%)
presentano metastasi a distanza diagnosticate prima o entro
30 giorni dall’intervento chirurgico
Prof. Salvatore Gorgone
10
Esami per l’inquadramento
diagnostico dei pazienti con
nodulo tiroideo
w Esami di laboratorio: FT3, FT4, TSH,
TRG, AbTRG, AbTPO, TRAB,
calcitonina, Ioduria
w Ecografia tiroidea, Eco Doppler
w Scintigrafia tiroidea con 99mTc di
base e dopo stimolo soppressivo
w Esame citologico con agoaspirato
(eventualmente ecoguidato)
w RX standard (esofago e trachea, torace),
TC, RM
w Ricerca di mutazioni germinali protooncogene RET
w FDG-PET
Prof. Salvatore Gorgone
11
Diagnosi
w Gli esami tireo-metabolici sono in genere nei
limiti della norma, eccetto che per un costante
aumento dei livelli di tireoglobulina, poco
significativo ai fini diagnostici
w Il dosaggio della tireoglobulina e del CEA
rivelano la loro importanza nel monitoraggio
postoperatorio dopo tiroidectomia totale: un
loro aumento dopo periodi di normalità è
indicativo di metastatizzazione, un loro
mancato ritorno alla normalità dopo intervento
chirurgico sta ad indicare un processo di
metastatizzazione in atto o una incompleta
tiroidectomia
w In presenza di patologia nodulare tiroidea è
sufficiente il dosaggio del TSH circolante,
senza aggiungere altre determinazioni, per
valutare l’assetto funzionale tiroideo. Infatti,
alla normalità del TSH corrisponde la normalità
degli ormoni tiroidei circolanti (il TSH si
modifica prima di una variazione degli ormoni
tiroidei in circolo)
Prof. Salvatore Gorgone
12
Diagnosi
Cesio,
indicatore
positivo
Iodio
131
w La scintigrafia tiroidea evidenzia un
nodulo freddo
w L’ecotomografia mette in evidenza
un’ecostruttura solida disomogenea
che in fase avanzata non è ben
delimitata dai tessuti vicini
w La TC e la RM evidenziano piccoli
noduli indovati nel parenchima o in
gozzi retrosternali
w L’esame citologico da agoaspirato
con ago sottile permette una diagnosi
accurata in un’alta percentuale di casi
Prof. Salvatore Gorgone
13
L’iter diagnostico di un nodulo tiroideo inizia
nel momento in cui esso viene identificato
clinicamente mediante palpazione
Prof. Salvatore Gorgone
14
Prognosi
w L’adenocarcinoma papillare è un
tumore a prognosi favorevole
w Sopravvivenza a 5 anni superiore al
90% e a 10 anni dell’80%
w Nel tempo può trasformasi in una
forma a malignità più elevata. La
maggior parte dei tumori papillari
non modifica le sue caratteristiche
strutturali, ma alcuni dopo un lungo
periodo di latenza improvvisamente
entrano in fase di anaplasia,
aumentano la loro invasività locale e
a distanza e possono provocare la
morte per metastatizzazione
Prof. Salvatore Gorgone
15
Prognosi
w Allo scopo di unicare l’interpretazione dei dati relativi alla
prognosi è stato definito un sistema a punteggio (score),
denominato AMES score e basato sui parametri età (Age),
metastasi (Metastasis), estensione della malattia
(Extension) e dimensioni del tumore primario (Size).
Successivamente è stata aggiunta anche la valutazione
della ploidia del DNA (DNA-ploidia) tumorale mediante
citometria a flusso (DAMES score)
w Un ulteriore metodo di valutazione a punteggio (AGES
score) è stato sviluppato in relazione ai parametri età
(Age), grado di differenziazione (Grade), estensione della
malattia (Extension) e dimensioni del tumore primario
(Size). Mediante l’applicazione di questo sistema, l’86%
dei pazienti rientrano nel gruppo di rischio minimo (AGES
score >4) con un rischio associato di mortalità specifica
dell’1%. Viceversa i pazienti con AGES score superiori
rientrano in categorie di alto rischio con una mortalità
specifica associata del 40%
w L’impiego di sistemi di valutazione del rischio prognostico
rendono possibile l’ottimizzazione del piano di trattamento
post-chirurgico del paziente
Prof. Salvatore Gorgone
16
Terapia
w Il trattamento elettivo è la tiroidectomia
totale con conservazione delle paratiroidi e
rispetto dei nervi ricorrenti
w Nei piccoli carcinomi (<1 cm) possibile la
lobectomia totale con istmectomia o la
tiroidectomia subtotale
w Tutti questi interventi sono efficaci e
consentono una sopravvivenza dell’80% a 10
anni ma presentano una percentuale del 7% di
recidive nel lobo controlaterale
w Lo svuotamento linfonodale laterocervicale in
genere è occasionale su linfonodi invasi
macroscopicamente quali quelli palpabili, di
colorito blu nero, (picking) che possono essere
rimossi singolarmente; di routine la
linfoadenectomia del comparto centrale
w Il trattamento con I131 in aggiunta alla
tiroidectomia è da attuare al III e IV stadio se
la captazione dello iodio è buona, altrimenti si
potrà ricorrere alla radioterapia esterna
w Trattamento con L-tiroxina a scopo sostitutivo
Prof. Salvatore Gorgone
17
Adenocarcinoma
follicolare
w Rappresenta il 10% di tutte le neoplasie
maligne della tiroide
w Predilige la fascia d’età compresa tra i 30 e i
50 anni
w Può essere definito come un tumore a lenta
crescita e con prognosi relativamente
favorevole, comunque è più aggressivo e
pericoloso del carcinoma papillare
w È più frequente nelle donne che negli
uomini (3:1)
w Presenta una incidenza dipendente
dall’apporto iodico: infatti la sua incidenza è
del 2-5% nelle aree geografiche dove
l’apporto iodico risulta sufficiente mentre in
aree iodo-carenti esso rappresenta fino al
25-30% delle neoplasie tiroidee
“una neoplasia epiteliale che presenta evidenza di differenziazione
cellulare follicolare ma perde le caratteristiche diagnostiche tipiche
del carcinoma papillare”.
Prof. Salvatore Gorgone
18
Storia naturale
w Metastatizza prevalentemente per via
ematogena ai polmoni e alle ossa (12% dei
casi) provocando lesioni osteolitiche
soprattutto a carico del cingolo scapolo
omerale, dello sterno e del cranio
w Sia il tumore che le metastasi mantengono
la capacità di captare e trattenere lo iodio
radioattivo
w Le metastasi ossee possono comparire anche
20 anni dopo l’exeresi chirurgica del tumore
primitivo
w Il carcinoma follicolare presenta
generalmente dimensioni maggiori rispetto
al papillare ed un grado di differenziazione
minore
Prof. Salvatore Gorgone
19
Anatomia Patologica
w Il carcinoma follicolare può
presentarsi ben capsulato o essere di
tipo invasivo
w Quando è di tipo circoscritto e
capsulato ha caratteristiche
macroscopiche simili a quelle di un
nodulo adenomatoso e al suo interno
possono verificarsi fenomeni
degenerativi simili a quelli degli
adenomi: emorragie, infarti, cisti,
fibrosi e calcificazioni
Prof. Salvatore Gorgone
20
Anatomia Patologica
w Istologicamente il carcinoma follicolare ha
caratteristiche strutturali simili a quelli degli adenomi
follicolari: cellule epiteliali cubiche con nuclei grandi
formano follicoli ripieni di colloide densa
w L’invasione della capsula, del parenchima
ghiandolare vicino, l’invasione dei linfatici e dei vasi
sanguigni, la presenza di uniforme aumento delle
dimensioni cellulari con ipercromia nucleare
consentono di porre diagnosi di carcinoma follicolare
della tiroide
Prof. Salvatore Gorgone
21
Anatomia Patologica
w Nella sua forma meno differenziata,
carcinoma insulare, manifesta una
particolare aggressività che lo rende
simile al carcinoma anaplastico, ma
essendo in grado di concentrare lo
Iodio131 risponde al trattamento
radiometabolico
w Il tumore a cellule di Hürthle è
costituito da cellule, che formano
colonne, di grosse dimensioni ricche
di citoplasma ad aspetto granulare e di
nuclei voluminosi con nucleoli
evidenti. Le atipie sono frequenti, ha
tendenza alla invasività locale, alla
metastatizzazione, a recidivare dopo
chirurgia
Prof. Salvatore Gorgone
22
Anatomia Patologica
w Le metastasi linfonodali sono estremamente rare nel
FTC tipico ed il tasso di recidiva linfonodale si attesta
intorno a 1% e 2% a 10 e 20 anni, rispettivamente. Il
6% circa dei tumori a cellule di Hurtle presenta invece
coinvolgimento linfonodale alla diagnosi ma il tasso di
recidiva linfonodale a 20 e 30 anni dalla diagnosi sale al
18% e 24%
w La prognosi del carcinoma follicolare è in rapporto al
grado di invasione rilevato all’esame istologico: se
l’invasione è minima essa è favorevole, se il tumore
mostra segni di aggressività la sopravvivenza a 5 anni è
inferiore al 50%
w Metastasi a distanza all’esordio, età del paziente
superiore a 45 anni, voluminose dimensioni del tumore
primitivo e presenza di invasione loco-regionale extratiroidea rappresentano fattori prognostici negativi. Con
minore significatività anche il sesso maschile ed un
grado di de-differenziazione tumorale elevato si
associano ad una prognosi peggiore. L’invasione
vascolare, il coinvolgimento linfatico alla presentazione,
l’aneuploidia del DNA nucleare e l’istotipo a cellule
ossifile rappresentano potenziali variabili prognostiche
peculiari del carcinoma follicolare della tiroide
Prof. Salvatore Gorgone
23
Terapia
w La tiroidectomia totale con svuotamento linfonodale nei
casi in cui si è avuto il superamento della capsula
w Sarà così possibile effettuare una scintigrafia total body
con I131 per l’identificazione e il trattamento
radiometabolico di eventuali metastasi scheletriche
w Per la sua scarsa capacità di invasione dei linfonodi si
potrà evitare lo svuotamento linfonodale di principio
specialmente se la neoplasia appare ben capsulata
w Ai pazienti tiroidectomizzati si somministra L-tiroxina
sia per mantenere uno stato di eutiroidismo sia per
prevenire la comparsa di recidive neoplastiche
w L’elevata concentrazione ematica di TSH provocata
dalla tiroidectomia è uno stimolo all’accrescimento di
piccoli focolai metastatici. È necessario somministrare
L-tiroxina a dosi sufficienti a sopprimere la secrezione
di TSH
w La chemioterapia è riservata alle forme diffuse
Prof. Salvatore Gorgone
24
Linfonodo sentinella
nel Carcinoma Tiroideo
w Utile alternativa alla linfoadenectomia elettiva
w Supporto decisionale nella selezione di pazienti che
necessitano di una chirurgia aggressiva o di una terapia
iodoablativa
w Linfonodo sentinella: Primo linfonodo che in un
bacino linfatico regionale riceve il flusso linfatico dal
tumore primario
w È possibile identificare il linfonodo sentinella sia
utilizzando un traccinate radioattivo sia un colorante
vitale (Blue Dye, isosulfan blue) o pancitocheratine a
basso peso melecolare
w Dopo l’individuazione il linfonodo sentinella viene
rimosso ed esaminato; in relazione al suo
interessamento metastatico si procede alla linfectomia
regolata
w Tasso di identificazione del 83,3-95,5%
w Metodica fattibile e sicura con precise indicazioni:
n
n
Selezionare pazienti con linfonodo sentinella positivo
per la dissezione linfonodale
Diminuire i casi da sottoporre a trattamento
postoperatorio con iodoablazione (tumore della tiroide a
“basso rischio” con linfonodi sentinella negativi)
Prof. Salvatore Gorgone
25
Follow-up
w I pazienti devono essere seguiti con visite mediche
periodiche, esami radiologici (scintigrafie total body o
risonanza magnetica nucleare), dosaggio della
tireoglobulina, per scoprire precocemente le recidive o
le metastasi
w Solo il 15% circa dei pazienti va incontro a ripresa
della malattia: le recidive locali avvengono nell’80%
di questi casi, le metastasi nel 20%
w La chirurgia totalizzatrice associata alla radioterapia
con Iodio131 possono controllare sia la recidiva locale
che le metastasi e così quasi il 50% di questi pazienti
possono nuovamente ritornare liberi da malattia
w Se le recidive non sono iodocaptanti (25% delle
recidive e delle metastasi di carcinomi differenziati
della tiroide) la radioterapia esterna può controllare la
malattia localmente mentre la chemioterapia può
controllare le metastasi a distanza
Prof. Salvatore Gorgone
26
n
La tiroidectomia totale è il trattamento
di scelta nei pazienti in età geriatrica
con carcinoma differenziato della
tiroide
q
q
q
q
rispetta i principi della radicalità
oncologica
ha minima incidenza di complicanze
consente più facilmente il follow-up
dà migliori risultati a distanza
(sopravvivenza libera da malattia)
Prof. Salvatore Gorgone
27
Cisti tiroidea Ecocolor Doppler Nodulo tiroideo
Ecografie
noduli
tiroidei
Prof. Salvatore Gorgone
28
Scintigrafie nodulo caldo e freddo
Ecocolor doppler
carcinoma tiroideo
Prof. Salvatore Gorgone
29
Tumori differenziati della Tiroide - Diagnostica
I° Consensus Conference – SIC 2001
Stadiazione T e N
n
n
n
n
n
n
n
n
Ecografia ad alta risoluzione del collo: valutazione della lesione
primitiva e delle metastasi linfonodali
EcoColorDoppler: valutazione della lesione primitiva e delle
metastasi linfonodali
FNAB: valutazione della lesione primitiva e delle stazioni linfonodali
cervicali
RM del collo e del mediastino: se lesione voluminosa e/o estensione
extracapsulare e/o linfonodi sospetti
TC: evidenzia l’interessamento della trachea
Scintigrafia con 99mTc-pertecnetato: caratterizzazione dello
struma nodulare, non trova indicazione nel carcinoma
Biopsia del linfonodo sentinella: individuazione intraoperatoria di
micrometastasi linfoghiandolari (colorante vitale Isosulfan blue o
radiocolloide marcato 99mTC Nanocol) con esame istopatologico
estemporaneo. È indicata quando l’esame clinico sembra escludere
l’esistenza di metastasi linfatiche
Biopsia intraoperatoria al congelatore:
q
q
in caso di mancata esecuzione o esito sospetto della citologia su
agoaspirato
per verificare linfonodi sospetti (picking dei comparti centrale e laterale)
Stadiazione M
n
n
n
n
n
n
Rx torace: ricerca ripetizioni polmonari macroscopiche
TC torace senza mezzo di contrasto: definire entità e distribuzione
delle lesioni
Rx scheletro del segmento interessato, eventualmente RM
Scintigrafia con I131: fondamentale nel follow-up
Scintigrafia con traccianti positivi (Tallio o 99mTC SestaMIBI):
studio whole body e nel follow-up delle riprese di malattia non
iodocaptanti (per la perdita di una specifica proteina di membrana
NIS che ha il ruolo di captare lo ioduro circolante e concentrarlo
nella cellula 40 volte più che nel plasma)
Positron Emission Tomography con Fluoro-Desossi-Glucosio:
stadiazione e nel follow-up delle riprese di malattia non iodocaptanti;
più sensibile ma più costosa
Prof. Salvatore Gorgone
30
Stadiazione TNM per i tumori
papillari e follicolari
età < 45
età > 45
stadio
T
N
M
T
N
M
stadio 1
ogni T
ogni N
M0
T1
N0
M0
stadio 2
ogni T
ogni N
M1
T2
N0
M0
T3
N0
M0
T4
N0
M0
ogni T
N1
M0
ogni T
ogni N
M1
stadio 3
stadio 4
Prof. Salvatore Gorgone
31
Tumori differenziati della Tiroide
I° Consensus Conference – SIC 2001
n
n
n
n
n
n
n
Il T, l’M, l’età e il grading influenzano la prognosi con
percentuali superiori al 90%
Intervento di scelta è la tiroidectomia totale per via
extracapsualre o di principio. Riservare la lobo-istmectomia
ai pazienti a basso rischio (sesso femminile, età inferiore a
40 anni, mai irradiati, con carcinomi papillari incidentali o
follicolari capsulati) o ai microcarcinomi papillari <1 cm
Durante la tiroidectomia va eseguita la palpazione della
catena giugulo-carotidea e sovraclaveare con
l’asportazione dei linfonodi periricorrenziali e mediastinici
antero-superiori. Node-picking su una unica adenopatia
latero-cervicale, nelle adenopatie multiple linfoadenectomia
funzionale (risparmiando il muscolo sternocleidomastoideo,
il nervo accessorio spinale e la giugulare interna)
Nei reinterventi la recidiva va operata se non è trattabile
con lo I131 o con la radioterapia esterna
Nei pazienti ad alto rischio va attuata la terapia ormonale
soppressiva a vita (rischio di complicanze cardiovascolari
specialmente nei giovani). Nei pazienti a basso rischio la
terapia ormonale sarà soppressiva per almeno 5 anni e
verrà seguita da una terapia semisoppressiva in modo da
tenere il TSH tra 0,1 e 0,3
Nei pazienti ad elevato rischio o in cui è stata fatta una
chirurgia parziale eseguire un follow up stretto cioè
controllo dell’evoluzione della malattia e del dopo
trattamento con molti esami ravvicinati. Nei pazienti a
basso rischio invece follow up largo con meno esami e più
distanziati nel tempo
Nei primi tre anni follow up stretto, dal quarto al ventesimo
anno follow up largo
Prof. Salvatore Gorgone
32
Tumori
indifferenziati
della
tiroide
Carcinoma Anaplastico
-
– Tumore tiroideo a più elevata malignità, a
crescita rapida, alta invasività locale e metastasi
diffuse. Colpisce l’età avanzata con una leggera
prevalenza nel sesso femminile (1.5:1)
5-10% delle neoplasie tiroidee maligne
– Si presenta come una neoplasia non capsulata e
diffusamente estesa nel contesto della tiroide, i cui
caratteri morfologici macroscopici appaiono
completamente distorti. La consistenza ghiandolare
varia dalla estrema durezza (stone-like) alla
presenza di aree soffici o friabili ed è comune il
rilievo di invasione delle strutture vascolari, nervose,
laringee, esofagee e tracheali, muscolari e cutanee
– Indifferenziato perché non sono osservabili
papille o follicoli e non vi è amiloide nello
stroma. Le cellule possono essere piccole o
giganti con nuclei polimorfi (il tipo a cellule
giganti è ancora più maligno)
1
Carcinoma
anaplastico
-
-
-
-
-
-
La presenza sporadica di abbozzi follicolari o
papillari fa presumere che abbia origine da un
precedente carcinoma follicolare o papillare;
all’anamnesi talvolta si denuncia un piccolo
nodulo trascurato; comuni aree necrotiche ed
infiltrazione polimorfonucleare
Difficile differenziarlo dal sarcoma
macroscopicamente ed istologicamente
Il quadro clinico prevalente è rappresentato da
un rapido ed indolore sviluppo di una massa
cervicale o dall’incremento dimensionale
rapido di un nodulo tiroideo già presente da
alcuni anni
Rapida e cospicua invasività locale:
compressione tracheale ed esofagea,
invasione nervosa e vascolare
I linfonodi regionali sono costantemente
palpabili e può esserci evidenza di metastasi a
distanza
Il carcinoma anaplastico non capta il radioiodio
e la diffusa infiltrazione neoplastica tiroidea
può causare ipotiroidismo associato
Generalmente inoperabili; la chirurgia palliativa
ha lo scopo di ridurre i fenomeni compressivi
Nel 50% dei casi la sopravvivenza è di pochi
2
mesi o settimane. La prognosi è pessima
Carcinoma
anaplastico
3
Carcinoma
midollare
10%
2%
9%
Midollare
Papillare
Follicolare
Anaplastico
Altri
23%
56%
-
-
-
-
Tumore aggressivo che colpisce
in genere pazienti sopra i 50 anni
d’età
Si sviluppa dalle cellule C o
parafollicolari secernenti
calcitonina: i livelli serici in questi
pazienti sono elevati
Le cellule C neoplastiche
possono secernere anche 5idrossitriptamina, ACTH, MSH,
prostaglandine, somatostatina ed
antigeni oncofetali (CEA)
4
Non capta lo Iodio radioattivo
-
-
-
Può presentarsi come entità
nosologica unica o nella metà dei
pazienti essere associato ad altri
tumori endocrini con
caratteristiche di familiarità, con
ereditarietà di tipo autosomico
dominante
MEN II (Multiple Endocrine
Neoplasia) o sindrome di Sipple:
carcinoma midollare +
feocromocitoma bilaterale +
adenoma paratiroideo. Meno
aggressivo della forma sporadica
Macroscopicamente si presenta
come un nodulo duro bianco
grigiastro ben demarcato,
localizzato nella parte superiore
della ghiandola
(in accordo con la normale
topografia delle cellule C
parafollicolari)
5
-
-
-
-
-
-
È costituito da gruppi di cellule rotonde o
poligonali con nuclei piccoli e rotondi. Nello
stroma del tumore e delle metastasi amiloide
Aspetto istologico simile al carcinoide
La neoplasia si presenta come massa di
consistenza aumentata ed usualmente non è
capsulata
Focolai di infiltrazione carcinomatosa, macro- o
microscopici, sono evidenziabili in altre regioni
della ghiandola oltre alla sede primaria e può
essere rilevata infiltrazione vasale
Cresce lentamente e invade facilmente i vasi
linfatici intra-ghiandolari, diffondendosi
all’interno della tiroide stessa, della regione
capsulare e dei linfonodi loco-regionali quindi
metastatizza al polmone, al fegato e alle ossa
Al momento dell’intervento la diffusione
linfonodale è presente nel 75% dei casi è
spesso controlaterale o bilaterale come
bilaterale è il tumore. Nelle forme scoperte
grazie allo screening familiare (MEN IIB, MEN IIA)
l’infiltrazione linfonodale incide più che nelle
forme sporadiche
Il primo comparto interessato è quello centrale:
linfonodi pre- e para-tracheali, tracheo-esofagei,
dei vasi tiroidei superiori. Il comparto laterale
non è sempre coinvolto, salvo infiltrazioni
microscopiche nei linfonodi più prossimi alla
tiroide. Il mediastino superiore viene spesso
raggiunto e da qui diffonde ai linfonodi
6
controlaterali
Diagnosi
-
-
-
Utile alla diagnosi l’aumento dei livelli basali di
calcitonina nel sangue e dopo infusione di calcio
La concentrazione basale di calcitonina risulta
elevata nel 30-60% dei pazienti affetti da MTC
mentre l’infusione di pentagastrina e calcio
gluconato evidenzia una esagerata secrezione
di calcitonina pressoché nella totalità dei
pazienti con MTC ed anche in quelli con
iperplasia delle cellule C
Utile la FNAB tiroidea
I parenti di primo grado dei pazienti affetti da
MTC, inclusi i bambini piccoli, devono essere
sottoposti a screening per la presenza del gene
mutante e controllati regolarmente per
evidenziare l’insorgenza di eventuali sintomi
sindromici
Un marcatore tumorale di notevole aiuto nel
monitoraggio è rappresentato dall’antigene
carcinoembrionario (CEA) che generalmente
risulta maggiormente elevato nei casi più
aggressivi, mentre la calcitonina è
maggiormente elevata in relazione ad una
maggiore differenziazione della neoplasia:
l’incremento dei livelli di CEA dopo l’intervento è
pertanto sospetto per lo sviluppo di una malattia
ad andamento maggiormente aggressivo
7
-
-
-
-
-
-
-
La prognosi è peggiore di quella del carcinoma
papillifero ma migliore di quella del carcinoma
anaplastico
Il trattamento consiste nella tiroidectomia totale
di principio con svuotamento linfonodale
preventivo
Terapia medica sostitutiva con L-tiroxina a dosi
di mantenimento (0,2 mg/die) perché i carcinomi
midollari, non sviluppandosi dalle cellule dei
follicoli, non rispondono alla soppressione del
TSH
Radioterapia esterna come terapia
complementare e nelle recidive, con intento
palliativo
Nessun trattamento chemioterapico ha
dimostrato reale efficacia clinica ed il tasso di
risposta non supera il 15%
Dopo trattamento chirurgico radicale il paziente
deve essere sottoposto a dosaggio della
calcitonina circolante stimolata mediante
somministrazione di pentagastrina (ed
eventualmente calcio-gluconato)
Follow up stretto con:
– ecografia ad alta risoluzione
– TC o RM del collo e del mediastino
– immunoscintigrafia con impiego di 123 o 131IMIBeG, 111In-pentetreotide, radiofarmaci
oncotropi (201Tl cloruro, 99mTc-sestaMIBI, 99mTctetrafosmina) o frammenti FAb di anticorpi
monoclonali anti-CEA marcati con 99mTc
– cateterismo venoso selettivo associato a stimolo
8
con pentagastrina
Stadiazione TNM per i tumori midollari
stadio
T
N
M
stadio 1
T1
N0
M0
stadio 2
T2
N0
M0
T3
N0
M0
T4
N0
M0
stadio 3
ogni T
N1
M0
stadio 4
ogni T
ogni N
M1
I tumori
indifferenziati sono sempre allo stadio 4
stadio
T
N
M
stadio 4
ogni T
ogni N
ogni M
9
-
Le cellule dell’organismo hanno un ciclo vitale
composto da tre fasi fondamentali:
Ø divisione cellulare
Ø differenziazione cellulare
Ø morte cellulare (apoptosi)
-
-
-
-
-
Queste diverse fasi del ciclo cellulare avvengono in
base a messaggi codificati da diversi gruppi di
proteine di segnale e di effettori proteici cellulari
L’insorgenza di neoplasie e la loro proliferazione
avviene quando la fase proliferativa è aumentata e/o
quando viene inibita la possibilità delle cellule di
differenziarsi o di andare incontro alla apoptosi
I geni codificanti per le proteine che promuovono la
normale proliferazione e divisione cellulare sono
definiti proto-oncogeni. I proto-oncogeni possono
sviluppare mutazioni che alterano la produzione delle
proteine codificate determinando una eccessiva
attività proliferativa cellulare
Altri geni, conosciuti come geni soppressori della
proliferazione cellulare tumorale o geni
oncosoppressori, codificano per proteine che
normalmente riducono la divisione e la proliferazione
cellulare oppure promuovono fenomeni di
differenziazione cellulare o di apoptosi. Anche
mutazioni a carico di questi geni possono predisporre
alla proliferazione tumorale
Il carcinoma midollare tiroideo familiare deriva da
una mutazione puntiforme nella regione del protooncogene RET. Il risultato di tali mutazioni
determina la sintesi di un recettore RET attivato
con conseguente attivazione dei meccanismi
cellulari che portano alla iperplasia delle cellule C
parafollicolari ed alla loro successiva
trasformazione neoplastica
10
Ipotesi patogenetica di
alcune neoplasie tiroidee
11
Prevenzione
Ricerca del carcinoma midollare in fase preclinica
Screening genetico
ricercando protoncogeni mutati o traslocati
con tecniche di amplificazione e restrizione
(studio del DNA su prelievo ematico)
Il gene responsabile è il protooncogene
RET localizzato sul cromosoma 10
Ripercussioni sulla pratica
clinica
CMT
Test negativo
Carcinoma Sporadico
Test positivo
FCMT
Consanguinei
Test negativo
Soggetto non a rischio
Test positivo
Soggetto a rischio
Profilassi chirurgica
Tiroidectomia totale
Rifiuto intervento
12 con Calcitonina
Follow-up
Tracheotomia
13
Altre neoplasie
tiroidee
-
linfoma tiroideo: relativamente
raro, insorge in genere in una
ghiandola da tempo affetta da
tiroidite di Hashimoto
– risponde bene alla radioterapia e
alla chemioterapia
-
neoplasie secondarie:
relativamente frequenti, sono
secondarie a metastatizzazione
per via ematica di tumori primitivi
di mammella, polmone, rene,
melanoma maligno
14












