L’insegnamento dell’energia:
problemi, approcci e strategie
Lo sviluppo dell’energia cinetica e potenziale, le considerazioni su calore e
temperatura, come riportate in alcuni libri scolastici, sono tali da risultare
difficilmente comprensibili. Una riflessione sull’energia non può trascurare i tanti
luoghi comuni che circondano l’argomento. E’ un classico di alcuni testi riportare
la seguente definizione:
L’energia è la capacità di compiere un lavoro,
e si aggiunge:
«Per fare un lavoro un corpo deve avere a disposizione una certa energia. Per un
atleta è energia muscolare, per il vento è energia di movimento dell’aria».
Leonardo Barsantini
L’insegnamento dell’energia:
problemi, approcci e strategie
I problemi che si pongono sono di due tipi:
1. Come tutte le definizioni poste a fondamento di un percorso sono di scarsa o nulla utilità.
E’ il percorso che deve aiutare a costruire dei concetti arrivando anche a degli enunciati
definitori condivisi.
2. La definizione è discutibile anche dal punto di vista della fisica.
E’ vero che si vuol dare un’idea della nuova grandezza energia, ed è anche vero che l’energia
posseduta da un dato sistema può essere utilizzata per fare “qualcosa”, ma è nell’eccesso di
specificazione che si commette l’errore confondendo “quello che un corpo può fare” con
“quello che è stato fatto sul corpo”.
Si ha l’impressione che si faccia confusione fra forze applicate a un corpo da altri corpi e forze
che il corpo applica su altri corpi.
Il discorso deve invece essere inquadrato da un diverso
punto di vista che privilegia il percorso rispetto alla
definizione, senza la pretesa di giungere a stabilire e
determinare quadri conoscitivi tanto completi quanto
effimeri. In una scuola secondaria di primo grado –
scuola media, il rapporto con i fenomeni è ancora
essenziale rispetto agli approcci teorici.
Nella scuola secondaria di primo grado, gli studenti
hanno i primi incontri con alcuni argomenti e non si può
pensare di esaurire la classificazione di tutti i vari tipi di
energia.
Considerando le competenze degli studenti e,
generalmente, il poco tempo a disposizione,
si deve privilegiare l’intensione su pochi o pochissimi
argomenti, rispetto all’estensione.
E’ inoltre opportuno che gli argomenti trattati siano il
più possibile ancorati fra loro, fino a formare una rete di
percorsi e di concetti che si rafforzano a vicenda.
• Le forze possono essere trattate e
approfondite per quanto riguarda la
correlazione che si può manifestare
con le deformazioni provocate, ma
non certo con le ben più astratte
leggi della dinamica. Sono proprio le
deformazioni che concretizzano la
forza che, anche attraverso l’idea di
vettore, permette di visualizzare i
fenomeni con rappresentazioni
grafiche.
• Altrettanto non vale per l’energia,
poiché con questa grandezza
l’astrazione richiesta è maggiore
rispetto a quella che accompagna il
concetto di forza.
E’ quindi necessario affrontare un
percorso sulle forze, senza definizioni da
dizionario e senza inutili enunciazioni dei
principi della dinamica, che chiarisca e
definisca gli ambiti nei quali si può parlare
correttamente di forza (anche se si tratta
pur sempre di ambiti parziali, perché, ad
esempio, la connessione fra forza e
accelerazione è al di là della
comprensione di molti studenti).
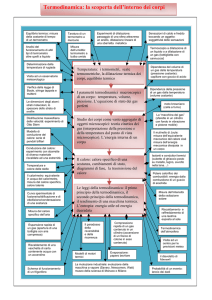
Anche in ambito termodinamico il
concetto di energia è difficile da
acquisire, ed è necessario procedere
con cautela, ad esempio, il calore non
è una sostanza che i corpi
acquisiscono o perdono, e i tentativi
di spiegazione portati da un punto di
vista microscopico non sono
sufficienti per far comprendere i
meccanismi nascosti
Il calore dovrebbe sempre essere
qualificato come calore trasmesso e non si
dovrebbe parlare di calore posseduto da
un corpo. Il calore è caratterizzato come
tale soltanto nel transito da un corpo ad
un altro. Ma anche in questo caso non si
possono prendere scorciatoie. I fenomeni
da analizzare devono essere semplici
perché gli studenti, pur conoscendo il
termometro, ragionano in termini di caldo
e freddo mediato dalle sensazioni
corporee.
Noi sappiamo che la temperatura è una
grandezza indice di uno stato del sistema, il
calore trasmesso è una grandezza di
interazione fra due o più sistemi, ed influenza
la temperatura raggiunta dal corpo.
Il corpo assorbe energia e aumenta la sua
temperatura: la temperatura è quindi un indice
dell’energia interna del corpo, di tutta
l’energia interna del corpo e non soltanto di
quella assorbita.
Occorre molto tempo affinché questi concetti
si radichino nella testa dei ragazzi.
Temperatura e calore vanno caratterizzate
come grandezze intensive e estensive.
E’ necessario che gli studenti prendano
coscienza di questa fondamentale differenza.
Quando si opera con un dato procedimento su
un sistema fisico, si ottiene un risultato
descritto da una o più grandezze. Ad esempio il
procedimento di porre un oggetto sulla
bilancia fornisce un valore alla grandezza fisica
peso. Il fatto è che le grandezze fisiche di
base con le quali interagiscono gli studenti
sono il peso, il volume, la lunghezza, la velocità
e tutte hanno una caratteristica che le
accomuna: sono grandezze estensive.
Ma non tutte le grandezze sono estensive,
alcune sono intensive e poiché gli studenti non
hanno alcuna concezione di grandezze
intensive ed estensive, è necessario portarli a
riflettere su questa differenza perché,
altrimenti, tutte le grandezze della fisica
finiscono per essere interpretate,
implicitamente, come estensive.
Tutte le grandezze che forniscono
informazioni su ciò che accade localmente,
all’interno del sistema, per la cui
determinazione è sufficiente l’analisi di una
piccola porzione del sistema, sono
intensive. La temperatura è un indice di
cosa accade localmente all’interno del
sistema, infatti, per determinarla,
supponendo di essere all’equilibrio termico,
è sufficiente portare il termometro a
contatto con una qualunque porzione del
corpo: in questo senso è una grandezza
intensiva
Al contrario, le grandezze estensive si caratterizzano
per la necessità di considerare tutto il sistema a
disposizione, ad esempio, il peso di un corpo è
determinato prendendolo tutto in considerazione e
non soltanto una porzione (una porzione, nel caso ci
sia omogeneità, è invece sufficiente per il peso
specifico). La quantità di calore trasmesso
va ad aumentare l’energia del corpo, cioè aggiunge
energia ad energia: siamo in presenza
di una grandezza estensiva.
Non si tratta di definire cosa significhi intensivo e estensivo, piuttosto far riflettere gli
studenti, con attività concrete e confronti, non soltanto sui fatti che osservano o sulle
misurazioni prese in laboratorio, ma anche sugli strumenti, in questo caso le grandezze
fisiche, utilizzate nello studio dei fenomeni fisici. Ecco due proposte sperimentali che
possono portare gli studenti ad un prima valutazione della temperatura come grandezza
intensiva:
1. Mescolare due uguali quantità d’acqua mantenute a temperatura differente e far
prevedere la temperatura finale.
2. Separare una data quantità d’acqua in due parti uguali e far prevedere la temperatura
finale.
E’ necessario che agli studenti sia chiesta la previsione dei
risultati prima di effettuare le prove. Non occorre fretta. E’
frequente che questi sommino o sottraggano le temperature nel
mescolamento o che suddividano, assieme all’acqua, anche la
temperatura trattandola alla stregua di una grandezza estensiva.
Al termine delle prove è necessario riflettere sulle ragioni di tali
risultati in un processo del tipo penso – agisco – penso.
E’ opportuno, nell’eseguire questi ragionamenti – esperimenti,
non chiedere valori precisi, piuttosto intervalli possibili per non
fuorviare l’attenzione verso precisioni numeriche inessenziali. Si
ricordi che il risultato della misurazione, la misura, non è mai un
valore preciso, ma sempre un intervallo. Si può ulteriormente
approfondire il discorso mescolando due diverse quantità di
acqua e riflettendo sul ruolo della media nel prevedere il
risultato finale.
Il laboratorio deve essere strettamente collegato al percorso, senza che si formi la
classica separazione fra esperienza in laboratorio e spiegazione in classe. Per
quanto il laboratorio scolastico sia importante, è necessario essere coscienti che il
vero laboratorio è nella testa degli studenti: è lì che si costruiscono i concetti.
Una prima riflessione sui fenomeni termici,
può partire dal riscaldamento dell’acqua
contenuta in un recipiente posto su un
fornello. Possiamo pensare che il fornello,
molto caldo, abbia trasferito parte del
proprio “esser caldo”, all’acqua.
Gli effetti di quanto trasferito, cioè del
calore trasmesso dal fornello al pentolino
con l’acqua, non determinano uno stesso
riscaldamento per una qualunque quantità
di acqua contenuta nel pentolino.
Si può eseguire l’esperienza con due
diverse quantità di acqua scaldate per lo
stesso tempo con la stessa quantità di
calore trasmesso.
Le temperature prese ad intervalli regolari, ad
esempio ogni minuto, riportate in grafico
tempo/temperatura forniscono, con buona
precisione, una retta. Al variare della
quantità di acqua riscaldata e mantenendo
costante la regolazione del fornello, cioè il
calore trasmesso, il grafico tempo –
temperatura fornisce una retta con pendenza
diversa.
Il confronto e l’interpretazione dei grafici
rinsalda l’uso di strumenti matematici creando
una retroazione positiva fra matematica e
scienza. Si può approfondire lo studio
considerando che a parità di tempo trascorso,
cioè di calore trasmesso, e di uguali
temperature iniziali, una quantità di acqua
doppia di un’altra dovrebbe raggiungere una
temperatura che è la metà. Ciò non accade
perché nel trasmettere calore non si scalda
soltanto l’acqua ma anche il contenitore.
Si noti, che mentre è possibile eseguire una misurazione
della temperatura per mezzo di un termometro, il calore
trasmesso può soltanto essere regolato a priori, ad
esempio posizionando l’indice del fornello su posizioni
diverse.
Nel primo caso si ha una misurazione, nell’altro una
regolazione: questi sono due modi diversi di agire su un
sistema.
L’esperienza mette in evidenza che si opera con due
grandezze diverse, come si comprende anche dal fatto
che, a parità di calore trasmesso per lo stesso tempo, le
temperature di due diverse quantità di acqua sono
differenti.
La cessione di energia non è
responsabile soltanto del
riscaldamento dei corpi, ma
di tanti altri fenomeni, alcuni dei
quali sono delle vere e proprie
trasformazioni.
Continuando a scaldare l’acqua, ad
un certo punto la temperatura non
sale più. Accade qualcosa di diverso:
l’energia fornita è utilizzata per
acquisire una “maggiore libertà”. Un
fenomeno analogo può essere
associato alla fusione del ghiaccio.
Si possono scaldare anche altre
sostanze, per alcune di queste è
facile mettere in evidenza una
dilatazione. E’ partendo da questa
nuova fenomenologia che si può
avviare una riflessione sui
termometri.
La comprensione dei fenomeni termici è fortemente condizionata
dall’interpretazione “corporea” spontanea che ci guida normalmente. Le forme
delle nostre sensazione, per noi assolutamente coerenti e spontanee, sono
spesso in contraddizione con l’interpretazione scientifica. Più che affrontare
questioni ben al di là della possibile comprensione degli studenti, potrebbe essere
opportuno indagare alcuni di questi aspetti.
L’attività non è semplice, ma iniziare a smontare alcune (certamente non tutte)
preconcezioni può essere importante.
La semplice, ma istruttiva esperienza, di porre le mani a contatto con acqua
tiepida dopo che, ad esempio, la mano destra è stata immersa in acqua calda e
quella sinistra in acqua fredda, mostra, per la diversa sensazione corporea rilevata
da ciascuna mano nel contatto con l’acqua tiepida, i limiti delle mostre percezioni
e la necessità di sviluppare e utilizzare strumenti di misura.
Altre sensazioni corporee, sviluppate dal contatto con alcuni materiali (legno
e metallo), che ci portano a caratterizzare corpi “caldi e freddi”, potrebbe
fornire la base, ad esempio in ambito tecnologico, per avviare un discorso sui
modi con cui si può facilitare o ostacolare la trasmissione del calore con
materiali conduttori e isolanti, riflettendo anche sulle sorgenti primarie (che
mantengono inalterate la loro temperatura pur trasferendo calore) e
secondarie. Siamo in un contesto, che pur essendo attinente alla scienza, ha
forti valenze tecnologiche permettendo un’integrazione fra i due campi di
studio.
L’esperienza di far sciogliere un cubetto di ghiaccio posto su una tavoletta di
metallo e su, ad esempio, una di legno, fa riflettere gli studenti sul fatto che la
velocità di scioglimento del ghiaccio non è in rapporto con le sensazioni che si hanno
toccando i due materiali.
Le sensazioni ingannevoli possono portare a conflitti concettuali utili nello studio dei
fenomeni termici. Se la lana “fa caldo”, allora un cubetto di ghiaccio avvolto in un
maglione dovrebbe sciogliersi molto rapidamente, ma l’esperienza dimostra che la
velocità con cui si scioglie un pezzo di ghiaccio avvolto in un maglione di lana è
inferiore rispetto al caso di un cubetto di ghiaccio lasciato all’aria.
Avviare il passaggio dai ragionamenti sui “corpi caldi e freddi” o sui “materiali che
fanno caldo o freddo”, verso l’interazione fra i corpi e ai modi di facilitare o
ostacolare la trasmissione del calore, permette di approfondire l’indagine sui
fenomeni termici.
Il concetto di energia
In precedenza si parlava dell’energia come della capacità di fare qualcosa (di fare
lavoro). E’ evidente che una definizione di così ampia genericità può andar bene per
tutto (anche le forze sono in grado di far qualcosa), ed anche il calore trasmesso è in
grado di fare qualcosa, e questo qualcosa consiste nell’aumentare la temperatura.
Iniziando a restringere il campo, si può affermare che la temperatura aumenta, non
perché agisce una forza (che è una delle grandezze sulle quali si può lavorare nella
scuola secondaria di primo grado), ma perché il corpo più caldo ha ceduto del calore al
corpo più freddo.
Storicamente, questo “qualcosa” ceduto, è stato indicato col termine calore, ma oggi
potremmo benissimo chiamarlo “energia”. L’energia è un concetto, come già detto,
astratto: non vediamo l’energia, ma gli effetti che essa produce. Questi effetti si
spiegano bene con l’introduzione della nuova grandezza.
In realtà, più che delle trasformazioni dell’energia, si dovrebbe parlare delle
trasformazioni dei sistemi, spiegate per mezzo del parametro energia.
Dovremmo fare il possibile affinché il concetto di energia sia visto come
unitario e non come tanti sottoelementi che si trasformano l’uno nell’altro:
energia chimica, termica, meccanica, nucleare e poi cinetica, potenziale,
elastica…. Questa proliferazione di energie, di gran moda, è, secondo me,
assolutamente da evitare perché sposta l’attenzione degli studenti verso la
memorizzazione della catalogazione dei vari tipi di energia, alcuni dei quali
al di fuori di un indagine possibile a scuola, piuttosto che verso la spiegazione
dei fenomeni. Al contrario di quanto avviene con l’onnipresente
classificazione dei vari tipi di energia, quest’ultima deve essere costruita
come un concetto unitario.
«non mi sorprenderei, visto i tempi che corrono, se qualcuno aggiungesse
alla lista l’energia mentale».
http://www.professionistiscuola.it/didattica/di
dattica-fisica/1641-una-favola-per-la-fisica-cose-l-energia.html
L’energia è un concetto molto importante in
fisica, ma alla domanda cos’è l’energia? Beh io
risponderei con una favola.
Già è proprio una favoletta che voglio
raccontarvi
Energia = capacità potenziale di compiere lavoro
meccanico
Il lavoro viene poi definito come il prodotto scalare tra la
forza e lo spostamento!
Cosa sia l’energia non è ben chiarito, essa viene legata al
concetto di lavoro meccanico, il quale è diverso da zero
soprattutto se c’è uno spostamento, ma come conciliare il
concetto di “consumo” di energia a cui siamo soliti pensare
quando teniamo in mano un oggetto “pesante” fermo?
Se guardiamo anche un altro libro molto usato nei nostri
Licei, l’Amaldi, troviamo una dissertazione lunghissima sul
lavoro, per poi definire anche qui l’energia come la
capacità fisica di un sistema di compiere lavoro
Il concetto di energia è legato al concetto di lavoro,
l’energia è vista come una sorta di azione, una specie di
forza viva, tramite la quale è possibile compiere lavoro di
tipo meccanico!
Cos’è l’energia?
Favoletta di Richard Feynman così come come è proposta agli alunni e che spiega
come i fisici considerano l’energia.
C’era una volta una piccola bambina di nome Elisabetta alla quale la madre aveva donato 30
piccole formine (non importa che forma abbiano o di cosa siano fatte, immaginatele come
volete), con le quali la nostra Elisabetta si divertiva a giocare.
Un giorno la madre entrò in stanza e trovò solo 29 formine. Elisabetta piangeva, non sapeva
dove potesse essere la sua trentesima formina! La madre cercò ovunque senza trovarla, fino
a quando ricordo' che il giorno prima Elisabetta aveva giocato fuori in giardino. Felice ritrovò
la 30sima formina nel prato.
Passa un mese e la mamma entrò in stanza per sistemare i giochi e contò 31 formine!!
Com’era possibile?
Le formine non erano state rotte, semplicemente se ne era aggiunta una nuova.
La madre si fece coraggio e si recò dalla vicina, dove trovò un bambino che stava cercando la
sua formina: il bambino era venuto due giorni prima a casa loro e aveva dimenticato lì la
formina!
Passò un altro mese e la madre trovò che le formine erano solo 28!
Cercò ovunque, dal vicino, in giardino, ma nulla!
La madre che era un fisico, sapeva che un corpo immerso in un liquido sposta una quantità di
liquido pari al volume del corpo immerso e notò che nella sua vasca dei pesci, l’acqua si era
innalzata. Dopo una serie di conti capisce che le due formine non potevano che essere lì!!
Tutto questo per dire che per i fisici le formine
sono come l’energia, non sappiamo bene cosa
siano, ma sappiamo una cosa: il loro numero
deve conservarsi, deve rimanere sempre lo
stesso.
«Noi fisici siamo disposti anche ad introdurre
nuove leggi, persino nuovi fenomeni, ma siamo
ben restii a negare la conservazione
dell’energia!»
Quando le formine sono in meno andiamo a
cercarle in nuove leggi fisiche; quando sono in
più, allora qualcuno ci ha dato delle sue
formine.
Possiamo dire che l’energia è “qualcosa” che si
conserva!
Ogni qualvolta però le formine si spostano,
oppure mancano di numero, vuol dire che è
intervenuto qualcosa che le ha solo
“trasformate“ “spostate” ed il modo per
trasferire questa energia (nella fisica classica) è
farlo tramite una forza o meglio attraverso un
movimento.
In sostanza non dico che
l’energia è la capacità di
compiere un lavoro, dico solo
che ogni qualvolta localmente
l’energia non si conserva, la sua
variazione si ritrova sotto forma
di lavoro fatto da una certa forza,
ovvero il trasferimento di energia
avviene in primis tramite una
energia di movimento (perché vi
è una forza, si veda teorema
dell’energia cinetica). Il lavoro
allora mi dà una misura di
quanta energia sto trasformando
in un’altra forma , ma il computo
finale deve restituirmi sempre le
mie 30 formine!
Tra tutte le forme di energia però ve ne è una un po’ speciale!
Supponiamo che le mie formine siano come 100 euro.
Elisabetta , ormai cresciuta, compra una bicicletta del valore di 20 euro, avrà così in tasca
80 euro ed in mano una bici.
Se decide di rivendere la bici (trascuriamo l’usura del mezzo e l’inflazione) otterrà
nuovamente i suoi 100 euro!
Il problema è che ogni volta che Elisabetta decide di comprare qualcosa, lo fa con la carta
di credito della madre e sa che per ogni operazione deve alla banca 1 euro di
commissione!
Compra la bici di 20 euro , paga 1 euro di commissione, e si ritrova in tasca 79 euro!
L’euro non è andato perduto, ma semplicemente non fa più parte del potere di acquisto
di Elisabetta.
L’euro di commissione è una forma di “energia” che non può più essere convertita per
comprare cose, è una sorta di energia che si è degradata!
L’euro di commissione è quanto di più vicino al concetto di calore (e poi di entropia) che noi
fisici conosciamo!
Associare al concetto di energia quello di
lavoro meccanico, quando si sa che la
termodinamica ci restituisce una visione più
ampia del fenomeno (e generalizza il concetto
di lavoro e di energia), significa non solo fare
un torto verso i nostri studenti, ma soprattutto
indurre una serie di misconcezioni che sono
difficili da eliminare!
La conservazione dell’energia è qualcosa di così
radicato in noi fisici che la ritroviamo anche
nella Cosmologia, dove parliamo di energia
oscura, quintessenza, ma anche in Meccanica
Quantistica.
La propagazione del calore richiede un set di esperimenti non alla portata dei laboratori
scolastici.
L'analisi quantitativa della propagazione del calore per conduzione, convezione o
irraggiamento, sostanzialmente non viene fatta a scuola!
E' possibili fare analisi, costruire un modello sperimentale "reale" della conduzione dei
metalli?
Laboratorio povero di Fisica: la
conduzione nei metalli
Materiale: sbarra di ferro o altro materiale,
righello, cronometro, candele, metro a
nastro
Obiettivo: studiare la conduzione nei
metalli
Fase 1 Esplorativa
Per verificare la conduzione del calore, prendiamo la
nostra sbarra metallica ed ad una sua estremità
facciamo colare la cera della candela, teniamo ben
presente la quantità di cera utilizzata e “attacchiamoci
sopra” un pezzo di gesso. Poniamo ad una certa
distanza (che misuriamo) una candela ed osserviamo
cosa accade!
Dopo quanto tempo la candela si stacca?
Perché si stacca?
A quale fenomeno stiamo assistendo?
Fase 2 Misure
Vogliamo studiare la propagazione del
calore in relazione ai parametri in gioco:
distanza candela, numero di
candele, quantità di cera,tempo.
Misurata la distanza a cui porre la
nostra candela (consiglio 10cm)
determinare il tempo di distacco del
pezzo di gesso, ripetere l’esperimento
fissando la distanza e aggiungendo 2,
3…candele. Determiniamo i dati in
tabella
Aumentando il numero di candele
aumentiamo la quantità di calore
proporzionalmente, pertanto secondo
la legge di Fourier ci aspettiamo che i
tempi di distacco diminuiscano
proporzionalmente: ovvero la
proporzionalità tra calore e tempo è
inversa!
Dai grafici ottenuti cosa puoi concludere?
La dispersione di calore in aria influenza la tua misura? Se sì in che modo?
(nb. LA DISPERSIONE DI CALORE IN ARIA è una costante nel tempo
pertanto se le misure sono veloci, possiamo dire che in percentuale tale
dispersione è controllabile!)
In questo esperimento bisogna stare attenti a far sì che la misura sia ripetibile
nelle medesime condizioni: quindi attenzione a cercare di usare sempre la
stessa quantità di cera!
Fase 3 legame calore e distanza
Utilizzando il metro determiniamo 4
distanze, a partire dall’estremità, alle quali
porre la nostra candela. In
pratica ponendo la candela a distanza
diversa determiniamo il tempo a cui si
stacca il nostro pezzo di gesso.
Costruiamo un grafico tempo distanza.
Che tipo di grafico ci aspettiamo? Che tipo
di grafico troviamo?
Dalla legge di Fourier ci aspettiamo che la
proporzionalità sia diretta, anche se…..
Perché il grafico è di proporzionalità
quadratica?
Conclusioni
Riflettere sul modello teorico e sul modello
sperimentale trovato
Quali punti di incontro? Quali le differenze?
Quali i fenomeni trascurati?
Didattica fisica, laboratorio povero: misura del
calore latente del ghiaccio
Basta procurarsi alcuni cubetti
di ghiaccio, un calorimetro,
una bilancia ed il gioco è fatto.
Il calore latente di fusione è una
caratteristica fisico-chimica
importante di un corpo.
Il ghiaccio deve essere
conservato a scuola dentro un
vano frigo, altrimenti un alunno
deve portare un frigo portatile
o una borsa termica.
Il nostro laboratorio non è molto attrezzato? Stiamo realizzando esperimenti sulla
calorimetria
e
non
ne
abbiamo
uno?
Si possono utilizzare dei becker di vetro “approssimati a dei calorimetri ideali”. Tale
forzatura permette di ottenere delle buone misure sul calore specifico ed il calore latente
di fusione del ghiaccio!
Come coibentare il becker di vetro e renderlo un “calorimetro”?
Materiale occorrente: Fogli di alluminio per alimenti, pezzi di polistirolo (in alternativa
cartone resistente), forbici.
Rivestire il nostro becker di vetro lateralmente con dei figli di alluminio. Tale operazione
permette di ridurre la dispersione del calore per irraggiamento.
La base e la parte superiore del becker non va rivestita!
Rivestire poi il bordo con del polistirolo o del cartone (se il polistirolo è troppo spesso e poco
deformabile, creare una struttura a parallelepipedo, in modo che il becker possa entrare
dentro). Chiudere il polistirolo con delle graffette (in alternativa usare dello scotch, ma
sconsiglio tale cosa, perchè con il calore esso può sciogliersi).
Con il polistirolo avanzato, creare un coperchio da porre sul calorimetro. Praticare sul
coperchio un foro circolare di diametro di 1 cm nel quale far entrare il nostro termometro.
Tale foro va tenuto più largo del diametro del termometro perchè nelle curve di
riscaldamento e raffreddamento, l'operazione deve essere isobara (altrimenti si crea un
calorimetro “pentola a pressione”)!
Rivestire il tutto con del cartone resistente.
Misura dell'equivalente in acqua del
calorimetro
La misura dell'equivalente in acqua di un
calorimetro è un procedimento standard, che
non necessita particolari accorgimenti.
l’equivalente in acqua del calorimetro è
quella massa di acqua che
assorbirebbe lo stesso calore che viene
sottratto dal calorimetro e dagli altri
oggetti contenuti in esso.
Il movimento delle molecole di un gas
disciolto in un liquido dipende dalla
temperatura del liquido in cui è
disciolto, e precisamente: la velocità delle
molecole del gas aumenta con
l’aumentare della temperatura
del liquido. Pertanto, in estrema sintesi
possiamo affermare che le molecole di un
gas a bassa temperatura (inferiore a 15°C)
sono lente, mentre risultano veloci a
temperatura più elevata (superiore a
20°C).
Gas veloce = Gas caldo | Gas lento = Gas
freddo
Che cosa vi occorre
Un vasetto da 750 ml, in vetro chiaro e di
forma bassa
Un bicchiere piccolo di plastica da 80ml
Un cucchiaio di plastica da 10 ml
Un cucchiaino di plastica da 2 ml
Un bicchiere di plastica chiara da 250 ml
Un bicchiere di plastica da 350 ml
Tintura di Iodio al 2 % (è reperibile in
farmacia)
Un contagocce a matita in plastica, con
gommino (è reperibile in farmacia)
Aceto bianco
Salda d’amido
Acqua non gasata
Procedimento
1- Versate, nel vaso in vetro chiaro da
750 ml, quattro bicchieri di plastica
piccoli pieni di acqua, prelevata da
una bottiglia di acqua minerale non
gasata lasciata a temperatura
ambiente.
2- Versate, con il contagocce a
matita, 25 gocce esatte di Tintura di
iodio al 2% e agitate con un
cucchiaio la soluzione, fino a quando
il liquido non è diventato
omogeneamente di un colore
giallino.
3- Versate, nel liquido giallino, tre
cucchiaini circa di plastica, uno alla
volta, colmi di Salda d’amido (lasciata
a temperatura ambiente ) fino a
quando il liquido non è diventato
blu- nero.
4- Riempite completamente di aceto bianco (a
temperatura ambiente) un bicchiere di plastica
trasparente da 250ml;
5- Versate l’aceto, dapprima lentamente e poi
tutto in una volta, nel vaso con il liquido nero;
Cosa accade?
1- Se il liquido nerastro si decolora (ritorna il
colore giallino dell’aceto bianco) quasi
immediatamente, significa che la temperatura
dell’ambiente in cui operate è “estiva”.
2- Se il liquido nerastro si decolora invece dopo
alcuni minuti, significa che la temperatura
dell’ambiente in cui operate è “ invernale”.
Spiegazione
L’aceto commerciale contiene il gas incolore, chiamato anidride solforosa, proveniente dal
vino bianco (l’aceto bianco si ottiene dal vino bianco per azione di alcuni batteri “aceto
bacter”, che trasformano per ossidazione l’alcool etilico del vino in acido acetico).
L’anidride solforosa si muove liberamente nell’aceto come succede ad esempio per il gas
anidride carbonica nell’acqua gasata.
Il liquido blu-nero (chiamato amido iodurato) è ottenuto dalla combinazione di iodio e
amido (salda d’amido). Quando l’amido iodurato viene a contatto con l’anidride solforosa,
avviene una reazione di ossido-riduzione. Lo iodio è trasformato in un composto chimico
chiamato ioduro, che non si lega con l’amido, e quindi il liquido si decolora, facendo
ritornare il colore giallino dell’aceto.
Se la temperatura della soluzione (liquido nero + aceto ) è bassa (inferiore a 15°C), le
molecole del gas anidride solforosa si muoveranno lentamente e impiegheranno più
tempo a raggiungere le molecole di iodio per trasformarlo in ioduro incolore. Se invece la
temperatura della soluzione è più alta (superiore a 20°C) le molecole di gas si muoveranno
più velocemente e impiegheranno meno tempo a reagire con lo iodio per trasformarlo in
ioduro incolore .
Taratura del termometro chimico
Per far funzionare perfettamente il termometro chimico occorre operare a basse
concentrazioni di iodio (25 gocce) e di anidride solforosa (quella contenuta in 250 ml di aceto
bianco).
Diamo uno sguardo alla velocità di reazione tra anidride solforosa + iodio.
• Velocità di reazione alta (immediata decolorazione della soluzione blu): quando la
temperatura della soluzione (aceto + amido ioduro blu) è alta (superiore a 20°C) e le
concentrazioni dei reagenti (anidride solforosa e iodio) sono basse.
• Velocità di reazione bassa (ritardata decolorazione della soluzione blu ): quando la
temperatura della soluzione è bassa (minore di 15°C) e le concentrazioni dei reagenti sono
basse.
Pertanto, il primo passo per costruire il nostro termometro chimico è quello di operare a
basse concentrazioni sia di anidride solforosa che di iodio poiché ad alte concentrazioni il
nostro termometro non funzionerebbe e si trasformerebbe (anche a basse temperature) in
uno smacchiatore istantaneo. Proprio per questo, inizialmente, la quantità giusta di anidride
reagente deve essere quella contenuta in un bicchiere pieno di aceto bianco, da 250 ml.
Siccome la quantità di anidride solforosa, contenuta nell’aceto bianco, varia a seconda della
marca di aceto utilizzata nell’esperimento, tarate il vostro termometro all’aceto bianco
secondo la procedura seguente.
Procedura:
- lasciate in frigo una bottiglia di acqua e una di aceto ancora chiuse, in modo da farle
raffreddare al di sotto dei 15°C (volendo, potete aggiungere 2 cubetti di ghiaccio nel vaso
contenente 4 bicchieri piccoli di acqua e altri 2 nel bicchiere contenente l’aceto);
- preparate il termometro utilizzando 4 bicchieri piccoli di acqua fredda e un bicchiere da 250
ml pieno di aceto freddo;
- versate l’aceto bianco nel vaso con liquido blu .
Se il liquido blu freddo, trascorsi circa 3 minuti, non si dovesse decolorare, dovete aumentare
la quantità di aceto (versare, in un bicchiere da 350 ml, 1 bicchiere da 250 ml colmo di aceto
freddo + 1 cucchiaio di plastica (10ml) colmo di aceto).
Se con questa quantità di aceto (260 ml) il liquido blu si decolora prima di 3 minuti, il
termometro è ben tarato; in caso contrario, occorre aumentare la quantità di aceto,
aggiungendo un altro cucchiaio (10ml) di aceto (in tutto 270 ml) e così via.
Se il liquido blu freddo si dovesse invece decolorare in pochi secondi, occorre diminuire la
quantità di aceto (togliete, da 250 ml di aceto, un cucchiaio da 10ml di plastica dello stesso, e
così via fino a quando il liquido non sarà arrivato a decolorarsi prima di 3 minuti).
In altre parole, per regolare la giusta concentrazione di anidride solforosa presente nell’aceto
bianco, iniziando da 250 ml di aceto, si deve togliere o aggiungere una quantità di aceto, 10
ml per volta, equivalente ad 1 cucchiaio di plastica, a seconda che il liquido si decolori quasi
immediatamente (si toglie aceto), oppure oltrepassi i 3 minuti per decolorarsi (si aggiunge
aceto).
Il percorso prevede un approccio di tipo fenomenologico alle problematiche affrontate,
trattate ad un primo livello di approssimazione elementare.
L'attività sperimentale viene vista come punto di partenza quando serve a porre un
problema, come attività intermedia nella fase in cui c'è necessità di esplorare il
comportamento dei corpi e infine come punto di arrivo quando occorre controllare
l'adeguatezza delle previsioni o l'attendibilità delle ipotesi emerse nella discussione in
classe.
Il percorso proposto pone l'accento su alcuni aspetti dei fenomeni più ricorrenti
nell'ambiente al fine di far pervenire gli alunni ad un'interpretazione univoca, anche nei casi
in cui coesistessero diversi modelli interpretativi.
Pertanto si è suggerisce un'attività sperimentale che permette di rispondere ai seguenti
quesiti:
• Nel passare dal caldo al freddo (o viceversa) variano sempre alcune caratteristiche dei
corpi come il peso (o la massa), la forma, il colore, la densità?
• Se variano, come variano?
Si potranno così individuare grandezze che non dipendono dalla temperatura, come il
peso, ed altre che ne dipendono, ma ogni volta in modo diverso da sostanza a sostanza.
Si conserva il peso di un corpo a freddo/a caldo?
I fase del percorso: Obiettivi
Riconoscere che la massa è una grandezza "indipendente" dalla temperatura, che si mantiene costante
finché si ha a che fare sempre con lo stesso corpo, senza che ad esso venga aggiunta o sottratta materia
Materiale necessario
una bilancia con sensibilità 0,01 g;
una beuta con tappo di gomma;
tappi di gomma;
pastiglia effervescente.
Descrizione della procedura
I corpi vanno inseriti nella beuta contenente inizialmente acqua calda e la beuta va tappata perché
non evapori l'acqua e asciugata all'esterno.
Si collochi il tutto sul piatto della bilancia.
Dopo avere letto il valore della massa, si attenda che l'acqua si raffreddi e si torna a leggere il valore
della massa. Non dovrebbe condensare vapore all'esterno, ma eventualmente è opportuno tornare ad
asciugare la parete esterna.
Massa di un solido a caldo/a freddo
Massa di un gas a freddo
Nella prima foto si legge il valore della massa della
beuta contenente acqua calda, nella seconda foto si
legge il valore della massa della stessa beuta dopo
che si è raffreddata fino a raggiungere l'equilibrio
termico con l'ambiente.
La massa è ancora la stessa di prima.
Massa di un gas a caldo
Nella prima foto sono poggiati sul piatto di una bilancia
una beuta con dell'acqua calda, un tappo di gomma,
una pastiglia effervescente.
Nella seconda foto la pastiglia è stata introdotta nella
beuta, che è stata tappata immediatamente. Si è avuta
una reazione che ha prodotto un gas, ma il valore della
massa è rimasta inalterata
Nella prima foto si legge il valore della massa
della beuta ancora tappata, contenente il gas,
dopo che si è raffreddata fino a raggiungere
l'equilibrio termico con l'ambiente.
La massa è ancora la stessa di prima.
Nella seconda foto la beuta è stata stappata.
Solo in questo caso si osserva una variazione
(una diminuzione) sensibile della massa per
fuoriuscita del gas.
Dati campione
I valori della massa, se si è fatta attenzione a non lasciar evaporare l'acqua o
non far condensare vapore sulle pareti esterne, si mantengono costanti sia per
i corpi solidi, che liquidi, che gassosi, anche se è variata la temperatura
Discussione dei risultati
È opportuno far notare che questo comportamento della grandezza che
chiamiamo "massa" la rende adatta ad esprimere la quantità di materia che
costituisce i corpi.
Considerazioni conclusive
Se non viene aggiunta o sottratta materia ad un corpo, la sua massa si
conserva costante a qualunque valore della temperatura.
Si conserva la forma di un corpo a freddo/a caldo?
I fase del percorso: Obiettivi
Riconoscere che il volume di un corpo varia al variare della temperatura, sia per i solidi, che
per i liquidi e per i gas.
Materiale necessario
una sorgente di calore;
una sferetta di acciaio sospesa con una catenella;
un anello di acciaio dello stesso diametro della sferetta;
una bottiglia di plastica;
un coltello zigrinato;
un congelatore;
una beuta munita di tappo forato attraversato da un tubicino di vetro;
un palloncino;
un calibro.
Descrizione della procedura
Il volume di un solido: Verificare che la sferetta di acciaio a freddo passa
attraverso l'anello a tenuta. Scaldare la sferetta di acciaio e provare a farla
passare di nuovo attraverso l'anello.
Riempire con acqua una bottiglia di plastica, lasciarla senza tappo e
metterla in congelatore. Quando è tutta congelata, estrarla e con un coltello
zigrinato asportare il ghiaccio che fuoriesce dal collo. Tapparla e attendere
che scongeli lasciandola esposta all'aria ambiente.
Il volume di un liquido: Riempire con acqua la beuta fino all'orlo e
chiuderla col tappo forato munito di tubicino di vetro: in quest'ultimo si
vedrà risalire una colonnina di acqua. Segnare con una tacca il livello
dell'acqua nel tubicino. Scaldare la beuta su un fornello e osservare.
Il volume di un gas: Soffiare un po' d'aria in un palloncino, chiuderlo bene
e controllare il diametro con un calibro. Tenere sommerso il palloncino per
alcuni minuti in acqua molto calda, estrarlo e ripetere la misura del diametro
col calibro.
Si conserva il volume di un corpo solido a
freddo/a caldo?
Un cubetto di metallo immerso per alcuni
minuti in acqua molto calda aumenta di
volume, ma rimane di forma cubica. La forma è
controllabile con un calibro nelle tre dimensioni
altezza, larghezza, profondità.
Si conserva la forma di un corpo
semisolido a freddo/a caldo
Nel caso del brodo il passaggio
dalla fase semiliquida (sol) a
quella semisolida (gel) è
determinato dall'abbassamento
di temperatura ed è reversibile:
basta infatti riscaldare il gel per
avere di nuovo il sol.
Nel caso dell'albume d'uovo il
passaggio dalla fase semiliquida
a quella semisolida è
determinato dall'innalzamento di
temperatura ed è irreversibile.
Dati campione
La sferetta di acciaio, dopo che è stata scaldata, non passa più attraverso l'anello
perché è aumentata di volume.
L'acqua ottenuta per fusione del ghiaccio invece occupa minore volume del ghiaccio
stesso.
L'acqua liquida aumenta di livello nel tubicino del tappo della beuta man mano che
procede il riscaldamento.
Il gas scaldato aumenta di volume.
Discussione dei risultati
Generalmente i corpi aumentano di volume quando aumenta la temperatura. Sarà
opportuno far notare l'anomalia di comportamento dell'acqua nella transizione da solido
a liquido (e viceversa).
Considerazioni conclusive
Se non viene aggiunta o sottratta materia ad un corpo, il suo volume varia al variare della
temperatura. Questo comportamento della grandezza che chiamiamo "volume" lo rende
inadatto ad esprimere la quantità di materia che costituisce i corpi.
Si conserva il colore di un corpo a freddo/a caldo?
I fase del percorso: Obiettivi
Riconoscere che il colore di un campione di sostanza non sempre si conserva quando
esso viene scaldato, in particolare se ciò comporta un cambiamento di fase, o un
processo di disidratazione- idratazione.
Materiale necessario
iodio in cristalli;
imbuto di vetro;
vetri d'orologio o capsule di Petri (o piattini resistenti al calore);
pinze di legno;
etanolo;
solfato di rame azzurro;
mortaio e pestello;
bilancia con sensibilità di 0,01 g;
sorgente di calore.
Descrizione della procedura
•In un vetro d'orologio sciogliere qualche cristallino di iodio in etanolo e osservare il
colore rossiccio della soluzione. In un altro vetro d'orologio porre qualche
cristallino di iodio e scaldare sulla fiamma. Tenere con le pinze di legno un imbuto
capovolto un po' inclinato in modo da raccogliere i vapori che si producono.
Osservare il colore viola dei vapori ottenuti e fare ipotesi sul tipo di sostanza.
Quando si osserva la formazione di microcristalli sulle pareti dell'imbuto, far cadere
un filo di etanolo per controllare se la sostanza depositata è ancora iodio.
•Sciogliere in acqua un piccolo campione di sale azzurro e osservare il colore della
soluzione. Pestare nel mortaio un po' di solfato di rame azzurro e metterne piccoli
campioni su 2 vetri d'orologio.
•Controllare il valore della massa di uno dei 2 vetri d'orologio col campione di sale
azzurro. Scaldare alla fiamma finché il sale non diventa bianco. Controllare il
valore della massa. Lasciare all'aria per alcuni giorni finché il sale non torna ad
assumere il colore azzurro. Controllare il valore della massa.
•Scaldare anche l'altro campione, scioglierlo in acqua e osservare il colore della
soluzione. Lasciare evaporare l'acqua dalla soluzione e osservare il colore del
sale.
Comprendere la diversa natura delle grandezze fisiche calore e temperatura
attraverso il modello microscopico della materia
Obiettivi.
Conoscenze: il calore come forma d’energia. La diversa natura delle grandezze
fisiche: calore e temperatura.
Abilità: distinguere il calore da altre forme d’energia. Individuare la relazione tra
calore e movimento. Rilevare la relazione tra il calore e la variazione della
temperatura di un corpo, riconoscendo le condizioni d’equilibrio. Riconoscere la
temperatura come una caratteristica fisica dei corpi. Utilizzare correttamente le
unità di misura del calore e della temperatura.
Contenuti. Il calore e la temperatura: diversa natura delle due grandezze fisiche.
Trasferimento di calore ed equilibrio termico. Unità di misura del calore e della
temperatura. Calore come forma d’energia: interpretazione microscopica.
Metodi e attività. Nella trattazione dell’argomento si farà ricorso in modo
preponderante, per la natura dei contenuti, al metodo induttivo-sperimentale. Il
percorso operativo sarà affrontato in maniera problematica, ricorrendo sempre
alla discussione. Si studieranno, infine, in modo qualitativo e semiquantitativo la
diversa natura delle grandezze fisiche calore e temperatura anche alla luce del
modello microscopico della materia
Itinerario didattico: s’ipotizza che gli allievi abbiano osservato sperimentalmente, negli anni
precedenti, il comportamento di alcuni materiali al calore; che abbiano lavorato sul modello
microscopico della materia e sui passaggi di stato; che abbiano, infine, interpretato, alla luce
del modello microscopico, vari fenomeni fisici dipendenti dal calore. Si proporranno, pertanto,
alcune esperienze per affrontare ad un primo livello il concetto di calore attraverso le seguenti
domande problematiche:
1. il calore è una sostanza oppure è " qualcosa" di immateriale?
2. Il calore può essere considerato come una forma d’energia ?
Come riferimento al primo problema s’indurranno gli alunni ad ipotizzare che, se il calore
fosse una qualche sostanza trasmissibile con il riscaldamento di un corpo, questo dovrebbe
pesare di più; se invece fosse ‘qualcosa d’immateriale’, lo stesso corpo, dopo il riscaldamento,
dovrebbe conservare inalterato il proprio peso. Per verificare l’ipotesi si faranno riscaldare tre
pesetti metallici rispettivamente da 100 g, 20 g, 10 g sulla piastra elettrica per 5 minuti,
pesandoli prima e dopo il riscaldamento. Il confronto tra le misure effettuate confermerà che
il peso di ciascun campioncino metallico rimane invariato, confermando l’ipotesi, ovvero che il
calore non è una sostanza ma qualcosa d’immateriale.
Ma se il calore non è una sostanza, che ‘cosa’ sarà invece? Può essere considerato come una
forma d’energia?
Il secondo problema scaturirà, pertanto, spontaneamente dal primo.
I ragazzi, attingendo alle conoscenze precedenti, ricavate dai diversi ambiti, sanno già che
l’energia genera movimento. Pertanto se, mediante un esperimento progettato ad hoc,
riusciranno ad ottenere il movimento come conseguenza del calore impiegato, potranno
rispondere affermativamente alla domanda.
Un semplice ma significativo esperimento funzionale allo scopo potrebbe consistere nel
riscaldare l’acqua contenuta in una beuta: il vapore acqueo, prodotto dall’evaporazione e
convogliato verso una leggera elica realizzata con carta stagnola, provocherà il movimento di
questa. L’evidenza sperimentale confermerà l'ipotesi formulata: il calore è una forma
d’energia poiché attraverso il vapore induce il movimento dell’elica, il quale cessa quando
non è più fornito calore e, di conseguenza, si riduce notevolmente la quantità di vapore
rilasciato .
A questo punto del percorso i ragazzi
hanno elementi sufficienti a discriminare
il calore dalla temperatura.
Hanno compreso che il primo è una
forma di energia legata al movimento
delle particelle materiali, che passa da un
corpo più caldo ad uno meno caldo
provocando il raffreddamento del primo
e il riscaldamento del secondo. Ad
esempio, immergendo un chiodo rovente
in un bicchiere contenente dell'acqua si
ha un trasferimento di calore dal chiodo
al liquido, che può essere rilevato
misurando, con un termometro, la
temperatura dell'acqua prima e dopo
l'immersione del chiodo.
Potranno verificare che, riscaldando, a
fiamma costante, masse d'acqua
disuguali, queste si riscaldano
diversamente. Precisamente, alla massa
più calda corrisponde una temperatura
maggiore, rilevata con il termometro.
I ragazzi discuteranno sulla diversa natura del
calore e della temperatura, rifacendosi o ad
esempi noti dal quotidiano o ai diversi
fenomeni studiati nel corso della propria
esperienza scolastica.
Dalla discussione emergerà che la temperatura
e il calore sono due grandezze fisiche diverse:
la seconda è una forma d’energia, la prima ci
dice quanto un corpo è caldo o freddo e, in un
certo senso, c’indica il grado di concentrazione
raggiunto dal calore in un corpo.
Dalle esperienze svolte negli anni passati, i ragazzi sono a conoscenza che la temperatura si
misura con il termometro e che la sua unità di misura è il grado centigrado. Mettendo a
contatto due corpi a diversa temperatura, osserveranno che quello più caldo cede calore a
quello meno caldo e che questo trasferimento continua fino a quando entrambi i corpi non
avranno raggiunto la stessa temperatura o temperatura d’equilibrio. Per esemplificare, si
faranno preparare due campioni della stessa quantità d’acqua a temperature diverse. Si
misurerà con accuratezza la temperatura T1 e T2 dei due campioni facendo una previsione
sulla temperatura che si otterrà dal loro mescolamento. Si mescoleranno quindi i due
campioni e si misurerà la temperatura finale. La temperatura sperimentale, nel limite delle
incertezze legate all’attività di misurazione, concorderà con la media aritmetica delle due
temperature iniziali.
S’introdurrà teoricamente il concetto di caloria,
rimandando la trattazione operativa della
questione al successivo corso di studi.
Si dirà, pertanto, che l'unità di misura del
calore si chiama caloria: essa è la quantità di
calore necessaria per aumentare di un grado
centigrado (da 14,5 °C a 15,5 °C) un grammo
d’acqua distillata.
La dilatazione termica dei corpi
Obiettivi.
Conoscenze: la dilatazione termica dei corpi solidi, liquidi e aeriformi. Abilità: distinguere
la dilatazione lineare da quella volumetrica . Rilevare la dipendenza della dilatazione
lineare da diverse variabili come: tipo di materiale, quantità di calore fornito, lunghezza,
spessore, tempo d’esposizione al calore. Rilevare che i gas si dilatano più dei liquidi e dei
solidi, a parità di calore fornito. Utilizzare il modello particellare della materia per
spiegare la diversa dilatazione dei corpi.
Contenuti. La dilatazione termica dei corpi. Dilatazione lineare e volumetrica. La diversa
dilatazione dei corpi e il modello microscopico della materia.
Metodi e attività. Gli argomenti Di questa unità di lavoro possono essere trattati come
prosecuzione dell’unità già pubblicata “Calore e temperatura” oppure in modo
indipendente. Si farà ricorso principalmente al metodo induttivo – sperimentale,
considerata la natura dei contenuti, partendo sempre dalle preconoscenze degli alunni
per guidarli a conquistare gradualmente la comprensione dei significati.
Itinerario didattico: si partirà dal presupposto che gli allievi siano in possesso delle
competenze previste dall’unità di lavoro su calore e temperatura, che abbiano lavorato sul
modello microscopico della materia, sugli stati fisici e sui passaggi di stato anche in termini
microscopici, che abbiano, infine, interpretato, alla luce del modello particellare, vari
fenomeni fisici dipendenti dal calore. Si proporranno, pertanto, tre diverse esperienze
riguardanti la dilatazione dei corpi nei diversi stati d’aggregazione: solido, liquido,
aeriforme.
1^ Esperienza: la dilatazione
dei corpi solidi
PROBLEMA - DOMANDA: "Che
cosa succede riscaldando delle
sbarrette metalliche di
materiale diverso?"
Lo scopo è osservare la
dilatazione di un corpo solido
(il cui spessore è trascurabile
rispetto alla sua lunghezza). Si
utilizzeranno: dilatometro
lineare, accendino, sbarretta di
ferro, sbarretta d’ottone,
sbarretta d’alluminio, alcool
denaturato. Le sbarrette
cilindriche avranno una
lunghezza di circa 20 cm e lo
spessore di 5 mm circa.
OSSERVAZIONE: l’asticella di metallo,
dilatandosi per effetto del calore, muoverà
una leva, che, a sua volta, attiverà un
indice su una scala graduata; l’indice
segnerà tre differenti valori per la
dilatazione di ciascuna delle sbarrette
metalliche.
CONCLUSIONI: il metallo che, a parità di
tempo d’esposizione alla fiamma,
evidenzia una maggiore dilatazione è
l'alluminio, seguito dall'ottone e dal ferro; la
dilatazione lineare di una sbarretta
metallica dipende, quindi, dal materiale di
cui è costituita, a parità d’altre variabili
(tempo d’esposizione alla fiamma,
lunghezza, spessore ).
NOTA: naturalmente le sbarrette si dilatano
volumetricamente ma tale dilatazione può
essere considerata trascurabile rispetto a
quella lineare.
POSSIBILI DOMANDE APERTE:
1. la lunghezza della sbarretta
influenza la dilatazione lineare del
metallo, a parità di altre variabili
( materiale metallico, spessore,
quantità di calore fornito)?
2. Lo spessore della sbarretta
influenza la dilatazione lineare del
metallo, a parità d’altre variabili
( materiale metallico, lunghezza,
quantità di calore fornito)?
2^ Esperienza: la dilatazione
dei corpi liquidi.
PROBLEMA – DOMANDA: "Che
cosa succede ad un liquido
fornendogli calore?"
Lo scopo è osservare la
dilatazione di un liquido. Si
utilizzeranno: termometro,
fornello elettrico, ampolla di
vetro pyrex, tappo di gomma
forato, tubicino di vetro, becker,
pennarello indelebile, acqua
colorata.
OSSERVAZIONE: il volume
dell'acqua colorata nell'ampolla
aumenterà progressivamente
all'aumentare della quantità di
calore assorbito, come si può
rilevare dall'elaborazione dei dati.
CONCLUSIONI: i liquidi riscaldati si
dilatano, aumentando di volume,
ed il fenomeno è più appariscente
di quello che si osserva nei solidi
3^ Esperienza: la dilatazione dei
corpi gassosi
PROBLEMA - DOMANDA: "Che
cosa succede ad un gas
riscaldandolo?"
Lo scopo è osservare la
dilatazione di un gas. Si
utilizzeranno: termometro, siringa
senz’ago, fornello elettrico,
supporto con pinze, becker,
acqua.
PROCEDIMENTO: prendere una
siringa senz’ago e chiuderne
ermeticamente il foro d’uscita
riscaldandola alla fiamma;
riempire un becker d’acqua e
disporlo sul fornello elettrico;
fissare la siringa sul supporto e
immergerla non completamente
nell’acqua; immergere un
termometro vicino alla siringa,
fissandolo sul supporto;
accendere il fornello.
OSSERVAZIONE: all’aumentare della
quantità di calore fornito, il gas all’interno
della siringa si dilata volumetricamente e lo
stantuffo scorre all'indietro.
CONCLUSIONI: si osserva che anche i gas
si dilatano, come succede ai solidi e ai
liquidi, e, inoltre, molto più di questi.
NOTA
E' importante notare che nel primo esperimento, relativo ala dilatazione
delle sbarrette metalliche, si misura una dilatazione lineare, anziché
una dilatazione volumetrica, perché si considera trascurabile lo
spessore della sbarretta rispetto alla sua lunghezza.
Nella dilatazione dell'acqua colorata ( secondo esperimento), si misura
un aumento di livello ovvero una lunghezza, quindi, può sembrare che
si misuri una dilatazione lineare. In realtà, si rileva una variazione di
volume tramite una misurazione di lunghezza, poiché l'aumento di
livello è determinato dall'aumento di volume del liquido.
Per finire, si può affermare che i gas si dilatano molto di più delle
sostanze liquide e solide, e che i solidi si dilatano meno di tutti. Questo
fa comprendere come, il non considerare, nel secondo esperimento, la
dilatazione dell'ampolla di vetro, porti ad un errore trascurabile.
La Propagazione Del Calore [Unità Di Lavoro]
Obiettivi.
Conoscenze: la propagazione del calore nei diversi mezzi fisici.
Abilità: osservare le diverse forme di propagazione del calore e
utilizzare il modello particellare della materia per interpretarne le cause;
osservare l'emissione e l'assorbimento delle radiazioni termiche in
semplici fenomeni e interpretarne in termini particellari la dipendenza
dalla superficie dei corpi.
Contenuti. I meccanismi di propagazione del calore: conduzione,
convezione e irraggiamento. Emissione e assorbimento delle radiazioni
termiche riguardo alle diverse superfici dei corpi: interpretazione
mediante il modello particellare della materia.
Metodi e attività. Il calore, la temperatura e la dilatazione termica dei
corpi sono stati già trattati pertanto, le forme di propagazione del calore
saranno introdotte operativamente per cercare di approfondire la natura
del calore.
S’illustrerà ai ragazzi lo scopo delle esperienze sulla propagazione del
calore, anticipando che i meccanismi fondamentali sono tre:
1. conduzione;
2. convezione;
3. irraggiamento.
Le esperienze saranno precedute da un’attività d’indagine sulle loro
preconoscenze e di riflessione su alcuni fenomeni termici quotidiani, ad
esempio le differenti sensazioni termiche percepite d'inverno, scendendo
dal letto e poggiando i piedi nudi sul pavimento oppure sul tappeto:
sensazione di freddo per il pavimento, sensazione "neutra" per il tappeto.
Qual è la causa delle differenti percezioni, se pavimento e tappeto
sono nello stesso ambiente e quindi a uguale temperatura?
1^ esperienza:
“Come si propaga il calore in un’asticciola
metallica e in una di vetro, di lunghezza e
spessore uguali?”
Lo scopo è di osservare la propagazione del
calore, per conduzione, in due materiali
diversi (un buon conduttore e un cattivo
conduttore).
Saranno utilizzati:
un ago da maglia o un'asticciola metallica,
un'asticciola di vetro, graffette metalliche,
pinza di legno, cera di candela per fissare le
graffette metalliche, due sorgenti di calore
L'esperimento conferma qualitativamente quanto già previsto:
l'asticciola metallica è una buona conduttrice del calore mentre quella di vetro non
lo è. La quantità di calore che si propaga nell'unità di tempo è maggiore nella
prima.
Si discuterà con i ragazzi quanto avviene dal punto di vista microscopico nella
conduzione del calore e per quale motivo certi materiali conducono il calore meglio
di altri, ricorrendo al modello cinetico molecolare
NOTA DIDATTICA.
In realtà i corpi metallici sono buoni conduttori del
calore non solo perché i loro atomi sono ordinati ma
anche e soprattutto perché l'energia cinetica viene
trasportata dagli elettroni liberi di muoversi nel
cristallo.
Nei liquidi le particelle sono abbastanza disordinate,
nei gas, infine, il disordine è massimo, quindi le
vibrazioni si propagano con molta difficoltà nel
volume da essi occupato. Questo spiega la
bassissima conduttività termica dell'aria.
Dal punto di vista teorico, il modello cinetico
molecolare ci offre un indizio molto interessante
sulla natura del calore: sembra che si tratti solo di
movimenti più o meno accentuati delle particelle
elementari.
2^ esperienza: "Come si propaga il calore in un liquido?"
Lo scopo dell’esperimento è di osservare la propagazione del calore nei liquidi per
convezione. Il materiale sarà un becker, una piastra elettrica, acqua e segatura. Dopo alcuni
minuti dall’inizio del riscaldamento, si osserveranno degli spostamenti sempre più intensi,
all’aumentare della temperatura: la segatura si muoverà descrivendo due vortici a spirale,
simili a due circoli chiusi.
Tolto il becker dalla piastra e messo a contatto con una superficie più fredda si noterà che il
movimento della segatura rallenterà con la perdita di calore. L'evidenza sperimentale
conferma che la propagazione del calore in un liquido avviene con trasporto di materia; i
movimenti osservati si chiamano moti convettivi.
Si farà notare agli alunni che le correnti ascensionali calde e quelle discendenti meno calde
continueranno fino a quando la sorgente di calore sarà attiva.
I moti convettivi osservati sono originati da differenze di densità del liquido, consequenziali
alle differenze di temperatura. Si farà, inoltre, notare che i moti convettivi avvengono anche
nell’aria per gli stessi motivi. Più avanti negli studi, i ragazzi avranno modo di comprendere
che, dal punto di vista molecolare, la conduzione non differisce molto dalla convezione. In
entrambi i casi, il calore si propaga, infatti, per gli urti delle molecole dal corpo caldo al corpo
freddo, ma,
mentre nei fluidi il processo si manifesta con spostamento di materia, nei solidi questo non
avviene, nel senso globale del termine. Perfezioneranno la comprensione di tali fenomeni
mediante lo studio dei moti molecolari browniani,
spontanei nei liquidi e nei gas, meno accentuati nei primi e intensi nei secondi.
DOMANDA: "Perché in un liquido la propagazione del calore avviene con
trasporto di materia e in un solido invece no?"
La domanda è sorta spontaneamente in alcuni gruppi e presto si è trasformata in
discussione generale.
I ragazzi in seconda media hanno studiato approfonditamente il modello
microscopico della materia, ricavandolo in maniera indiretta, ovviamente, dallo
studio di particolari fenomeni come la dissoluzione di zucchero o sale nell'acqua, la
diffusione di una goccia di blu di metilene in acqua, i passaggi di stato dell'acqua e
alcuni comportamenti termici della materia. Pertanto, hanno messo in relazione la
modalità di diffusione del calore in un liquido con la struttura microscopica di tale
stato di aggregazione.
Queste le conclusioni alle quali sono giunti, formulate con le
loro parole:
" Sappiamo che in un liquido i legami interparticellari sono più deboli
che in un solido, tanto da permettere alle particelle materiali di
allontanarsi abbastanza fra di loro ma fino ad un certo punto.
Assorbendo calore da una sorgente le particelle allentano ancor di più
i legami di richiamo distanziandosi ulteriormente.
Osservando i movimenti delle correnti ascensionali di acqua nel
becher, messi in evidenza dalla segatura che appare trascinata verso
l'alto, sembrerebbe quasi che le particelle siano diventate più leggere.
Ma le cose stanno proprio così oppure l'energia termica acquistata le
ha velocizzate facendole risalire in superficie?
Forse sono vere entrambe le ipotesi. In effetti l'acqua calda,
dilatandosi è anche meno densa e di conseguenza più leggera di
quella meno calda, che si trova nelle altre parti.
Le correnti discendenti verso il basso in effetti sembrano essere inevitabili perché le
particelle" più calde" risalite "scacciano"quelle più fredde costringendole verso il basso.
Le particelle della corrente discendente sono anche più lente perché meno calde ed è come
se rimanessero indietro rispetto a quelle più veloci che risalgono. Quando, a loro volta,
acquistano energia in vicinanza alla sorgente di calore, risalgono richiamando le particelle più
fredde e il processo continua finchè la sorgente di calore è attiva.
Quando, infatti, questa viene spenta si assiste ad un progressivo rallentamento dei
movimenti, prima vorticosi, fino a quando cessano completamente a raffreddamento
raggiunto.
In definitiva, i moti convettivi osservati sembrano originati da differenze di densità del
liquido, consequenziali alle differenze di temperatura.
Questi moti, prodotti naturalmente da differenze di temperatura, vengono sfruttati in molti
impianti solari per acqua calda mediante la disposizione dei pannelli in basso e il serbatoio in
alto. Tale disposizione permette all'acqua di circolare per convezione naturale senza
l'impiego di costose pompe.«
Un' altra considerazione dei ragazzi è stata la seguente:
"Ci sembra che la convezione del calore avvenga anche nell'aria. Infatti,
nell'esperimento dell'elica di stagnola, questa si è messa in moto per azione delle correnti
ascensionali di aria calda, generate nell'ambiente dal sistema scaldante fornello/beuta, ,
quindi, ancora per differenze di densità dell'aria, dovute alle differenze di temperatura."
NOTA DIDATTICA:
Le conclusioni dei ragazzi sono veramente interessanti e, anche se il
fenomeno è molto più complesso, stanno acquisendo il giusto modo di
affrontare lo studio dei fatti scientifici.
Avranno modo di comprendere che, dal punto di vista molecolare, la
conduzione non differisce molto dalla convezione.
Infatti, in entrambi i casi, il calore si propaga per urti delle molecole
dal corpo caldo al corpo freddo, ma, mentre nei fluidi il processo si
manifesta con spostamento di materia, nei solidi questo non avviene, nel
senso globale del termine.
Nel livello scolare superiore avranno modo di approfondire le questioni
poste mediante lo studio dei moti molecolari browniani, spontanei nei
liquidi e nei gas, meno accentuati nei primi e intensi nei secondi.
Prima di passare agli esperimenti sull’irraggiamento si
specificherà che questa forma di propagazione del
calore è la più complessa per il suo elevato grado di
"astrattezza"
Sarà anche utile avviare una riflessione su
alcune trasformazioni energetiche,
conosciute dall'esperienza quotidiana, in
cui interviene l'irraggiamento, specificando
che esiste una forma di energia raggiante,
proveniente da sole o da altre sorgenti ad
alta temperatura, che può trasformarsi in
energia termica, chimica, elettrica e in altre
forme secondo la natura del corpo che la
riceve.
L' irraggiamento può essere considerato
una modalità di trasmissione di energia da
un corpo (sorgente) ad un altro, senza
trasporto di materia; infatti, i raggi solari
attraversano lo spazio vuoto tra la terra e il
sole
Prima di passare agli esperimenti ho avviato una riflessione su
alcune trasformazioni energetiche, conosciute dall'esperienza
quotidiana, in cui interviene l'irraggiamento per prepararne lo
"scaffolding" più appropriato, ponendo le seguenti domande:
1. "Quando ci esponiamo sulla spiaggia ai raggi solari, è solo l'aria
che ci scalda o anche l'energia che proviene direttamente dal
sole?".
2. "E quando esponiamo la nostra mano ad una fiamma o ad un
riscaldatore qualunque, a temperatura elevata?".
I ragazzi hanno convenuto che, in effetti, in queste situazioni la
convezione non è sufficiente a dare spiegazione del fenomeno, per
cui è necessario ipotizzare un'altra modalità di propagazione del
calore, l'irraggiamento, appunto.
Altra domanda:
"L'energia, proveniente dal sole o da altre sorgenti ad alta temperatura,
si trasforma, secondo voi, soltanto in energia termica?".
I ragazzi,dopo aver discusso fra di loro, hanno risposto di no, portando a
sostegno della loro conclusione alcuni esempi:
le foglie degli alberi utilizzano l'energia solare per produrre energia
chimica con la fotosintesi clorofilliana;
l'abbronzatura della pelle è un effetto chimico che si aggiunge al
riscaldamento della pelle;
nella cella solare fotovoltaica al silicio, costruita in Educazione tecnica,
si ottiene energia elettrica in grado di far funzionare un motorino.
Le conclusioni dei ragazzi non fanno una grinza, pertanto possiamo
convenire che esiste una forma di energia raggiante proveniente da sole
o da altre sorgenti ad alta temperatura, che può trasformarsi in energia
termica, chimica, elettrica e in altre forme a seconda del corpo che la
riceve.
3^ esperienza: “Come si riscaldano
differenti quantità d’acqua e quantità
uguali di sostanze diverse, esposte ai
raggi solari?”
Lo scopo dell’esperimento è osservare
il riscaldamento di materiali uguali (presi
in quantità diverse) e di materiali diversi
(presi in quantità uguali), come effetti
dell'irraggiamento solare.
S’impiegheranno quattro termometri
(sensibilità un grado centigrado),
L’evidenza sperimentale porterà alla
quattro secchielli da spiaggia di plastica conclusione che, a parità d’esposizione ad
trasparente, acqua e sabbia
una stessa sorgente termica: masse
diverse di sostanze uguali (acqua, nella
fattispecie) si riscaldano in maniera diversa
(di più la quantità minore); parimenti masse
uguali di sostanze diverse (acqua e
sabbia) si riscaldano in maniera diversa (di
più la sabbia).
Si potranno svolgere esperimenti per
verificare come le radiazioni termiche sono
filtrate in maniera differente dai diversi
materiali
PROCEDIMENTO:
scegliere per l'esperimento una calda giornata soleggiata ( come
abbiamo fatto noi);
predisporre due diverse quantità di acqua in due dei quattro secchielli
(ne abbiamo utilizzato 1+1/2 litro nel primo; 1/2 litro nel secondo
secchiello);
predisporre due uguali quantità di acqua e di sabbia ( 1/2 litro per la
prima e l'equivalente quantità per la seconda) negli altri due secchielli;
esporre contemporaneamente, la mattina verso le dieci; i quattro
secchielli in una zona soleggiata, all'aperto e aspettare;
verso le 12.30, rilevare la temperatura raggiunta dall'acqua e dalla
sabbia, inserendo due termometri uguali contemporaneamente nei due
secchielli.
Verso le 15.30 del pomeriggio, ripetere la stessa procedura per i due
secchielli contenenti acqua in quantità diverse.
In particolare, una superficie nera assorbe
più energia termica radiante rispetto ad
una superficie lucida; materiali come il
plexiglas o la carta sono opachi rispetto
alla radiazione; i cristalli di cloruro di sodio
sono trasparenti rispetto ad essa.
Per quanto riguarda l’emissione d’energia
termica radiante, una superficie nera ed
opaca ne emette di più rispetto ad una
superficie lucida e levigata; una superficie
ruvida e annerita emette molta più energia
radiante nell'unità di tempo di una
superficie speculare