![Metalli 1 [modalità compatibilità] - Associazione Studenti di Agraria](//s1.studylibit.com/store/data/001082019_1-ef2165bb8ef8e40db2967c102b73dc32-768x994.png)
Inquinamento del suolo, industriale,
agricolo e zootecnico.
Il suolo: centro degli equilibri ambientali
Aria e acqua rappresentano sistemi
relativamente fragili
Il suolo rappresenta il nodo centrale degli
equilibri biogeochimici degli elementi
contenuti nelle sostanze che vi arrivano,
esso costituisce l’interfaccia attraverso cui
avvengono gli scambi con gli altri comparti
ambientali: acqua, aria e piante.
Il suolo
rappresenta il comparto ambientale che reagisce
in misura maggiore all’inquinamento da metalli
a) Capacità di diluizione;
b) Diversi meccanismi che può mettere in atto al fine di opporsi ai
cambiamenti indotti dagli input “immissione” di metalli;
IMMOBILIZZAZIONE /PRECIPITAZIONE
I metalli pesanti non sono soggetti ad alcun
processo di decomposizione
MECCANISMI di TRASPORTO
1)
2)
3)
Chimico
Fisico
Biologico
ALTRO COMPARTO AMBIENTALE
il contenuto totale di metallo nel suolo, da
solo, non è indicativo della sua pericolosità
•la nocività dei metalli pesanti dipende dalla
loro mobilità;
•La mobilità è in relazione alla forma chimica
in cui esso si presenta;
•Lo ione libero (acquoione) è la forma più
tossica;
•La forma complessata o adsorbita sul
materiale colloidale è meno tossica: fa
eccezione il mercurio.
Gli effetti tossici dei metalli non sono in relazione al contenuto totale
presente nel suolo, ma alla frazione mobile potenzialmente biodisponibile;
MOBILITA’
•Biodisponibilità per le piante;
•Potenziale lisciviabilità nelle acque profonde
INGRESSO NELLA CATENA ALIMENTARE.
NOCIVITÀ
1) Suolo
2) Piante
La Biodisponibità: significato ecotossicologico
•Bioaccessibilità o disponibilità ambientale: frazione
del metallo totale disponibile (solubile) a causa di
fattori fisici, chimici, e biologici; capacità di un metallo
di interagire con matrici ambientali e subire processi di
trasporto, es Cu2+ (al contrario di CuS) può essere
disponibile per interagire con gli organismi,
l’ossigenazione del suolo può trasformare CuS in Cu2+
rendendolo ambientalmente disponibile;
•Biodisponibilità: frazione del metallo bioaccessibile
che interagisce con le membrane cellulari;
•Bioaccumulo: accumulo netto del metallo in un
organismo esposto
Il
concetto
di
biodisponibilità
deriva
dalla
consapevolezza che gli effetti che i metalli presenti
nelle varie matrici ambientali hanno sugli organismi e
la loro tossicità nei confronti di questi, non sono
correlabili con la quantità di metallo totale ma con una
frazione biodisponibile.
1)Forme chimiche biodisponibili;
2)Biodisponibilità di un metallo.
Nei vari comparti ambientali a quale fase è
associabile il concetto di specie biodisponibile?
•Alla fase liquida che nei suoli e sedimenti riguarda
essenzialmente l’acqua interstiziale;
•Alla fase solida (Adsorbimento fisico e chimico).
Concetto dinamico di biodisponibilità
Le varie forme dei metalli partecipano ad
equilibri che si instaurano tra fase solida e
fase liquida.
Può essere quindi difficile identificare la
frazione “disponibile” e la frazione “non
disponibile”.
Frazione biodisponibile: frazione di composto
chimico (metallo) presente in uno specifico
comparto che è disponibile o può diventare
disponibile per organismi o piante;
•Biodisponibilià attuale;
•Biodisponibilità potenziale;
La biodisponibilità di un metallo è un fenomeno
complesso, che dipende dal metallo, dalla matrice
e dalla specie ed è influenzato da una serie di
parametri fisici, chimici e biologici;
Percorso per l’assorbimento dei metalli da parte delle piante
•In un suolo (contaminato), il percorso principale di assorbimento di un
metallo è l’assorbimento per via radicale che avviene dalla soluzione del
terreno;
•La concentrazione dei metalli nella soluzione del terreno,è un buon
indicatore della biodisponibilità;
•La concentrazione dei metalli nella soluzione del terreno è determinata
dalla speciazione dei metalli;
•La speciazione dipende dalle caratteristiche del terreno (pH, sostanza
organica, argille, CSC)
•Le proprietà del vegetale selezionato sono un fattore essenziale per la
valutazione del rischio effettivo.
Speciazione chimica
Il termine di “speciazione” si riferisce al fatto che un contaminante
(metallo) può essere presente in una varietà di “forme chimiche”
con differente “valenza ambientale”
esempio la concentrazione molare del piombo nel suolo è:
ƩPb = 1) Pb2+, 2) Pb(OH)+, 3) PbCO3, 4) PbHCO3+, 5) PbSO4 + 6) PbAds +
Pb (Solidi sospesi) + ecc
METALLO
•Ione libero;
•Complessi solubili;
•Composti poco solubili;
•Ione adsorbito;
•Diversi stati di ossidazione.
Misura della biodisponibilità
Impiego dell’organismo “target” bersaglio = Bioavaibility target organism
Questa biodisponibilità può essere approssimata mediante l’impiego di test
chimici e biologici, nei quali i processi chimici o biologici agiscono per un
determinato periodo di tempo.
Sia i test chimici che biologici devono essere considerati solo degli strumenti
per la misura della biodisponibilità nei confronti di un organismo target
«bersaglio», ma i risultati ottenuti non possono essere considerati l’espressione
della biodisponibilità.
Estrazione sequenziale metalli pesanti con H2O < Ca(NO3) 2 < EDTA
Uno ione metallico complessato da una molecola di
EDTA; i sei atomi – due di azoto, quattro di ossigeno –
che coordinano lo ione M sono disposti al vertice di una
bipiramide a base quadrata che ha M al centro.
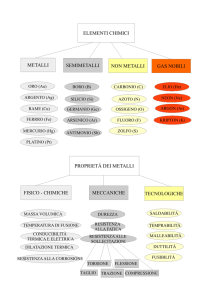
METALLI PESANTI
•I metalli sono costituenti naturali della crosta terrestre e sono presenti in
varie concentrazioni in tutti gli ecosistemi;
•Differiscono da altre sostanze tossiche perché non possono essere né
creati né distrutti;
•Tendono ad accumularsi nel suolo, sedimenti, acque marine ecc;
•I metalli pesanti sono le tossine più vecchie conosciute dall’uomo: il Pb
veniva usato per la lucidatura dell’argento già nel 2000 a.c.; l’arsenico era
usato durante la fusione del rame e dello stagno ed un primo uso è stato
scoperto per le decorazioni delle tombe egiziane;
•I metalli pesanti più diffusi sono:
•Pb, Cd, Zn, Cr, Hg, Cu
Tempo di persistenza del cadmio nei principali comparti ambientali
SERBATOIO
TEMPO di
PERSISTENZA
SERBATOIO
TEMPO DI
PERSISTENZA
BIOSFERA
ATMOSFERA
7d
OCEANI
DISCIOLTO
21.000 anni
PARTICOLATO
ORGANICO
1-3 anni
SEDIMENTI
3 – 6 anni
PIANTE MARINE
18 giorni
PIANTE ERBACEE TERRESTRI
20 giorni
BIOMASSA UMANA
1 – 40 anni
LETTIERA TERRESTRE
42 anni
LITOSFERA
109 anni
SUOLO (fina a 100 cm)
3000 anni
FRAZIONE ORGANICA
> 200 anni
Input di metalli pesanti antropici
•Agricoltura
•Industrie
•Traffico
•Questi input (immissione) potrebbero influenzare fortemente il
contenuto di metalli pesanti nel suolo e nelle falde e quindi
influenzare enormemente la qualità dell’ambiente e la salute umana;
Il contenuto di metalli pesanti nel suolo
Limite di legge soglia di contaminazione
Concentrazione soglia di contaminazione
Sostanze
mg/kg)
Contenuto
normale suoli
(min e max)
Uso Verde
Pubblico
Uso Industriale
e commerciale
Uso Agricolo
Arsenico (As)
6 (0,10-40)
20
50
Inesistenti
Cadmio (Cd)
0,35 (0,01-2)
2
15
Inesistenti
Cromo (Cr)
70 (5-1500)
150
800
Inesistenti
Rame (Cu)
30 (2-250)
120
600
Inesistenti
Mercurio (Hg)
0,06 (0,01-0,050)
1
5
Inesistenti
Piombo (Pb)
35 (2-300)
100
1000
Inesistenti
Zinco (Zn)
90 (1-900)
150
1500
Inesistenti
Concentrazione soglia di contaminazione (Csc): i livelli di contaminazione
delle matrici ambientali che costituiscono valori al di sopra dei quali è
necessaria la caratterizzazione del sito e l’analisi di rischio specifica come
individuati nell’allegato 5 alla parte quarta del Decreto Legislativo 152/06.
Fonte: NE Nomisma Energia
Sb = Antimonio Sn = Stagno In = Indio Te = Tellurio
•World Healt Organisation (WHO) limite: 10 µg/l per As (arsenico)
nelle acque;
Limiti previsti dalla legge per la presenza di metalli pesanti nelle acque
potabili e nelle acque minerali.
Valore limite di alcune sostanze contenute nell’acqua potabile e
nell’acqua minerale
Valori limite acque minerali
Valori limite acque potabili
Decreto 542/92 – Dm
Decreto L. 31/2001
31/05/2001
Arsenico totale
50
200
(mg/l)
Bario (µg/l)
1
Cromo (µg/l)
50
50
Piombo (µg/l)
10-25
10
Nitrati (mg/l)
50
45-10*
Alluminio (µg/l)
200
Nessun limite
Ferro (µg/l)
200
Nessun limite
Manganese
50
2000
(µg/l)
Cadmio (mg/)
5
10
Cianuri (mg/l)
50
10
Mercurio (mg/l)
1
1
Nichel (mg/l)
50
Nessun limite
Selenio (mg/l)
50
50
Fluoruro (mg/l)
1,50
Nessun limite
Fungicidi e Insetticidi utilizzati in agricoltura
•Più del 10% di fungicidi e insetticidi utilizzati in agricoltura contengono;
•Cu, Cd, Ni, Mn, Pb, Zn;
•L’arseniato di Pb, il solfato di Cu, i carbammati sono stati impiegati fin
dall’inizio del secolo scorso, ripetutamente e in quantità non trascurabili;
•Calcitazioni e concimazioni apportano come impurezze metalli pesanti
Attività mineraria in Sardegna
Argentiera: stabilimenti della miniera
dell’Argentiera: l’attività estrattiva cessò nel
1962; i minerali estratti erano piombo
argentifero e zinco: PbS galena e ZnS con
percentuali sensibili di argento; S = zolfo
solfuro di piombo, solfuro di zinco.
Montevecchio:
PbS galena e ZnS sphalerite
La contaminazione da metalli pesanti in Sardegna:
la situazione dell’Iglesiente:
I principali minerali estratti erano:
•sphalerite (ZnS) solfuro di zinco;
•Galena (PbS) solfuro di piombo
Il giacimento di Piombo – Zincifero di Montevecchio –
Ingurtosu – Gennamari, (Guspini, - Arbus) è suddiviso in tre
zone con le corrispondenti e relative miniere.
Contenuto di metalli nel suolo inquinato (ppm) di S.
Nicolò D’Arcidano:
Piombo
Cadmio
Zinco
3266
35,40
1495
Miniere di Iglesias – Gonnesa, Iglesias – Marganai (Domusnovas), (Barraxiuta)
Minerali estratti
Formula
Calcite
(CaCO3)
Galena argentifera
PbAgS
Sphalerite
[(Zn,Fe)S
Emimorfite
(Zn4Si2O7(OH )2 x (H2O)
Leadhillite
Pb4(SO4)(CO3) 2(OH )2
Galena argentifera
La laveria di barraxiutta in una foto d’epoca
Miniera di Barraxiutta
Miniera di Iglesiente – Marganai si estraevano
minerali sulfurei di Pb, Zn e Cu.
La parte superiore dell’impianto
Il contenuto totale in elementi nei suoli agrari, risultato degli input
(delle immissioni), provenienti da sorgenti diverse può essere
calcolato dalla relazione:
Elemento totale = (Er + Ed + Ef+ Epc + Ero + Eia) apporti – (Ea + Ev + Ee + EI) perdite
E = elemento
apporti
r = roccia madre
d= deposizione atmosferica
f= fertilizzanti
pc= prodotti chimici di varia natura utilizzati in agricoltura
ro= rifiuti organici
ia= immissioni accidentali di varia origine
perdite
a= assimilazione nei raccolti
l= lisciviazione
v= volatilizzazione
e= erosione
Passaggi di metalli pesanti dal suolo alla pianta
•Hanno una densità superiore a 5,0 g/cm3;
•Si comportano in genere come cationi;
•Presentano una bassa solubilità dei loro idrati;
•Hanno una spiccata attitudine a formare complessi;
•Hanno una grande affinità per i solfuri, nei quali tendono a concentrarsi;
•Hanno diversi stati di ossidazione a seconda delle condizioni di pH e di Eh.
Proprietà chimico–fisiche di alcuni metalli
Elemnto
Carica
Elettroneg
atività
Potenziale
ionico (eV)
Densità
(g/cm3 )
Diametro
ionico
idratato Å
Numero
coordinazione
rispetto a O2-
Potenziale redox
standard (V)
Cd
2
1,5
2,2
8,7
-
>6
-0,40
Co
2
1,7
2,6
8,9
6
6
-0,28
Cr
3
1,6
4,3
7,2
9
6
-0,74
Cu
2
2,0
2,5
8,9
6
6
+0,34
Hg
2
1,4
1,8
13,6
-
-
+0,85
Mn
2
1,5
2,0
7,4
6
6
-1,13
Mo
6
1,8
12
10,2
-
4
-1,05
Ni
2
1,7
2,6
8,9
6
6
-0,25
Pb
2
1,8
1,4
11,3
4,5
>6
-0,13
Sn
2
1,8
1,5
7,3
-
8
-
Zn
2
1,7
2,4
7,1
6
6
-0,76
Metalli pesanti
Ag, Cd, Co, Cr, Mn, Hg, Mo, Ni, Pb, Cu, Sn,Tl, Ti, V, Zn
Metalloidi: con proprietà simili a quelle dei metalli pesanti
As, Sb, Bi, Se
Tl = Tallio Ti = Titanio Sn = Stagno V = Vanadio
La definizione di biodisponibilità implica necessariamente la “interazione” tra
metallo e membrane cellulari;
Membrana cellulare: doppio strato fosfolipidico;
altri componenti:
•Carboidrati;
•Glicolipidi;
•Glicoproteine;
•Colesterolo;
•Proteine periferiche disposte su entrambe le facce
della membrana;
Alcune proprietà chimico - fisiche dei metalli pesanti
che condizionano il loro comportamento nel terreno
•Il raggio ionico e la valenza indicano la capacità vicariante del metallo
nelle diverse strutture cristalline;
•Il potenziale ionico (carica/raggio) risulta utile:
•A) per prevedere l’affinità dello ione per le superfici caricate;
•B) il potere flocculante dell’elemento;
•C) l’energia con la quale è ritenuto dalle superfici colloidali;
•La mobilità:
•<30 molto mobili (Fe++)
•30 – 95 idrossidi (Fe3+, Al3+, Cd2+, Pb2+, Cu2+, Zn2+;
•> 95 ossianioni solubili (Cr, V)
•L’elettronegatività ed il prodotto di solubilità dei solfuri danno
indicazioni sulla tendenza del metallo a formare derivati con radicali
alchilici elettropositivi, e sulla affinità per i gruppi amminici, imminici e
sulfidrilici della sostanza organica del terreno.
fine
![Metalli 1 [modalità compatibilità] - Associazione Studenti di Agraria](http://s1.studylibit.com/store/data/001082019_1-ef2165bb8ef8e40db2967c102b73dc32-768x994.png)