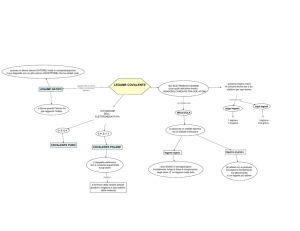
LEGAME CHIMICO:
Un legame tra due elementi che presentano elettronegatività uguale o
confrontabile viene detto covalente (E >= 1.9 ) per esempio H2 e N2. Un
legame che si forma tra un elemento molto elettropositivo e uno molto
elettronegativo viene detto ionico (per esempio NaCl; Uno >1.9 e uno <
1.9). Un legame tra elementi molto poco elettronegativi prende il nome di
legame metallico (E<1.9 entrambi).
LEGAME IONICO:
Il legame ionico si stabilisce quando è richiesta una modesta quantità di
energia per rimuovere uno o più elettroni dal guscio di valenza di un
atomo con bassa energia di ionizzazione e contemporaneamente libera
una grande quantità di energia quando l’atomo elettronegativo acquista
uno o più elettroni dall’altro.
Esempio: NaCl
Tutti i composti ionici allo stato solido non conducono la corrente perchè
gli ioni sono fortemente legati tra loro mediante legame ionico, mentre in
soluzione gli ioni sono liberi di muoversi e dunque conducono la corrente.
LEGAME COVALENTE:
Il legame covalente si instaura tra due atomi con elettronegatività uguale
o confrontabile. (esempio H2).
Possiamo definire l’energia di legame per una molecola biatomica A-B
come l’energia necessaria per rompere omoliticamente il legame
covalente, ottenendo così due atomi A e B nel loro stato energetico più
basso (stato fondamentale dell’atomo). Una rottura omolitica si ha
quanto gli elettroni di legame vengono equamente ripartiti tra i due
atomi originariamente legati.
LEWIS:
Regola dell’ottetto
1) Tutti gli elettroni di valenza degli atomi devono comparire nella
struttura.
2) Tutti gli elettroni sono generalmente accoppiati.
3) In genere ogni atomo completa il proprio ottetto nel livello esterno
(eccezione idrogeno).
4) Si possono formare legami multipli (specialmente con C,N,O,P,S ).
ORDINE DI LEGAME:
Per indicare il numero di legami che uniscono due atomi, si usa il concetto
di ordine di legame, definito come il numero di coppie elettroniche che
partecipano al legame tra due atomi (legame singolo, doppio e triplo).
All’aumento dell’ordine di legame corrisponde una diminuzione della
lunghezza del legame e un aumento dell’energia di legame.
CARICA FORMALE:
La carica formale di un atomo in una struttura di Lewis è data dalla
differenza tra il numero degli elettroni di valenza presenti nell’atomo
isolato e il numero di elettroni che gli vengono assegnati nella struttura di
Lewis.
𝐶𝐹 =
−
𝑒(𝑣𝑎𝑙𝑒𝑛𝑧𝑎)
−
−
[𝑒(𝑙.𝑝)
+
−
𝑒(𝑙𝑒𝑔𝑎𝑚𝑖)
2
]
L.P=doppietti solitari
RISONANZA O MESOMERIA:
Lo spostamento di doppietti elettronici da origine ad una serie di
strutture caratterizzate dallo stesso assetto di atomi ma una diversa
collocazione degli elettroni di legame e delle coppie solitarie (simili
formule di struttura).
ENERGIA DI RISONANZA:
Pauling notò che una molecola è più stabile quando risuona tra varie
formule limite rispetto a quando viene rappresentata dalla formula limite
più stabile.
ECCEZIONI ALLA REGOLA DELL’OTTETTO:
1) Quando il numero degli elettroni di valenza in una struttura di Lewis
è dispari, deve essere presente un elettrone spaiato (NO). Queste
molecole vengono dette radicali liberi.
2) Ottetti incompleti (BF3). Essendo l’atomo di Boro elettrondeficiente
ha una forte tendenza a formare legami covalenti con molecole
capaci di donare una coppia di elettroni ( legame dativo o di
coordinazione).
3) Guscio di valenza espanso.
Teoria VSEPR:
Lewis non da nessuna informazione riguardo la disposizione spaziale degli
atomi in una molecola. Quindi la teoria VSEPR formula:
1) I gruppi di elettroni nel guscio di valenza attorno ad un atomo
centrale tendono a disporsi in modo da rendere massima la loro
distanza e quindi minima la reciproca repulsione.
2) Lo spazio occupato da una coppia solitaria di elettroni è maggiore
dello spazio occupato da una coppia di legami.
3) Lo spazio occupato da una coppia di elettroni di legame diminuisce
all’aumentare dell’elettronegatività degli atomi legati all’atomo
centrale.
4) Le due coppie di elettroni di un legame doppio o le tre coppie di un
legame triplo occupano uno spazio un po’ più grande di una coppia
di elettroni di un legame singolo.
Teoria LEGAME DI VALENZA:
Parte dal principio fondamentale secondo cui un legame covalente tra
due atomi si forma quando gli orbitali si sovrappongono e sono occupati
da una coppia di elettroni con spin opposti; la coppia elettronica ha,
inoltre, la più alta probabilità di essere localizzata tra i due nuclei.
Quando il legame è formato da due atomi uguali viene detto covalente
omopolare, se no legame covalente eteropolare.
Legame sigma: presenta simmetria cilindrica.
Legame pi greco: cambia il segno ogni 180°.
ORBITALI IBRIDI:
Ibridazione sp : quando si combina un orbitale atomico s con un orbitale
atomico p si ottengono due orbitali ibridi. I due orbitali p non ibridati
giacciono a 90° rispetto all’asse su cui si trovano gli orbitali ibridi sp.
Ibridazione sp2: quando si combinano un orbitale s e due orbitali p si
formano tre orbitali sp2 lasciando non ibridato il terzo orbitale p
(orientati a 120° l’uno risp all’altro). L’orbitale p non ibridato è ortogonale
rispetto al piano xy e contiene i 3 orbitali ibridati.
Ibridazione sp3: per combinazione di un orbitale atomico s con 3 orbitali
atomici p si ottengono quattro orbitali ibridi sp3. I quattro orbitali sono
diretti verso i vertici di un tetraedro al cui centro è situato il nucleo e
formano tra loro un angolo di 109,47°.