Le radiazioni elettromagnetiche vanno dai raggi (a minori
lunghezze d’onda ed alta energia/frequenza) alle onde radio (a
maggiori lunghezze d’onda e bassa energia/frequenza).
La lunghezza d'onda () è la distanza tra 2 creste o 2 ventri
(m,cm,nm); la frequenza () è il numero di oscillazioni al secondo
(Hertz, Hz, sec-1); l’energia si misura in calorie o Joules (1 cal=
4,17 J).
E=h
h è la costante di Planck (6.6 x 10-34 Joules x sec)
Frequenza = velocità della luce (nel vuoto, 3 x 108 m/sec) /
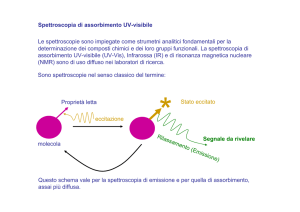
L’interazione delle radiazioni nelle regioni dell’ultravioletto (UV, 200-350 nm) e del visibile (VIS, 350-800 nm)
con la materia è la base delle tecniche spettroscopiche ampiamente utilizzate in biochimica per analisi qualitative e
quantitative.
Gli elettroni di legame di tipo (presenti nei legami doppi o tripli, negli anelli aromatici) sono costituiti da coppie
di elettroni la cui maggiore densità è situata al di fuori dell’asse di unione dei nuclei; questi elettroni sono “meno
legati” e più facilmente eccitabili rispetto a quelli di tipo presenti nei legami semplici. Le molecole che
contengono elettroni assorbono la luce passando da stati ad energia minore a stati ad energia maggiore e si
chiamano cromòfori. Lo spettrofotometro è lo strumento che consente la misura dell’assorbimento di cromofori
in soluzione.
I0
La sorgente può essere
una lampada a
tungsteno (VIS) o una
lampada ad idrogeno
o deuterio (UV)
Il monocromatore consente
di ottenere un fascio di luce
ad 1 lunghezza d’onda
partendo da una sorgente di
radiazioni policromatica
It
Il rivelatore produce un
segnale elettrico che
dipende dall’energia
delle radiazioni che lo
investono
La cella contenente il campione si chiama cuvetta. Le cuvette possono differire per
natura del materiale (vetro/plastica per lettura nel VIS, quarzo per lettura nell’UV) e
cammino ottico (la distanza tra il raggio entrante e quello uscente), ma hanno
sempre 2 facce opposte che non possono essere attraversate dalla luce (attenzione al
loro posizionamento nello spettrofotometro !)
I0 (Intensità luce incidente) e It (Intensità luce trasmessa)
It = I0 non c’è assorbimento
It < I0 se c’è assorbimento
Il nostro occhio funziona come uno
spettrofotometro che rivela la
radiazione trasmessa dal cromoforo
che ha assorbito solo una parte della
luce solare composta da radiazioni
nel VIS, nell’UV e nell’infrarosso
Una semplice considerazione che riguarda i cromofori nel VIS ci
consente di capire il fenomeno dell’assorbimento. La luce bianca è
il risultato della mescolanza di 7 colori. Quando la luce bianca
passa attraverso un cromoforo, una porzione caratteristica della
miscela di lunghezza d'onda viene assorbita. La luce restante, non
assorbita, assumerà allora il colore complementare alla lunghezza
d'onda (o di onde), che sono state assorbite. Questa correlazione è
descritta dalla ruota dove i colori complementari sono
diametralmente opposti l'un l'altro. Di conseguenza, l'assorbimento
della luce di 420-430 nm rende una sostanza gialla; un
assorbimento a 500-520 nm la rende di colore rosso. Il verde ha un
comportamento unico, in quanto esso può essere creato da un
assorbimento vicino a 400 nm, come pure dall'assorbimento
intorno a 800 nm.
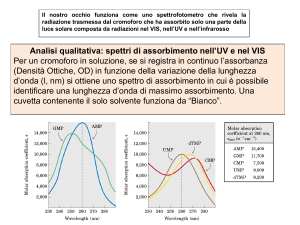
Analisi qualitativa: spettri di assorbimento nell’UV e nel VIS
Per un cromoforo in soluzione, se si registra in continuo l’assorbanza (Densità Ottiche, OD) in funzione della
variazione della lunghezza d’onda (, nm) si ottiene uno spettro di assorbimento in cui è possibile identificare
una lunghezza d’onda di massimo assorbimento. Una cuvetta contenente il solo solvente funziona da “Bianco”.
ESERCITAZIONE
Determinazione dello spettro di assorbimento di:
una soluzione in acqua di Albumina di Siero Bovino (BSA) da 240 a 320 nm
una soluzione in acqua di blu destrano da 400 a 800 nm
Analisi quantitativa: determinazione della concentrazione di un cromoforo
La Trasmittanza (T, It /I0) diminuisce in modo esponenziale in rapporto alla concentrazione del cromoforo, del
cammino ottico e di un parametro (caratteristico del cromoforo) perché aumenta l’Assorbanza (A).
-cl
T = 10
da cui -log10 T = A (cioè log10 1/T = A)
quindi,
A=cl
(Legge di Lambert-Beer)
C rappresenta la concentrazione del cromoforo espressa in moli/litro (M).
l è il cammino ottico (cm)
è il coefficiente di estinzione molare e coincide con l’A (in Densità Ottiche, OD) di una soluzione 1 M della
sostanza in esame quando viene letta in una cuvetta con cammino ottico uguale ad 1 cm ad una determinata
lunghezza d’onda. E’ evidente che il coefficiente di estinzione molare lo si può calcolare solo se è disponibile il
valore del peso molecolare. Quando, soprattutto nel caso di macromolecole come le proteine e gli acidi nucleici,
non è disponibile il peso molecolare si fa uso di un altro parametro, il coefficiente di estinzione percentuale che
indica l’assorbimento di una soluzione all’ 1% della sostanza in esame.
La legge di Lambert-Beer è l’equazione di una retta
passante per l’origine degli assi (A sulle y e C sulle x) in cui
l è il coefficiente angolare. La proporzionalità tra A e C
(entro un certo intervallo) consente misure quantitative.
ESERCITAZIONE
Calcolo della concentrazione della soluzione di BSA sapendo che il coefficiente di estinzione
percentuale a 280 nm è di 6,75 O.D.
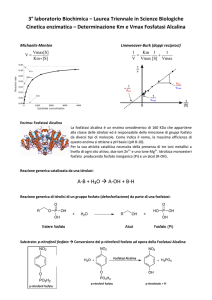
Il dosaggio di un enzima: la fosfatasi alcalina
La concentrazione degli enzimi viene determinata attraverso il dosaggio della loro attività catalitica e viene
espressa in termini di Unità Enzimatiche: 1 Unità è la quantità di enzima che catalizza la trasformazione di 1
mole di Substrato in Prodotto, in 1 min, a 25 °C, in condizioni di pH e forza ionica ottimali.
Il calcolo della quantità di Substrato che scompare nel tempo della reazione, o il calcolo della quantità di
Prodotto che si forma nel tempo della reazione consentono parimenti di dosare un enzima. Se il Substrato o il
Prodotto dell’enzima sono cromofori, la spettrofotometria consente di dosare facilmente l’enzima.
Le fosfatasi (numero EC 3.1.3) sono una classe di idrolasi che catalizzano la reazione di rimozione di gruppi
fosfato (defosforilazione). A seconda del pH ottimale di reazione, si distinguono la fosfatasi alcalina e la fosfatasi
acida. La fosfatasi alcalina è presente in procarioti ed eucarioti; nei mammiferi, forme isoenzimatiche tessutospecifiche hanno importanza diagnostica (si distinguono per carica netta, sensibilità ad inibitori e al
riscaldamento). L’enzima della mucosa intestinale bovina utilizzato per l’esperienza è un omodimero di 70 kDa.
Per il dosaggio della fosfatasi alcalina si utilizza un Substrato sintetico, il p-nitrofenilfosfato (incolore) che
l’enzima trasforma in un Prodotto giallo, il p-nitrofenolo.
ESERCITAZIONE
Dosaggio dell’attività della fosfatasi alcalina al variare del pH
Allestiamo in cuvette di plastica le miscele di reazione che differiscono per il valore del pH della soluzione
tampone. La concentrazione di Enzima è la stessa in tutte le miscele e la concentrazione del Substrato è tale da
saturare l’enzima: dunque, la velocità della reazione varia unicamente per il pH.
Subito dopo l’aggiunta dell’enzima si agita con Parafilm e si segue in continuo l’aumento di assorbanza a 405
nm (lettura contro aria) a temperatura ambiente. Il A/min diviso per l’ del p-nitrofenolo (18,2 densità ottiche)
dà le moli di P formate per min, cioè le Unità contenute nel volume di campione usato per il dosaggio.
Tampone
Tris-HCl 0,1 M, pH 7
Tris-HCl 0,1 M, pH 8
Glicina-NaOH 0,1 M, pH 9
Glicina-NaOH 0,1 M, pH 10
Glicina-NaOH 0,1 M, pH 12
500 l
500 l
500 l
500 l
500 l
Substrato 25 mM
30 l
30 l
30 l
30 l
30 l
Acqua (a 1 ml)
470 l
470 l
470 l
470 l
470 l
Enzima
5 l
5 l
5 l
5 l
5 l
A/min
unità