Attivitá e cinetica
enzimatica
PAS : Classe di insegnamento A60
Biologia e scienze
A.A . 2013/2014
09/05/2014
Cinetica Enzimatica
La cinetica enzimatica è misurata come velocità di conversione del substrato nel
prodotto finale, ossia quantità di prodotto generato per unità di tempo
Cinetica Enzimatica
La cinetica enzimatica è influenzata da vari fattori:
-
Concentrazione del enzima
-
PH nel mezzo di reazione (ogni enzima possiede un PH ottimale, generalmete intorno a
valori medi)
-
Concentrazione del substrato
-
Presenza di eventuali inibitori e della loro concentrazioni (gli inibitori allosterici sono
generalmente più potenti degli inibitori competitivi)
Substrato enzimatico
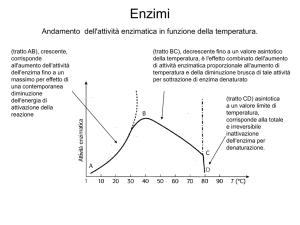
Quando la concentrazione enzimatica è mantenuta constante, un incremento della
concentrazione del substrato porta ad un aumento della velocità di reazione fino al
(Abs/time)
raggiungimento della velocità massima (Vmax)
• La concentrazione di substrato cui la velocità di reazione
è ½ Vmax è definita come constante di Michaelis, Km
• La saturazione dei siti attivi si ha con il raggiungimento di Vmax
(mM)
Inibitori enzimatici
Gli inibitori enzimatici agiscono riducendo la velocità di reazione enzimatica
-
Inibitori competitivi: legame al sito attivo (linibizione competitiva può essere superata aumentando le
concentrazioni del substrato)
-
Inibitori allosterici: legano l’enzima al di fuori del sito attivo (sito allosterico) inducendone un
cambiamento conformazionale
-
Inibitori non-competitivi: legano l’enzima nel sito attivo ed anche il complesso enzima-substrato
NB:
la cellula preferisce limitare l’attività di un enzima attraverso la modulazione delle concentrazioni di substrato
oppure mediante l’azione di enzimi con attività opposta, piuttosto che mediante l’impiego di inibitori (gli inibitori delle
ribonucleasi ne sono un raro esempio)
Fosfatasi alcalina
La fosfatasi alcalina è un enzima che si trova prevalentemente nel sangue, nell’intestino,
nel fegato e nel tessuto osseo.
Alterati livelli di questa proteina nel sangue possono essere indicativi di diversi fenomeni
patologici.
• La fosfatasi alcalina catalizza l’idrolisi di fosfati monoestere
per generare gruppi fosfato inorganici
Saggio della fosfatasi alcalina
La fosfatasi alcalina ha un’attività maggiore a PH alcalini (PH 8.0).
• Il saggio più comune per la rilevazione dell’attività della fosfatasi alcalina
prevede l’impiego di p-nitrofenil fosfato (o 4-nitrofenil fosfato),
un substrato cromogenico.
• La quantità di prodotto enzimatico formato (p-nitrofenolato) può essere
misurata mediante uno spettrofotometro
NB: nei saggi di rilevazione dei livelli di fosfatasi alcalina la quantità di
substrato prodotto è impiegata come misurazione indiretta della quantità
di enzima
Spettrofotometro
Lo spettrofotometro misura in maniera quantitativa la frazione di luce che attraversa una
determinata soluzione campione.
L’assorbanza (o densità ottica OD) è la grandezza (priva di unità di misura) utilizzata in
spettrofotometria per misurare la quantità di luce assorbita da una soluzione.
• L’assorbanza è determinata dalla formula:
A= εxlxC
ε: coefficiente di assorbimento molare
La differenza tra la luce incidente e la luce trasmessa
determina l’assorbanza del campione
l: cammino ottico della cuvetta
C: concentrazione di soluto (mol/L)
Molarità
La molarità (M) è un'unità di misura della concentrazione di una specie chimica in una
soluzione, è definita come le moli di soluto presenti in un litro di soluzione (mol/L).
La mole di una sostanza contiene tante entità elementari quanti sono gli atomi contenuti in
12 grammi dell'isotopo 12 del carbonio: tale numero è noto come numero di Avogadro, pari a
6,022 × 1023 .
Nel caso di un composto chimico, si può definire la mole come la quantità di sostanza avente
massa, espressa in grammi, numericamente uguale alla massa molecolare della singola
molecola (peso molecolare).
NB:
nelle reazioni in vitro, si impiegano concentrazioni di reagenti nell’ordine del milli molare (mM) ma nei sistemi
cellulari le sonstanze (inclusi i substrati enzimatici) hanno concentrazioni nel nano o micro molare (nM, uM)
Utilizzo delle pipette Gilson
p10
p20
p200
p1000
Utilizzo di Excel
Utilizzo di Excel
Equazione di regressione logaritmica
Y
Y = a x ln(x) + b
a: pendenza
B: intercetta
X
Utilizzo di Excel
Approssimazione di Vmax
• Vmax si ottiene al raggiungimento del
plateau di reazione
Y
Vmax
• La pendenza della curva (a)
rappresenta l’incremento di velocità di
reazione (reaction rate)
X
X: tempo
Y: Abs
PEROSSISOMA: organello cellulare presente in tutte
le cellule eucariotiche, separato dal citoplasma
mediante membrana, al cui interno si svolgono diverse
reazioni metaboliche tutte caratterizzate dalla
formazione di H2O2.
FUNZIONE DEI PEROSSISOMI
Reazioni di ossidazione che utilizzano O2 per rimuovere H2
da un substrato organico (R) come ad esempio l’ossidazione
degli acidi grassi o dell’etanolo
RH2 + O2 R + H2O2
Il perossido di idrogeno é altamente tossico per le cellule
(interferenze con ioni metallici delle proteine e mutazione
del DNA) e i perossisomi lo eliminano grazie alla catalasi
2H2O2
Catalasi
2H2O + O2
REAZIONI NEI PEROSSISOMI
Degradazione degli acidi grassi
a catena molto lunga
Da: http://www.ncbi.nlm.nih.gov/books/NBK21624/figure/A
4363/?report=objectonly
CATALASI
• Enzima localizzato nei perossisomi
• indispensabile per l’eliminazione del perossido di
idrogeno all’interno della cellula
• L’eliminazione del perossido di idrogeno deve essere
immediata: ogni secondo una molecola di catalasi puó
degradare milioni di molecole di H2O2.
• La velocitá della reazione é garantita da un gruppo
eme, uno per ogni subunitá della proteina.
• La concentrazione dell’enzima varia a seconda
dell’organismo e del tessuto (molto alta in fegato)
• ph ottimale ca. 7 (variabile a seconda della specie)
ESPERIENZA DI LABORATORIO
Obiettivo:
Riconoscere l’attività enzimatica della catalasi e
valutare in quali circostanze viene alterata.
In particolare vedremo:
- Attivitá della catalasi in prodotti di origine animale e
vegetale
- Effetto del calore e del pH sull’attivitá enzimatica
Prodotti utilizzati e frasi di rischio
H 2 O2
H302
H318
HCl
H290
H314
H335
NH3
Nocivo se ingerito.
Provoca gravi lesioni oculari.
Può essere corrosivo per i metalli.
Provoca gravi ustioni cutanee e gravi lesioni oculari.
Può irritare le vie respiratorie
H221 Gas infiammabile.
H280 Contiene gas sotto pressione; può esplodere se
riscaldato.
H314 Provoca gravi ustioni cutanee e gravi lesioni oculari.
H331 Tossico se inalato.
H400 Molto tossico per gli organismi acquatici.