Università degli Studi di Enna “Kore”
Facoltà di Scienze dell’Uomo e della
Società
Corso di Laurea in
Scienze delle Attività Motorie e Sportive
Biochimica: prove scritte
AA 2010-2011/2011-2012/2012-2013/20132014
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 11-02-2011
Nome……………………….Cognome…………………………..n° matricola…………. .
1.
a)
b)
c)
La prima fase della respirazione cellulare
E’ la via metabolica che determina la produzione di due molecole di piruvato da una molecola di glucosio.
Produce 4 molecole di ATP.
Avviene nei mitocondri.
2.
a)
b)
c)
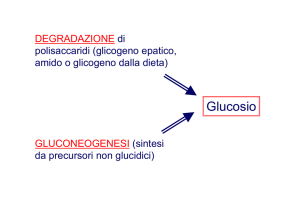
La gluconeogenesi
Corrisponde alla sintesi di glucosio dal glicogeno.
E’ un processo che richiede energia.
Utilizza i prodotti della -ossidazione.
3.
a)
b)
c)
La produzione di ATP dalla fosfocreatina
E’ un esempio di processo anaerobico lattacido.
E’ un esempio di processo anaerobico alattacido.
Richiede ossigeno.
4. La formazione di acido lattico dal piruvato
a) E’ un processo mediante il quale viene rigenerato coenzima NAD+.
b) Determina un aumento del pH citosolico.
c) attiva la glicolisi.
L’accumulo di acido lattico ha qualche effetto sulla prima fase della respirazione cellulare? Dare una breve
spiegazione.
5.
a)
b)
c)
La trasformazione del piruvato ad ossalacetato catalizzata dalla piruvato carbossilasi è
Una reazione fondamentale per la biosintesi degli acidi grassi.
Una reazione coinvolta sia nella gluconeogenesi che nel ripristino degli intermedi del ciclo di Krebs.
Attivata da basse concentrazioni di acetil-CoA.
6. La struttura primaria delle proteine è determinata
a) Dal legame ammidico tra AA (legame peptidico).
b) Da legami d’idrogeno.
c) Da interazioni tra AA lipofili.
Descrivere brevemente i diversi motivi strutturali tipici della struttura delle proteine e le interazioni che le
caratterizzano.
7.
a)
b)
c)
Gli acil-CoA sono
Molecole contenenti un gruppo tioestereo la cui idrolisi richiede energia.
Molecole gluconeogeniche.
Molecole ad alta energia.
8.
a)
b)
c)
L’insulina attiva
La gluconeogenesi.
La biosintesi di trigliceridi negli adipociti.
La beta-ossidazione degli acidi grassi.
9.
a)
b)
c)
La sintesi del glucosio-6-fosfato catalizzata dall’esochinasi
E’ una reazione che produce una molecola ad alta energia confrontabile all’ATP.
E’ una reazione reversibile che rientra sia in processi anabolici che catabolici.
E’ un processo che permette tra l’altro alla cellula di mantenere al proprio interno il glucosio.
10. Nella terza fase della respirazione cellulare
a) L’ossigeno si riduce ad acqua.
b) Si ha produzione di coenzimi ridotti.
c) Avviene in condizioni di anaerobiosi.
Che cosa si intende per catena di trasporto degli elettroni? Qual è il suo fine ultimo?
11.
a)
b)
c)
Una proteina di membrana intrinseca
E’ probabilmente più idrofila rispetto ad una proteina citosolica.
E’ probabilmente più lipofila rispetto ad una proteina citosolica.
Ha sempre una struttura globulare.
12.
a)
b)
c)
La trasformazione del succinato a fumarato è una reazione di deidrogenazione che
Corrisponde ad una ossidazione del succinato mediata dalla riduzione di FAD.
Corrisponde ad una riduzione del succinato con ossidazione di FAD.
Corrisponde ad una degcarbossilazione del succinato. Infatti il fumarato contiene un minor numero di atomi di
carbonio.
13. La acido grasso sintasi catalizza la biosintesi di
a) Acidi grassi a catena lunga (numero di atomi di C>18).
b) Acidi grassi essenziali.
c) Acidi grassi con catena non più lunga di 16 atomi di carbonio.
Definire un acido grasso essenziale facendo almeno due esempi.
14.
a)
b)
c)
Quale delle seguenti affermazioni è scorretta?
Un catalizzatore aumenta la velocità di una reazione.
Un catalizzatore si trasforma irreversibilmente dopo la catalisi.
La catalisi non altera G della reazione.
15. La trasformazione della gliceraldeide 3-fosfato a 1,3-difosfoglicerato permette
a) Di ottenere una molecola a bassa energia che deve essere attivata affinché la degradazione del glucosio
prosegua.
b) E’ una reazione di riduzione che permette di riottenere coenzimi ridotti.
c) Di ottenere una molecola ad alta energia utilizzabile per la produzione di ATP.
Descrivere i due principali meccanismi di produzione dell’ATP nelle cellule.
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 25-02-2011
Nome……………………….
1.
a)
b)
c)
Cognome …………………………. .n° matricola………….
L’ingestione di bicarbonato di sodio
Potrebbe essere utile per limitare l’acidificazione ematica determinata da un’intensa attività anaerobica.
Potrebbe essere utile per limitare l’acidificazione ematica determinata da un’intensa attività aerobica.
Non avrà alcun effetto sul pH ematico.
2. La struttura ad alfa elica delle proteine
a) Coincide con la struttura primaria delle proteine.
b) È’ stabilizzata da legami ad idrogeno.
c) È determinata dall’avvolgimento destrorso di catene polinucleotidiche.
Ricordando che la glicina è l’amminoacido più semplice, che tipo di struttura avrà una proteina o un peptide
costituiti principalmente da tale amminoacido?
3.
a)
b)
c)
Quale processo o via metabolica è comune sia al catabolismo aerobico che anaerobico del glucosio?
L’ossidazione mitocondriale di NADH.
Il ciclo di Krebs.
La glicolisi.
4.
L’ossidazione di FADH2 nella fosforilazione ossidativa determina la formazione di circa 2 molecole di ATP
mentre quella di NADH porta alla sintesi di circa 3 molecole di ATP. Perché?
a) L’ossidazione di FADH2 determina un maggiore gradiente protonico rispetto a quello che si ottiene mediante
ossidazione di NADH.
b) L’ossidazione di FADH2 non coinvolge il complesso I.
c) FADH2 cede i propri elettroni direttamente all’ossigeno attraverso il complesso II.
5. Il glucagone
a) Attiva la lipasi ormone sensibile e la sintesi di trigliceridi negli adipociti.
b) Determina l’aumento dell’espressione dei trasportatori Glut4 negli adipociti.
c) Attiva la lipasi ormone sensibile e la lipolisi dei trigliceridi negli adipociti.
Quali sono le principali tappe del processo di accumulo e rilascio di acidi grassi negli adipociti? I lipidi
introdotti con la dieta sono inglobati direttamente negli adipociti?
6.
a)
b)
c)
La conversione del fosfoenolpiruvato a piruvato è
Una reazione fortemente endoergonica.
Una reazione moderatamente esoergonica che comporta l’idrolisi di un legame fosfoanidridico.
una reazione estremamente esoergonica.
7.
a)
b)
c)
Nelle reazioni di transaminazione
Il glutammato viene trasformato in alfa-chetoglutarato per rimozione del gruppo amminico.
Tutti gli amminoacidi vengono trasformati in alfa-chetoacidi.
Si produce ammoniaca.
8.
a)
b)
c)
Un acido grasso
Viene catabolizzato senza alcuna preliminare trasformazione.
Viene preliminarmente trasformato in estere.
Viene preliminarmente trasformato in tioestere.
Descrivere in modo sintetico le principali fasi del catabolismo degli acidi grassi.
9.
a)
b)
c)
Il ciclo di Krebs può essere definito anfibolico perché
è coinvolto in processi anabolici e catabolici.
è un processo essenzialmente esoergonico.
vengono prodotti coenzimi ossidati.
10. Il processo di gluconeogenesi
a)
b)
c)
Può essere realizzato percorrendo inversamente tutte le reazioni della glicolisi catalizzate dagli stessi enzimi.
Avviene nel muscolo.
Avviene prevalentemente nel fegato
Motivare la risposta.
11.
a)
b)
c)
Il trasporto del glucosio nella cellula avviene
Per trasporto mediato passivo.
Per diffusione semplice.
Per trasporto attivo in quanto il glucosio è uno ione in condizioni fisiologiche.
12.
a)
b)
c)
L’aspartato per transaminazione genera ossalacetato ed è quindi
Un amminoacido chetogenico.
Un amminoacido essenziale.
Un amminoacido glucogenico
13.
a)
b)
c)
Un coenzima è
Una molecola organica coinvolta nella catalisi enzimatica.
Uno ione inorganico necessario alla catalisi enzimatica.
Un inibitore allosterico.
14. L’adenosina 5’-monofosfato
a) È’ una molecola ad alta energia in quanto l’idrolisi del legame fosfoanidridico è altamente esoergonica.
b) E’ una molecola a bassa energia.
c) Contiene un legame fosfoestereo la cui idrolisi esoergonica può essere accoppiata a processi endoergonici.
Definire una molecola ad alta energia facendo esempi di molecole contenenti gruppi funzionali diversi. Che
cosa si intende per accoppiamento di reazioni e quando viene utilizzato?
15.
a)
b)
c)
Le decarbossilazioni dell’isocitrato e dell’alfa-chetoglutarato con produzione di anidride carbonica
Sono processi di riduzione.
Sono processi di ossidazione.
Avvengono per idrolisi di legami ad alta energia.
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 20-06-2011
Nome……………………….
Cognome …………………………. .n° matricola………….
1.
b.
c.
d.
Gli acidi grassi liberi
Costituiscono la forma prevalente dei lipidi nell’organismo.
Non determinano alcuna variazione del pH delle loro soluzioni.
Sono una frazione ridotta degli acidi grassi totali che sono di solito esterificati.
Descrivere brevemente le principali funzioni delle differenti classi di lipidi nella cellula
2.
a)
b)
c)
La struttura a foglietto beta delle proteine
È tipica di proteine costituite da più di una catena polipeptidica.
È tipica di sequenze ricche di glicina, l’amminoacido più semplice .
È stabilizzata da legami d’idrogeno e interazioni tra gruppi apolari degli AA.
3.
a)
b)
c)
Che cosa si intende per effetto Bohr?
L’effetto della temperatura sull’affinità di Hb per O2.
L’effetto del pH sull’affinità di Hb per O2.
L’effetto dell’aumento delle concentrazioni ematiche di H+ che determina un aumento dell’affinità di Hb per
O2.
Come può l’emoglobina opporsi alla variazione del pH del sangue venoso? Perché il pH del sangue venoso
tende a diminuire?
4.
a)
b)
c)
La trasformazione del piruvato in lattato
Permette alla cellula di ottenere NAD+.
Avviene nei mitocondri.
È una ossidazione accoppiata alla riduzione di NAD+.
5.
a)
b)
c)
La reazione catalizzata dalla malato deidrogenasi nel ciclo di Krebs
Ha G maggiore di 0.
Permette la conversione del malato a fumarato.
È esoergonica ed avviene con produzione di molecole ad alta energia.
Perché il ciclo degli acidi tricarbossilici può essere definito anfibolico?
6.
a)
b)
c)
Gli acidi grassi sintetizzati dalle cellule hanno
Spesso insaturazioni a 3 atomi di carbonio dalla fine della catena.
Sono costituiti da un numero di atomi di carbonio dispari.
Contengono sempre un numero di atomi di carboni pari.
7. In condizioni di ipossia la cellula
a) Produce energia prevalentemente mediante processi mitocondriali.
b) Produce ATP prevalentemente attraverso le conversioni di 1,3-difosfoglicerato e fosfoenolpiruvato nei
rispettivi prodotti.
c) Ossidando gli atomi del glucosio ad anidride carbonica.
8.
a)
b)
c)
La biosintesi del glicogeno
Utilizza molecole di glucosio non modificato.
Richiede l’attivazione del glucosio mediante UTP.
Essendo un processo anabolico non richiede energia
9. Il catabolismo degli amminoacidi
a) Permette di ottenere da diversi AA degli intermedi del ciclo di Krebs.
b) Non è correlato alla gluconeogenesi.
c) È di solito un processo riduttivo.
10. La produzione e l’aumento delle concentrazioni cellulari di lattato
a) Attiva la degradazione del glucosio.
b) Inibisce la degradazione del glucosio.
c) Determina un aumento del pH.
Qual è il meccanismo mediante il quale il lattato regola la glicolisi?
11.
a)
b)
c)
Il succinil-CoA è
Una molecola ad alta energia in quanto contiene un legame tioestereo.
Una molecola ad alta energia che contiene un gruppo fosfoestereo come il glucosio 6-fosfato.
Una molecola a bassa energia che contiene un gruppo tioestereo.
12.
a)
b)
c)
Un amminoacido essenziale
È un amminoacido prodotto dalla cellula.
Un amminoacido che deve essere introdotto nella cellula.
Un amminoacido chetogenico.
13.
a)
b)
c)
Un’alterazione della temperatura (T) rispetto al valore ottimale
Non ha alcun effetto sull’attività enzimatica.
Di solito aumenta la velocità delle reazioni catalizzate da enzimi.
Può denaturare l’enzima.
Definire brevemente il concetto di catalisi enzimatica.
14.
a)
b)
c)
Gli elettroni ceduti all’ossigeno nella catena di trasporto degli elettroni
Provengono dai coenzimi ridotti.
Provengono dai coenzimi ossidati.
Provengono dall’anidride carbonica.
15.
a)
b)
c)
La produzione di energia nella beta-ossidazione degli acidi grassi è
Un processo sempre anaerobico.
Un processo sia aerobico che anaerobico.
Richiede sempre ossigeno.
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 11-07-2011
Nome……………………….Cognome…………………………..n° matricola…………. .
1.
a)
b)
c)
Il lattato prodotto dai miociti durante un’ intensa attività anaerobica
Viene immesso in circolo e trasportato al fegato.
Genera elevate concentrazioni di NADH citosoliche.
Viene trasformato in glucosio dal miocita.
2.
a)
b)
c)
La cottura dei cibi
Rende di solito le proteine meno digeribili in quanto la denaturazione determina la loro insolubilità in acqua.
Non intacca la struttura secondaria delle proteine.
Rende le proteine di solito più digeribili a causa dell’idrolisi di legami ammidici che facilita l’azione degli
enzimi proteolitici
3.
a)
Nella catena di trasporto degli elettroni
Gli elettroni provenienti dai coenzimi ridotti sono ceduti all’acqua che ha un potenziale di riduzione normale
più elevato.
b) Gli elettroni provenienti dai coenzimi ridotti sono ceduti all’ossigeno che ha un potenziale di riduzione
normale più elevato.
c) Viene prodotto un gradiente protonico a livello della membrana mitocondriale esterna e del citoplasma.
Quali sono le principali fasi della catena di trasporto degli elettroni? Perché l’ossidazione di FADH2 genera
meno ATP della riossidazione di NADH?
4. Un amminoacido basico è
a) Un amminoacido che come il glutammato contiene un gruppo carbossilico nella catena laterale.
b) Un amminoacido che come l’alanina ha una catena laterale apolare.
c) Un amminoacido che come la lisina contiene un gruppo amminico nella catena laterale.
Descrivere brevemente la struttura degli amminoacidi e la loro classificazione sulla base delle caratteristiche
chimiche della catena laterale.
5.
a)
b)
c)
La trasformazione del piruvato ad acetil-CoA
Non richiede riduzione di coenzimi.
È un processo irreversibile che avviene con formazione di CO2.
Avviene con produzione di ATP
6.
a)
b)
c)
Il glicerolo ottenuto dall’idrolisi del legame estero dei trigliceridi
Può entrare nella gluconeogenesi.
Viene trasformato in acidi grassi.
Viene semplicemente escreto dall’organismo.
Qual è il destino dei grassi introdotti con la dieta? Come vengono conservati e mobilizzati?
7. Perché l’idrolisi di ATP ad ADP nella cellula non avviene spontaneamente?
a) Non è vero! L’ATP è instabile e si idrolizza ad ADP e fosfato appena formata.
b) L’energia di attivazione per l’idrolisi del legame fosfoanidridico è elevata. Per questo l’idrolisi esoergonica di
ATP richiede l’intervento di enzimi.
c) Perché l’acqua non può reagire con legami fosfoanidridici. I due composti non sono reattivi.
Descrivere brevemente il concetto di energia di attivazione.
8.
a)
b)
c)
Il glucagone attiva
La gluconeogenesi.
La glicolisi.
La biosintesi degli acidi grassi.
9.
a)
b)
c)
Il 3-fosfoglicerato
E’ un fosfoestere ed è quindi un composto ad alta energia che la cellula usa per produrre ATP.
Deve essere convertito in 2-fosfoglicerato precursore della molecola ad alta energia fosfoenolpiruvato.
E’ il prodotto della riduzione del 1, 3-difosfoglicerato.
10. Gli acid grassi liberi sono veicolati nell’organismo attraverso l’apparato cardiocircolatorio. Quale delle tre
affermazioni è corretta?
a) Gli acidi grassi liberi sono infatti estremamente solubili in soluzione acquosa.
b) Tale trasporto è mediato da proteine come l’albumina.
c) Il trasporto avviene senza l’intervento di molecole più idrofile.
11.
a)
b)
c)
La beta ossidazione degli acidi grassi
Avviene nei mitocondri.
Avviene nel citoplasma.
E’ un processo anaerobico.
12.
a)
b)
c)
L’idrolisi del succinil-CoA a succinato
Corrisponde ad una ossidazione del succinato mediata dalla riduzione di FAD.
Equivale energeticamente all’idrolisi di un legame fosfoestereo.
E’ una reazione esoergonica che porta alla formazione di molecole ad alta energia.
13.
a)
b)
c)
La catena laterale dell’amminoacido acido aspartico è R=-CH2-COOH. Per transaminazione l’aspartato genera
L’ossalacetato. Quindi è un amminoacido gluconeogenico.
Il piruvato. Quindi è un amminoacido gluconeogenico.
L’-chetoglutarato. Si comporta come il glutammato.
14. La principale differenza tra proteine integrali di membrana e proteine di membrana periferiche (o estrinseche)
consiste
a) Nella struttura primaria e nella solubilità..
b) Nel peso molecolare.
c) Nell’affinità per specifici substrati.
Descrivere principali meccanismi di trasporto attraverso la membrana citoplasmatica.
15. L’ 1,3-difosfoglicerato può essere convertito negli eritrociti in 2,3-difosfoglicerato che ha un’elevata affinità
per le catene di Hb e ne riduce l’affinità per O2. La produzione di 2,3-difosfoglicerato è importante
a) Per la produzione di ATP.
b) Per il controllo del pH ematico.
c) Nell’adattamento a condizioni di ipossia.
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 07-09-2011
Nome……………………….
Cognome …………………………. .n° matricola………….
14.
a)
b)
c)
L’enzima succinato deidrogenasi
Catalizza una reazione irreversibile.
È specifico della prima fase della respirazione cellulare.
Partecipa alla catena di trasporto degli elettroni.
Descrivere brevemente i concetti di catalisi enzimatica e di regolazione dell’attività di un enzima
15.
a)
b)
c)
La conversione del fruttosio 6-fosfato in fruttosio 1,6-difosfato
È irreversibile.
È reversibile.
È altamente endoergonica.
16.
a)
b)
c)
L’acido grasso sintasi
Catalizza la beta-ossidazione degli acidi grassi.
Permette di ottenere acidi grassi a catena pari.
Permette di ottenere acidi grassi a catena dispari.
17.
a)
b)
c)
L’amminoacido glutammato (R=-CH2CH2COO-) è un amminoacido
Gluconeogenico perché fornisce alfa-cheto-glutarato.
Non può essere deamminato ossidativamente.
Gluconeogenico perché fornisce piruvato
Descrivere le principali fasi del catabolismo degli amminoacidi.
18.
a)
b)
c)
La sintesi dell’UDP-glucosio
Permette di ottenere un composto più reattivo del glucosio 1-fosfato.
Permette di ottenere un composto meno reattivo di un fosfoestere.
Avviene a partire direttamente dal glucosio 6-fosfato.
Motivare la risposta descrivendo brevemente il ciclo in cui è coinvolto il composto.
19.
a)
b)
c)
Gli acidi grassi introdotti con la dieta vengono inglobati nei chilomicromi che
Contengono soprattutto trigliceridi.
Contengono soprattutto fosfolipidi.
Non contengono proteine
20.
a)
b)
c)
Il colesterolo
È un importante substrato energetico.
Ha funzione strutturale.
Ha attività enzimatica.
21.
a)
b)
c)
L’ossidazione di nicotinammide-adenina-dinucleotide ridotto
Avviene solo nel mitocondrio.
Avviene solo nel citoplasma.
Può avvenire sia nel mitocondrio che nel citoplasma.
22.
a)
b)
c)
Gli eritrociti
Non contengono proteine che agevolano il trasporto del glucosio.
Ricavano energia dalla fosforilazione ossidativa.
Sono caratterizzati da un catabolismo anaerobico.
23.
a)
b)
c)
L’acido lattico
Può essere convertito nuovamente in piruvato dall’organismo.
Non può essere convertito in piruvato.
Non può essere utilizzato come precursore del glucosio
Il lattato può regolare la glicolisi? Come?
11.
a)
b)
c)
Il potenziale elettrochimico di membrana
È nullo.
Non ha alcun effetto sul trasporto di soluti.
È dovuto al gradiente di cariche e di concentrazione.
12.
a)
b)
c)
Nella mioglobina e nell’emoglobina
L’EME interagisce con residui amminoacidici apolari.
L’EME è legata stabilmente alla proteina mediante residui amminoacidici polari.
L’EME ha forte carattere idrofilo.
13.
a)
b)
c)
La gluconeogenesi avviene
Principalmente nel muscolo.
Principalmente a livello del sistema nervoso centrale.
In fegato e reni
Perché? Descrivere le principali tappe della gluconeogenesi.
14.
a)
b)
c)
L’anidride carbonica prodotta dalla degradazione del glucosio
Viene convertita rapidamente in bicarbonato senza l’ausilio di enzimi.
È estremamente solubile in acqua.
Genera i componenti di tamponi importanti a livello ematico.
15.
a)
b)
c)
L’insulina
Disattiva la trigliceride lipasi negli adipociti.
Attiva la trigliceride lipasi negli adipociti.
Non ha effetto sul catabolismo adipocitario.
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 26-09-2011
Nome……………………….
Cognome …………………………. .n° matricola………….
1.
a)
b)
c)
Elevati rapporti di concentrazione ATP/ADP e NADH/NAD+
Inibiscono il ciclo degli acidi tricarbossilici.
Non hanno alcun effetto sul ciclo di Krebs.
Attivano il ciclo del citrato.
Motivare brevemente la risposta facendo riferimento alle reazioni coinvolte nella regolazione del ciclo.
2.
a)
b)
c)
I fosfolipidi possono essere definiti anfipatici perché
Sono molecole polari.
Sono molecole lipofile.
Contengono una parte lipofila ed una polare.
3.
a)
b)
c)
Il 2,3-difosfoglicerato
Regola allostericamente l’affinità dell’emoglobina per l’ossigeno.
E’ una molecola ad alta energia come l’1,3-difosfoglicerato.
Aumenta la pendenza della curva di saturazione dell’emoglobina.
Quali sono i principali meccanismi di regolazione dell’affinità dell’emoglobina per O2?
4.
a)
b)
c)
Un amminoacido chetogenico può generare acetil-CoA e quindi
Essere utilizzato per la biosintesi di glucosio.
Generare corpi chetonici in condizioni di digiuno.
È un precursore del glicogeno.
5. La beta ossidazione degli acidi grassi
a) Non richiede l’attivazione dell’acido grasso libero.
b) Nelle fasi iniziali richiede consumo d’energia.
c) Avviene nel citoplasma.
Descrivere le fasi principali della beta ossidazione e discuterne il bilancio energetico nel caso dell’acido
palmitico
Il ferro emico deve essere nello stato di ossidazione 2+. Ragionando sui potenziali di riduzione E0 (Fe3+ +e-
Fe2+)=0,771 V e E0 (1/2O2 +2H++2e-H2O)=0,816 V dove e- indica l’elettrone e V=volt si può affermare che
a) Il ferro non si ossida all’aria.
b) Il ferro si ossida all’aria.
c) Fe3+ ossida l’ossigeno.
6.
7.
a)
b)
c)
La struttura primaria delle proteine
Contiene gruppi ammidici che sono i derivati più reattivi degli acidi carbossilici.
Contiene gruppi esterei particolarmente stabili.
Contiene gruppi ammidici poco reattivi.
8.
a)
b)
c)
Le reazioni di decarbossilazione ossidativa avvengono con
Produzione di CO2 e ossidazione di coenzimi.
Produzione di CO2 e riduzione di FAD.
Produzione di CO2 e riduzione di NAD+.
9.
a)
b)
c)
La vita media degli eritrociti è breve perché
Durante la maturazione da cellule staminali perdono gli organelli e non sono in grado di replicarsi.
Sono particolarmente suscettibili allo stress ossidativo riconducibile ad un’intensa attività mitocondriale.
Nei tessuti periferici rilasciano l’ossigeno e muoiono.
10. La reazione catalizzata dalla alalina amminotransferasi (ALT)
a) Genera citrato.
b) Genera alanina o piruvato.
c) Catalizza reazioni irreversibili.
Descrivere brevemente il ciclo glucosio-alanina e sottolinearne l’importanza a livello sistemico
11.
a)
b)
c)
Il fruttosio 2,6-difosfato è un regolatore allosterico di PFK1 e della fruttosio 1,6-difosfatasi 1 e
Attiva allostericamente sia PFK1 che fruttosio 1,6-difosfatasi 1.
Attiva allostericamente solo PFK1.
Attiva allo stericamente solo 1,6-difosfatasi
Descrivere i principali meccanismi di regolazione di glicolisi e gluconeogenesi.
12.
a)
b)
c)
La produzione di ATP nella fosforilazione ossidativa
Può essere spiegata sulla base del consumo di un potenziale elettrochimico.
Utilizza l’energia proveniente dalla riduzione dei coenzimi che avviene nello spazio intermembrana.
E’ un processo esoergonico.
13.
a)
b)
c)
La glicogenolisi è attivata
Dall’insulina.
Da un pasto abbondante.
Da uno strenuo esercizio fisico.
14.
a)
b)
c)
La fosfocreatina può
Generare ADP.
Generare ATP.
Non può essere considerata una molecola ad alta energia.
15.
a)
b)
c)
I Sali biliari
Agevolano l’emulsione e l’assorbimento intestinale dei lipidi.
Hanno una funzione strutturale.
Sono substrati energetici.
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2010/2011
Biochimica, prova scritta del 17-10-2011
Nome……………………….
Cognome …………………………. .n° matricola………….
1.
a)
b)
c)
Il ciclo alanina-glucosio
Ha un ruolo importante nel processo di glicogenolisi epatica.
È fondamentale nel processo di glicogenosintesi muscolare.
Permette di eliminare i gruppi amminici degli amminoacidi ottenuti dal catabolismo proteico muscolare.
Descrivere le principali fasi del ciclo e dare le motivazioni della risposta.
2.
a)
b)
c)
Una molecola anionica
Non può diffondere passivamente attraverso la membrana citoplasmatica.
Non è un processo endoergonico.
Diffonde quando il gradiente di concentrazione è favorevole.
Definire il potenziale elettrochimico di membrana e descrivere i principali meccanismi di trasporto.
3.
a)
b)
c)
Gli acidi grassi liberi che entrano nel citoplasma attraverso il sangue
Reagiscono direttamente con la carnitina nel citoplasma.
Una volta attivati entrano nei mitocondri e reagiscono con la carnitina.
Vengono trasformati in acil-CoA mediante un processo endoergonico.
4.
a)
b)
c)
La conversione del fosfoenolpiruvato (PEP) a ossalacetato da parte dell’enzima PEP-carbossichinasi
E’ irreversibile.
È una reazione che avviene nel mitocondrio.
Può essere considerata una reazione anaplerotica.
5. Il D-fruttosio presente in molti tipi di frutta
a) Può entrare nella glicolisi sotto forma di fruttosio-6P.
b) Non può essere catabolizzato.
c) È un aldoesoso
Qual è il bilancio energetico della degradazione del glucosio a piruvato? Come è possibile riossidare i
coenzimi ridotti formati nel processo indipendentemente dalla catena di trasporto degli elettroni?
6.
a)
b)
c)
Esochinasi e glucochinasi sono isoenzimi
Che hanno la stessa affinità per il glucosio.
Hanno Km diversa.
Si attivano a concentrazioni di glucosio confrontabili.
7.
a)
b)
c)
La biosintesi dei coenzimi NAD+ e FAD
E’ sempre possibile nella cellula.
È un processo fortemente esoergonico.
Richiede l’introduzione di nutrienti essenziali
8.
L’amminoacido cisteina contiene nella catena laterale gruppi tiolici (R-SH) che nelle proteine possono dare
legami tioetere (R-S-S-R′).
a) Tali legami sono formati irreversibilmente nelle proteine.
b) Sono importanti per la stabilizzazione della struttura terziaria di alcune proteine.
c) Sono il motivo strutturale di base della struttura primaria delle proteine.
9.
a)
b)
c)
Le lipoproteine a densità molto bassa (VLDL)
Contengono soprattutto fosfolipidi e colesterolo.
Sono prodotte dalle lipoproteine a bassa densità (LDL).
Sono trasportate dal fegato al muscolo ed al tessuto adiposo.
10. Il sistema navetta del glicerolo 3-fosfato.
a)
Permette l’ossidazione di una molecola di NADH nel citoplasma e la contemporanea produzione di FADH2
nel mitocondrio.
b) È uno dei sistemi che permette di recuperare energia mediante ossidazione dell’ossigeno.
c) È un sistema di trasporto localizzato nelle membrane citoplasmatiche
Descrivere i principali sistemi navetta e discuterne la funzione. Ricordate qualche ciclo anabolico che
coinvolge sistemi navetta?
11.
a)
b)
c)
Gli amminoacidi ottenuti dalle proteine introdotte con la dieta
Vengono assorbiti nell’intestino tenue.
Vengono deamminati nello stomaco.
Sono unicamente substrati energetici.
Descrivere la digestione delle proteine assunte e il destino degli amminoacidi ottenuti.
12.
a)
b)
c)
La beta ossidazione di un acido grasso saturo a 13 atomi di carbonio
Non può avvenire.
Produce 6 molecole di acetil-CoA e una di CO2 in una reazione di decarbossilazione ossidativa.
Genera 5 molecole di acetil-CoA ed una di proionil-CoA.
13.
a)
b)
c)
La glicogenolisi e la glicogeno sintesi
Sono regolate contemporaneamente.
Sono regolate indipendentemente.
Avvengono prevalentemente nel sistema nervoso centrale.
14.
a)
b)
c)
Un abbassamento del pH
Attiva la glicolisi.
Inibisce l’aldolasi.
Inibisce la fosfofruttochinasi 1.
15.
a)
b)
c)
La conversione del fumarato a succinato
Produce molecole ad alta energia.
Permette l’ossidazione di FADH2.
Non è coinvolta nella catena di trasporto degli elettroni
Università degli Studi Kore di Enna
Facoltà di Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 13-2-2012
Nome……………………….
Cognome …………………………. .n° matricola………….
1. La lattato deidrogenasi (LDH) è l’enzima che catalizza la trasformazione reversibile dell’acido chetopropanoico in acido -idrossipropanoico ed è costituito da quattro sub-unità. LDH
a) Non può avere stuttura terziaria.
b) Contiene solo legami covalenti.
c) È caratterizzata da struttura quaternaria.
Descrivere i diversi motivi strutturali caratterizzanti le proteine e definire il concetto di denaturazione.
2.
a)
b)
c)
L’idrolisi del pirofosfato
Genera due molecole di orto-fosfato in un processo endoergonico.
È catalizzato dalla pirofosfatasi ed è un processo esoergonico.
È un processo sfavorito cineticamente
Spiegare le motivazioni della risposta e citare almeno due processi metabolici che prevedono tale reazione.
3.
a)
b)
c)
Qual è il principale sistema tampone citosolico?
Il sistema acido carbonico/ idrogeno carbonato.
Il sistema di-idrogenofosfato/idrogeno fosfato.
L’emoglobina.
4.
a)
b)
c)
L’acido -chetobutandioico (acido ossalacetico)
Non può diffondere attraverso la membrana mitocondriale interna.
È coinvolto solo in processi metabolici localizzati nella matrice mitocondriale.
È un importante intermedio della catena di trasporto degli elettroni (ETC).
5.
a)
b)
c)
Il catabolismo dei mono, di e triacil-gliceroli
Genera molecole di acil-CoA che sono gluconeogenici.
Porta sempre alla formazione di propionil-CoA.
Genera glicerolo che può entrare nella biosintesi del glucosio
Descrivere le principali fasi della digestione dei lipidi e del loro trasporto.
6.
L’assunzione di alcool etilico che viene convertito in acetaldeide, acetato ed infine acetil-CoA dall’organismo
determina un aumento della temperatura corporea perché
a) Il processo catabolico è ossidativo e produce elevate concentrazioni di coenzimi ridotti.
b) Vengono rigenerati coenzimi ossidati.
c) Produce energia mediante un processo catabolico prevalentemente citosolico
7.
a)
b)
c)
Gli isoenzimi
Hanno la stessa Km.
Hanno la stessa struttura primaria.
Catalizzano la stessa reazione.
8.
a)
b)
c)
L’acido linoleico (acido octadecadienoico, C18:2 n-6)
Può essere sintetizzato dalle cellule umane.
È precursore di importanti molecole lipidiche che hanno funzione simile a quella degli ormoni.
Non può entrare nella beta-ossidazione.
9.
a)
La fosforilazione delle proteine è un’importante modificazione post-traduzionale che
Prevede di solito la formazione di un legame fosfoestereo o la sua rimozione da residui amminoacidici
contenenti gruppi ossidrilici.
b) È di solito irreversibile.
c) Non modifica la struttura di un enzima
10.
a)
b)
c)
La formazione di carbamil-fosfato da ammoniaca e bicarbonato
Attiva l’ammoniaca che può così reagire con l’ornitina.
È un processo esoergonico.
È attivato da basse concentrazioni di glutammato libero.
11.
a)
b)
c)
Elevate concentrazioni intracellulari di adenina dinucleotide ridotto (NADH).
Attivano il ciclo degli acidi tricarbossilici.
Inibiscono diversi enzimi del ciclo di Krebs.
Inibiscono la fermentazione omolattica.
Quali sono i meccanismi di regolazione del ciclo dell’acido citrico? Quali sono le reazioni regolate?
12. La biodisponibilità di uno zucchero dipende dalla sua struttura. L’integrazione con zuccheri complessi
(polisaccaridi)
a) È indicata per intense attività fisiche aerobiche.
b) È indicata per attività fisiche anaerobiche
c) È ideale nel caso degli sport di potenza.
13.
a)
b)
c)
L’adrenalina
Innesca la lipolisi negli adipociti.
Aumenta la concentrazione ematica di corpi chetonici.
Stimola l’espressione di trasportatori GluT4 negli epatociti
14.
a)
b)
c)
Al di là della dieta, la principale fonte di glucosio ematico.
È il muscolo.
È il fegato.
È l’apparato renale
15.
a)
b)
c)
Il potenziale elettrochimico di membrana
Agevola la diffusione di specie cariche.
Si forma senza consumo di energia.
È fondamentale per la trasduzione del segnale innescato da diverse molecole
Cosa si intende per potenziale elettrochimico di membrana? Quali sono le sue principali funzioni?
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 23-2-2012
Nome……………………….
Cognome …………………………. .n° matricola………….
a)
b)
c)
Un farmaco inibitore della lipasi pancreatica
Inibisce la -ossidazione.
Interferisce con l’assorbimento dei lipidi a livello enterocitario.
Aumenta la concentrazione plasmatica degli acidi grassi liberi agendo sul tessuto adipocitario.
Valutare il numero di molecole di ATP ottenibili dalla degradazione ossidativa dell’acido butanoico
evidenziando le diverse fasi della -ossidazione.
a)
b)
c)
Il trasporto del glucosio attraverso l’epitelio intestinale
Avviene per diffusione semplice.
Richiede trasportatori del glucosio secondo un meccanismo di diffusione facilitata.
È mediato da un gradiente favorevole di ioni Na+ secondo un meccanismo definito attivo secondario.
Discutere i principali possibili meccanismi di trasporto del glucosio in relazione alle sue proprietà chimicofisiche.
3.
La carenza di acido ascorbico inibisce l’idrossilazione della prolina. Quest’ultima stabilizza la struttura
quaternaria del collagene
a) Mediante la formazione di legami d’idrogeno.
b) Mediante interazioni dipolo-dipolo indotto.
c) Mediante interazioni ione-dipolo.
4.
a)
b)
c)
L’aumento delle concentrazioni ematiche di lattato
Attivano la seconda e terza fase della respirazione cellulare.
Inibiscono l’affinità dell’emoglobina per l’ossigeno.
Attivano la trasformazione anaerobica del piruvato.
5.
a)
b)
c)
L’allenamento aerobico
Aumenta l’espressione dell’enzima carnitina aciltransferasi I.
Determina una minore capacità di accumulo di triacilgliceroli nel miocita.
Aumenta l’ipertrofia muscolare e la sintesi proteica.
Motivare la risposta.
6.
a)
b)
c)
La fosforilazione del glucosio a glucosio 6-fosfato è
Termodinamicamente favorita.
Disattiva il glucosio.
Trasforma il glucosio in un composto anionico.
7.
a)
b)
c)
Amido e cellulosa
Sono ugualmente biodisponibili.
Sono fonte di fruttosio.
Sono polisaccaridi catabolizzati in modo differente.
8. L’alanina
a) È l’unico amminoacido che può essere deamminato ossidativamente.
b) Viene utilizzata per trasportare al fegato gruppi amminici provenienti dal catabolismo muscolare di altri
amminoacidi.
c) Per transaminazione genera l’acido -cheto butandioico.
Spiegare brevemente le motivazioni della risposta.
9.
La produzione di GTP attraverso la trasformazione di succinil-CoA a succinato
a) E’ risultato di un accoppiamento di reazioni.
b) È dovuta ad una dissipazione di potenziale elettrochimico.
c) Rigenera coenzimi ossidati.
10.
a)
b)
c)
La trasformazione del di-idrossi acetone fosfato a gliceraldeide 3-fosfato
È una reazione di ossidoriduzione.
È un processo irreversibile.
È un’isomerizzazione.
11.
a)
b)
c)
La conversione del piruvato a fosfoenolpiruvato
È un processo fortemente esoergonico.
Avviene in un’unica reazione.
È catalizzata da due enzimi.
Quali sono i meccanismi di regolazione della prima fase della respirazione cellulare e della gluconeogenesi?
Quali sono le reazioni regolate nei due processi?
12.
a)
b)
c)
L’insulina e gli steroidi sono ormoni che
Diffondono passivamente attraverso la membrana cellulare.
Sono caratterizzati da un meccanismo di trasduzione del segnale diverso.
Presentano proprietà chimico-fisiche simili.
13.
a)
b)
c)
Il sistema navetta malato-aspartato
Avviene solo nel mitocondrio.
Permette il trasporto di coenzimi ossidati dal mitocondrio al citoplasma.
Inibisce la catena di trasporto degli elettroni.
14.
a)
b)
c)
Adenosina 5’-trifosfato e adenosina 5’-difosfato
Sono stabilizzate da ioni positivi.
Interagiscono con ioni negativi.
Sono molecole idrofobe.
15.
a)
b)
c)
Il cervello, pur costituendo il 2-3% della massa corporea, consuma il 20-30% del glucosio disponibile
Perché svolge un catabolismo fondamentalmente anaerobico.
Perché la polarizzazione dei neuroni richiede energia.
Perché costituisce la principale riserva di glucosio.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 18-06-2012
Nome……………………….Cognome…………………………..n° matricola…………. .
1.
a)
b)
c)
La membrana mitocondriale interna
E’ generalmente permeabile a diverse molecole che possono diffondere passivamente.
Isola la matrice mitocondriale.
E’ sede dei meccanismi di regolazione dell’influsso di glucosio.
2.
a)
b)
c)
La conversione del glucosio 6-fosfato a glucosio
E’ una reazione endorgonica.
E’ una reazione esoergonica.
Avviene solo nel muscolo.
Spiegare brevemente le motivazioni della risposta.
3.
a)
b)
c)
La creatina
E’ fonte di ATP.
E’ una molecola ad alta energia.
Può essere attivata.
4.
a)
b)
c)
La conversione del lattato a piruvato
Non può avvenire.
Consente di utilizzare il lattato come precursore in processi anabolici.
Non richiede l’intervento di enzimi.
5. Indicare qual è l’ordine di reattività crescente dei derivati degli acidi carbossilici tra quelli proposti
a) Ammidi>anidridi>esteri.
b) Esteri>anidridi>ammidi.
c) Anidridi> esteri> ammidi.
6.
a)
b)
c)
La perdita della struttura primaria di una proteina
Richiede la rottura di legami covalenti stabili.
Prevede la scissione di interazioni di Van der Waals.
Praticamente non avviene
Descrivere le prime fasi della digestione delle proteine ed il destino degli amminoacidi.
7.
a)
b)
c)
Un aumento dei livelli plasmatici di acilcarnitine
Può indicare un’alterazione della sintesi del glicogeno nelle fasi di recupero da intensa attività fisica.
Una riduzione dell’efficienza della beta-ossidazione.
Può essere dovuto ad un aumento della sensibilità all’insulina.
8.
a)
b)
c)
L’allenamento aerobico
Limita capacità del muscolo di utilizzare glucosio.
Aumenta la capacità del muscolo di produrre e conservare glicogeno.
Riduce il numero di mitocondri nel muscolo.
9.
a)
b)
c)
L’energia di attivazione
E’ l’energia corrispondente allo stato di transizione.
Non cambia se nella reazione interviene un catalizzatore.
E’ una grandezza che può essere definita solo per processi endoergonici.
Descrivere brevemente il concetto di catalisi facendo riferimento ai diagrammi dell’energia.
10.
a)
b)
c)
Il potenziale normale di riduzione per l’ossigeno (E0O2/O(2-)) è
Minore rispetto a E0FAD/FADH2.
Maggiore rispetto a E0Q/QH2 (Q=coenzima Q).
Nullo.
Descrivere come la catena di trasporto degli elettroni determini produzione di energia chimica.
11.
a)
b)
c)
Il ciclo dell’urea coinvolge mitocondri e citoplasma
Grazie a sistemi navetta che permettono il trasporto tra i due compartimenti cellulari.
Non è vero, avviene solo nel citoplasma.
E’ estremamente esoergonico.
12.
a)
b)
c)
L’acido alfa-chetobutanoico è
Generato esclusivamente dalla riduzione dell’acido alfa-idrossi butanoico.
È’ un importante intermedio della prima fase della respirazione cellulare.
Può essere ottenuto da amminoacidi.
Cosa si intende per reazione anaplerotica?
13.
a)
b)
c)
L’acetil-CoA
E’ precursore di acidi grassi.
E’ una molecola a bassa energia.
Non può essere ottenuto da corpi chetonici.
14.
a)
b)
c)
Il carbamilfosfato è
Un intermedio della lipolisi.
Viene ottenuto dall’ammoniaca prodotta dalla degradazione degli zuccheri.
E’ un prodotto del bicarbonato.
15.
a)
b)
c)
Lo zinco ha nei sistemi viventi un unico numero di ossidazione (+2)
E può partecipare a processi di ossidoriduzione.
È’ un importante coenzima.
E’ cofattore di vari enzimi.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 23-07-2012
Nome…………………………………..Cognome………………………………..n° matricola…………………… .
1.
a)
La combustione alla fiamma di 10 g glucosio
Produce teoricamente una quantità di energia equivalente a quella prodotta metabolicamente una volta che tale
quantità viene ingerita.
b) Genera idrogeno-carbonato come prodotto finale.
c) E’ cineticamente favorita.
Spiegare brevemente le motivazioni della risposta.
2.
a)
b)
c)
L’alfa-idrossi propanoato
E’ neutro a pH fisiologico.
Diffonde passivamente nelle cellule.
E’ un prodotto del piruvato che a sua volta può essere ottenuto dall’alfa-idrossi propanoato stesso.
Descrivere brevemente le principali tappe e la funzione del ciclo di Cori.
3.
a)
b)
c)
L’anidride carbonica generata nei tessuti
Determina l’alcalinizzazione del citoplasma.
E’ convertita in bicarbonato negli eritrociti.
Può essere utilizzata in processi anabolici dai mammiferi.
4.
a)
b)
c)
L’aspartame è un dipeptide costituito da aspartato e fenilalanina che sono
Due amminoacidi polari carichi.
Caratterizzati da elevata lipofilia che inibisce la solubità dell’aspartame in acqua.
Legati tra loro mediante un gruppo ammidico.
5.
a)
b)
c)
Il legame di un neurotrasmettitore al proprio recettore post-sinaptico
È di solito un legame covalente stabile e irreversibile.
Determina il cambiamento della struttura del recettore.
Lascia inalterato il potenziale elettrochimico di membrana
6.
a)
b)
c)
Un acido grasso
Entra nella beta ossidazione mediante un preliminare consumo di energia.
Può essere un precursore del piruvato.
E’ conservato sotto forma di fosfoanidridi.
Calcolare la resa energetica complessiva del catabolismo del 1,2,3-butanoil-glicerolo.
7.
a)
b)
c)
L’ortofosfato
E’ utilizzato nella sintesi di diverse biomolecole.
E’ il principale componente della matrice extracellulare.
A pH fisologico presenta tre cariche positive.
8.
a)
b)
c)
L’inibizione della lattato deidrogenasi
Limita la produzione di lattato.
Inibisce la gluconeogenesi.
Teoricamente riduce contemporaneamente i livelli intracellulari di lattato e piruvato.
9. Alcuni metalli come rame e ferro
a) Sono importanti coenzimi.
b) Sono coinvolti in importanti processi di ossidoriduzione.
c) Sono di solito liberi nel citoplasma.
Citare e descrivere brevemente almeno due processi biochimici differenti nei quali rame e ferro hanno
indipendentemente l’uno dall’altro un ruolo determinante.
10. Elevati livelli di alanina
a) Inibiscono la piruvato chinasi.
b) Attivano la glicolisi.
c)
Non hanno alcun effetto sulla produzione mitocondriale di citrato.
11.
a)
b)
c)
La conversione del fruttosio 6-fosfato a glucosio 6-fosfato
E’ un processo endoergonico.
E’ un processo irreversibile.
E’ catalizzata dallo stesso enzima che catalizza la reazione inversa
12. L’acido glutammico
a) Funge esclusivamente da substrato energetico.
b) Partecipa a reazioni anaplerotiche.
c) E’ l’unico amminoacido transaminabile.
Giustificare brevemente la risposta. Il glutammato può essere gluconeogenico? Perché? Dare una definizione di
amminoacidi gluco- e chetogenici.
13.
a)
b)
c)
Il fumarato
Può essere prodotto sia nel citoplasma che nel mitocondrio.
Contiene una funzione alcolica.
E’ prodotto dalla riduzione dell’acido alfa-idrossi butandioico.
14.
a)
b)
c)
Il meccanismo d’azione dell’insulina
E’ del tutto simile a quello degli ormoni steroidei.
Richiede specifici recettori.
E’ tipico di tutte le cellule.
15.
a)
b)
c)
I corpi chetonici possono essere considerati
Solubili in acqua come gli acidi grassi a catena media.
Delle vitamine.
Maggiormente biodisponibili rispetto agli acidi grassi liberi.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 05-10-2012
Nome…………………………………..Cognome………………………………..n° matricola…………………… .
1.
a)
b)
c)
Il potenziale normale di riduzione E°FAD/FADH2.
E’ minore rispetto al potenziale normale E°Q/QH2.
E’ maggiore del potenziale E°O2/O(2-).
E’ uguale al potenziale normale E°CitC Ox/CitC Red (CitC Ox=citocromo C ossidato, CitC Red=citocromo C
ridotto).
Motivare brevemente la risposta.
2.
a)
b)
c)
L’idrolisi di adenosina-5’-trifosfato
E’ meno esoergonica in presenza di ioni Mg2+ che in acqua.
Non risente della presenza di ioni divalenti positivi.
E’ estremamente veloce.
3. Una proteina ricca di residui di serina
a) Sarà fortemente lipofila.
b) Sarà caratterizzata da una prevalenza di avvolgimento casuale.
c) È un probabile substrato di chinasi.
Cosa si intende per avvolgimento casuale? Qual è l’amminoacido che favorisce la prevalenza di questo motivo
strutturale? Come può essere classificato l’amminoacido Serina?
4.
a)
b)
c)
L’anidride carbonica
Si scioglie facilmente nel citoplasma.
E’ prodotta nei mitocondri delle cellule eucariotiche.
Viene quantitativamente legata all’emoglobina.
5.
a)
b)
c)
La resa energetica complessiva della fermentazione omolattica
È di 2 molecole di ATP.
È di 2 molecole di ATP e 2 molecole di NADH+.
È di 4 molecole di ATP.
6.
a)
b)
c)
La conversione di glutammato ad alfachetoglutarato
Non avviene nelle cellule eucariotiche.
Può essere considerata una reazione anaplerotica.
Produce corpi chetonici.
7.
a)
b)
c)
La fosforilazione della glicogeno sintasi
Attiva l’enzima.
Avviene a carico di residui di lisina.
Inibisce la sintesi del glicogeno.
Descrivere la regolazione concertata di glicogenolisi e glicogenosintesi facendo riferimento sia agli ormoni che
intervengono nel processo che alle modificazioni post-traduzionali catalizzate dagli enzimi coinvolti
8.
a)
b)
c)
Il glucagone
Inibisce la lipolisi.
Attiva la gluconeogenesi.
Favorisce il deposito di trigliceridi nel tessuto adiposo.
9.
Perché il catabolismo di un acido grasso a catena lunga genera più energia rispetto al catabolismo di un
monosaccaride?
Perché genera un maggior numero di molecole di coenzimi ridotti.
Perché non ha bisogno di ossigeno.
Perché gli acidi grassi si riducono anziché ossidarsi.
Descrivere brevemente il catabolismo dei lipidi dall’introduzione mediante la dieta alla beta-ossidazione.
a)
b)
c)
10. I sali biliari
a) Favoriscono l’assorbimento intestinale dei polisaccaridi.
b) Agevolano la solubilità delle proteine nel citoplasma.
c) Sono fondamentali per l’idrolisi del legame estereo di trigliceridi.
11.
a)
b)
c)
I chilomicroni
Sono precursori di lipoproteine a bassa densità.
Sono composti solo da proteine.
Si accumulano nel tessuto adiposo.
12.
a)
b)
c)
Il muscolo di un soggetto che pratica prevalentemente discipline aerobiche
Capta in modo meno efficiente il glucosio dal flusso ematico.
Non risente della regolazione ormonale da parte di insulina.
È più efficiente nel catabolizzare substrati mediante consumo d’ossigeno
Qual è l’effetto dell’allenamento aerobico sul catabolismo lipidico a livello muscolare? Spiegare i meccanismi
che sottendono questo tipo d’adattamento.
13.
a)
b)
c)
L’alanina
È un amminoacido gluconeogenico.
Può essere deamminato ossidativamente.
Partecipa al ciclo di Cori.
14.
a)
b)
c)
La formazione del carbamilfosfato
Non richiede consumo di ATP.
È un processo endoergonico.
Coinvolge direttamente l’anidride carbonica.
15.
a)
b)
c)
La mioglobina
È localizzata a livello ematico.
È una proteina fibrosa.
È fonte d’ossigeno in condizioni d’ipossia.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 23-10-2012
Nome……………………….
Cognome …………………………. .n° matricola………….
1.
a)
b)
c)
La mioglobina
Richiede ioni ferrosi per poter legare O2.
Non risente di alterazioni del pH o della temperatura.
È espressa principalmente negli eritrociti.
Quali sono le principali differenze tra mioglobina ed emoglobina? Descrivere le curve di saturazione per le due
proteine.
2.
a)
b)
c)
Le cellule eucariotiche nei mammiferi
Possono sintetizzare l’acido oleico.
Sintetizzano l’acido nonadecanoico.
Non possono ottenere acidi grassi dal glucosio.
Descrivere le principali tappe della biosintesi degli acidi grassi.
3.
a)
b)
c)
Il catabolismo anaerobico del glucosio genera
Piruvato.
Coenzimi ossidati.
Acidi grassi.
4.
a)
b)
c)
La defosforilazione reversibile di proteine è catalizzata da
Chinasi.
Deidrogenasi.
Fosfatasi.
5.
a)
b)
c)
Nell’inibizione irreversibile di enzimi
L’inibitore si lega in siti alternativi al sito attivo.
L’inibitore ha una ridotta affinità per il sito attivo.
L’inibitore è strutturalmente molto simile al substrato.
Quali sono i principali meccanismi d’inibizione dell’attività enzimatica?
6.
a)
b)
c)
Il citrato
Inibisce la fosfofruttochinasi 1.
Attiva l’esochinasi.
Ha un’azione confrontabile con quella dell’adenosina 5’-monofosfato sulla glicolisi.
7.
a)
b)
c)
In condizioni normali nel mitocondrio lo spazio intermembrana
E’ caratterizzato da un pH più basso rispetto alla matrice mitocondriale.
Non presenta differenze nella concentrazione di ioni idronio rispetto alla matrice.
Contiene più ioni ossidrilici rispetto alla matrice.
8.
a)
b)
c)
La diffusione facilitata
Avviene grazie ad un gradiente elettrochimico favorevole.
E’ dovuta ad una differenza di concentrazione.
Richiede energia.
9.
a)
b)
c)
La membrana mitocondriale esterna
È permeabile rispetto a quella interna.
Permette di isolare la matrice.
È impermeabile al piruvato.
10. I chetoacidi prodotti nelle transaminazioni
a) Non possono essere usati per produrre energia.
b) Hanno un ruolo anabolico.
c) Sono composti sia anabolici che catabolici
11.
a)
b)
c)
L’insulina
Attiva la glicogeno fosforilasi.
Attiva la piruvato deidrogenasi.
Non agisce sulla trigliceride-lipasi.
Descrivere l’azione dell’insulina e del glucagone sulla mobilizzazione (accumulo e rilascio) dei trigliceridi dal
tessuto adiposo.
12.
a)
b)
c)
La conversione del glucosio 1-fosfato a glucosio 6-fosfato dopo la glicogeno lisi
È una riduzione.
È una fosforilazione.
È un’isomerizzazione.
13.
a)
b)
c)
Il di-idrossiacetone fosfato
Viene convertito esclusivamente in gliceraldeide 3-fosfato.
Può essere trasformato in glicerolo 3-fosfato.
Non può essere ridotto.
14. Un ridotto rapporto [NAD+]/[NADH] (dove le parentesi quadre indicano le concentrazioni) nel muscolo
favorisce
a) La conversione del lattato a piruvato.
b) La formazione di alanina.
c) La riduzione dell’acido alfa-cheto propanoico ad acido alfa-idrossi propanoico.
Descrivere il ciclo di Cori.
15.
a)
b)
c)
La conversione dell’isocitrato ad alfa-cheto glutarato
È endoergonica.
È irreversibile.
È una riduzione.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2011/2012
Biochimica, prova scritta del 04-02-2013
Nome……………………….
Cognome …………………………. .n° matricola………….
1) Quale delle curve riportate in figura rappresenta al meglio l'eventuale spostamento della curva di saturazione
dell'emoglobina in seguito all'aumento pH ematico? La curva A rappresenta la curva di saturazione
dell'emoglobina a pH 7,4.
a) curva B.
b) curva A.
c) curva C.
2) La regolazione della biosintesi degli acidi grassi
a) si basa soprattutto sulla regolazione del complesso acido grasso sintasi.
b) avviene principalmente a carico della acetil-CoA carbossilasi.
c) dipende dai livelli citoplasmatici di carnitina.
3) L'alanina e la glutammina sono prodotte nel muscolo rispettivamente
a) da ossalacetato e glutammato.
b) da alfa-chetoglutarato e aspartato.
c) da piruvato e glutammato.
Discutere il significato biochimico della produzione di alanina e glutammina nel muscolo sottolineando
le differenze nel catabolismo dei due amminoacidi.
4) Il 5-fluorouracile è utilizzato come farmaco chemioterapico che inibisce la produzione di timina ed in tal modo
compromette principalmente
a) la sintesi degli acidi deossiribonucleici.
b) la sintesi degli acidi deossiribonucleici e quindi la sintesi di lipidi di membrana.
c) la sintesi degli acidi ribonucleici e di conseguenza quella degli acidi deossiribonucleici.
5) Il complesso III della catena di trasporto degli elettroni catalizza
a) l'ossidazione dell'ubichinone ridotto.
b) l'ossidazione del Fe(II) a Fe(III) nei citocromi.
c) la riduzione dell'ossigeno.
Descrivere le principali fasi della catena di trasporto degli elettroni focalizzando l'attenzione sul ruolo e
le proprietà chimiche del coenzima Q e dei citocromi e sull’anadamento dei potenziali normali di riduzione delle
coppie ossidoriduttive coinvolte.
6) L'attività dell' amilasi salivare è massima
a) a pH acido (pH<6).
b) in condizioni di sostanziale neutralità.
c) in ambiente alcalino (pH>8).
7) La degradazione dell'alcool etilico da parte dell'alcool deidrogenasi porta alla formazione di acetaldeide che
viene convertita nel fegato in acido acetico. La degradazione ossidativa del metanolo, alcool che può essere
presente in alcune bevande alcoliche in seguito a frode alimentare, porta
a) alla stessa aldeide.
b) all'acetil-CoA.
c) alla formaldeide.
8) Il fruttosio 2,6-difosfato è prodotto mediante una reazione catalizzata dall'enzima fosfofruttochinasi II (PFKII).
La regolazione di tale enzima prevede
a) l'attivazione da parte dell'insulina.
b) l'attivazione da parte del glucagone.
c) la fosforilazione irreversibile di alcuni suoi residui di serina.
Descrivere i principali meccanismi di regolazione di glicolisi e gluoconeogenesi.
9) Perchè la funzione del ciclo di Krebs può essere definita catalitica?
a) Perchè avviene anche in assenza di Acetil-CoA.
b) Perchè rigenera ossalacetato, primo intermedio del ciclo.
c) Perchè è costituito da processi cineticamente favoriti.
10) La produzione di una molecola UDP-glucosio è
a) esoergonica.
b) cineticamente favorita.
c) possibile grazie all'accoppiamento con la lisi di molecole ad alta energia.
11) Quale di questi tessuti non è sensibile all'insulina?
a) il tessuto muscolare.
b) il tessuto adiposo.
c) l'epitelio intestinale.
12) Qual è tra quelli indicati il corretto ordine per densità decrescente?
a) VLDL>Chilomicroni>LDL>HDL.
b) HDL>VLDL>Chilomicroni>LDL.
c) HDL>LDL>VLDL>Chilomicroni.
Descrivere i processi di digestione e assorbimento dei triglicerridi evidenziando il ruolo fisiologico dei
diverse complessi lipoproteici coinvolti.
13) La deficienza dell'enzima acil-CoA deidrogenasi determina
a) l'aumento nella matrice mitocondriale delle concentrazioni di beta-chetoacil-CoA
b) l'aumento delle concentrazioni di carnitina nel plasma.
c) l'aumento plasmatico di acilcarnitine.
14) Nei mammiferi, la deamminazione ossidativa dell'aspartato
a) genera ossalacetato.
b) produce anidride carbonica.
c) non avviene.
15) Il malonato è un inibitore competitivo della succinato deidrogenasi. Tale tipo di inibizione
a) dipende dalle concentrazioni relative di malonato e succinato.
b) è irreversibile.
c) induce la diminuzione di Km dell'enzima.
Perchè il malonato ha tale effetto sulla succinato deidrogenasi? Qual è il significato biochimico di tale
inibizione?
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie e del Benessere
CdL in “Scienze delle attività motorie e sportive”
AA 2012/2013
Biochimica, prova scritta del 19-02-2013
1) Le reazioni di transaminazione a carico degli amminoacidi
a) sono reazioni di ossidoriduzione.
b) sono reazioni di condensazione.
c) sono reazioni di lisi.
2) La gluconeogenesi epatica da alanina
a) richiede meno energia della gluconeogenesi da lattato.
b) produce più energia rispetto alla gluconeogenesi da lattato.
c) è complessivamente più endoergonica della gluconeogenesi da lattato
Qual'è il bilancio energetico della gluconeogenesi? Discutere tutte le reazioni nelle quali siano coinvolte
molecole ad alta energia.
5) L'emoglobina fetale
a) è caratterizzata da modificazioni post-traduzionali che inibiscono il legame di ossigeno.
b) non ha una struttura quaternaria.
c) è sintetizzata a partire da geni diversi rispetto all'emoglobina materna.
6) Il metabolismo di neonati e bambini in età prescolare
a) è caratterizzato dall'attivazione della sintesi di corpi chetonici.
b) da una prevalenza della gluconeogenesi rispetto agli adulti.
c) da un ridotto fabbisogno energetico cerebrale.
7)
L'idrolisi di ATP in presenza di Mg2+
a) produce la stessa quantità di energia dell'idrolisi in acqua.
b) produce meno energia rispetto all'idrolisi in acqua.
c) produce più energia rispetto all'idrolisi in acqua.
Motivare la risposta.
8) Il cianuro è un inibitore del complesso IV della catena di trasporto degli elettroni e quindi
a) compromette l'ossidazione del Fe (II) a Fe (III) del citocromo c.
b) attiva la riduzione dell'ossigeno.
c) inibisce l'ossidazione di nicotinammide adenina dinucleotide ridotto.
9) La beta ossidazione dell'acido pentacosanoico (eìcosi=venti, dal greco)
a) richiede 22 molecole di ATP.
b) genera 11 molecole di Acetil-CoA.
c) avviene mediante 12 cicli di beta ossidazione.
10) Quali tra le seguenti affermazioni è corretta:
a) HDL e LDL sono ricche di colesterolo utile per la biosintesi dei colati.
b) Le HDL riducono il rischio di accumulo di lipidi sulle pareti arteriose.
c) Le LDL convogliano trigliceridi nel fegato.
11) I foglietti beta sono più stabili delle alfa eliche perchè
a) fattori sterici favoriscono coppie ioniche strette.
b) per la presenza di ponti disolfuro.
c) per la maggiore stabilità dei legami d'idrogeno.
Discutere l'effetto dei due motivi strutturali sulla solubilità in acqua e la suscettibilità alla proteolisi di
proteine caratterizzate prevalentemente dall'uno o dall'altro motivo strutturale. Qual'è l'effetto di una
prevalenza di alfa-elica sulla solubiltà in acqua? Qual'è l'effetto di una prevalenza di foglietto beta sulla
degradazione proteolitica della proteina stessa?
12) Elevati livelli di acetil-CoA mitocondriale
a) attivano piruvato carbossilasi.
b) attivano piruvato deidrogenasi.
c) inibiscono la citrato sintasi.
Descrivere brevemente la regolazione del ciclo degli acidi tricarbossilici.
Attività enzimatica (%)
13) Le curve mostrate in figura rappresentano almeno sommariamente
10-3
10-7
[H3O+]
a) l'andamento dell'attività enzimatica per glucochinasi e esochinasi.
b) l'andamento dell'attività enzimatica per pepsina e chimotripsina.
c) l'andamento dell'attività enzimatica per tripsina e pepsinogeno.
14) L'emoglobina esercita il suo potere tampone
a) legando principalmente idrogenocarbonato.
b) protonandosi a livello di residui basici.
c) legando principalmente ossigeno.
15) La sintesi di glicogeno
a) aumenta la pressione arteriosa.
b) diminuisce l'osmolarità del sangue.
c) aumenta la pressione osmotica degli eritrociti.
16) L'endocitosi di complessi lipoproteici da parte dei tessuti
a) avviene mediante diffusione semplice.
b) prevede la preliminare degradazione del complesso.
c) richiede recettori proteici specifici.
17) Perchè la funzione della pompa Na+, K+ ATP-asi è associata all'idrolisi di molecola ad alta energia?
a) Perchè genera un accumulo di cariche negative nella zona extracellulare della membrana citoplasmatica.
b) Perchè genera un gradiente elettrochimico di membrana.
c) Perchè catalizza l'influsso endoergonico di ioni sodio.
Descrivere brevemente le funzioni del potenziale elettrochimico di membrana focalizzando l’attenzione
sui processi di produzione di energia chimica.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie.
CdL in “Scienze delle attività motorie e sportive”
AA 2012/2013
Biochimica, prova scritta del 24-06-2013
1) La glicogenolisi muscolare
a) fornisce glucosio al miocita.
b) genera glucosio utilizzabile dal sistema nervoso centrale.
c) è un processo esoergonico.
2) Quali tra le seguenti coppie di amminoacidi è costituita da amminoacidi essenziali?
a) alanina e ornitina.
b) glutammina e glutammato.
c) valina e isoleucina.
Motivare brevemente la risposta e descrivere le principali classi di amminoacidi sulla base delle loro
proprietà chimico fisiche e dei loro gruppi funzionali.
18) La conversione della fosfocreatina a creatina
a) richiede ossigeno.
b) può avvenire in condizioni di anaerobiosi.
c) è irreversibile.
19) La biosintesi del malonato
a) prevede una reazione di condensazione.
b) non richiede ATP.
c) coinvolge direttamente il piruvato.
20)
Elevati livelli di acetil-CoA
a) inibiscono la glicolisi.
b) attivano la glicogenosintesi.
c) attivano la gluconeogenesi.
Motivare la risposta e discutere il meccanismo di regolazione dell’attività enzimatica coinvolto.
21) Quale tra i seguenti interventi nutrizionali dovrebbe favorire la sintesi di corpi chetonici?
a) La somministrazione di fruttosio.
b) La somministrazione di acidi grassi a catena medio-corta.
c) La somministrazione di proteine ricche di aspartato e glutammato.
22) L’adenosina 5’-monofosfato è
a) una molecola a bassa energia.
b) una fosfoanidride.
c) una molecola neutra.
23) Sapendo che la variazione di energia libera di Gibbs per la trasformazione di glucosio in due molecole di alfaidrossi propanoato è pari a -192 KJ/mol è possibile affermare che la resa energetica della fermentazione
omolattica è pari a:
a) 80%.
b) 10%.
c) 31%.
Come viene calcolata la resa energetica % del processo? Calcolare il numero di molecole di ATP
ottenute dalla conversione del glucosio in lattato considerando le molecole consumate e prodotte nell’intero
processo catabolico.
24) Il fumarato
a) partecipa esclusivamente al ciclo di Krebs.
b) partecipa al ciclo di Krebs, al ciclo dell’urea ed alla catena di trasporto degli elettroni.
c) è ottenuto per riduzione dell’acido butandioico.
25) La mioglobina
a) è una proteina allosterica.
b) è espressa principalmente nel muscolo.
c) è un trasportatore di ossigeno.
26) In condizioni di scarso fabbisogno energetico
a) i trigliceridi vengono mobilizzati dal tessuto adiposo.
b) l’alanina proveniente dal muscolo viene convertita in piruvato a livello epatico.
c) gli amminoacidi introdotti con la dieta vengono utilizzati per la sintesi proteica.
Qual è il ruolo fisiologico comune di alanina e glutammina prodotte nel muscolo?
27) L'aumento della temperatura
a) aumenta l’affinità dell’emoglobina per l’ossigeno.
b) diminuisce l’affinità dell’emoglobina per l’ossigeno.
c) non ha alcun effetto sull’affinità dell’emoglobina per l’ossigeno.
28) Il trasporto del glucosio a livello del lume intestinale prevede un sistema di trasporto
a) uniporto.
b) antiporto.
c) simporto.
Descrivere le principali tappe del trasporto del glucosio a livello intestinale.
29) Le fibre muscolari si distinguono in fibre a contrazione lenta o veloce. Quali delle seguenti affermazioni è
corretta?
a) Le fibre muscolari lente sono ricche di mitocondri.
b) Le fibre muscolari veloci prediligono acidi grassi come substrati energetici.
c) Le fibre muscolari lenete producono elevate quantità di alfa-idrossi propanoato.
30) La fosfofruttochinasi II è attivata da
a) glucagone.
b) epinefrina.
c) insulina.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie.
CdL in “Scienze delle attività motorie e sportive”
AA 2012/2013
Biochimica, prova scritta del 22-07-2013
Nome:
Cognome:
Numero di matricola:
1) Tre isoenzimi I1, I2, I3 hanno costanti di Michaelis-Menten che variano secondo il seguente ordine:
Km1<Km3<Km2. Quale delle seguenti affermazioni è corretta?
a) I3 si attiva alle concentrazioni più basse di substrato.
b) La reazione catalizzata da I1 è la più veloce.
c) I2 è l'enzima con maggiore affinità per il substrato.
●Definire la costante di Michaelis-Menten e il concetto di isoenzima facendo alcuni esempi.
2) Perché l'aumento di protoni nel citoplasma determina l'inibizione di PFK1?
a) Si ha la protonazione dei gruppi amminici nelle catene laterali.
b) I protoni reagiscono con i residui acidi della proteina.
c) Ha luogo un'inibizione competitiva.
3) Il ciclo dell'urea
a) coinvolge mitocondri e citoplasma.
b) coinvolge ribosomi e mitocondri.
c) avviene nello spazio intermembrana.
4) Sapendo che l'idrolisi di GTP libera circa 30KJ per mole, la sintesi di tale nucleoside trifosfato può avvenire
a) in concomitanza con la scissione di un legame ammidico.
b) mediante l'accoppiamento con la rottura di un legame fosfoestereo.
c) per idrolisi di un tioestere.
●Motivare la risposta.
5) Se siamo in condizioni tali da favorire la gluconeogenesi epatica
a) la reazione inversa catalizzata dalla lattato deidrogenasi è inibita.
b) le ammino transferasi sono attivate.
c) il pancreas produce elevate quantità di insulina.
6) I legami d'idrogeno tra unità amminoacidiche nei foglietti beta
a) coinvolge amminoacidi lontani tra loro.
b) coinvolge amminoacidi adiacenti.
c) coinvolge residui carichi positivamente e negativamente.
7) La degradazione di una molecola di acetoacetato può produrre
a) quattro molecole di succinil-CoA
b) due molecole di GTP.
c) tre molecole di anidride carbonica.
8) Le decarbossilazioni di isocitrato e alfa-chetoglutarato
a) sono reazioni acido-base.
b) sono reazioni di ossidoriduzione.
c) sono reazioni di condensazione.
9) Indicare quale tra quelli proposti sia l'ordine secondo il quale cambia la % di proteine nei complessi lipoproteici.
a) LDL>VLDL>Chilomicrone>HDL.
b) HDL>LDL>VLDL>Chilomicrone.
c) Chilomicrone>VLDL>LDL>HDL.
● Discutere l'assorbimento ed il trasporto dei lipidi a livello enterocitario ed a livello ematico.
10) Glucagone e adrenalina
a) favoriscono il catabolismo lipidico e la replicazione cellulare.
b) innescano la sintesi proteica e del colesterolo.
c) attivano la degradazione ossidativa dei lipidi e degli amminoacidi.
11) Il citrato
a) è un importante intermedio nella sintesi degli acidi grassi.
b) è un acido dicarbossilico.
c) genera acetil-CoA nel mitocondrio.
12) Quale tra le seguenti molecole lipidiche non può formare legami d'idrogeno?
a) fosfolipide.
b) colesterolo.
c) trigliceridi.
13) Ridotti livelli di ossalacetato e aspartato citosolici
a) possono essere riconducibili all'attivazione della sintesi proteica.
b) suggeriscono una condizione di scarso fabbisogno energetico.
c) Indicano la possibile alterazione del trasporto tra mitocondrio e citoplasma.
14) Secondo l'ipotesi chemiosmotica
a) ATP viene generata per fosforilazione a livello del sustrato.
b) ATP viene prodotta da GTP.
c) ATP viene ottenuta mediante dissipazione di un gradiente elettrochimico.
● Cosa ipotizza la teoria chemiosmotica?
15) La formazione del pirofosfato nella sintesi del glicogeno
a) sposta la reazione verso la sintesi di un legame fosfoanidrico.
b) rende possibile la formazione di glucosio 6-fosfato.
c) è esoergonica.
●Discutere il ruolo del pirofosfato nella biosintesi del glicogeno e citare almeno un altro processo metabolico
che coinvolge tale composto.
Università degli Studi Kore di Enna
Facoltà di Ingegneria, Architettura e delle Scienze Motorie.
CdL in “Scienze delle attività motorie e sportive”
AA 2012/2013
Biochimica, prova scritta del 02-09-2013
Nome:
Cognome:
Numero di matricola:
1) Nell'ambito di una catena peptidica, serina e fosfoserina
a) sono amminoacidi polari neutri.
b) possono formare legami d'idrogeno.
c) contengono rispettivamente una funzione alcoolica e una funzione fosfoanidridica
● Serina e fosfoserina sono tra loro correlate dal punto di vista chimico e biochimico? Citare e descrivere un
processo metabolico che coinvolge entrambi gli amminoacidi.
2) L'ornitina partecipa al ciclo dell'urea ed è
a) prodotto dell'arginosuccinato.
b) una molecola ad alta energia.
c) presente sia a livello citosolico che mitocondriale.
3) La beta-ossidazione di un acido grasso
a) è un processo complessivamente endoergonico.
b) richiede l'attivazione dell'acido grasso con consumo di due molecole di ATP.
c) genera sempre propionil-CoA.
4) Nella catena di trasporto degli elettroni
a) gli elettroni vengono ceduti da coppie a potenziale normale di riduzione minore a coppie a potenziale normale di
riduzione maggiore.
b) gli elettroni vengono ceduti da coppie a potenziale normale di riduzione elevato mediante processi che non richiedono
catalisi.
c) gli elettroni vengono ceduti da coppie a potenziale normale di riduzione maggiore a coppie a potenziale normale di
riduzione minore.
● Definire il potenziale normale di riduzione e le variazioni DE°. Qual è la relazione con la variazione di energia
libera di Gibbs? Come varia DE° durante la catena di trasporto degli elettroni?
5) La biosintesi degli acidi grassi
a) parte dal citrato.
b) parte dal malonil-CoA.
c) parte dall'acetil-CoA.
6) La lipasi ormone sensibile
a) catalizza la lipolisi negli adipociti.
b) rende possibile l'accumulo di grassi negli adipociti.
c) non è regolata dall'insulina.
●Descrivere i principali stadi dell'accumulo e del rilascio di grassi a livello adipocitario.
7) La glicina è un amminoacido chetogenico ovvero
a) genera un precursore del glucosio.
b) genera un intermedio del ciclo di Krebs.
c) genera acetil-CoA
8) La sintesi proteica
a) avviene a livello ribosomiale.
b) avviene nel nucleo.
c) avviene a livello del reticolo endoplasmatico liscio
●Citare almeno tre processi che avvengono specificamente nei tre compartimenti subcellulari citati.
9) Nel DNA, basi puriniche e pirimidiniche
a) interagiscono mediante interazioni ione-dipolo.
b) interagiscono mediante legami d'idrogeno.
c) interagiscono mediante forze didispersione di London.
10) La conversione del propionil-CoA ad acido butandioico
a) è una reazione di ossidazione.
b) prevede una decarbossilazione.
c) è una reazione anaplerotica.
11) La conversione del 3-fosfoglicerato a 1,3-difosfoglicerato
a) è una reazione della gluconeogenesi.
b) è una reazione esoergonica.
c) è una tappa cruciale della degradazione ossidativa del glucosio.
12) La glutammina prodotta nel muscolo viene trasferita al fegato dove
a) viene deamminata ossidativamente.
b) è convertita in glutammato.
c) è utilizzata nella sintesi proteica.
●Descrivere brevemente le principali tappe della deamminazione ossidativa.
13) Il fumarato prodotto nel ciclo dell'urea può generare
a) 2 molecole di GTP.
b) 13 molecole di ATP.
c) 11 molecole di ATP e 2 molecole di GTP.
14) L'aumento di glucosio 6-fosfato citosilico
a) determina l'inibizione competitiva di esochinasi.
b) inibisce PFK1 in modo non competitivo.
c) attiva piruvato chinasi.
15) L'insulina
a) attiva la sintesi dei corpi chetonici.
b) induce l'aumento delle concentrazioni plasmatiche di alanina.
c) innesca l'accumulo di lipidi negli adipociti.
Università degli Studi di Enna Kore
Facoltà di Ingegneria, Architettura e delle Scienze Motorie.
CdL in “Scienze delle attività motorie e sportive”
AA 2012/2013
Biochimica, prova scritta del 16-09-2013
Nome:
Cognome:
Numero di matricola:
1) L'isomerizzazione del glucosio 6-fosfato a glucosio 1-fosfato è una reazione fondamentale
a) della glicolisi.
b) della gluconeogenesi.
c) della glicogenosintesi.
2) La regolazione dell'attività enzimatica mediante fosforilazione reversibile
a) è un esempio di regolazione competitiva.
b) è un esempio di regolazione non competitiva.
c) è un esempio di regolazione per formazione di legami covalenti.
● Descrivere i principali meccanismi di regolazione dell'attività enzimatica e discutere in modo esauriente il ruolo
della fosforilazione in tale fenomeno.
3) La fruttosio 1,6-difosfatasi
a) catalizza una reazione endoergonica.
b) genera un composto a peso molecolare minore rispetto al precursore.
c) rende cineticamente favorita una reazione di isomerizzazione.
4) In conseguenza di un'attività muscolare massimale e prolungata
a) i miociti consumano tutte le molecole di ATP disponibili.
b) la sensazione di fatica è riconducibile all'acidificazione del citoplasma dei miociti.
c) Il consumo di ossigeno si riduce.
● Descrivere le principali alterazioni metaboliche che avvengono a livello muscolare durante lo svolgimento di
attività fisica prolungata ad elevata intensità.
5) Il glucagone a livello epatico induce
a) la fosforilazione della fosfofruttochinasi 2.
b) la defosforilazione della glicogenosintasi.
c) la defosforilazione della glicogeno fosforilasi.
6) L'aumento di acido carbonico e dei suoi prodotti di dissociazione nel sangue
a) favoriscono il rilascio di ossigeno dall'emoglobina.
b) alcalinizzano il citoplasma degli eritrociti.
c) neutralizzano gli ioni idronio plasmatici.
●Spiegare in modo dettagliato perché l'emoglobina così come il bicarbonato possa essere considerata un tampone
ematico.
7) L'enzima piruvato carbossilasi
a) è attivato da elevati livelli di acetil-CoA.
b) è inibito da bassi livelli di adenosina 5'-difosfato.
c) è attivato da elevati livelli di fruttosio 2,6-difosfato.
8) L'enzima lattato deidrogenasi è un enzima tetramerico costituito da subunità H e M in numero variabile. La prevalenza
di subunità H favorisce la catalisi della reazione inversa. Quindi
a) l'espressione del gene della subunità H è minore nelle fibre muscolari di tipo II che nel cuore.
b) l'espressione del gene della subunità M è maggiore nel cuore che nelle fibre muscolari di tipo II.
c) l'espressione dei due geni è sostanzialmente equivalente nei due tessuti.
●Motivare la risposta facendo riferimento al differente metabolismo delle diverse fibre muscolari.
9) Il potenziale normale di riduzione E° (diidrossiacetone fosfato/glicerolo 3-fosfato)
a) è minore rispetto al potenziale E° (Q/QH2).
b) è maggiore rispetto a E° (O2/O2-).
c) è circa uguale a E° (diidrossiacetone fosfato/gliceraldeide 3-fosfato).
10) Il sistema nervoso centrale consuma elevate quantità di glucosio
a) per alimentare la pompa Na+/K+ ATP dipendente.
b) specificamente durante un'intensa attività intellettuale.
c) in modo insulino-dipendente.
11) L'immagine mostra
a) un procariota.
b) una cellula eucariotica.
c) un organismo pluricellulare.
12) L'enzima acetil-CoA carbossilasi
a) è inibito dall'attività fisica.
b) è attivato dal'aumento della secrezione di glucagone.
c) è inibito in condizioni di scarso fabbisogno energetico.
●Descrivere brevemente la biosintesi degli acidi grassi, dare una breve definizione di acido grasso essenziale e citare
alcuni esempi di tale classe di acidi grassi
13) la sintesi dell'acido oleico dall'acido octadecanoico
a) è una reazione di riduzione.
b) richiede nicotinammide adenina dinucleotide ossidato.
c) è un esempio di sintesi di un acido grasso omega-3.
14) L'allenamento aerobico
a) aumenta l'attività della carnitina acil transferasi I.
b) attiva la sintesi proteica.
c) inibisce la glicogeno sintasi.
15) La gluconeogenesi da piruvato richiede il consumo di
a) 12 molecole di ATP.
b) 2 molecole di ATP e 2 molecole di GTP.
c) 2 molecole di GTP e 4 molecole di ATP.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 3-02-2014
Nome:
Cognome:
Numero di matricola:
1) Il fruttosio 2,6-bi-fosfato
a) inibisce fosfofruttochinasi 1.
b) inibisce la fruttosio 1,6-difosfatasi.
c) è un effettore allosterico positivo dell'emoglobina.
2) Il trasporto di gruppi amminici dal muscolo al fegato
a) è più efficiente quando coinvolge la glutammina.
b) avviene solo attraverso il trasporto di glutammina.
c) non dipende dalle concentrazioni di glutammina nel muscolo.
● Descrivere brevemente il destino della glutammina prodotta nel muscolo.
3) Un elevato rapporto NAD+/NADH citosolico
a) inibisce la conversione del piruvato a lattato.
b) non ha alcun effetto sull'attività della lattato deidrogenasi.
c) inibisce la conversione del lattato a piruvato.
4) La reazione complessiva del ciclo dell'urea è
a) NH3 + CO2 + ossalacetato + 3ATP + 2H2O ==> urea + aspartato + 2 ADP + 2Pi + AMP + PPi
b) NH3 + CO2 + alfachetoglutararto + 3ATP + 2H2O ==> urea + glutammato + 2 ADP + 2Pi + AMP + PPi
c) NH3 + CO2 + aspartato + 3ATP + 2H2O ==> urea + fumarato + 2 ADP + 2Pi + AMP + PPi
● Come avviene la sintesi del carbamilfosfato? E' endo- o esoergonica? Il carbamilfosfato è una molecola a bassa o
alta energia?
5) L’antimicina è un inibitore del complesso III quindi
a) favorisce la fosforilazione ossidativa.
b) interrompe la catena di trasporto degli elettroni.
c) aumenta il consumo di ossigeno.
6) Nelle fasi di recupero dopo un’intensa attività fisica la somministrazione di carboidrati
a) favorisce la lipolisi.
b) induce la produzione di glucagone e adrenalina.
c) ripristina le scorte di glicogeno.
●Nella fase di recupero qual è il destino degli amminoacidi introdotti con la dieta? Discutere l’argomento
considerando l’azione degli ormoni prodotti in tali condizioni.
7) la reazione catalizzata dall’enolasi
a) prevede una disidratazione.
b) è NAD+ dipendente.
c) è irreversibile.
8) Una dieta ricca in acidi grassi a catena corta
a) teoricamente favorisce il metabolismo energetico cerebrale.
b) favorisce la gluconeogenesi.
c) è determinate per la proliferazione cellulare.
●Quante molecole di acetoacetato possono essere ottenute da una molecola di acido decanoico? Mediante quale
processo ed in quali condizioni? Qual è il destino dell’acetoacetato?
9) La diminuzione delle concentrazioni di acetilcarnitine plasmatiche
a) può indicare un’attivazione della biosintesi degli acidi grassi.
b) è indotta dal glucagone.
c) denota l’inibizione degli enzimi carnita acil-transferasi.
10) Un elevato livello di ribosio 5-fosfato nelle cellule indica che
a)i mitocondri sono estremamente attivi.
b) le cellule sono pronte alla duplicazione.
c) che le cellule hanno un aumentato fabbisogno di ossigeno.
Descrivere brevemente il dogma centrale della biologia molecolare. Qual è il motivo per il quale l’affermazione
“un gene=una proteina” non è corretta?
11) Il consumo di etanolo determina l’aumento dei depositi adiposi perchè
a) l’etanolo è un precursore del piruvato.
b) l’etanolo viene convertito in lattato nel fegato.
c) l’etanolo produce acido acetico.
12) Il manganese è
a) cofattore di enzimi.
b) un coenzima di un enzima.
c) un elemento non essenziale per l’organismo.
13) I cicli di beta-ossidazione necessari alla degradazione dell’acido octadecanoico sono
a) 10
b) 9
c) 8
14) La conversione di un acido grasso in acil-CoA
a) è esoergonica.
b) richiede un accoppiamento di reazioni.
c) genera un fosfoestere.
15) Il trasporto antiporto
a) coinvolge specie con cariche di segno opposto.
b) coinvolge di solito specie neutre a basso peso molecolare.
c) coinvolge specie che hanno la stessa carica.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 3-02-2014
Nome:
Cognome:
Numero di matricola:
1) In quale delle patologie indicate l'attivazione della sintesi di tripsina da tripsinogeno aumenta a tal punto da indurre un
danno tissutale spesso fatale?
a) Il morbo di Alzheimer.
b) Sclerosi laterale amiotrofica.
c) Pancreatite acuta.
2) Le principali reazioni della biosintesi degli acidi grassi dopo l'attivazione di acetil-CoA e malonil-CoA sono
a) Sintesi di enoil-CoA ==> idratazione con formazione di -idrossiacil-CoA ==> ossidazione a -chetoacil-CoA.
b) Sintesi di -chetoacil-ACP==>riduzione a-idrossi-acil-ACP==>disidratazione a enoil-ACP ==>riduzione ad acil-ACP
c) Sintesi di -idrossi-acil-ACP ==> ossidazione a -chetoacil-CoA ==> riduzione a enoil-CoA ==> idrogenazione ad
acil-ACP
● Descrivere la biosintesi degli acidi grassi e i meccanismi di regolazione del processo. Qual è l'enzima chiave che
viene regolato?
3) La iper-espressione di superossido dismutasi non associata all'aumento dei livelli di catalasi è tipica della trisomia 21 e
a) inibisce la produzione di anione superossido
b) attiva la sintesi di perossido d'idrogeno.
c) aumenta le difese da stress ossidativo.
4) La seguente reazione
HO
O
C
H
HO
C
C
CH2
HO
O
C
C
NH2
HO
C
O
CH2
O
O
a) E' una transaminazione.
b) Produce corpi chetonici.
c) E' indispensabile al trasporto di NAD+ citosolico nel mitocondrio.
● Denominare i due composti utilizzando la nomenclatura comune e citare almeno tre processi nei quali la reazione
è coinvolta specificandone il ruolo.
5) Molte chinasi richiedono ioni positivi, come Mg2+, come cofattori. Infatti tali ioni
a) minimizzano le repulsioni tra substrato e ATP.
b) aumentano l'energia di attivazione dello stato di transizione.
c) rendono più reattiva l'ATP coinvolta.
6) Tutta l'anidride carbonica prodotta nei tessuti è trasportata direttamente nei polmoni.
a) Infatti l'emoglobina lega avidamente tutta l'anidride carbonica gassosa prodotta.
b) Non è vero, l'anidride carbonica è trasportata attraverso il plasma essendo molto solubile in acqua.
c) Tale affermazione è scorretta poiché la maggior parte dell'anidride carbonica prodotta viene immediatamente
trasformata.
●Descrivere i meccansmi di regolazione dell'affinità dell'emoglobina per l'ossigeno.
7) Il massimo consumo di ossigeno (VO2max) varia tra 69-95 mL Kg-1 min-1 negli atleti che praticano sci nordico e tra
40-60 mL Kg-1 min-1 negli atleti che praticano baseball. Si può quindi prevedere che
a) un giocatore di baseball consuma più efficacemente acidi grassi.
b) la produzione di ATP è complessivamente più alta nel muscolo dello sciatore.
c) la sintesi di glicogeno muscolare è attivata in entrambi gli atleti rispetto ad una persona sedentaria.
8) Il fosfoenolpiruvato
a) è una molecola a bassa energia.
b) è una molecola ridotta rispetto alla gliceraldeide 3-fosfato.
c) è un intermedio della gluconeogenesi.
9) Il potenziale normale di riduzione E° (FADH2/FADH)
a) è minore rispetto a E° (NADH/NAD+).
b) è minore rispetto a E° (QH2/Q).
c) è minore rispetto a E° (acil-CoA/enoil-CoA).
10) Le HDL
a) contengono prevalentemente colesterolo.
b) hanno densità minore rispetto alle VLDL.
c) contengono complessivamente più lipidi rispetto ai chilomicroni.
●Descrivere il meccanismo di sintesi e la funzione dei complessi lipoproteici, evidenziando le differenze chimicofisiche tra tali complessi.
11) L'acetil-CoA
a) è un inibitore della piruvato carbossilasi.
b) inibisce piruvato deidrogenasi.
c) attiva la piruvato chinasi
12) I ponti disolfuro
a) sono estremamente termolabili.
b) si scindono a pH pari a 7.4.
c) sono sensibili a forti riducenti.
●Che cos'è chimicamente un ponte disolfuro rispetto ai tioli? Quali amminoacidi possono generarlo? Descrivere la
struttura terziaria delle proteine e le interazioni che la stabilizzano.
13) il fumarato prodotto nel ciclo dell'urea può produrre
a) 24 molecole di ATP.
b) 12 molecole di ATP.
c) 11 molecole di ATP.
14) L’acidità degli acidi carbossilici come il lattato
a) aumenta il pH.
b) attiva la glicolisi.
c) è dovuta all’elevata stabilità dei prodotti.
15) Il trasporto dell'ornitina dal citoplasma al mitocondrio avviene mediante
a) diffusione semplice.
b) trasporto passivo facilitato
c) trasporto attivo.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 01-07-2014
Nome:
Cognome:
Numero di matricola:
1) Quale delle seguenti osservazioni è corretta?
a) L’EME è il coenzima dell’emoglobina.
b) L’EME è il cofattore della mioglobina.
c) L’EME è covalentemente legato al citocromo c.
2) Le variazioni del pH rispetto a quello fisiologico
a) possono incidere solo sullo stato di carica delle catene laterali di amminoacidi polari carichi.
b) determinano gradi di protonazione differenti dei residui ammino e carbossiterminale così come dei residui polari
carichi.
c) non hanno alcun effetto sulle interazioni che stabilizzano la struttura terziaria di una proteina.
● In condizioni di ipossia come varia il pH nei miociti? Dare una breve spiegazione del fenomeno e specificare quali
siano le principali conseguenze metaboliche di tale variazione.
3) Il perossido d’idrogeno (H2O2)
a) corrisponde ad una specie dell’ossigeno più ridotta dell’acqua.
b) può essere accidentalmente prodotto nella catena di trasporto degli elettroni.
c) è un forte riducente.
4) Se una reazione richiede l’idrolisi simultanea di una molecola ad alta energia allora
a) la trasformazione complessiva sarà fortemente endoergonica.
b) la reazione stessa è endoergonica.
c) l’intero processo è cineticamente sfavorito.
● Definire brevemente il concetto di accoppiamento di reazioni e fare almeno tre esempi di trasformazioni nelle
quali avviene.
5) Il disulfiram è un farmaco che blocca l’enzima aldeide ossidasi legandosi al sito attivo. Questo è un esempio di
a) inibizione competitiva.
b) inibizione non competitiva.
c) inibizione per formazione di legame covalente.
6) L’influsso e l’efflusso di acido lattico a livello cellulare avviene mediante
a) trasporto attivo.
b) diffusione facilitata.
c) diffusione semplice.
●Spiegare perché il lattato è un composto gluconeogenico.
7) Le carni rosse rispetto alle carni bianche
a) contengono più proteine.
b) contengono più ferro emico.
c) contengono più polisaccaridi.
8) La condensazione di un gruppo aldeidico con un gruppo alcolico genera
a) un emiacetale.
b) un estere.
c) un’anidride.
9) Il potenziale normale di riduzione E° (NAD+/NADH)
a) è maggiore rispetto a E° (fumarato/succinato).
b) è minore rispetto a E° (citocromo c (Fe3+)/citocromo c (Fe2+)).
c) è maggiore rispetto a E° (acetaldeide/etanolo).
●Dare la definizione di potenziale normale di riduzione e motivare brevemente la risposta facendo riferimento alle
specifiche reazioni indicate ed ai processi nelle quali sono coinvolte.
10) Le reazioni irreversibili del ciclo di Krebs sono
a) le decarbossilazioni ossidative.
b) le riduzioni NAD+ dipendenti.
c) le ossidazioni FAD dipendenti.
11) Un ciclo di beta ossidazione genera complessivamente
a) 2 molecole di FADH2 e due molecole di acetil-CoA
b) 2 molecole di NADH e una molecola di Acetil-CoA
c) 1 molecola di NADH, 1 molecola di FADH2 e 1 molecola di Acetil-CoA
●Giustificare la risposta commentando il meccanismo della beta ossidazione.
12) Le ammine biogene
a) sono prodotti della deamminazione ossidativa.
b) sono prodotti da transaminazioni.
c) sono ottenute mediante decarbossilazione di AA.
13)L’insulina
a) attiva la fosforilazione della glicogeno fosforilasi.
b) attiva l’enzima fosfatasi che defosforila la glicogeno fosforilasi.
c) inibisce la fosforilazione della glicogeno sintasi.
14) L’allenamento aerobico
a) induce l’iper-epressione dell’enzima lattato deidrogenasi muscolare.
b) aumenta espressione e attività dell’enzima glicerolo 3-fosfato deidrogenasi nel muscolo.
c) riduce la mitocondriogenesi nel muscolo.
15) Gli amminoacidi ramificati vengono utilizzati come integratori nell’allenamento di forza
a) perché vengono prevalentemente utilizzati dal muscolo.
b) perché la loro ossidazione produce più energia rispetto a quella prodotta da AA appartenenti a classi diverse.
c) perché, essendo i più solubili in acqua, sono anche i più biodisponibili.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 22-07-2014
Nome:
Cognome:
Numero di matricola:
1) Quale delle seguenti affermazioni NON è corretta?
a) Il coenzima Q accetta elettroni nelle reazioni catalizzate dai complessi I e II.
b) Il citocromo C accetta elettroni dal complesso II.
c) Il complesso II è la succinato deidrogenasi.
2) La fatica associata all’anemia ed alla carenza di ferro può essere spiegata considerando
a) la carenza di coenzima Q.
b) l’attivazione della sintesi di coenzimi ridotti.
c) una diminuzione dei livelli di citocromo c.
● Motivare la risposta dimostrando mediante adeguata argomentazione che due delle risposte sono errate.
3) A pH fisiologico glicina e aspartato
a) sono entrambi neutri.
b) hanno entrambi carica complessiva negativa.
c) sono caratterizzati da cariche diverse.
4) La proteina chinasi attivata da AMP
a) attiva la acetil-CoA carbossilasi.
b) fosforila ed inibisce la acetil-CoA carbossilasi.
c) defosforila e inibisce la acetil-CoA carbossilasi.
● Dare una breve definizione della funzione svolta dagli enzimi chinasi, fosfatasi e fosforilasi evidenziando le
differenze nei processi catalizzati da tali enzimi.
5) L’enzima malico
a) catalizza la reazione da malato ad ossalacetato.
b) è un enzima NADP+ dipendente.
c) catalizza una reazione fortemente esoergonica.
6) La tirosina viene degradata ad acetil-CoA e fumarato ed è quindi
a) una amminoacido chetogenico.
b) un amminoacido gluconeogenico.
c) un amminoacido sia gluconeogenico che chetogenico.
●Definire gli amminoacidi chetogenici e descrivere brevemente il destino dei corpi chetonici specificando nome e
ruolo degli enzimi coinvolti nella via.
7) Le forme di acidosi lattica congenita determinano
a) un aumento di NADH citosolico e l’inibizione di LDHM4.
b) l’aumento della concentrazione di ADP è l’attivazione della glicolisi.
c) l’attivazione dell’enzima piruvato deidrogenasi.
8) La fatica associata ad esercizio fisico ad alta intensità è dovuta
a) alla diminuzione di ADP nelle cellule.
b) all’aumento delle concetrazioni di piruvato
c) all’incapacità di produrre una sufficiente quantità di ATP
● Motivare brevemente la risposta.
9) Quale di tali enzimi non è presente nel muscolo?
a) Glicogeno sintasi.
b) Glucochinasi.
c) Fruttosio 1,6-difosfatasi.
10) Quale tra i seguenti enzimi richiede ATP?
a) Arginosuccinato sintasi.
b) glutammato deidrogenasi.
c) alanina amminotransferasi.
11) Differenti enzimi possono agire sullo stesso substrato generando lo stesso prodotto. Tali enzimi
a) hanno la stessa struttura primaria.
b) sono inducibili.
c) sono definiti coenzimi.
12) La produzione netta di ATP nei processi che portano da glucosio e da glicogeno a piruvato è
a) 2 molecole di ATP da glucosio e 3 molecole di ATP dal glicogeno.
b) 2 molecole di ATP da glucosio e 2 molecole di ATP da glicogeno.
c) 2 molecole di ATP da glucosio e 1 molecola di ATP da glicogeno.
●Giustificare la risposta commentando i meccanismi della prima fase della respirazione cellulare e della
glicogenolisi.
13) L’esercizio di resistenza
a) attiva il catabolismo anaerobico alattacido.
b) attiva il catabolismo dei grassi.
c) attiva la fermentazione.
14) Qual è tra quelli indicati il valore più vicino al potenziale di membrana a riposo di una cellula eucariotica?
a) + 70 mV
b) -60 mV
c) -100mV
15) Il trasporto del glucosio negli eritrociti è un esempio di
a) trasporto attivo.
b) trasporto mediato da ioni.
c) diffusione facilitata.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 01-09-2014
Nome:
Cognome:
Numero di matricola:
1) La degradazione ossidativa dell’acido acetico
a) fornisce meno energia rispetto alla degradazione aerobica del glucosio.
b) fornisce la stessa quantità di energia rispetto alla degradazione aerobica del glucosio.
c) fornisce più energia rispetto alla degradazione aerobica del glucosio.
● Motivare la risposta calcolando il numero di molecole di ATP ottenute dalla degradazione ossidativa
dell’acido acetico.
2) L’allungamento della catena lineare di una molecola di glicogeno mediante la formazione di 4 legami alfa1,4 glicosidici
a) richiede una molecola di UTP.
b) richiede il consumo di circa 120 KJ/mol.
c) è agevolata dalla formazione di una molecola di pirofosfato.
3) Quale tra questi organelli è sede sia della sintesi di complessi lipoproteici che della maturazione posttraduzionale delle proteine?
a) Il reticolo endoplasmatico liscio.
b) Il reticolo endoplasmatico rugoso.
c) L’apparato del Golgi.
4) Quale i seguenti motivi strutturali è maggiormente suscettibile ad un aumento dei livelli di ROS?
a) Il ponte disolfuro.
b) Il foglietto beta.
c) Il legame ammidico.
● Motivare la risposta e discutere brevemente le differenze nella stabilità del gruppo estereo, del gruppo
tioestereo e del gruppo ammidico. Che cosa determina una differente reattività tra ammidi ed esteri? E
tra esteri e tioesteri?
5) L’attività motoria aerobica diminuisce l’insulino-resistenza. Quale tra i seguenti meccanismi è quello
coinvolto in tale effetto?
a) L’ iper-espressione della ATP-citrato liasi.
b) L’iper-espressione di Glut4.
c) L’iper-espressione della lattato deidrogenasi A.
6) Sapendo che l’energia prodotta dalla scissione del legame fosfoestereo del fosfoenolpiruvato è pari a circa 50
KJ/mol si può prevedere che
a) l’energia liberata nella decima reazione della glicolisi è di circa 50 KJ/mol.
b) l’energia consumata nella decima reazione della glicolisi è di circa 30 KJ per mole.
c) l’energia residua e dispersa sotto forma di calore nella stessa reazione è pari a circa 31KJ/mol.
7) Le traslocasi mediano
a) il trasferimento della carnitina dalla matrice allo spazio intermembrana.
b) il trasferimento dell’acil-CoA dallo spazio intermembrana alla matrice.
c) il trasferimento delle acilcarnitine dal citoplasma allo spazio intermembrana.
8) L’alanina
a) inibisce la fosfofruttochinasi I.
b) inibisce l’esochinasi.
c) inibisce la piruvato chinasi.
● Spiegare il motivo per cui l’alanina ha un’azione inibitoria sulla prima fase della respirazione cellulare
e definire il meccanismo di regolazione attuato.
9) La figura 1 riportata in seguito rappresenta:
a) il processo di maturazione post-traduzionale delle proteine e la loro secrezione.
b) la trascrizione e la traduzione dei geni e la loro secrezione nel flusso linfatico.
c) la biosintesi ed esocitosi dei chilomicroni.
10) La figura 2 riportata in seguito rappresenta
a) un processo a due stadi.
b) un sistema all’equilibrio.
c) un processo spontaneo dal punto di vista cinetico.
● Disegnare un diagramma dell’energia per un processo endoergonico ed uno esoergonico indicando le
variabili in ascissa ed ordinata. Dare le definizioni di energia di attivazione, stato di transizione ed
intermedio di reazione.
11) Quale tra le seguenti affermazioni è corretta?
a) Le VLDL contengono in percentuale più colesterolo che trigliceridi.
b) Le LDL contengono più colesterolo rispetto alle HDL.
c) Le HDL contengono più trigliceridi rispetto ai chilomicroni.
12) L’assunzione di saccarosio
a) determina livelli glicemici inferiori rispetto all’assunzione di glucosio
b) determina una maggiore produzione di insulina rispetto all’assunzione di glucosio.
c) induce in modo più probabile l’insulino resistenza rispetto all’assunzione di glucosio.
● Definire l’indice glicemico degli alimenti ed argomentare la risposta fornita.
13) La saponificazione
a) consiste nella sintesi di un legame ammidico.
b) consiste nell’idrolisi di un legame estereo.
c) è una reazione di condensazione.
14) DNA ed RNA
a) contengono le stesse basi nucleotidiche.
b) sono localizzati negli stessi compartimenti cellulari.
c) contengono unità monosaccaridiche diverse.
15) Quale delle seguenti affermazioni è corretta (DG=variazione di energia libera di Gibbs)?
a) DG (malato ossalacetato) > DG (succinil-CoA succinato) >DG (ossalacetato citrato)
b) DG (alfa-chetoglutarato succinil-CoA) > DG (malato ossalacetato) >DG (fumarato malato)
c) DG (succinato fumarato) > DG (alfa-chetoglutarato isocitrato) > DG (ossalacetato malato)
Figura 1
Figura 2
Reticolo
endoplasmatic o
liscio
Golgi
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 22-09-2014
Nome:
Cognome:
Numero di matricola:
1) In seguito ad unaumento delle concentrazioni di CO2 la curva di saturazione dell’emoglobina
a) non subisce particolari alterazioni.
b) si sposta a sinistra rispetto alle condizioni normali.
c) Si sposta a destra rispetto alle condizioni normali.
● Motivare la risposta rappresentando graficamente la risposta considerata corretta.
2) La fosfofruttochinasi 2
a) è un isoenzima della fosfofruttochinasi 1.
b) catalizza una reazione che richiede consumo di ATP.
c) partecipa alla prima fase della respirazione cellulare.
3) L’alanina si forma nel muscolo
a) quando manca l’ossalacetato.
b) durante la sintesi proteica.
c) in condizioni di iperinsulinemia.
4) L’ipotesi chemiosmotica prevede che l’energia prodotta da reazioni redox
a) sia conservata come gradiente elettrochimico.
b) sia convertita in calore.
c) sia direttamente accoppiata a reazioni endoergoniche.
● Descrivere il meccanismo della fosforilazione ossidativa evidenziando le differenze con la fosforilazione
a livello del substrato.
5) L’iperespressione dell’enzima ATP-citrato liasi suggerisce
a) L’attivazione della glicolisi.
b) L’attivazione della sintesi proteica.
c) L’attivazione della biosintesi degli acidi grassi.
6) Quale delle seguenti affermazioni è scorretta?
a) I fosfolipidi sono carichi a pH fisiologico.
b) I fosfolipidi costituiscono un componente essenziale del citoplasma.
c) I fosfolipidi possono formare legami d’idrogeno.
7) In condizioni di scarso fabbisogno energetico il malato citosolico
a) è convertito in piruvato dall’enzima malico.
b) è convertito in ossalacetato dalla malato deidrogenasi citosolica.
c) è convertito in aspartato dall’aspartato ammino transferasi.
8) Il glicerolo 3-fosfato necessario alla biosintesi dei trigliceridi negli adipociti
a) è di origine esogena.
b) è prodotto dagli adipociti stessi dal glicerolo.
c) è sintetizzato dagli adipociti mediante la glicolisi
● Descrive il meccanismo e la regolazione della biosintesi dei trigliceridi negli adipociti.
9) La reazione di tiolisi è convolta
a) esclusivamente nel metabolismo dei corpi chetonici.
b) sia nella beta ossidazione che nel catabolismo periferico del beta-idrossibutirrato.
c) principalmente nella sintesi di acetil-CoA dagli acidi grassi.
10) Se una reazione cellulare ha G>0
a) avverrà grazie ad un processo di accoppiamento di reazioni.
b) avverrà sempre per idrolisi del legame fosfoanidridico di ATP.
c) costituisce di solito una tappa regolatoria.
● Quali sono le tappe regolatorie di un processo metabolico? Discutere l’argomento dal punto di vista
termodinamico.
11) Se un composto ha un elevato potenziale normale di riduzione avrà
a) una bassa affinità per gli elettroni.
b) un’elevata tendenza ad acquistare protoni.
c) un elevato potere riducente.
12) Quale tra i seguenti processi è una transaminazione?
a) glutammato glutammina.
b) glutammato alfa-chetoglutarato + NH3.
c) glutammato + ossalacetato aspartato + alfachetoglutarato.
● Descrivere la principali tappe del catabolismo ossidativo degli amminoacidi che preludono al ciclo
dell’urea.
13) Il colesterolo è una molecola anfipatica
a) per via della struttura policiclica.
b) grazie all’estesa metilazione della catena alifatica.
c) per la presenza di un gruppo ossidrilico.
14) Il numero di cicli di beta ossidazione necessari a degradare una molecola di C17:0 sono
a) 8
b) 9
c) 7
15) L’esochinasi e la glucochinasi
a) sono inibite dal glucosio 6-fosfato in modo diverso.
b) hanno stessa Km.
c) sono entrambi enzimi inducibili.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2013/2014
Biochimica, prova scritta del 27-10-2014
Nome:
Cognome:
Numero di matricola:
1) La chetogenesi può essere attivata adottando una dieta
a) povera di proteine e povera di grassi
b) ricca di grassi e ricca di carboidrati.
c) povera di carboidrati e ricca di grassi
● Motivare la risposta e discutere l’origine ed il destino dei corpi chetonici.
2) L’ossidazione mitocondriale di FADH2
a) genera un numero di molecole di ATP equivalente a quelle ottenute dall’ossidazione di NADH.
b) produce un gradiente protonico superiore rispetto a quello prodotto dall’ossidazione di NADH.
c) comporta la riduzione di fumarato a succinato.
3) La glutammina prodotta nel muscolo
a) viene degradata a glutammato ed ammoniaca.
b) genera ossalacetato.
c) è ottenuta mediante deamminazione ossidativa.
4) La lattato deidrogenasi
a) catalizza esclusivamente la trasformazione di lattato a piruvato.
b) catalizza esclusivamente la trasformazione di piruvato a lattato.
c) catalizza entrambe le reazioni citate prima.
● Qual è la principale funzione della lattato deidrogenasi in condizioni di anaerobiosi?
5) Esistono due isoforme della piruvato chinasi: PKM1, più attiva e PKM2, meno attiva. L’iper-espressione di
PKM2 induce
a) l’attivazione del metabolismo aerobico del glucosio.
b) un aumento della produzione di acido lattico.
c) l’iper-espressione di piruvato deidrogenasi.
6) Gli amminoacidi ramificati
a) sono degradati soprattutto a livello epatico.
b) sono amminoacidi apolari con catena laterale alifatica.
c) stabilizzano la struttura terziaria delle proteine mediante formazione di coppie ioniche.
7) Condizioni di scarso fabbisogno energetico attivano la produzione di
a) insulina.
b) glucagone.
c) adrenalina.
8) L’acetil-CoA
a) è una molecola ad alta energia.
b) contiene un legame fosfoanidritico.
c) è prodotto esclusivamente dal glucosio.
● Descrivere il destino dell’acetil-CoA in condizioni di alto e basso fabbisogno energetico.
9) Le vitamine
a) possono essere prodotte dall’organismo.
b) devono essere introdotte con la dieta.
c) inibiscono il catabolismo.
10) Il citrato
a) attiva la piruvato chinasi.
b) inibisce la fosfofruttochiansi 1.
c) attiva la fosfofruttochinasi 2.
● Descrivere i principali meccanismi di regolazione della prima fase della respirazione cellulare.
11) La beta-ossidazione degli acidi grassi
a) è inibita dal glucagone.
b) è inibita dal malonato.
c) è inibita dalla carnitina.
12) L’allenamento aerobico determina
a) la sottoespressione degli enzimi glicolitici.
b) l’aumento dell’espressione della glicogenosintasi.
c) l’inibizione della mitocondriogenesi
● Discutere il consumo dei substrati energetici durante un esercizio aerobico prolungato. Come varia il
consumo di tali substrati nelle diverse fasi dell’esercizio?
13) L’urea è ottenuta
a) mediante un processo esoergonico.
b) nel muscolo.
c) per attivazione dell’ammoniaca.
14) La produzione di ossalacetato dal malato prevede
a) il consumo di molecole ad alta energia.
b) una reazione di ossidazione.
c) l’ossidazione di NADH.
15) La costante di Michaelis-Menten corrisponde
a) alla velocità della reazione enzimatica.
b) alla concentrazione del substrato corrispondente a ½ Vmax.
c) all’energia di attivazione del processo.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2014/2015
Biochimica, prova scritta del 3-02-2015
Nome:
Cognome:
Numero di matricola:
1) Una proteina ricca di ponti disolfuro sarà maggiormente vulnerabile a
a) variazioni di T.
b) alterazioni del pH.
c) variazioni dei livelli di agenti riducenti.
2) Negli alveoli polmonari l’emoglobina
a) rilascia prevalentemente CO2.
b) rilascia prevalentemente ioni H+.
c) rilascia prevalentemente ferro.
● In cosa consiste il cosiddetto effetto Bohr?
3) L’anione bicarbonato (HCO3-) in seguito ad acidificazione
a) cede il protone generando il carbonato (CO32-).
b) tende a protonarsi.
c) diventa insolubile poiché perde la propria struttura terziaria.
4) Ogni ciclo di beta-ossidazione richiede
a) 2ATP+1NAD++1FAD
b) 1ATP+1NAD++1FAD
c) 2ATP + 1NAD+ + 1FAD + PPi
● Calcolare la resa energetica della beta-ossidazione delle tre catene di acido grassi che compongono il tri-butanoilglicerolo ipotizzando che la lisi dei legami esterei non abbia alcune effetto sulla produzione finale di ATP.
5) La sintesi di fruttosio 2,6-difosfato è regolata
a) da un unico enzima.
b) da due enzimi diversi.
c) dall’azione di proteasi.
6) L’acido aspartico a pH fisiologico
a) ha una carica positiva.
b) è neutro.
c) ha una carica negativa.
7) La reazione stechiometrica della gluconeogenesi è
a) 2Piruvato+4ATP+2GTP+2NADH+6H2O glucosio+4ADP+2GDP+2NAD++6Pi+2H+
b) 2Piruvato+2ATP+2GTP+2NADH+6H2O glucosio+4ADP+2GDP+2NAD++6Pi+2H+
c) 2Piruvato+4ATP+2NADH+6H2O glucosio+4ADP+2NAD++6Pi+2H+
●Descrivere brevemente il destino gluconeogenico dell’acido lattico e dell’alanina.
8) Un basso rapporto ATP/AMP
a) attiva la biosintesi degli acidi grassi.
b) attiva la glicolisi.
c) attiva l’anaplerosi.
9) L’allenamento aerobico
a)aumenta l’espressione della LDH nel muscolo.
b) aumenta l’espressione della glicerolo 3-fosfato deidrogenasi.
c) aumenta l’attività della glicogeno fosforilasi muscolare.
10) L’accumulo di lipidi nel tessuto adiposo
a) è indipendente dal glucosio.
b) non è condizionato dai livelli di glucagone.
c) prevede l’attivazione di trasportatori Glut4.
11) La sintesi di un legame fosfoestereo mediante idrolisi di ATP
a) produce circa 20 KJ/mol.
b) ha un G~0
c) richiede circa 30 KJ/mol.
Motivare la risposta e fare degli esempi che la avvalorino.
12) La seguente rappresentazione della membrana citoplasmatica non è corretta perchè
Spazio extracellulare
H
H
O
O
O
HO P O HO P O HO P O
H
R
R
R
R
R
R
O P OH O P OH O P OH
O
O
O
H
H
H
Citoplasma
a) le “teste polari” dovrebbero essere rivolte all’interno del doppio strato.
b) i gruppi R sono polari e si respingono.
c) non sono indicate le cariche negative dei gruppi fosfato.
●Descrivere la struttura, la composizione e la funzione della membrana cellulare evidenziandone le proprietà
chimiche ed elettriche.
13) La mioglobina
a) ha una struttura terziaria.
b) è una proteina fibrosa.
c) è un enzima.
14) La combustione alla fiamma del glucosio
a) richiede un’energia di attivazione.
b) produce ammoniaca.
c) non richiede ossigeno.
15) Le decarbossilazioni sono reazioni
a) reversibili.
b) di solito irreversibili.
c) cineticamente favorite.
Università degli Studi di Enna Kore
Facoltà di Scienze dell'Uomo e della Società.
CdL in “Scienze delle attività motorie e sportive”
AA 2014/2015
Biochimica, prova scritta del 25-02-2015
Nome:
Cognome:
Numero di matricola:
1) Rispondere al seguente quesito completando le possibili risposte aperte. L’acidità degli acidi carbossilici è riconducibile
a) alla …………………. indotta dall’ibridazione sp2 dell’atomo di carbonio.
b) alla …………...……dell’anione prodotto.
c) alla ridotta differenza di………………tra ossigeno e carbonio.
2) Negli organismi eucarioti la produzione di CO2
a) avviene nel mitocondrio.
b) può avvenire sia nel mitocondrio che nel citoplasma.
c) è fondamentalmente citosolica.
● Motivare la risposta commentando le diverse reazioni che portano alla formazione di CO2 nelle cellule
eucariotiche.
3) L’affinità della mioglobina per l’ossigeno
a) è inferiore rispetto a quella di Hb per O2.
b) non dipende da PO2.
c) può essere regolata dal pH.
4) Nella struttura primaria delle proteine le catene laterali degli AA
a) si dispongono dalla stessa parte rispetto al legame ammidico.
b) formano il legame ammidico.
c) sono disposte in modo da minimizzare l’ingombro sterico.
● Motivare la risposta e descrivere dettagliatamente le caratteristiche della struttura primaria delle proteine
discutendone in particolare la stabilità.
5) Sapendo che E°fumaratosuccinato= 0.030V e che E°FADFADH2=-0.220 si può prevedere che E° della conversione del
succinato in fumarato sarà pari a
a) + 0.250 V
b) + 0.190 V
c) circa 0 V
6) La membrana mitocondriale esterna
a) è sede della catena di trasporto degli elettroni.
b) è impermeabile al piruvato.
c) è caratterizzata dall’espressione di porine.
●Disegnare un mitocondrio indicandone univocamente i diversi compartimenti. Quali sono le principali evidenze
alla base della teoria che descrive le cellule eucariotiche come risultato di un processo di simbiosi?
7) Il glutammato viene convertito in
a) acetil-CoA per degradazione ossidativa.
b) glutammina per condensazione
c) in alfa-chetoglutarato per riduzione.
8) Il di-idrossiacetone fosfato può essere
a) ossidato a gliceraldeide 3-fosfato.
b) ridotto a glicerolo 3-fosfato.
c) isomerzzato a 2,3-difosfoglicerato.
●Discutere le diverse funzioni metaboliche del DHAP nelle cellule.
9) L’allenamento di resistenza aumenta la capacità del muscolo di
a) utilizzare carboidrati e grassi.
b) ricorrere al catabolismo anaerobico alattacido.
c) utilizzare il catabolismo anaerobico lattacido.
10) Le fibre veloci sono caratterizzate
a)da un elevato numero di mitocondri ed una bassa attività ATPasica.
b) da un elevato numero di mitocondri ed una elevata attività ATPasica.
c) da un basso numero di mitocondri ed elevata attività ATPasica.
11) Quale dei seguenti amminoacidi è presente nella struttura primaria delle proteine?
a) Arginina.
b) Ornitina.
c) Citrullina.
12) Elevati livelli di malonil-CoA
a) attivano la sintesi del colesterolo.
b) attivano il ciclo di Krebs.
c) attivano la biosintesi di acidi grassi.
Motivare la risposta avvalorando la risposta potenzialmente corretta e dimostrando che altre due sono
scorrette.
13) La rottura omolitica di un legame genera
a) un catione.
b) un radicale.
c) un anione.
14) Il legame dell’insulina al proprio recettore attiva
a) l’espressione del gene codificante Glut4.
b) la glicogeno fosforilasi.
c) la lipasi ormone-sensibile.
15) Gli ormoni steroidei sono
a) polari.
b) liposolubili.
c) proteici.