ESAMI DI STATO
ANNO SCOLASTICO 2013/2014
I.S.I.S. GIULIO NATTA - BERGAMO
L’URANIO
Il dualismo Progresso e Distruzione
TRUSSARDI SIMONE
CLASSE 5C LST
1
Indice:
Introduzione:
L’elemento
Gli isotopi
Gli impieghi principali
Processi di arricchimento dell’uranio
L’uranio impoverito
Le radiazioni e la radioattività:
Nozioni generali sulle radiazioni
Le radiazioni ionizzanti
Il decadimento e il tempo di dimezzamento
Decadimenti alfa, beta e gamma
La fissione nucleare:
La scoperta
Gli esperimenti di Enrico Fermi
La nascita del Progetto Manhattan
Gli esiti degli studi americani
Gli effetti delle prime bombe nucleari
Il reattore nucleare:
I primi prototipi
Le evoluzioni successive
I meccanismi di funzionamento
Le varie tipologie di reattore
L’acqua pesante
2
Introduzione
L'uranio è l'elemento più pesante presente in natura. Fu scoperto (ma non isolato come
metallo) nel 1789 da M.H. Klaproth in un campione di pechblenda della Sassonia: Peligot
isolò il metallo puro nel 1841, e nel 1896 A.H. Becquerel ne scoprì la radioattività.
L'importanza dell'uranio crebbe con la scoperta (1934-39, a opera di Fermi, Hahn e
Strassman, Joliot, Szilard, Anderson e altri scienziati dell’epoca) della fissione nucleare
con liberazione di energia (e liberazione di altri neutroni atti a mantenere una reazione
nucleare a catena) che subisce l'isotopo (naturale ma poco abbondante) 235U per
bombardamento con neutroni lenti.
L'uranio è un elemento notevolmente distribuito in natura, anche se abbastanza raro,
costituendo circa lo 0,0004% della crosta terrestre; è contenuto per circa 3·10-6 g/l nelle
acque marine. I suoi principali minerali primari (generalmente di colore scuro), nei quali
l'uranio si trova in stati di ossidazione prossimi a +4, sono gli ossidi anidri uraninite,
l'uraninite (detta anche pechblenda) e inoltre la carnotite, ma sono noti almeno altri
150 minerali uraniferi, con contenuti di uranio di potenziale rilevanza commerciale.
L'uranio puro è un metallo bianco lucido, ad alta densità, duttile e malleabile, poco più
tenero dell'acciaio e debolmente paramagnetico.
Chimicamente è un metallo molto reattivo: a temperatura ambiente, se è in massa si
ossida lentamente all'aria (assumendo colorazione bruna), mentre allo stato di fine
suddivisione è piroforico, si incendia cioè spontaneamente all’aria.
Si combina facilmente con l'idrogeno e con il fluoro anche a temperature vicine a quella
ambiente, mentre a temperature più elevate reagisce con gli altri alogeni, con il
fosforo, con l’azoto e con il carbonio e i suoi ossidi.
A temperature elevate è un forte riducente rispetto a molti ossidi e alogenuri. L'uranio
naturale (non arricchito in 235U) e i suoi composti non sono particolarmente pericolosi
per la salute.
Isotopi
Un isotopo è un atomo di uno stesso elemento chimico, e quindi con lo stesso numero
atomico Z, ma con differente numero di massa. La differenza dei numeri di massa è
dovuta ad un diverso numero di neutroni presenti nel nucleo dell'atomo.
L'uranio naturale è composto da una miscela di tre isotopi, 234U, 235U, e 238U, di cui 238U è
il più abbondante (99,3%), mentre il 234U costituisce una percentuale trascurabile del
totale.
3
Questi tre isotopi sono radioattivi; quello dotato di tempo di dimezzamento più lungo è
il 238U (emivita: 4,468 × 109 anni), seguono 235U (7,038 × 108 anni) e 234U
(2,455 × 105 anni).
L' 238U emette prevalentemente particelle alfa decadendo in 234Th. A sua volta, questo
decade beta, continuando la catena fino a giungere al 206Pb, stabile.
Impieghi
Gli isotopi dell'uranio vengono separati per aumentare la concentrazione di 235U rispetto
a 238U; questo processo è chiamato arricchimento. L'uranio si considera "arricchito"
quando la frazione di 235U è considerevolmente maggiore del livello naturale (circa lo
0,7204%), tipicamente su valori compresi tra il 3% ed il 7%. 235U è il tipico
materiale fissile per i reattori nucleari a fissione ed è utilizzabile per la produzione di
armi nucleari se sufficientemente puro.
L’ 238U nella reazione di fertilizzazione con un neutrone si trasforma in 239Pu, che a sua
volta può essere utilizzato come fissile o per scopi bellici, ciò avviene ad esempio nei
reattori nucleari dove i neutroni liberati dalla fissione di uranio 235 vengono in parte
catturati dai nuclei di uranio 238, che si trasforma così in uranio 239, soggetto a sua
volta a due rapidi decadimenti beta, trasformandosi prima in nettunio 239 e
successivamente in plutonio 239, quest'ultimo usato tipicamente nella fabbricazione di
ordigni nucleari, ma anche per la realizzazione di MOX, una miscela di uranio naturale
e plutonio usata come combustibile per particolari centrali nucleari.
La preparazione dei combustibili nucleari mediante arricchimento in 235U dei sali di
uranio ha reso disponibili a costi moderati discrete quantità di 238U che è solo
debolmente radioattivo e possiede una elevata densità (circa 19 g/cm 3), una discreta
lavorabilità meccanica e una elevata capacità schermante verso radiazioni tipo raggi X o
raggi γ. Mentre l'uranio puro è impiegato per schermi antiradiazioni e per contrappesi
dei dispositivi per il controllo aerodinamico nei missili, negli aerei e negli elicotteri, è
utilizzato per rendere le corazzature dei carri armati particolarmente resistenti e le
leghe con 0,75% di titanio o con 2% di molibdeno sono utilizzate nei proiettili penetranti.
Gli impieghi non nucleari dell'uranio sono piuttosto trascurabili: colorazione di vetri e
ceramiche, catalisi di talune reazioni chimiche, applicazioni in chimica analitica,
fotografia e medicina.
4
Arricchimento
Per ottenere un materiale fissile che sia adatto a scopi nucleari, cioè che emetta una
quantità sufficiente di neutroni, è necessario aumentare la concentrazione
dell'isotopo 235U rispetto al più comune e meno radioattivo 238U. La concentrazione
di 235U deve passare a valori superiori al 3% per i reattori nucleari ad acqua leggera LWR.
Il processo di concentrazione dell'uranio è un compito estremamente difficile: non è
possibile separarli per via chimica, essendo due isotopi dello stesso elemento, e l'unico
modo è sfruttare la piccolissima (meno dell'1,5%) differenza di peso.
Per fare questo si fa reagire l'uranio metallico con fluoro ottenendo esafluoruro di
uranio (UF6), un composto solido bianco, che sublima in fase gassosa al di sopra di
56,4 °C.
Questo composto in fase gassosa è usato nei due più comuni processi di arricchimento,
l'arricchimento per diffusione gassosa (utilizzata soprattutto negli Stati Uniti) e quello
per centrifuga a gas (principalmente utilizzato in Europa).
Esistono molte diverse tecniche usate per il processo di arricchimento, la più utilizzata
dagli scienziati agli inizi fu la diffusione gassosa: costringendo l'esafluoruro di
uranio gassoso a passare attraverso una serie di membrane. Questo produce una lieve
separazione tra le molecole che contengono 235U e 238U. Durante la Guerra Fredda, la
diffusione gassosa giocò un ruolo fondamentale come tecnica per l'arricchimento
dell'uranio, anche se attualmente è stata completamente sostituita con nuove
metodiche.
Il processo di separazione isotopica elettromagnetica (EMIS) consiste nella
vaporizzazione dell'uranio metallico e successivamente nella provocazione di una
ionizzazione che produca ioni carichi positivamente. Questi vengono quindi accelerati e
successivamente deflessi da campi magnetici sui loro rispettivi bersagli di collimazione.
Il processo di arricchimento dell'uranio tramite centrifuga a gas utilizza un gran numero
di cilindri rotanti in serie e formazioni parallele. Questa rotazione crea una forte
accelerazione centrifuga in modo che le molecole di gas più pesanti, contenenti 238U si
muovono verso l'esterno del cilindro e le molecole di gas più leggero, con maggiore
concentrazione di 235U si raccolgono presso il centro.
Per ottenere la stessa separazione isotopica si richiede molta meno energia rispetto al
vecchio metodo della diffusione gassosa, metodica che ha in gran parte soppiantato.
5
L'uranio impoverito
L'uranio impoverito è ottenuto come scarto del procedimento di arricchimento
dell'uranio. Il materiale risultante consiste principalmente in 238U, che ha una
minore attività specifica dell'uranio naturale.
Il termine è una traduzione dall'inglese depleted uranium, che a volte viene tradotto
gergalmente con il termine uranio depleto.
Il terzo isotopo naturale dell'uranio (234U), si concentra a sua volta nell'uranio arricchito
e si disperde nell'uranio impoverito.
Da 12 kg di uranio naturale si ottengono all'incirca 1 kg di uranio arricchito al 5% di
e 11 kg di uranio impoverito.
235
U
Quasi tutto (circa il 95%) l'uranio impoverito è conservato sotto forma di esafluoruro di
uranio (UF6), in cilindri stoccati all'aperto, per evitare il pericolo di accumulo di acido
fluoridrico in caso di incidenti.
Dopo l'uso in reattori, si ottiene il "combustibile esausto" che presenta
elevata radiotossicità e complesse problematiche di trattamento: il materiale può essere
soggetto a riprocessamento o allo smaltimento come scorie radioattive.
L'uranio impoverito può essere miscelato con il plutonio ottenuto dal riprocessamento
per la produzione di combustibile MOX, che ha un comportamento fisico simile a quello
del combustibile originario e può essere utilizzato assieme all'uranio.
La radioattività dell’uranio impoverito
La radioattività dell'uranio impoverito (DU) viene considerata "di basso livello"
confrontata con quella ad "alto livello" dell'uranio arricchito in uranio-235 (o di altri
materiali), perché l'uranio impoverito è costituito principalmente dall'isotopo uranio-238
(T1/2 = 4,5 Ga) dotato di emivita più lunga di quella dell'isotopo uranio-235 (T1/2 = 0,7038
Ga), nonostante entrambi siano prevalentemente emettitori di particelle alfa.
Infine, in questo contesto, il terzo isotopo uranio-234 (T1/2 = 0,2455 Ma), presente in
percentuale molto bassa nell'uranio naturale (0,0055%), si trova a sua volta
maggiormente concentrato nell'uranio-235 arricchito aumentandone ulteriormente
l'attività specifica e quindi la radiotossicità.
L'energia di una particella alfa è estremamente alta: essa, tuttavia, agisce solo a breve
distanza e non oltrepassa la pelle, e per questo motivo diventa il tipo più pericoloso di
contaminazione se la sorgente è contenuta nel corpo, e praticamente innocuo se questa
si trova all'esterno. Un foglio di alluminio o carta spesso 0,02 millimetri o la stessa
epidermide umana, può infatti fermare questo tipo di radiazione.
6
Gli isotopi di uranio decadono inoltre, seppure con piccola probabilità, mediante fissione
nucleare spontanea, nonché emissione di cluster di particelle e decadimento doppio
beta.
Tossicità dell’uranio impoverito
Uno studio effettuato da Diane Stearns, biochimico presso la Northern Arizona
University, ha stabilito che cellule animali esposte al sale di uranio solubile in acqua
(acetato di uranile, UO2(CH3COO)2) vanno soggette a mutazioni genetiche determinando
tumori e altre patologie, indipendentemente dalle sue proprietà radioattive.
L'esposizione sia a composti chimici di uranio impoverito sia di uranio naturale può, in
generale, indipendentemente dalle sue proprietà radioattive, causare danni
ai reni, pancreas, stomaco e intestino.
Le radiazioni
Col termine “radiazione” si definisce la particolare modalità con cui l’energia si propaga
da un punto all’altro dello spazio, in assenza di trasporto di quantità macroscopiche di
materia e senza il supporto di un substrato materiale.
Le radiazioni possono essere distinte in elettromagnetiche e corpuscolate: le prime sono
costituite da campi elettromagnetici oscillanti con una certa frequenza (onde
elettromagnetiche) che si propagano nel vuoto con velocità pari a quella della luce (3 x
108 m/s); le seconde sono costituite da particelle atomiche o subatomiche dotate di
elevata velocità (prossima a quella della luce nel caso di elettroni e positroni) e quindi
di elevata energia cinetica.
Le radiazioni sono classificate in ionizzanti o non ionizzanti (NIR) in base alla loro
capacità di produrre o meno la ionizzazione del mezzo attraversato.
Quando le radiazioni attraversano la materia, infatti, cedono ad essa, tutta o in parte,
l’energia che posseggono e possono produrre lungo il loro tragitto, se dotate di energia
sufficiente, alterazioni a livello atomico. E’ questo il primo evento (di tipo fisico) di una
lunga sequenza di reazioni secondarie (di tipo chimico) che, nella materia vivente,
possono dare luogo ad effetti biologici. In particolare, l’interazione iniziale delle
radiazioni con la materia dipende, sia quantitativamente che qualitativamente, dalla
natura, dalla massa, dalla carica e soprattutto dall’energia delle radiazioni considerate.
L’energia delle radiazioni, siano esse corpuscolate o elettromagnetiche, si misura in
elettronVolt (eV) dove un elettronvolt é l'energia che acquista una particella elementare
nell'attraversare una differenza di potenziale di 1 volt.
7
Le radiazioni con energia sino a 10 eV, poiché tale valore corrisponde all’energia di
legame degli elettroni più esterni degli atomi, non riescono a produrre ionizzazione e
dunque sono definite non ionizzanti (NIR).
Tutte le radiazioni di energia superiore a 10 eV, riescono invece ad indurre
modificazioni fisiche conseguenti alla deposizione di parte o tutta la loro energia, come
ad esempio fenomeni di ionizzazione e di eccitazione, e vengono definite radiazioni
ionizzanti (IR).
Radiazioni ionizzanti
I meccanismi con cui le radiazioni ionizzanti interagiscono a livello atomico con la
materia sono le eccitazioni e le ionizzazioni.
Nelle eccitazioni, l’energia ceduta è inferiore a quella necessaria ad espellere
dall’atomo uno dei suoi elettroni dell’orbitale più esterno (elettroni di valenza), la cui
energia di legame è dell’ordine di 10 eV. A causa dell’interazione di queste radiazioni a
bassa energia, l’atomo passa dallo stato fondamentale ad uno stato eccitato per
spostamento di orbitale di uno o più elettroni, sempre nell’ambito dello stesso atomo.
Nelle ionizzazioni l’energia ceduta dalle radiazioni supera quella del legame
dell’elettrone di valenza che viene quindi espulso dall’atomo di appartenenza. A seguito
di tale evento si crea una coppia di ioni: da una parte l’elettrone, o ione negativo, e
dall’altra l’atomo, che perdendo l’elettrone ed è divenuto uno ione positivo.
La radioattività
La radioattività venne scoperta da Becquerel alla fine dell’800. È un fenomeno naturale
per il quale isotopi instabili di alcuni elementi, per eccesso di protoni o neutroni,
emettono radiazioni denominate α, β e γ per stabilizzarsi.
Questo processo di stabilizzazione è il decadimento e può durare da pochi secondi a
milioni di anni. In natura quasi tutti gli elementi si sono stabilizzati nel corso della lunga
storia dell’universo.
Le radiazioni α sono particelle di Elio-4, con carica positiva e massa atomica 4; le
radiazioni β sono elettroni, dunque con carica negativa e le radiazioni gamma sono onde
elettromagnetiche ad altissima frequenza (superione ai raggi x).
Sono radioattivi elementi pesanti come l’Uranio, il Torio, il Radio e la maggior parte
degli elementi artificiali ottenuti in laboratorio.
8
Nei primi del ‘900 Rutherford prosegue le ricerche nel campo della radioattività e
ottiene la trasmutazione degli elementi: scoprì che bombardando nuclei di
azoto con particelle α otteneva nuclei di ossigeno e protoni liberi.
Il decadimento
Il decadimento radioattivo è un insieme di processi fisico-nucleari attraverso i quali
alcuni nuclei atomici instabili o radioattivi (radionuclidi) decadono (trasmutano), in un
certo lasso di tempo detto tempo di decadimento, in nuclei di energia inferiore
raggiungendo uno stato di maggiore stabilità con emissione di radiazioni.
Il processo continua più o meno velocemente nel tempo fintantoché gli elementi via via
prodotti, eventualmente a loro volta radioattivi, non raggiungono una condizione di
stabilità attraverso la cosiddetta catena di decadimento.
Storia
Nel 1896 Antoine Henri Becquerel, durante uno studio sulle relazioni intercorrenti tra
fosforescenza e Raggi X, scopre la radioattività naturale dell’uranio.
Gli esperimenti di Becquerel consistevano nell'esporre alla luce del sole una sostanza
fosforescente disposta su un involucro di carta opaco in cui vi era una lastra fotografica
destinata a rivelare l'emissione non luminosa della sostanza. La scelta cadde sul solfato
di uranio che sviluppava una fosforescenza molto viva. Gli esperimenti mostravano che
la lastra fotografica veniva impressionata dopo una debita illuminazione, il che
confermava l'ipotesi di Becquerel.
Ben presto però Becquerel osservò un fenomeno del tutto nuovo e inatteso: si accorse
che la lastra veniva impressionata anche al buio. Becquerel ipotizzò che la sostanza
continuasse a emettere radiazioni derivate dall'illuminazione anche dopo la fine
dell'esposizione ai raggi solari.
Dopo ripetuti esperimenti con materiali diversi, si verificò che le radiazioni non
dipendevano dalla caratteristica della fosforescenza della sostanza ma dal materiale:
l'uranio.
9
Emivita
Come molti processi quantistici, anche il decadimento è descritto da leggi statistiche: la
percentuale di atomi che, in un certo intervallo di tempo, subisce il decadimento, è una
costante.
Per dare un'unità di misura standard, si indica solitamente il tempo in cui metà
degli atomi di un certo isotopo di un elemento decadono. Tale periodo prende il nome
di emivita dell'isotopo. Esistono isotopi con emivita brevissima, poche frazioni di
secondo, ed altri con emivita di migliaia di anni.
Nella maggior parte dei casi, gli isotopi instabili subiscono decadimenti dei vari tipi in
successione, e pertanto si parla di catena di decadimento di un isotopo, intendendo la
sequenza di decadimenti che tale atomo percorre.
Quasi tutte le catene di decadimento finiscono con un isotopo del piombo (che è
stabile).
Tipi di decadimento
In seguito agli studi di Ernest Rutherford, i decadimenti nucleari sono stati raggruppati
in tre classi principali:
decadimento alfa
decadimento beta
decadimento gamma
Mentre il decadimento alfa e il decadimento beta cambiano il numero di protoni nel
nucleo e quindi il numero di elettroni che vi orbitano attorno (cambiando così la natura
chimica dell'atomo stesso), il decadimento gamma avviene fra stati eccitati dello stesso
nucleo e comporta solo la perdita di energia.
Il decadimento alfa avviene in accordo con la legge di conservazione della
massa/energia con l'emissione di una particella, detta appuntoparticella alfa, composta
da due protoni e due neutroni (nucleo di elio) da parte dell'isotopo di un elemento con
elevato numero atomico(Z>83).
10
Il decadimento beta può avvenire in due modi:
un neutrone decade (trasmuta) in una coppia protone-elettrone più un antineutrino
(spin opposto al neutrino) elettronico (decadimento beta meno). Il protone resta
nel nucleo atomico, mentre le altre due particelle vengono espulse (emesse).
un protone decade (trasmuta) in una coppia neutrone-positrone più un neutrino
(massa piccolissima e carica elettrica zero) elettronico (decadimento beta più).
Questo tipo di decadimento può avvenire solo o dentro ad alcuni nuclei oppure,
molto di rado, libero e solo in presenza di sufficiente energia avendo il protone una
massa inferiore a quella del neutrone: dai dati sperimentali risulta che il protone è
una particella stabile e quindi spontaneamente non decade.
La scoperta della fissione
La prima fissione nucleare artificiale (cioè provocata dall'uomo) avvenne nel 1932 ad
opera di Ernest Walton e John Cockcroft, che accelerando protoni contro un atomo
di Litio-7 riuscirono a dividere il suo nucleo in due particelle alfa(cioè due nuclei
di Elio); il fenomeno era noto come splitting the atom.
Il 22 ottobre 1934 la prima fissione nucleare artificiale di un atomo di Uranio fu
realizzata dal gruppo di fisici italiani guidati da Enrico Fermi (i cosiddetti "ragazzi di via
Panisperna"), il gruppo di fisici italiani però non si accorse di ciò che era avvenuto ma
ritenne invece di aver prodotto dei nuovi elementi transuranici.
Alla fine del dicembre 1938, esattamente nella notte tra il 17 e il 18, due chimici
nucleari tedeschi, Otto Hahn e il suo giovane assistente Fritz Strassmann, furono i primi
a dimostrare sperimentalmente che un nucleo di uranio 235, qualora assorba un
neutrone, può dividersi in due o più frammenti dando luogo così alla fissione del nucleo
(fu la chimica Ida Noddack ad ipotizzare per prima la fissione nel 1934, mentre i
fondamenti teorici si devono a Otto Frisch e a sua zia Lise Meitner).
A questo punto per i chimici e fisici iniziò a prendere forma l'idea che si potesse
utilizzare questo processo, costruendo dei reattori che contenessero la reazione, per
produrre energia o degli ordigni nucleari.
11
Gli esperimenti di Fermi del 1934
Nel 1934 Irene Curie mostra di aver ottenuto radioattività artificiale bombardando
diversi elementi con particelle α, tuttavia questi esperimenti risultano difficoltosi
perché le particelle α avendo carica positiva devono superare la repulsione
elettrostatica del nucleo.
È in questo momento che Enrico Fermi intuisce che può rendere più produttivo il
processo usando come “proiettili” neutroni liberi che aggirano facilmente la repulsione
elettrostatica essendo privi di carica.
In breve Fermi e il suo gruppo a Roma, in via Panisperna, ottengono diversi radioisotopi
artificiali, compresi isotopi con numero atomico > 90 bombardando atomi di uranio.
Una delle scoperte fondamentali di Fermi in via Panisperna sono i neutroni lenti: egli
scoprì che per urti successivi con nuclei di idrogeno (acqua, paraffina) i neutroni
rallentano e in questo stato (neuroni lenti) rendono il processo di bombardamento fino a
100 volte più efficace, sicuro e stabile; la scoperta di Fermi fu importantissima poiché
rese più produttivi e sistematici (e quindi più “scientifici”) gli studi sulla radioattività
artificiale e, in seguito, sulla fissione.
Le ricerche di Fermi dunque furono fondamentali per lo sviluppo della nascente fisica
nucleare.
La lettera di Einstein a Roosvelt
Nell’ambito della comunità scientifica la possibilità di arrivare alla costruzione dell’arma
nucleare si diffonde già a partire dalla scoperta di Hahn e Strassmann.
Il mondo già nell’autunno del 1938 è in attesa di una nuova devastante guerra, dalla
Germania giungono notizie allarmanti, tutti gli scienziati di origine ebraica sono fuggiti,
privando il paese di un patrimonio scientifico straordinario.
In America la maggior parte della popolazione è isolazionista e non vuole l’intervento
degli StatiUniti in un’eventuale nuova guerra.
Tuttavia i grandi fisici Szilard e Teller, a conoscenza del possibile sviluppo bellico della
fissione, informano Einstein e gli spiegano la situazione, convincendolo a contattare il
presidente Roosevelt (Einstein era il fisico più autorevole negli Stati Uniti).
Nell’agosto del 1939 Einstein e Szilard inviano una lettera a Roosevelt.
12
Il progetto Manhattan
Solo nel 1941, dopo l’attacco giapponese a Pearl Harbour e dopo l’ingresso degli Stati
Uniti in guerra, Roosevelt crea un “comitato per l’incremento della ricerca” dopo che
i servizi segreti inglesi confermano che la Germania sta lavorando alla bomba
(nonostante la fuga di cervelli dovuta alle persecuzioni razziali la Germania disponeva di
un gruppo di fisici e scienziati di primissimo livello, primo fra tutti Heisenberg che
dirigerà le ricerche nucleari tedesche). Circa 12 università si attivano nella ricerca sul
nucleare e nel 1942 Fermi realizza il primo reattore nucleare a fissione (la pila di
Fermi).
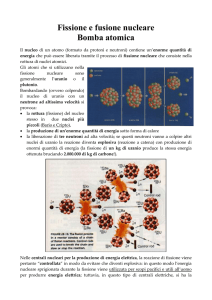
Ebbe così chiaro che sarebbe stato possibile generare una reazione a catena in grado di
produrre energia su scala macroscopica. Infatti la fissione oltre a produrre energia e a
spezzare il nucleo genera alcuni neutroni liberi e, con un’adeguata composizione della
massa di Uranio e con un adatto controllo dei neutroni emessi nella fissione,è possibile
ottenere una reazione auto sostenuta nella quale i nuovi neutroni causano nuove
reazioni e così via.
Se la massa di materiale fissile è insufficiente la reazione presto si esaurisce; se la massa
è sufficiente (critica) la reazione prosegue e in questo caso se è lasciata libera le
reazioni aumentano esponenzialmente e si produce in pochissimo tempo un’enorme
quantità di energia (la bomba), se il processo è moderato con degli ostacoli che
bloccano parzialmente la diffusione dei neutroni la reazione si mantiene stabile,
duratura e controllabile e produce energia in modo stabile e continuo.
La struttura che Fermi realizza per creare la fissione controllata (la pila di Fermi) era
costituita da un cubo di grafite (moderatore), barre di uranio (materiale fissile) e barre
di controllo, con la funzione di assorbire i neutroni in eccesso. La pila fu la prova
inconfutabile della possibilità di sfruttare l’energia derivata dalla fissione per produrre
energia creando una reazione a catena.
A questo punto Roosevelt approva la costruzione di installazioni industriali per
l’estrazione massiccia si U235, elemento base della fissione. I migliori fisici e scienziati
presenti negli Stati Uniti vengono riuniti in un centro di ricerca sul nucleare costruito ex
novo in pochi mesi a Los Alamos, una zona desertica del New Mexico; tutto questo
dispiegamento di forze (e denaro per 400 milioni di $) venne chiamato “Progetto
Manhattan” ed era esplicitamente finalizzato allo sviluppo atomico per fini bellici.
Il Progetto Manhattan mette in moto una macchina produttiva e di ricerca che non ha
precedenti nella realizzazione di un singolo manufatto e che trasformerà profondamente
il rapporto tra militari, industria e mondo della ricerca scientifica.
Qui i migliori geni possono lavorare a stretto contatto e isolati dal mondo, questo
permise di dimezzare i tempi della ricerca. La direzione del centro fu affidata a Julius
Oppenheimer.
13
I fisici del progetto andarono incontro a numerosi problemi, primo fra tutti quello di
stimare accuratamente la cosiddetta massa critica, cioè la quantità minima di materiale
fissile necessaria per innescare una reazione a catena di tipo esplosivo: infatti, la
potenza dell'esplosione dipendeva dalla rapidità con cui si verificava l'assemblaggio del
materiale fissile fino al raggiungimento della massa critica.
Un primo sistema su cui si iniziò a lavorare consisteva nello sparare con la velocità di un
proiettile di artiglieria una piccola quantità di materiale fissile all'interno di una massa
dello stesso materiale al di sotto del valore critico, in modo che le due masse, così
assemblate, superassero la massa critica con una rapidità sufficiente ad innescare una
reazione a catena divergente, ottenendo l'esplosione.
I risultati degli studi: Trinity test e il giappone
Il primo ordigno nucleare della storia venne fatto detonare nel deserto di Alamogordo,
New Mexico, 300 chilometri a sud del sito sperimentale di Los Alamos, teatro dello
sviluppo principale del progetto.
Il sito venne scelto perché la rarefatta atmosfera del deserto avrebbe reso osservabile
l’esplosione anche al di là della distanza di sicurezza. La bomba al Plutonio venne
piazzata in cima ad un traliccio, collegata ad un dispositivo che l’avrebbe fatta
esplodere a distanza.
La problematica industriale fu incentrata sulla produzione di una quantità sufficiente di
materiale fissile con adeguata purezza. Il progetto seguì due strade parallele, che
portarono alla produzione di due bombe diverse.
La prima, Little Boy, sganciata su Hiroshima, era composta da uranio-235, un isotopo
minore dell'uranio che fu separato fisicamente dal più prevalente uranio-238, non adatto
all'uso in una bomba.
La separazione venne effettuata principalmente per diffusione gassosa dell'esafluoruro
di uranio (UF6), ma anche con altre tecniche. Il grosso di questo lavoro di separazione fu
svolto all'Oak Ridge National Laboratory.
La bomba sganciata su Nagasaki, Fat Man, invece, era costituita principalmente di
plutonio-239, un elemento sintetico che diventa critico solo tramite implosione.
Venne ideato un metodo a implosione: inizialmente le masse di uranio o plutonio
vengono tenute separate in un nocciolo sferico perfettamente simmetrico costituito
da strati di materiale fissile e strati isolanti, quando delle cariche esplosive che
circondano il nocciolo vengono fatte saltare, l’onda d’urto concentrica produce
l’implosione simmetrica del nocciolo che raggiunge la massa super critica
istantaneamente e la reazione si attiva incontrollata.
14
Così il 6 agosto 1945 la bomba “Little Boy” all’U235 venne sganciata su Hiroshima,
popolosa città del Giappone meridionale; 70000 persone morirono all’istante,
carbonizzate dalle altissime temperature.
Il 9 agosto un’altra bomba, “Fat Boy” al Plutonio venne sganciata sulla città di Nagasaki;
qui il bilancio fu di75000 morti. Pochi giorni dopo il Giappone accettò la resa
incondizionata.
La maggior parte degli scienziati di Los Alamos rimase scioccata a traumatizzata dal
prodotto e dall’impiego del loro lavoro, Einstein in particolare rimase colpito dalla
vicenda e negli anni successivi fu un profondamente ostile a tutte le ricerche che
vennero (immediatamente) avviate per lo sviluppo ulteriore delle armi nucleari.
In particolare dopo la creazione e il test della bomba-H, Einstein redisse in
collaborazione con Bertrand Russell il “Manifesto Einstein-Russell”. Qui in poche parole
si afferma che, giunti all’attuale progresso, le armi hanno raggiunto una potenza tale
che una qualsiasi guerra combattuta con le armi nucleari potrebbe essere fatale per
l’intera civiltà umana.
Il reattore nucleare
In ingegneria nucleare un reattore nucleare a fissione è un sistema complesso in grado di
gestire una reazione nucleare a fissione a catena in maniera controllata (diversamente
da quanto accade invece per una ordigno nucleare) ed utilizzato come componente base
nelle centrali nucleari le quali possono contenere anche più reattori nucleari nello stesso
sito.
Esistono reattori nucleari sperimentali di ricerca, nei quali l'energia prodotta è
trascurabile, e reattori di potenza utilizzati dalle centrali nucleari nei quali l'energia
termica prodotta dal reattore viene usata per vaporizzare dell'acqua, la cui energia
viene convertita prima in energia meccanica attraverso l'uso di turbine ed infine
in energia elettrica dagli alternatori.
Storia e primi sviluppi
Volendo essere precisi, i primi 16 reattori a fissione nucleare naturale divennero critici
(cioè "accesi"), circa 1,7 miliardi di anni fa. In Gabon, nell’Africa centrale, furono trovati
minerali di uranio con una concentrazione anormalmente bassa di 235U; il fenomeno è
stato spiegato, anche grazie al ritrovamento di prodotti di fissione, con la presenza
naturale di concentrazioni di 235U intorno al 3%, disposte in modo da costituire
una massa critica e con la presenza di acqua liquida.
15
Storicamente invece il primo reattore nucleare di costruzione umana fu quello
sperimentale-dimostrativo realizzato dall'équipe di Enrico Fermi a Chicago, nel reattore
CP-1 (Chicago Pile-1), in cui si ottenne la prima reazione a catena controllata ed
autosostenuta il 2 dicembre 1942. Quasi contemporaneamente venivano allestiti ad Oak
Ridgel'impianto pilota l'X-10 (critico nel 1943) nell'ambito del laboratorio MetLab e
a Hanford il B-reactor (critico nel settembre 1944), ambedue finalizzati alla produzione
di plutonio, il primo come unità pilota ed il secondo per la produzione in grande scala.
Nel dicembre 1954 il reattore di Obninsk, URSS divenne critico, e fu il primo reattore
nucleare per uso civile; esso produceva solo 5 MW elettrici, ma fu comunque un
precursore. Come i successori della filiera sovietica, era un reattore del tipo acquagrafite, in cui il raffreddamento del nocciolo veniva assicurato da acqua leggera e la
moderazione dei neutroni da blocchi di grafite, ottimo conduttore del calore oltre che
efficace moderatore del flusso neutronico.
In Italia, il primo reattore nucleare, chiamato Avogadro RS-1 fu costruito a Saluggia, in
provincia di Vercelli, nel 1959 da un gruppo di aziende private, di cui la Fiat era
capofila, comprendente anche la Montecatini; era un reattore di ricerca di tipo a
piscina, fu utilizzato principalmente per scopi sperimentali e non venne mai connesso
alla rete elettrica nazionale, il suo funzionamento venne arrestato nel 1971 e quindi
trasformato in deposito per elementi di combustibile nucleare irraggiato.
La prima centrale Italiana per la produzione di elettricità (sempre del tipo gas-grafite
GEC-Magnox, acquistata dall'Inghilterra) fu quella di Latina, critica il 27 dicembre 1962 e
che produceva 153 MWe (megawatt elettrici), seguita da quella del Garigliano (1963),
del tipo BWR General Electric da 150 MWe e da quella di Trino Vercellese (1964), del
tipo PWR Westinghouse, da 260 MWe.
L'IAEA al 31 dicembre 2009 elencava nel mondo 443 reattori nucleari a fissione in attività
e 56 in costruzione destinati alla produzione di energia, soprattutto in oriente (Cina,
India, Russia, Korea), mentre altri 142 sono pianificati e 327 proposti.
Meccanismo di un reattore
La sorgente di energia del reattore è dunque il combustibile presente nel nocciolo o
nucleo del reattore, composto da materiale fissile (tipicamente una miscela di 235U
e 238U), arricchita fino al 5% in 235U. È poi possibile utilizzare il combustibile MOX che è
una miscela di ossidi di uranio e plutonio, oppure uranio naturale. Per il secondo
combustibile si devono operare modifiche nel reattore, mentre per l'uranio naturale si
devono utilizzare reattori che utilizzano come moderatore acqua pesante o grafite.
16
Per rallentare i neutroni e termalizzarli, cioè rallentarli fino ad un'energia cinetica
inferiore all'eV ed aumentare così la probabilità di fissionare il combustibile, secondo la
fisica stessa della reazione, è necessario utilizzare un moderatore.
La fissione del nucleo del combustibile genera energia, principalmente sotto forma
di energia cinetica dei frammenti della fissione e di raggi gamma. I frammenti di fissione
rallentando nel combustibile generano calore che viene asportato da un fluido
refrigerante termovettore (gassoso o liquido, o che subisce un cambio di fase nel
processo) che lo trasporta ad un utilizzatore, direttamente o indirettamente per mezzo
di generatori di vapore, quasi sempre un gruppo turbo-alternatore per la produzione
di energia elettrica nella parte termoelettrica della centrale nucleare.
Il termovettore refrigerante può anche essere il moderatore stesso, come avviene nel
caso dei reattori ad acqua leggera.
Il reattore raggiunge la cosiddetta condizione di criticità ovvero possiede una massa
critica tale che la reazione di fissione a catena possa autosostenersi in maniera stabile.
Il reattore dispone anche delle cosiddette barre di controllo cioè barre metalliche (in
genere leghe di argento, cadmio e indio o carburi di boro) atte ad assorbire i neutroni in
eccesso liberati dalla reazione che a loro volta alimentano; possono essere inserite nel
nocciolo e servono a modulare in funzione della potenza energetica da generare, a
tenere sotto controllo ed eventualmente arrestare la reazione a catena di fissione in
caso di criticità.
Questo evita ad esempio che la reazione diventi incontrollata con la liberazione di
enormi quantitativi di energia che possano condurre alla cosiddetta fusione del
nocciolo (parziale o totale) per temperature elevatissime, al successivo cedimento dei
vari strati di contenimento del reattore incapaci di resistere a tali livelli di temperatura
con dispersione nell'ambiente del materiale radioattivo, e/o alla produzione di gas
esplosivi come l'idrogeno con conseguente possibile esplosione del reattore stesso e
gravissime conseguenze sulla sicurezza pubblica per diffusione diretta di grandi quantità
di materiale altamente radioattivo e livelli di radiazione altrettanto nocivi.
Spesso anche a reattore arrestato deve continuare l'afflusso del fluido termovettore
refrigerante per abbassare la temperatura del reattore e continuare a dissipare il calore
residuo prodotto dalla radioattività del materiale combustibile evitando ancora una
volta i problemi di surriscaldamento.
Il consumo progressivo del combustibile nucleare nel nocciolo comporta la formazione di
materiale di scarto detto anche residuo o prodotto di fissione non più utile alla fissione
stessa e a sua volta radioattivo (le ben note scorie nucleari) e che quindi deve essere in
qualche modo periodicamente rimosso dal reattore e successivamente smaltito.
17
Tipologie di reattore
Reattori di Ia e IIa generazione
I reattori cosiddetti "provati" sono quelli di cui è stata verificata la stabilità operativa
per usi civili commerciali. Oggi sono conosciuti vari tipi di reattore nucleare,
generalmente classificati in base al tipo di combustibile utilizzato, al sistema di
raffreddamento/generazione vapore e al tipo di moderatore.
I primi modelli, come si è visto, a partire dal CP-1, erano del tipo gas-grafite, poi
commercialmente sviluppato in varie versioni : Magnox ,GEC e RBMK ( il reattore del
disastro di Chernobyl ). Ambedue usavano uranio arricchito come combustibile.
Il grande vantaggio dei modelli a gas è nella possibilità di utilizzare fluidi inerti come
fluido refrigerante, evitando così i problemi di corrosione propri dell'acqua ad alta
temperatura (che inoltre, quando irradiata, si scinde parzialmente nei componenti,
generando pericoloso idrogeno nonché ossigeno libero che aggrava ulteriormente i
problemi di corrosione) e nella bassa densità del refrigerante che non assorbe quindi
neutroni in maniera significativa.
Il problema maggiore, viceversa, sta nel relativamente basso coefficiente di scambio
termico del gas, e nell'impossibilità di ottenere la moderazione dei neutroni attraverso il
fluido stesso, obbligando quindi all'utilizzazione di costose (e instabili, a temperature
elevate) strutture in grafite o all'utilizzo dell'acqua.
Si sono quindi affermati i modelli raffreddati (e moderati) ad acqua, che
sostanzialmente sono delle caldaie in cui il focolare è sostituito dall'insieme degli
elementi di combustibile.
Di questi esistono due modelli: quelli in cui la vaporizzazione dell'acqua avviene a
contatto degli elementi di combustibile, o comunque nello stesso recipiente che le
contiene, detti di tipo BWR (Boiling Water Reactor) , che quindi inviano in turbina un
vapore più o meno debolmente radioattivo, e quelli che utilizzano un circuito
intermedio, per cui un fluido refrigerante (di solito ancora acqua) entra a contatto del
combustibile, si scalda e, senza cambiare di fase, circola in un generatore di vapore
esterno in cui cede calore ad altra acqua, che stavolta vaporizza e genera energia
elettrica nel gruppo turbina-alternatore. Sono detti PWR (Pressurized Water Reactor).
Il vapore che arriva in turbina in condizioni di normale funzionamento non è più
radioattivo.
18
Reattori di IIIa generazione
I reattori cosiddetti di "3° generazione" sono versioni migliorate dei reattori di 2°
generazione, di cui riprendono le caratteristiche fondamentali. Non apportano quindi
sostanziali differenze concettuali di funzionamento nè riguardo ai fluidi refrigeranti nè
al "combustibile" (se non la possibilità di arrivare a tassi di bruciamento più elevati) e
pertanto non si hanno miglioramenti sostanziali per quanto riguarda le scorie prodotte.
Prevedono però un approccio diverso alla filosofia di progettazione, includendo gli
incidenti severi negli incidenti base di progetto. Ciò ha portato all'implementazione di
ulteriori salvaguardie ingegneristiche (core catcher, sistemi di refrigerazione passivi,
ecc.) che dovrebbero rendere queste nuove tipologie di impianto in grado di evitare
contaminazioni esterne in caso di incidente.
Reattori di IVa generazione
I reattori nucleari di IV generazione sono un gruppo di progetti per nuove tipologie di
reattore nucleare a fissione che, pur essendo da decenni allo studio, non si sono ancora
concretizzati in impianti utilizzabili diffusamente in sicurezza.
Alcuni ritengono che saranno disponibili commercialmente fra alcune decine di anni
(2030-2040).
A differenza dei reattori di 2ª generazione (la stragrande maggioranza di quelli
attualmente in funzione) e 3ª generazione (attualmente proposti sul mercato e realizzati
o ordinati), quelli di 4ª generazione dovrebbero introdurre marcate differenze
soprattutto nei materiali impiegati, pur continuando ad usare come "combustibile"
principalmente uranio e plutonio.
Gli obiettivi primari di chi lavora allo sviluppo dei nuovi reattori sono quelli di migliorare
la sicurezza nucleare, ridurre la produzione di scorie nucleari, sottrarsi alla
proliferazione nucleare (uso militare), minimizzare gli sprechi e l'utilizzo di risorse
naturali, e di diminuire i costi di costruzione e di esercizio di tali impianti.
19
Caratteristiche dei reattori più diffusi
Reattori nucleari a gas (GCR)
Sono moderati ad anidride carbonica-grafite.
I GCR, ormai in disuso, erano in grado di usare l'uranio naturale come combustibile,
permettendo così alle nazioni che li avevano sviluppati di produrre uranio arricchito per
fabbricare plutonio e armi nucleari, senza dover dipendere dalle importazioni di altri
paesi di cui, al tempo, gli unici fornitori erano solo Stati Uniti e Unione Sovietica.
L'evoluzione inglese di questa tipologia fu l'AGR, acronimo per advanced gas-cooled
reactor (reattore avanzato raffreddato a gas) è un tipo di reattore nucleare sviluppato
dalla Gran Bretagna di seconda generazione.
Filiera RBMK
Sono reattori moderati ad acqua leggera-grafite.
Il moderatore è sia la grafite che l'acqua, che fa anche da termovettore. Questa
caratteristica dà al reattore un pericoloso coefficiente di vuoto positivo che generano
forti escursioni di potenza, soprattutto alle basse potenze. La filiera è stata costruita
solamente in paesi ex-URSS; l'incidente di Chernobyl ha coinvolto un reattore di questo
tipo.
Filiera BWR
Sono reattori ad acqua leggera bollente.
In questi reattori l'acqua nel vessel cambia stato ed è sia moderatore che termovettore,
passando da liquido a vapore, con un titolo medio in uscita dal nocciolo del reattore di
circa il 15%. Il vapore prodotto è inviato direttamente alla turbina per la generazione
elettrica, questo consente di avere un rendimento termodinamico leggermente
superiore rispetto alla filiera PWR.
Filiera PWR
Sono reattori ad acqua leggera in pressione.
In questi reattori l'acqua nel vessel viene mantenuta allo stato liquido aumentandone di
molto la pressione. L'acqua è sia moderatore che termovettore, per la generazione
elettrica si passa però per degli scambiatori di calore, chiamati generatori di vapore.
Essendoci quindi uno scambiatore termico fra la fonte di calore e la turbina,
il rendimento termodinamico è leggermente inferiore rispetto alla filiera BWR.
20
Filiera HBWR
Per i reattori ad acqua pesante della classe BWR si segnala il grave problema
dell'instabilità, per il loro coefficiente positivo temperatura-potenza. Attualmente non
esistono modelli in funzione.
Filiera PHWR
Un tipo di reattore PWR di seconda generazione moderato ad acqua pesante.
Acqua pesante
L'acqua pesante (D2O) è semplicemente acqua che ha il Deuterio al posto dell'idrogeno.
La sostituzione isotopica con deuterio altera l'energia di legame del legame idrogenoossigeno dell'acqua, alterando le caratteristiche fisiche, chimiche e, soprattutto, le
proprietà biologiche. L'acqua pesante pura non è radioattiva ed è circa l'11% più densa
dell'acqua.
Con la scoperta della fissione nucleare alla fine del 1938, e la necessità di
un moderatore di neutroni che catturasse pochi neutroni, l'acqua pesante è diventata
una componente importante dei primi programmi di energia nucleare durante la seconda
guerra mondiale (1939-1945).
Da allora, l'acqua pesante è un componente essenziale nella progettazione di alcuni
reattori nucleari, sia per la produzione di energia elettrica che per la produzione di
isotopi nucleari, come ilplutonio-239. La maggior parte dei reattori nucleari
contemporanei funzionanti con uranio arricchito fanno uso di normale "acqua leggera"
(H2O) per la moderazione dei neutroni.
L'acqua pesante, D2O, si trova naturalmente mescolata all'acqua normale in quantità di
circa 1 parte su 20 milioni di molecole di acqua normale.
Si ottiene in genere separandola per distillazione dall'acqua demineralizzata; data la
piccola differenza di temperatura di ebollizione rispetto all'acqua leggera, il processo è
piuttosto lungo e richiede colonne di distillazione molto alte (cioè con molti "piatti
equivalenti") e rapporto di riflusso elevato.
21
Fonti, bibliografia e sitografia:
http://www.sermig.org/armi-nucleari
http://www.eniscuola.net/
http://www.sapere.it/
http://fisica.cattolica.info/
http://it.wikipedia.org/
http://www.fisicamente.net/
http://www.enel.com/
http://ebook.scuola.zanichelli.it/
http://scienzapertutti.lnf.infn.it/
G. De Luna, M. Meriggi, G. Albertoni, “La storia al presente 3”, Paravia, 2008
James Walker, “Corso di fisica, volume 3”, Linx, 2010
James E. Brady, Fred Senese, “Chimica, la materia e le sue trasformazioni”, Zanichelli,
2008
22
Conclusioni
L’argomento dell’uranio è sempre stato di mio personale interesse durante tutto il
percorso scolastico fin dalle scuole medie.
In particolare, come si può notare nel sottotitolo del lavoro, i suoi diversi aspetti e i
molteplici utilizzi per cui può essere sfruttato hanno sempre destato stupore per la loro
varietà.
Può essere usato per produrre energia elettrica senza sfruttare altre fonti di energia più
comuni, ma attualmente in via di esaurimento; tuttavia gli effetti catastrofici a cui un
utilizzo improprio o una cattiva progettazione possono portare scoraggiano la ricerca e
lo sviluppo di questa fonte energetica.
Inoltre c’è l’elemento non di poco conto delle armi di distruzione di massa con
meccanismo nucleare, un elemento ben peggiore degli incidenti nelle centrali.
Ecco, ciò che mi ha sempre affascinato di questo elemento è il suo duplice
funzionamento: migliorare la vita, ma anche poterla distruggere in solo attimo.
23