Le disfunzioni dell’area sacrale nella patologia neurologica
Catania, 11 -12 giugno 2013
Hotel Excelsior
Interazioni brain-gut axis: nuove prospettive
Dott. Simone Vigneri
Dipartimento di Biomedicina sperimentale e Neuroscienze Cliniche (Bio.Ne.C.) - Università di Palermo
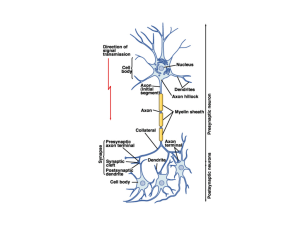
• Brain-gut axis: complesso apparato che regola le interazioni e le reciproche influenze tra il
sistema nervoso e l’intestino. Si articola in vari livelli attraverso un sistema di recettori,
fibre afferenti, centri di intergrazione, fibre efferenti ed effettori, e si avvale di multipli
messaggeri appartenenti
al sistema nervoso,
immunitario
e ormonale. Il suo
coinvolgimento è implicato nella fisiopatologia di numerose patologie funzionali.
Central autonomic network (CAN)
Central autonomic network (CAN)
• Nel 1993 Benarroch identificò l’ insula (IC)
come la corteccia viscerale sensitiva primaria
e la corteccia cingolata anteriore (ACC) come
importante area viscerale motoria coinvolta
nell’ avvio e nella modulazione dell’ output
autonomico in risposta a dolore. L’ amigdala
avvia risposte endocrine, autonomiche e
motorie successive alle emozioni;
• L’ ipotalamo, (zona paraventricolare, mediale
e
laterale)
possiede
invece
un
ruolo
fondamentale nel controllo neuroendocrino,
dell’omeostasi, nelle risposte comportamentali
e nelle efferenze al tronco encefalo;
American Academy of Neurology (AAN), 2007
Central autonomic network (CAN)
• Il grigio periacqueduttale (PAG) attiva risposte
antinocicettive. Il nucleo parabrachiale (PBN)
riceve, informazioni da rec. viscerali, termici e
nocicettori. Il nucleo del tratto solitario (NTS) è
la prima stazione per afferenze nocicettive
(corna posteriori e V n.c.), gustative e viscerali
(VII,
IX,
X
n.c.)
nonchè
per
i
riflessi
cardiovascolari, respiratori e gastrointestinali.
Bulbo ventromediale (VLM): porzione rostrale
(neur. C1 adrenergici e glutammatergici: input
simpatico pregangliare) e caudale (neuroni A1
noradrenergici e GABA: riflex CV). I nuclei del
rafe forniscono output pregangliari simpatici:
vasocostrizione cute.
AAN, 2007
Brain-gut axis
Sebbene alcune risposte intestinali a
stiramento o stimoli chimici coinvolgano
riflessi enterici, la maggior parte dei
riflessi del tratto gastroenterico (e.g.,
feedback
duodeno-gastrico
per
lo
svuotamento gastrico) coinvolge riflessi
mesenterici (ruolo dei gangli mesenterici)
o riflessi vago-vagali. Risposte intestinali
a stimoli nocicettivi coinvolgono riflessi
spinali e sopraspinali, dando avvio a
risposte emotive e autonomiche.
www.nature.com
Brain-gut axis
Nuclei ponto-bulbari (e.g., rafe e locus
coeruleus) esercitano un azione inibitoria
sui riflessi mentre le aree prefrontali
(PFC) regolano l’output simpato-vagale e
midollare
tramite
modulazione
di
le
vie
discendenti:
risposta
a
stimoli
ambientali (intestinali o esterni) e al
“recall”. Il NTS riceve input da afferenze
vagali
e
interneuroni
e
invia
ai
motoneuroni del nucleo motorio dorsale
del vago (DMN). A1, A2 e A5 inviano alla
VLM. Il PAG riceve input da PBN e
prosencefalo. La PFC inoltre modula IC e
ACC.
www.nature.com
Innervazione dell’ intestino
Le funzioni intestinali sono assicurate da
innervazione estrinseca ed intrinseca:
• Innervazione estrinseca: n. vago,
fibre
simpatiche
splancniche
e
parasimpatiche sacrali;
• Innervazione
intrinseca:
sistema
nervoso enterico (SNE) costituito dai
neuroni del plesso sottomucoso e
mioenterico. Sebbene SNC e SNA
possano modulare il sistema, l’attività
dei
motoneuroni
dipendente
intrinseci
da
è
per
neuroni
primari
lo
afferenti
(IPANs)
interneuroni interni al SNE.
più
e
Sistema nervoso enterico
Sistema nervoso enterico
• Plesso mioenterico (Auerbach): controllo
della motilità GI;
• Plesso sottomucoso (Meissner): trasporto
ionico, flusso ematico, afferenze sensitive.
Neuroni afferenti primari
Funzioni:
Controllo dell’ apparato gastroenterico:
• Generare appropriate risposte riflesse in base al contenuto del lume intestinale;
• Mediare riflessi tra organi diversi;
• Trasmettere afferenze dal SNE al SNC:
Avvio risposte riflesse;
Coordinazione con altri apparati;
Trasmissione di sensazioni come discomfort, nausea, dolore e sazietà.
Neuroni afferenti primari intrinseci (IPANs)
• IPANs mioenterici, responsivi a:
Distorsione delle terminazioni
negli strati muscolari esterni;
Variazioni di pH nel lume
(terminazioni).
• IPANs sottomucosi, rispondono a:
Distorsione meccanica della
mucosa;
Variazioni di pH nel lume.
LM, muscolatura longitudinale; CM, muscolatura circolare;
MP, plesso mioenterico; SM, sottomucosa; Muc, mucosa.
Ma tenga presente che un verme,
con pochissime eccezioni, non è un
essere umano…
Dr. Frederick Frankenstein
Innervazione estrinseca
• Innervazione vagale:
a) afferente --> 70-90% fibre amieliniche il cui soma si trova nel ganglio nodoso e che
terminano nel NTS. Prevalentemente sensibili a stimoli meccanici. Azione eccitatoria o
inibitoria sulle vie nocicettive spinali;
b) efferente --> comprendono il nucleo ambiguo (NA) e il DMN. Quest’ultimo riceve
afferenze dal NTS e innerva la muscolatura liscia dei visceri (via plesso mioenterico);
c) riflessi vago-vagali --> originano nel tronco encefalo (NTS e DMN);
d) controllo del SNC --> 1. il NTS invia a neuroni motori nel DMN/NA e delle colonne
intermedio-laterali (IML); 2. il NTS invia ai nuclei motori del V, VII, XII n.c. e NA; 3.
afferenze viscerali giungono al tronco encefalo (e.g., PBN) che ritrasmette alle aree
cortico-sottocorticali; 4. fibre lunghe giungono a talamo, ipotalamo, aree limbiche e IC,
che mediano risposte autonomiche, endocrine e comportamentali. Connessioni multiple
tra nuclei vagali e prosencefalo (e.g., ACC) --> circuiti viscerali.
Innervazione estrinseca
• Innervazione sacrale/parasimpatica:
S1-S5 --> nn. pelvici --> gangli pelvici --> f. postgangliari --> colon distale, retto e sf. anale
int. Afferenze dai nervi pelvici --> DRG --> riflex spinali (e.g., defecazione). SNC agisce sul
midollo sacrale modulando la motilità del colon.
• Innervazione splancnica/simpatica:
a) afferenti --> afferenze viscerali e spinali (C e Ad) --> gangli para/prevertebrali --> via
spino-talamica mediale/laterale --> c. limbica, IC, SI, PFC;
b) efferenti --> midollo toraco-lombare --> f. pregangliari Ach (IML) --> gangli spinali,
celiaco/mesenterico sup. (stomaco, tenue e crasso prox), mesenterico inf. (crasso), pelvico
(retto) --> f. postgangliari NA --> gangli del plesso mioenterico --> inibiz. rilascio Ach dai
neuroni mioenterici e sottomucosi;
c) controllo del SNC --> ipotalamo stimola, prosencefalo mediale inibisce la motilità colica.
Neuroni afferenti primari estrinseci
• Includono:
Neuroni primari afferenti vagali
(soma nei gangli nodoso e
giugulare);
Neuroni
primari
afferenti
spinali (soma nei gangli delle
radici dorsali).
• Neuroni centripeti:
Braccio afferente dei riflessi
entero-enterici;
Soma nel SNE.
Innervazione della muscolatura striata del tratto GI
• Deglutizione: corteccia precentrale --> tronco encefalo (CPG dorsale e ventrale)
Afferenze periferiche
• V, VII, NA (IX e X), XII n.c.
NA, DMN
• C1-C3
Esofago
Orofaringe
• Defecazione: corteccia motoria (area 4a)
Corna anteriori S1-S2 (nucleo di Onuf)
Afferenze periferiche
Sfint. anale est.
Nervo pudendo
Neurochimica
Cellule
che
trasducono
il
segnale
includono c. enterocromaffini (EC) e
enteroendocrine
rispettivamente
che
rilasciano
serotonina
(5-HT)
e
colecistochinina (CCK). Elevate quantità
di neurotrasmettitori vengono dismesse
(ciò
può
renderne
difficoltoso
il
metabolismo) per colmare il gap tra EC e
targets.
Le
EC
hanno
un
ruolo
importante nella motilità gastrointestinale
e
nell’
IBS
grazie
al
ruolo
della
serotonina nella trasduzione del segnale
di avvio di riflessi peristaltici e secretivi.
Neurotrasmettitori del SNE
Goyal RK, Hirano I. The enteric nervous system.
N Engl J Med. 1996. 334(17): 1106-1115.
A che ci serve conoscere ciò?
IBS
• Dismotilità;
• Stress:
alterazione
asse
ipotalamo-ipofisi-
surrene --> aumento rilascio CRF --> stimolo
vagale --> aumento peristalsi colica;
• Ipersensibilità viscerale: coinvolge ogni livello
(afferenze, SNE, SNP,SNC);
• Alterata modulazione centrale: aumento di
arousal (e.g. amigdala, ACC), ridotta attività in
aree modulanti (e.g. tronco encefalo);
• Neuroimmunità: infiammazione cronica low
grade
con
squilibrio
rapporto
citochine
pro/antiinfiammatorie;
• Neuropeptidi:
alterato
rilascio
di
5-HT,
espressione EC e trasportatori (i.e.,SERT);
• Alterata composizione della flora intestinale.
Katsanos AH, Giannopoulos S, Tsivgoulis G. The Brain-Gut
axis in the pathophysiology of irritable bowel syndrome.
Immuno-Gastroenterology 1:1, 23-26; Jul/Aug/Sep 2012
Ipersensibilità e memoria viscerale
Kennedy PJ, Clarke G, Quigley EM et al. Gut memories:
towards a cognitive neurobiology of irritable bowel syndrome.
Neurosci Biobehav Rev. 2012 Jan;36(1):310-40.
Apkaraian et al, 2005
Meccanismi patologici: sensibilizzazione
Sensibilizzazione periferica
• Ridotta soglia di attivazione;
• Aumentata
risposta
agli
stimoli nocivi successivi;
• Scariche neurali spontanee
aberranti;
• Allargamento
recettivo.
del
campo
Sensibilizzazione centrale
Sensibilizzazione centrale
• Aumento
dell’
affinità
recettoriale;
• Riduzione della soglia di
scarica;
• Sintesi C-FOS;
• Formazione
di
contatti sinaptici.
nuovi
Sensibilizzazione
• Le modificazioni plastiche avviate dagli stimoli nocicettivi diventano
indipendenti da questi per il loro mantenimento; sono reversibili o
possono prolungarsi fino a divenire dolore cronico.
“Chronic pain is a chronic condition, not just a symptom”
Whitten et al., 2005
Meccanismi di cronicizzazione
Meccanismi di cronicizzazione
Nuove prospettive
TMS
“Subthalamic deep brain stimulation can improve the dysfunction in patients with Parkinson’s
disease possibly by altering the neural system that controls gastrointestinal function”.
Effetti della DBS sull’ attività motoria intestinale
• La stimolazione subtalamica unilaterale agisce sulla motilità intestinale nei ratti
anestetizzati aumentando significativamente la motilità colica, presumibilmente
tramite modulazione di aree cerebrali;
• La stimolazione sham non ha effetti significativi in confronto al baseline;
• La somministrazione preventiva di atropina o D1/D2 - antagonisti antagonizza
gli effetti della stimolazione;
• Aumento cellule c-fos positive in aree del CAN (implicate nel controllo GI) dei
ratti trattati rispetto a quelli sottoposti a sham.
Derrey S et al., 2011
Barker, 1984
Stimolazione magnetica
transcranica (TMS)
Magstim
Dantec
La
stimolazione
magnetica
transcranica (TMS) permette di
effettuare
una
stimolazione
corticale sicura, non invasiva e
non dolorosa
Cadwell
Campi elettromagnetici
Principali vantaggi
“Lesioni” reversibili;
Ripetibile;
Alta risoluzione spaziale e temporale;
Relazione causale tra attivazione corticale e risposta;
Può misurare la plasticità corticale;
Può modulare la plasticità corticale;
Possibili finalità terapeutiche.
Principali limiti
Solo regioni superficiali;
Possibile scarsa compliance;
Pazienti a rischio;
Comitato etico;
Diffusione dello stimolo incerta;
Grado di stimolazione incerta.
Controindicazioni
• Protesi metalliche in prossimità del coil:
- Pacemaker;
- Pompe di infusione;
- Shunts ventricolo-peritoneali;
- Non segnalate complicazioni in pz con stimolatori cerebrali;
• Storia di epilessia o familiarità in parente di I grado;
• Farmaci epilettogeni;
• Donne in gravidanza;
• Storia di severi traumi cranici;
• Storia di tossico-dipendenza;
• Condizioni a rischio di crisi epilettiche (e.g., ipertensione intracranica).
Considerazioni pratiche:
forma del coil
La geometria del coil
determina
la focalità
del campo magnetico
e dunque la corrente
indotta
dell’
bersaglio.
Courtesy of Dr. R. Newport
area
Considerazioni pratiche: profondità
70x60
5mm
55x45
40x30
0
15mm
20mm
25mm
Non è possibile stimolare direttamente aree profonde
Courtesy of Dr. R. Newport
Considerazioni pratiche: localizzazione del coil
Trova una risposta funzionale:
M1 - twitch muscolare (MEP)
V5 - fosfeni
Trova un repere anatomico:
Sistema EEG 10/20
Trova la distanza da un punto di
partenza (e.g., FEF: 2-4 cm
anteriormente
e
2-4
cm
lateralmente all’area della mano)
Ma…
Courtesy of Dr. R. Newport
… aree vegetative (CAN)!!!
Condizioni di controllo
Reale
Differenti emisferi
Effetti differenti o
assenti
Sham
Differenti siti
Courtesy of Dr. R. Newport
Raphael JL, Tariq L. Repetitive Transcranial Magnetic Stimulation
(rTMS) in Experimentally Induced and Chronic Neuropathic Pain: A
Review The Journal of Pain 2007; Vol 8, No 6 (June),: pp 453-459
Effetti sul dolore post-TMS
• La rTMS ad alta frequenza (> 5 Hz) maggiormente efficace sul dolore centrale o
neuropatico;
• Sedi preferenziali di stimolo: M1, DLPFC, SI, SII;
• Variabilità dei risultati legata a: durata e frequenza di stimolazione, numero di
treni, numero di sessioni di trattamento e sede di stimolazione;
• Spettro progressivamente crescente di patologie trattate: stroke talamico,
nevralgia del trigemino, sindrome da arto fantasma, CRPS...
Effetti sul dolore viscerale intestinale???
Patrizi F, Freedman SD, Pascual-Leone A et al. Novel therapeutic approaches to the
treatment of chronic abdominal visceral pain. ScientificWorldJournal. 2006 Apr
18;6:472-90.
Effetti sulla motilità post-TMS
La stimolazione bi-emisferica (+ 1-3 cm
antero-posteriormente
e
+
1-5
cm
lateralmente al vertice) con TMS evoca
MEP
rettali
e
anali
riproducibili
in
soggetti sani:
• Tecnica riproducibile;
• Basso costo di esecuzione;
• In combinazione con CEPs Valuta
l’intero arco riflesso;
• Strumenti diffusi in neurofisiologia;
• Utile per studi comparativi pre vs
post trattamento;
• Comprensione brain-anorectal axis e
patologie dell’intestino distale.
Remes-Troche JM, Tantiphlachiva K, Attaluri A et al. A bidirectional assessment of the human brain-anorectal axis.
Neurogastroenterol Motil. 2011 Mar;23(3):240-8, e117-8.
Stimolazione transcranica con correnti dirette
• La stimolazione transcranica con correnti dirette
(tDCS) è una forma di neurostimolazione sicura e
non invasiva che utilizza correnti costanti, a
bassa intensità, erogate direttamente all’ area
cerebrale interessata tramite piccoli elettrodi;
• La stimolazione anodica incrementa mentre la
catodica riduce l’eccitabilità neuronale dell’area
corticale stimolata;
• Effetti a breve (potenziale di membrana) e a
lungo termine (LTP, LTD).
Funzione neuromodulatoria a maggiore durata ma bassa risoluzione spaziale!
Felipe Fregni, Steven Freedman, Alvaro Pascual-Leone. Recent advances in the treatment of chronic pain with non-invasive
brain stimulation techniques. Lancet Neurol 2007; 6: 188–91
Effetti sul dolore post-tDCS
Alcuni studi hanno documentato l’efficacia della tDCS:
• Nell’attenuare il dolore post-ERCP;
• Nel trattare il dolore cronico in corso di nevralgia trigeminale, LBP, sindrome dolorosa
post-stroke, fibromialgia, dolore neuropatico cronico secondario ad altre patologie;
• Mancano dati sul dolore gastrointestinale.
Ma...
Una recente revisione Cochrane ha suggerito un possibile ruolo a breve termine nel
controllo del dolore cronico post HF-rTMS e post tDCS anodica sulla M1. Tuttavia
servono ulteriori studi...
In atto: evidenze non significative!
O’ Connell NE et al, 2010
Effetti sulla motilità post-tDCS
Nuove metodiche di studio
• fMRI;
Alta risoluzione spaziale
• PET;
Bassa risoluzione temporale
P318
• MEG (alta risoluzione spazio-temporale);
• EEG: variazioni bande delta e theta ai potenziali
P106
evocati corticali (CEP) dopo stimolo doloroso
GI. Dopo un elevato numero di stimoli e
averaging
è
possibile
ottenere
delle
componenti con specifiche ampiezze e latenze.
Tali parametri risultano alterati in specifiche
patologie GI --> plasticità neuronale del SNC.
N54
N174
Sharma A, Lelic D, Brock C et al. New technologies to investigate the brain-gut axis. World J
Gastroenterol 2009; 15(2): 182-191.
Example from painful CEP from the gut performed in a healthy volunteer. The figure
shows the topographies at different frequency bands from one subject, and the
percentage of the presence of each frequency band in the overall signal.
Sharma A et al. 2009
Conclusioni
• Autonomia (relativa) del SNE;
• Numerose aree specializzate del SNC e SNA coinvolte nella regolazione nella
percezione e risposta al dolore e nella motilità;
• Neurochimica complessa;
• Meccanismi di sensibilizzazione centrale e periferica essenziali nella fisiopatologia del
brain-gut axis;
• Possilità di studiare il brain-gut axis nelle componenti sensitiva e motoria;
• Studi sull’ efficacia sul dolore della neuromodulazione non invasiva tuttora non
dirimenti.
!
“C'è una meta, ma non una via; ciò che chiamiamo via è un indugiare”.
F. Kafka
Grazie!!!