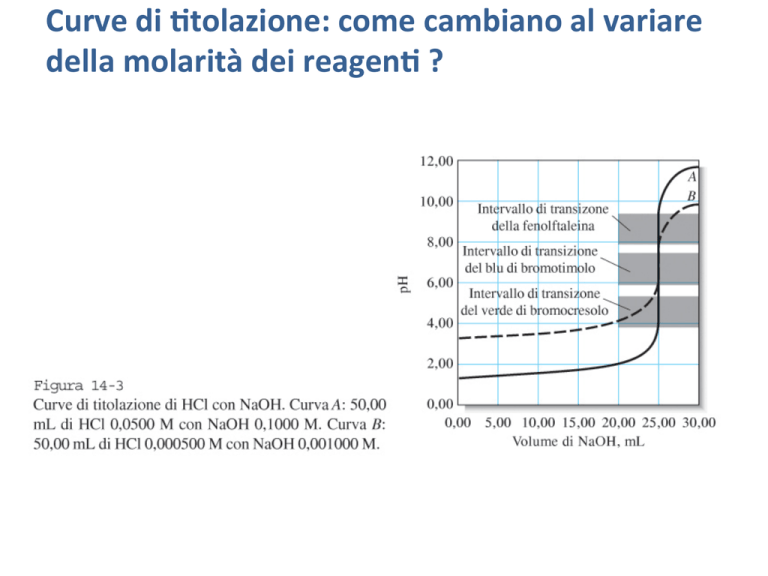
Curvedi)tolazione:comecambianoalvariare
dellamolaritàdeireagen)?
Misceleacidoforte+acidodebole
Titolazionidineutralizzazione:standardprimari
• Perstandardizzareunasoluzionedi/tolanteacido,viene
frequentementeu/lizzatocarbonatodisodio
• Lostandardprimariopiùcomuneperlastandardizzazionedelle
basièlo;alatoacidodipotassio(pKa=5,4)
Acido;alico
Erroredelcarbonato
• Lesoluzionibasichetendonoadassorbireanidridecarbonica
dall’atmosferasecondolaseguentereazione:
CO2+2OH-àCO32-+H2O
• Questopuòcausareunerroredi/tolazionenelcasoincuisi
u/lizzinoindicatoriaviraggiobasico.
• L’acquachesiu/lizzaperlapreparazionediunasoluzionebasica
puòesseresoQopostaabolliturapereliminareilgas.
Erroredelcarbonato:esempio
• UnasoluzionediNaOHliberadacarbonatohaun/tolodi
0,05118M.1,000Lditalesoluzionevieneespostoall’ariaper
diversigiorni,duranteIqualiassorbe0,1962gdianidride
carbonica.
• Calcolarel’errorerela/vochesicommeQerebbeu/lizzandola
soluzionebasicarisultantedall’esposizioneall’aria,inuna
/tolazionediacidoace/coimpiegandocomeindicatorela
fenol;aleina.
Determinazionedell’Alcalinità
• Sidefiniscealcalinitàlacapacitàdiunasoluzioneacquosadireagire
completamenteconunacidoforteinuna/tolazioneperraggiungereunpHdi
4.5(secondopuntodiequivalenzanella/tolazionedelcarbonatoconunacido
forte).
• Ingenerel’alcalinitàdiunasoluzioneèprincipalmenteassociataallapresenzadi
ioniOH-(dovu/allapresenzadiunabaseinsoluzione)ovverodiioniHCO3-e
CO32-(dovu/allareazionedellasoluzioneconl’anidridecarbonica).
• Tali/tolazionihannoloscopodidedurrelaconcentrazioneditaliioniin
soluzionesianelcasoincuiessisianopresen/dasolicheinmisceladidue
componen/
• Sino/chenonpiùdiduecos6tuen6possonoesserepresen6
contemporaneamenteinunamiscelapoichéilmescolamentodiNaOHe
NaHCO3produceNa2CO3finoaconsumazionediunodeiduereagen/.Lesole
miscelepossibilisonoquindiNaOH+Na2CO3ovveroNaHCO3eNa2CO3.
• Ladeterminazionedell’alcalinitàdiunasoluzionenecessitadiunadoppia
/tolazionedivolumiugualidisoluzione,unaconunindicatoreaviraggioacido
(verdedibromocresolopH4.5)el’altraconunindicatoreaviraggiobasico
(feno?aleinapH8.3)
Situazione1:soloOH-Presente
feno;aleina
Veq
verdedi
bromocresolo
Veq
SelafontedialcalinitàinsoluzioneèsoltantoOH-duevolumiiden/cidi
soluzionerichiederannounugualevolumedi6tolantesiachesiusiun
indicatoreacido(viraggioa4.5),sicheseneusiunobasico(viraggioa8.3)
Situazione2:soloCO32-Presente
feno;aleina
verdedi
bromocresolo
Veq
Veq
SelafontedialcalinitàinsoluzioneèsoltantoCO32-la6tolazioneal
verdedibromocresolorichiederàesaDamenteunvolumedi6tolante
doppiodiquellaallafeno?aleinapoichéilcarbonatoèunabase
dipro/caediduepun/equivalen/diunaspeciepolipro/casono
sempreequi-distan/.
Situazione3:soloHCO3-Presente
feno;aleina
Veq
Veq
verdedi
bromocresolo
SelafontedialcalinitàinsoluzioneèsoltantoHCO3-la/tolazioneal
verdedibromocresolosaràlaunicapossibilementreperalcun
volumedi6tolanteaggiuntosiregistreràviraggiodellafeno?aleina
Situazione4:MisceladiOH-eCO32-
InunamisceladiOH-eCO32-labasepiùforte,cheviene/tolata
perprima,saràOH-.Alpuntodiviraggiodellafeno;aleinaanchegli
equivalen/diCO32-sono/tola/aHCO3-.Questospostaavolumi
unpo’piùeleva/ilprimopuntodiviraggiofacendosicheilvolume
di/tolantenecessarioperla6tolazioneconilverdedi
bromocresolorichiedaunvolumeminoredeldoppiodelvolume
necessarioperla6tolazioneallafeno?aleina
SITUAZIONE5:MISCELADIHCO3-ECO32-
InunamisceladiHCO3-eCO32-labasepiùforte,cheviene/tolata
perprima,saràCO32-.Lapresenzadellaspecieanfipro/ca
intermediapos/cipailsecondopuntodiviraggiorispeQoalcaso
delsolocarbonato.Dunqueilvolumedi/tolanterichiestoperla
6tolazionealverdedibromocresolosaràpiùdeldoppiodelvolume
di6tolanterichiestoperla6tolazioneallafeno?aleina.
Riassumendo
Qualita6vamentelacomposizionediunamiscelaalcalinasipuòderivare
secondolaseguenteTabella
Quan6ta6vamente,sitraQadirisolvereunsistemalinearedi2equazioni
indueincognitedoveleincognitesonolemolidiciascunaspecie
presenteeleequazionisonoleleggidiequivalenzariferiteaciascun
puntoequivalente.
Esercizi
• Esercizion°1
Unasoluzionecon/eneNaHCO3,Na2CO3e
NaOHodasolioinunacombinazione.
Stabilirequalita/vamentee
quan/ta/vamentedichecombinazionesi
traQase/tolare50.0mldisoluzionecon
viraggioallafeno;aleinarichiedel’impiego
di22.1mldiunasoluzione0.100MdiHCl,
mentrelastessaaliquotadisoluzione
/tolataconverdedibromocresolorichiede
48.4mldellastessasoluzionediHCl
.
Esercizi
• Esercizion°2
Lapurezzadiunapreparazionefarmaceu/ca
disulfanilammideC6H8N2O2Spuòessere
determinataossidandolosolfoaSO2e
facendogorgogliarelaSO2nell’H2O2per
produrreH2SO4.l’acidovienequindi/tolato
conunasoluzionestandarddiNaOHconblu
bromo/molocimeindicatore.Calcolarela
purezzadellapreparazione,sapendocheun
campionedi0.5236grharichiesto48.13ml
diNaOH0.1251Mperessere/tolata.