SCHEDA
8.9
Il trasferimento dei frammenti monocarboniosi
Nel corso della loro degradazione, molti amminoacidi subiscono reazioni che liberano
da essi frammenti a un solo atomo di carbonio che vengono trasferiti su altre molecole accettrici.
I principali frammenti monocarboniosi sono il metile (OCH 3), l’idrossimetile
(OCH2OH), il formile (OCH PO), l’imminoformile (OCPNH) e il CO2 attivato; per
essere trasferiti sull’accettore finale dagli
specifici enzimi responsabili del loro tra-
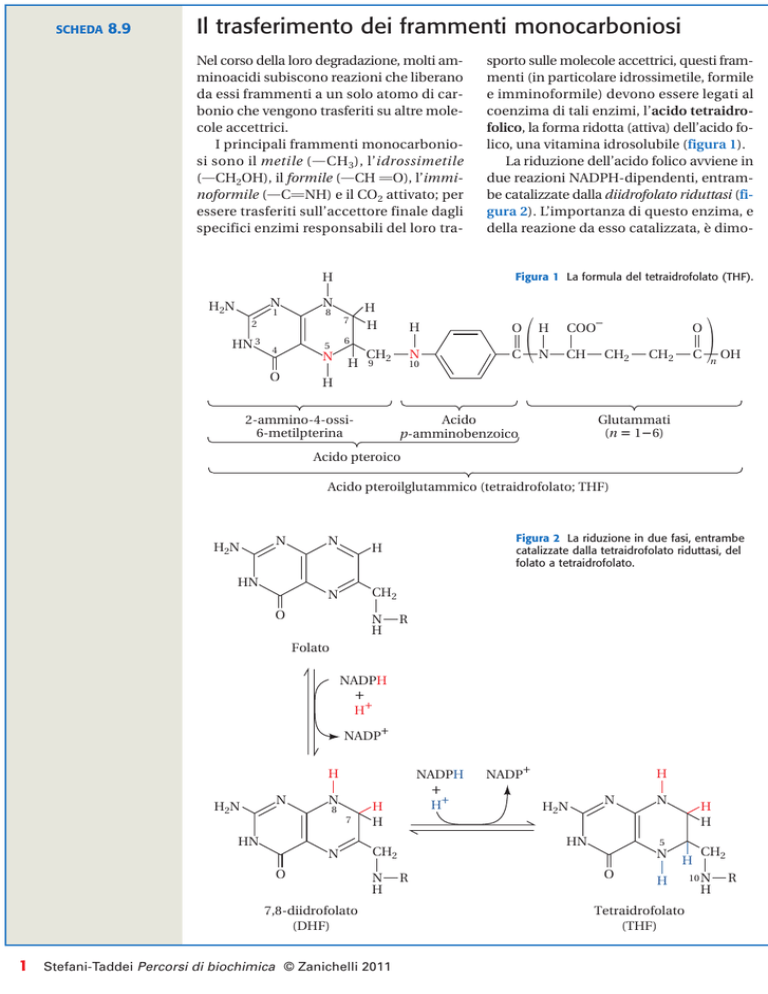
Figura 1 La formula del tetraidrofolato (THF).
H
N
H2N
1
N
8
HN 3
4
O
H
H
7
2
sporto sulle molecole accettrici, questi frammenti (in particolare idrossimetile, formile
e imminoformile) devono essere legati al
coenzima di tali enzimi, l’acido tetraidrofolico, la forma ridotta (attiva) dell’acido folico, una vitamina idrosolubile (figura 1).
La riduzione dell’acido folico avviene in
due reazioni NADPH-dipendenti, entrambe catalizzate dalla diidrofolato riduttasi (figura 2). L’importanza di questo enzima, e
della reazione da esso catalizzata, è dimo-
H
O
N
C
6
5
N
H
CH2
9
10
1
–
H
COO
N
CH
O
CH2
CH2
C
2
n
OH
H
2-ammino-4-ossi6-metilpterina
Glutammati
(n 5 126)
Acido
p-amminobenzoico
Acido pteroico
Acido pteroilglutammico (tetraidrofolato; THF)
H2N
N
N
Figura 2 La riduzione in due fasi, entrambe
catalizzate dalla tetraidrofolato riduttasi, del
folato a tetraidrofolato.
H
HN
CH2
N
O
N
H
R
Folato
NADPH
+
H+
NADP+
H
H2N
N
NADPH
N
8
7
HN
N
O
H+
H
H
H
N
H
Stefani-Taddei Percorsi di biochimica © Zanichelli 2011
H2N
N
HN
CH2
7,8-diidrofolato
(DHF)
1
NADP+
+
N
5
N
R
H
H
O
H
H
Tetraidrofolato
(THF)
CH2
10 N
H
R
strata dall’uso, come farmaci antitumorali,
di sostanze come il metotrexato capaci di
inibirne l’attività. Infatti questi farmaci impediscono la sintesi delle basi puriniche e
della timina (che richiedono reazioni di metilazione) impedendo la replicazione del
DNA e quindi la divisione cellulare. I batteri sono capaci di sintetizzare l’acido folico,
e i primi farmaci chemioterapici sviluppati nel corso del ventesimo secolo, i sulfamidici, in uso ancora oggi, devono il loro
potere antibatterico all’azione inibitrice
competitiva sugli enzimi batterici che catalizzano la biosintesi dell’acido folico, che
per questi microrganismi non è una vitamina.
Le reazioni di trasferimento di frammenti monocarboniosi sono frequenti nelle vie biosintetiche. La carbossilazione dell’acetil CoA svolge un ruolo centrale nella
sintesi degli acidi grassi, mentre quella del
piruvato è alla base del rifornimento di ossalacetato nel mitocondrio e quindi dell’accoppiamento del catabolismo dei carboidrati con quello dei lipidi per una loro
utilizzazione ottimale a fini energetici. In
molte reazioni di metilazione la molecola
donatrice del gruppo metile è una forma at-
tivata dell’amminoacido metionina (S-adenosilmetionina). Queste reazioni sono importanti per la sintesi di molecole di grande importanza biologica come certi fosfolipidi costituenti integrali delle membrane
cellulari (fosfatidilcoline), la creatina o l’ormone adrenalina.
–OOC
NH3+
NH2
H
N
S+
O
N
N
+ Pi + PPi
N
H3C
HO
OH
S-adenosilmetionina (SAM)
Quando cede il gruppo metilico, l’S-adenosilmetionina si trasforma in S-adenosilomocisteina e quindi in omocisteina, una
molecola contenente zolfo che può essere
nuovamente convertita in metionina attraverso una reazione di metilazione. Si noti
che questo sistema non assicura la sintesi
netta di molecole di metionina, un amminoacido essenziale che non può essere sintetizzato dalle cellule dell’organismo.
Stefani-Taddei Percorsi di biochimica © Zanichelli 2011
2