Anno 3
Società Italiana della Contraccezione • I quadrimestre 2009
in questo numero
n° 1
• Contraccezione ormonale e
inquinamento ambientale
• Nuova formulazione
contraccettiva a base di
drospirenone
• Effetto di due estroprogestinici
contenenti etinilestradiolo
30 µg e drospirenone 3 mg
ed etinilestradiolo 30 µg e
clormadinone 2 mg sulle
manifestazioni
iperandrogeniche cutanee
ed ormonali
• Effect of an oral
contraceptive with
Chlormadinone acetate
on depressive mood
• Dispositivi contraccettivi
intrauterini:
un aggiornamento
• Appuntamenti 2009
XII CONGRESSO NAZIONALE S.I.M.
SOCIETà ITALIANA DELLA MENOPAUSA
Napoli
10 •12 Dicembre 2009
Presidente: C.Nappi
Complesso Universitario di Monte Sant'Angelo
Via Cinthia 26 • Napoli
Richiesti i crediti ECM
SOCIETà ITALIANA PER LA MENOPAUSA
Segreteria Scientifica
Segreteria Organizzativa
Costantino Di Carlo
Giuseppe Bifulco
◆ MKT Consulting
Dip.di Scienze Ostetrico Ginecologiche
Urologiche e Medicina della Riproduzione
Università degli Studi di Napoli Federico II
Via Pansini, 5 - 80131 Napoli
Tel. e Fax 081.7462903-05
[email protected]
Phone:+39 06 39746189
Fax: +39 06 45438292
via Cassia, 1110 - 00189 Rome - Italy
e.mail: [email protected]
E D I TEDITORIALE
O R I A L E
S.I.C. DONNA News
D
al 7 al 9 Maggio si sono tenuti a Modena, congiuntamente,
il 3° Congresso Nazionale della Società Italiana della
Contraccezione e il 1° Congresso Nazionale della Società
Medica Italiana per la Contraccezione.
Il Congresso organizzato dalla Clinica Ginecologica dell’Università di
Modena diretta dal Prof. A. Volpe, è stato inaugurato dai presidenti
delle due Società, Professori Carmine Nappi e Emilio Arisi ed ha visto
la partecipazione dei più importanti esperti italiani della materia e
di alcuni selezionati ospiti stranieri.
Durante i tre giorni dei lavori sono stati dibattuti numerosi aspetti
inerenti le problematiche della contraccezione.
Il programma scientifico è risultato molto ricco e ben articolato.
Nella prima giornata, il tema della contraccezione è stato
inizialmente affrontato dal punto di vista sociale e politico, in una
tavola rotonda cui hanno partecipato rappresentanti di Società
Scientifiche, delle Istituzioni e del mondo dell’informazione.
Particolare rilievo è stato dato all’influenza sulla riproduzione dei
mutamenti sociali e delle sfide rappresentate dalla necessità da
parte degli operatori di confrontarsi con donne di etnie diverse,
abituate a differenti modelli culturali.
Anche il problema dell’interruzione volontaria di gravidanza è stato
affrontato in una sessione cui hanno partecipato illustri esponenti del
settore, con riferimenti alle diverse realtà nazionali, ponendo
l’accento su quelle che sono le più recenti direttive europee in tema
di aborto.
Si è inoltre dibattuto sull’importanza della “personalizzazione” delle
terapie estroprogestiniche, ovvero sulla necessità di rispondere alle
differenti caratteristiche cliniche della donna mediante una scelta
contraccettiva che passi attraverso le più recenti formulazioni
contenenti bassi dosaggi di estrogeno e nuove tipologie di
progestinici. Rimanendo nell’ambito di tale discussione, hanno trovato
ampio spazio specifiche tematiche inerenti l’uso dei contraccettivi
ormonali ai due estremi della vita riproduttiva della donna,
l’adolescenza e la premenopausa.
Un altro tema dibattuto, nell’ambito di una tavola rotonda che ha
avuto come protagonisti sessuologi e ginecologi, è stato quello della
contraccezione e della salute sessuale della donna nell’ottica
dell’equilibrio che viene a stabilirsi tra meccanismi biologici e fattori
socio-individuali.
La seconda giornata del Congresso, si è aperta con un dibattito
incentrato sulla scelta contraccettiva in donne che presentano fattori
di rischio, come patologie autoimmuni o disordini metabolici, alla luce
anche delle nuove formulazioni estro-progestiniche comparse
recentemente sul mercato e delle nuove acquisizioni nel campo della
ricerca farmacologica.
L’impiego di vie alternative di somministrazione e la farmacologia di
nuovi progestinici hanno trovato ampio risalto.
Un riferimento particolare è stato fatto alla recente introduzione
dell’uso dei contraccettivi ormonali con somministrazione continua.
Anche la possibilità di ricorrere alla sterilizzazione tubarica per via
isteroscopica, che ormai data 10 anni dalla sua comparsa, è stata
oggetto di una esaustiva trattazione.
Nella terza giornata è stata affrontata la tematica, sempre
scottante, del rischio oncologico legato all’assunzione dei
contraccettivi ormonali, ampiamente ridimensionato dai relatori.
Il Congresso si è concluso con un’ultima sessione dedicata agli effetti
terapeutici della contraccezione.
L’affluenza è stata elevata, con presenza giornaliera media di oltre
400 specialisti che hanno partecipato con interesse al dibattito
congressuale.
www.sicontraccezione.it
DIRETTIVO S.I.C.
Presidente
C. Nappi
Past President
A. Volpe
Presidenti Onorari
G. Benagiano
P.G. Crosignani
Vice Presidenti
G. B. Melis
G. Scarselli
Tesoriere
V. Bruni
Segretario
P. Rita
Consiglieri
A. Cagnacci
A. Cianci
V. De Leo
F. Fruzzetti
M. Moscarini
F. Vicariotto
S.I.C. DONNA NEWS
Direzione Scientifica
C. Nappi
C. Di Carlo
Responsabile
Comunicazioni Esterne
A. La Marca
Direttore Responsabile
G. Rita
Editore
MKT Consulting
[email protected]
www.mkt-consulting.it
Stampa
BC Graph • Pomezia
Autorizzazione Tribunale
di Roma
N. 229 del 12 giugno 2007
Finito di stampare
maggio 2009
Questo periodico è associato
all’Unione Stampa Periodica Italiana
Ai sensi della legge sul diritto d’autore e del
codice civile è vietata la riproduzione di questi
articoli o di parte di essi con qualsiasi mezzo,
elettronico, meccanico, per mezzo di fotocopie,
microfilms, registrazioni o altro.
La responsabilità del contenuto degli articoli è
interamente ascrivibile agli Autori.
3
S.I.C. DONNA News
s.I.C. n ews
3° Congresso Nazionale S.I.C. 7-9 Maggio • Modena
• Durante il 3° Congresso Nazionale della S.I.C. il Direttivo ha voluto consegnare una targa ricordo
per l'alta professionalità e l'elevato contributo scientifico dato alla Ginecologia ed Ostetricia Italiana
ai Professori:
Giuseppe BENAGIANO
Piergiorgio CROSIGNANI
Vincenzina BRUNI
• In occasione del 3° Congresso Nazionale della S.I.C. il Direttivo, tra le diverse iniziative ha deciso di
fondare la Società Italo-Albanese della Contraccezione, il Presidente sarà il Prof. Halim Kosowa di
Tirana e Presidenti Onorari i Professori Carmine Nappi e Annibale Volpe.
4
www.sicontraccezione.it
S.I.C. DONNA News
articoli s cientifici
Contraccezione ormonale
e inquinamento ambientale
C. Nappi
Professore Ordinario di Ginecologia e Ostetricia Università di Napoli Federico II
Presidente della Società Italiana della Contraccezione (S.I.C.)
I
l gennaio scorso, l’Osservatore Romano ha
pubblicato un articolo dal titolo “L’Humanae vitae,
una profezia scientifica”, a firma di Marìa Simón
Castellví, Presidente della “Federazione Internazionale
delle Associazioni dei Medici Cattolici”, contenente
alcune affermazioni sulla contraccezione ormonale a
dir poco opinabili. Secondo Castellvì, la pillola
funzionerebbe in molti casi con effetto abortivo e
avrebbe effetti ecologici devastanti, disseminando
“tonnellate di ormoni” nell’ambiente, possibile causa
di infertilità maschile.
Tali affermazioni hanno avuto naturalmente ampio
risalto mediatico, suscitando comprensibile allarmismo,
pur non avendo esse alcuna solida base scientifica.
Invero, con molto equilibrio, in alcune dichiarazioni
riportate sempre dalla stampa, lo stesso Monsignor
Elio Sgreccia, Presidente Emerito della Pontificia
Accademia per la Vita, considerato uno dei massimi
esperti mondiali di Bioetica, pur ribadendo la
posizione della Chiesa nei riguardi della
contraccezione, ha ridimensionato la portata delle
apodittiche affermazioni di Castellví.
L’affermazione che la pillola possa avere un effetto
anti-impiantatorio può essere facilmente confutata
per l’accertato suo effetto di inibizione
dell’ovulazione.
Anche l’evenienza, da taluni propugnata (Holt et al.,
2002), che in rarissimi casi, nelle donne gravemente
obese che fanno uso di pillole a basse e bassissime
dosi, possa effettivamente verificarsi l’ovulazione è
negata da altri (Brunner Huber L.R. & Toth J.L., 2007).
Cioè, il rischio di ovulazione è più ipotetico che reale.
In ogni caso, laddove la paziente ovuli, la pillola non
può avere effetto abortivo, perché se non c’è blocco
dell’ovulazione, allora c’è formazione del corpo luteo
che, in caso di concepimento, può solo favorire
l’impianto. Infatti, nessuno studio ha dimostrato che
nelle utenti di contraccettivi un’eventuale gravidanza
esiti in aborto; anzi del tutto recentemente, è stato
evidenziato che l’esposizione a contraccettivi orali in
periodo periconcezionale non aumenta il rischio di
outcome gravidico negativo (Ahn et al, 2008).
www.sicontraccezione.it
Per quanto riguarda invece il presunto effetto
inquinante sull’ambiente dei contraccettivi ormonali,
va premesso che, fra i vari inquinanti che contaminano
l’ambiente, è stato recentemente posto in luce, ma
spesso trascurato, un ruolo rilevante svolto dai
cosiddetti Endocrine Disruptors, che sono sostanze
esogene in grado di alterare le funzioni del sistema
endocrino, attivando o inibendo i recettori ormonali
(degli estrogeni, degli androgeni, degli ormoni tiroidei)
e, quindi, di causare effetti nocivi sulla salute
dell’organismo vivente e sulla sua progenie. E proprio
come Endocrine Disruptors, potrebbero agire anche
gli ormoni contenuti nei contraccettivi ormonali.
Questi, una volta escreti nelle urine, raggiungerebbero
attraverso gli scarichi fognari, le acque dei fiumi e del
mare, contribuendo al loro inquinamento.
Studi condotti nel Regno Unito hanno evidenziato la
presenza, negli scarichi fognari “trattati”, di
17βestradiolo, di estrone e di etinilestradiolo.
Quest’ultimo, tuttavia, era presente in quantità al
limite della sensibilità del sistema adoperato e solo in
alcuni casi. (Desbrow et al., 1998).
In Italia, la possibilità che sostanze farmacologiche
possano giungere ad inquinare le acque è stata valutata
in uno studio condotto nel 2000 in Lombardia, che ha
evidenziato la presenza di quantità minime, ma
misurabili, di vari farmaci nelle acque e nei sedimenti
fluviali del Po, dell’Adda e del Lambro e nell’acqua
potabile di Lodi. Tuttavia, non veniva valutata la
presenza di sostanze ormonali (Zuccato et al., 2000).
Più recentemente, Pojana e coll. (2007) in uno studio
sulle acque della laguna veneta hanno rilevato la
presenza di 17βestradiolo e di etinilestradiolo a basse
concentrazioni sia nelle acque che nei mitili.
Pertanto, in ogni caso, le concentrazioni ambientali di
estrogeni sono minime, ai limiti della dosabilità
(Desbrow et al., 1998), e solo in minima parte,
determinate dai contraccettivi ormonali.
Infatti, è ben noto che le urine di tutti i mammiferi,
maschi e femmine, sono ricche di ormoni steroidei. Le
urine di una donna gravida, ad esempio, contengono
concentrazioni di estrogeni molte volte superiori a
quelle di una donna che assume contraccettivi
5
S.I.C. DONNA News
Contraccezione ormonale e inquinamento ambientale
ormonali. Una donna alla 40 a settimana di gestazione
ha infatti concentrazioni estrogeniche 10.000 volte più
elevate rispetto ad una donna che prende la pillola.
Inoltre, i famosi estrogeni coniugati equini, largamente
utilizzati in terapia, sono estratti dalle urine di cavalle
gravide. D’altra parte, si immagini quali sono le
concentrazioni di ormoni steroidei negli scarichi degli
allevamenti bovini o suini, dove le femmine sono
costantemente in fase gravidica! E ciò senza voler
considerare l’inquinamento ambientale che deriva
dall’uso più che diffuso di additivi alimentari, ormoni e
antiparassitari che si fa negli animali da allevamento
(Zuccato et al, 2000) e in agricoltura (Greenlee et al.,
2003), con dimostrate conseguenze negative sulla
funzione riproduttiva umana.
Allo stesso modo, steroli di origine vegetale ad azione
estrogenica, i cosiddetti fitoestrogeni, liberati nel
corso di varie lavorazioni (come quella della carta)
possono contribuire a questo tipo di inquinamento.
È pur vero poi che molte sostanze chimiche, oltre ad
esercitare un documentato effetto mutageno o
cancerogeno oppure rientrare nella categoria dei Pbt
(presunti bioaccumulanti tossici, cioè sostanze che
si degradano lentamente nell’ambiente e che
si accumulano nei tessuti adiposi dell’uomo
e dell’animale), possono svolgere un ruolo anche
di Endocrine Disruptors. Pesticidi come
il
diclorodifeniltricloroetano più noto come il DDT,
residui di lavorazioni chimiche come la diossina,
l’organotina utilizzata nella fabbricazione delle
condutture in PVC, i policlorobifenili (PCB) utilizzati
fino a poco tempo fa in numerose lavorazioni
manifatturiere, gli ftalati utilizzati come plastificanti,
i residui di detergenti come il nonilfenolo, e il
bisfenolo A, utilizzato per la preparazione delle
tettarelle per i neonati. La presenza di alte
concentrazioni di queste sostanze, è stata ampiamente
documentata nell’ambiente, a seguito della dispersione
in corso di lavorazioni industriali (Falconer et al.,
2006).
Per quanto riguarda specificamente i pesticidi usati in
agricoltura e nell’industria, l’ultimo rapporto ISPRA
(Istituto Superiore per la Protezione e la Ricerca
Ambientale) ha evidenziato che essi sono contenuti
nel 57.5% delle acque superficiali; nel 36.6% oltre i
limiti previsti per l’acqua potabile; per le falde
sotterranee la contaminazione riguarda il 31.5% dei
siti esaminati. Comunque, l’esposizione più elevata
nell’uomo agli Endocrine Disruptors, sta nel consumo
di pasti “normali”, particolarmente dei vegetali, frutta
e noccioline (Safe, 2005).
Infine, non vanno trascurati gli effetti di alcuni metalli
pesanti (bronzo, cadmio, cromo, manganese e piombo)
nei confronti della ferilità. Fino a non molti anni fa, il
problema sembrava limitato agli addetti alla
lavorazione di queste sostanze. Dati recenti, alcuni
presentati proprio dall’Università di Napoli Federico
II, hanno evidenziato invece come gli scarichi del
traffico veicolare, possano agire pesantemente sulla
sfera riproduttiva. Infatti, una diminuzione significativa
della maggior parte dei parametri seminologici
funzionali è stata riscontrata nei lavoratori della
trafficatissima Tangenziale di Napoli, correlata a livelli
ematici elevati di piombo e di idrocarburi aromatici
policiclici (De Rosa et al., 2003)
In conclusione, il problema della presenza degli
Endocrine Disruptors nell’ambiente è reale: quindi
appare opportuna una piena presa di coscienza da
parte di tutti, specialmente delle autorità sanitarie, del
rischio connesso alla loro presenza. Tuttavia, appare
quanto meno azzardato voler attribuire all’utilizzo dei
contraccettivi ormonali, soprattutto a basse e
bassissime dosi, un ruolo di rilievo per questo tipo di
inquinamento ambientale.
Bibliografia
Bi
1.
compounds: a review of their challenge to sustainable and safe water supply and
water reuse. Environ. Toxicol. 21: 181-191, 2006.
6. Greenlee AR, Arbuckle TE, Chyou PH. Risk factors for female infertility in an
agricultural region.
Epidemiology, 14: 429-36, 2003.
7. Holt V.L, Cushing-Haugen K.L., Daling J.R.: Body weight and risk of oral
contraceptive failure. Obstet. Gynecol., 99 (5), 820-827, 2002.
8. Pojana G., Gomiero A., Jonkers N., Marcomini A., Natural and synthetic endocrine
disrupting compounds (EDC) in water, sediment and biota of a coastal lagoon.
Environ. Int. 33: 929-936, 2007.
9. Safe S.: Clinical correlations of environomental endocrine disruptors. Trends in
Endocrinology and Metabolism, 16 (4), 139-144, 2005.
10. Zuccato E., Calamari D., Natangelo M., Fanelli R. Presence of therapeutic drugs in
the environment. The Lancet 335: 1789-1790, 2000.
2.
3.
4.
Ahn HK, Choi JS, Han JY, Kim MH, Chung JH, Ryu HM, Kim MY, Yang JH, Koong MK,
Nava-Ocampo AA, Koren G.: Pregnancy outcome after exposure to oral contraceptives
during the periconceptional period. Hum. Exp. Toxicol., 27 (4): 307-13, 2008.
Brunner Huber L.R., Toth: Obesity and oral contraceptive failure: Findings from the
2002 National Survey of Family Growth. Am J Epidemiol. 166: 1306-1311, 2007.
De Rosa M, Zarrilli S, Paesano L, Carbone U, Boggia B, Petretta M, Maisto A,
Cimmino F, Puca G, Colao A, Lombardi G. Traffic pollutants affect fertility in men.
Hum Reprod, 18(5):1055-61, 2003.
Desbrow C., Routledge E.J., Brighty G.C., Sumpter J.P., Waldock M. Identification of
estrogenic chemicals in STW effluent. 1. Chemical fractionation and in vitro
biological screening. Environ. Sci. Toxicol. 32: 1549-1558, 1998.
Falconer I.R., Chapman H.F., Moore M.R.,Ranmithugala G. Endocrine disrupting
6
5.
www.sicontraccezione.it
S.I.C. DONNA News
articoli s cientifici
Nuova formulazione
contraccettiva a base
di drospirenone
Paolo Quartararo
Clinica Ostetrica e Ginecologica - Università di Palermo
Y
www.sicontraccezione.it
Ciononostante alcuni sintomi possono trarre
beneficio dall’uso della pillola e non è un caso che
un recente sondaggio svela che fra le utilizzatrici
della pillola solo il 35% soffre di sindromi
premestruali, mentre, fra le non utilizzatrici, la
percentuale sale a quota 61%.
Queste percentuali si riducono ulteriormente
grazie a YAZ. Infatti, fra i vari ormoni di sintesi,
quello che si è rivelato particolarmente efficace
contro la sintomatologia premestruale è proprio il
drospirenone che esercita un’ottima azione
antimineralcorticoide: contrasta cioè la ritenzione
idrica causata dalle variazioni ormonali, che è a sua
volta è la causa principale dei disagi fisici.
10
10
8
8
8
8
6
6
6
FSH (mlU/ml)
10
FSH (mlU/ml)
10
LH (mlU/ml)
LH (mlU/ml)
AZ, nuova pillola contraccettiva a base di
drospirenone, negli Stati Uniti ha avuto già un
grande successo ed in pochi mesi ha
conquistato milioni di donne, diventando la pillola
più venduta oltreoceano.
Le peculiari caratteristiche di Yaz permettono di
contrastare, e nella maggior parte dei casi risolvere
la sintomatologia premestruale, un problema che
interessa molte donne.
Attualmente il mercato si diversifica per la presenza
di numerosi contraccettivi orali differenti per
caratteristiche e dosaggi.
Perché allora una nuova pillola?
La risposta è semplice: rispetto alle esigenze del
passato, che si basavano soprattutto su efficacia e
tollerabilità, alla contraccezione moderna sono
richiesti non solo benefici dal punto di vista
cosmetico e dell’immagine di sé, ma anche eventuali
benefici che possano riflettersi sulla sfera del
benessere.
Yaz rappresenta l’evoluzione di due precedenti
formulazioni con gli stessi principi attivi, anche se a
dosaggi differenti di etinilestradiolo (30
microgrammi per Yasmin, 20 microgrammi per
Yasminelle).
Mentre lo schema classico prevede 21 giorni di
assunzione e 7 giorni di pausa, il nuovo schema a
24+4 si basa su 24 giorni di assunzione e 4 giorni
senza ormoni con placebo.
Questo regime continuativo permette infatti una
riduzione del rischio di dimenticanze ed errori di
assunzione (più frequenti nelle adolescenti).
La ridotta pausa di assunzione contribuisce al
miglioramento dei sintomi premestruali.
L’efficacia sulla sintomatologia premestruale con
l’uso di preparati tradizionali indipendentemente
dalle loro caratteristiche, è risultata contraddittoria.
Spesso, infatti, il classico schema a 21 giorni è in
grado di riproporre la ciclicità fisiologica del ciclo
mestruale, incidendo pertanto poco su tale
sintomatologia o addirittura amplificando alcuni
sintomi correlati con le fluttuazioni ormonali.
6
**
4
4
4
**
2
**
**
coc
0
1
68
7
**
2
0
13 24 35 46 57
Cycle daysCycle days
**
**
2
coc
2
**
**
**
2
0
4
8
coc
0
1
coc
2
13 24 35 46 57
Cycle daysCycle days
68
7
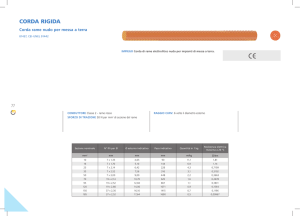
Serum estradiol, inhibin B, FSH and LH compared between a 21/7 and
a 24/4 regimen containing 3 mg drospirenone and 30g ethinylestradiol.
day 0 is the last day of COC use for all groups. In the 7-day hormonefree interval (HFI), days 1-7 represent hormone-free days,
with day 8 representing the first day of COC use in the next cycle. In the
3- or 4-day HFI, days 1-3 or 1-4, respectively, represent hormone-free
days, with the remaining days rapresenting the first days of COC use in
the next cycle. *p < 0.05, **p < 0.01 indicate days where ovarian
hormones (top panels) or gonadotropin levels (bottom panels) differ
within patients between cycles. Adapted from [5].
Non solo, il drospirenone ha anche un effetto sul
sistema nervoso centrale, tanto che l’uso dei
suddetti contraccettivi orali ha dimostrato
un’influenza positiva sull’atteggiamento psicologico
delle donne che manifestano una sintomatologia
premestruale, mentre non è stato dimostrato
questo effetto per altre composizioni.
7
8
S.I.C. DONNA News
Nuova formulazione contraccettiva a base di drospirenone
Sembra, infatti, il drospirenone comporti una
migliore modulazione neuroendocrina, riducendo
così l’impatto delle variazioni ormonali a livello
centrale.
Grazie alle sue proprietà antiandrogeniche, il
Drospirenone è in grado infine di contrastare
problemi come ipertricosi (peluria eccessiva), pelle
grassa e acne, mentre l’attività antimineralcorticoide
può contrastare la ritenzione idrica legata agli
estrogeni.
La formulazione del nuovo contraccettivo ne
amplifica al massimo gli effetti: grazie all’assunzione
di ulteriori tre compresse, si ottiene infatti una
maggiore presenza di drospirenone nell’arco di un
mese con un ulteriore rafforzamento dei benefici
del Drospirenone.
Se si considera poi che il drospirenone ha
un’emivita di 30 ore, si può dire che si ha una
copertura quasi del 100% (più di 25 giorni al mese).
Ecco perché Yaz può essere considerato un’alleato
di quelle donne che soffrono dei sintomi
premestruali.
Oltre a una più costante presenza mensile del
drospirenone, Yaz garantisce una riduzione delle
fluttuazioni ormonali che con i preparati tradizionali
tendono a verificarsi nei sette giorni di
sospensione.
Lo schema di assunzione a 24/4 giorni, infatti, è in
grado di minimizzare quelle fluttuazioni ormonali
tipiche del ciclo mestruale e spesso alla base di
molti sintomi fastidiosi in fase premestruale, cosa
che le pillole tradizionali a 21 giorni, come ricordato
prima, spesso non sono in grado di fare.
Questo aumenta anche il controllo del ciclo e
l’efficacia contraccettiva.
Bibliografia
Bibl
•
•
•
•
Radhika D. Rible, Daniel R. Mishell Jr Shortening the hormone-free interval
Gynaecology Forum Vol. 13, No. 2, 2008, p 3-8
Sulak PJ, Scow RD, Preece C, et al. Hormone withdrawal symptoms in oral
contraceptive users. Obstet Gynecol 2000;95:261–6.3.
Sulak PJ, Kuehl TJ, Ortiz M, et al. Acceptance of altering the standard 21-day/7-day
oral contraceptive regimen to delay menses and reduce hormone withdrawal
symptoms. Am J Obstet Gynecol 2002;186:1142–9.
Gloria Bachmann, Patricia J. Sulak, Carole Sampson-Landersc, Norbert Bendad,
8
•
Drospirenone level
Steady-state level
Cycle 2
6
14
22 24 28
Luteal phase
Cycle days
Dosing with drospirenone in a 24/4 regimen extends its
properties into the hormne-free interval
•
•
Joachim Marrd, Efficacy and safety of a low-dose 24-day combined oral
contraceptive containing 20 mcg ethinylestradiol and 3 mg drospirenone
Contraception 70 (2004) 191–198
Koltun et al., efficacy and safety of 3 mg drospirenone/20mcg ethinylestradiol
contraceptive administred in 24/4 in the treatment of acne vulgaris; a randomized,
double-blind, placebo controlled trial. Contraception 2008; 77, 249-256.
Yonkers et al., Efficacy of a new low-dose oral contraceptive with drospirenone in
Premenstrual Dysphoric Disorder. Am J Obstet Gynecol 2005; Vol 106, N°3..
www.sicontraccezione.it
S.I.C. DONNA News
articoli s cientifici
“Effetto di due estroprogestinici contenenti
etinilestradiolo 30 µg e drospirenone 3 mg
ed etinilestradiolo 30 µg e clormadinone 2 mg
sulle manifestazioni iperandrogeniche
cutanee ed ormonali”
Stefano Lello, Grazia Primavera, Laura Colonna, Giorgio Vittori, Francesca Guardianelli,
Roberto Sorge, Desanka Raskovic
I­ ntroduzione
L’iperandrogenismo nelle donne è un problema
clinico importante e frequente. L’aumento dei livelli
ematici e/o dell’attività degli androgeni circolanti è
legato, dal punto di vista clinico, ad irregolarità
mestruali, diminuita fertilità e manifestazioni
cutanee (seborrea, acne, irsutismo) [1], che
rappresentano ragioni frequenti di malessere
psicologico [2,3] con conseguenze negative sulla
qualità della vita e sull’autostima.
Il trattamento ormonale con estroprogestinici orali
(EP) è un’opzione importante nella pratica clinica
[4]. Gli EP orali sembrano in grado di ridurre i
livelli plasmatici di testosterone (T) libero
(biologicamente attivo) sia riducendo la sua
produzione a livello ovarico che aumentando la
produzione epatica della globulina legante gli
ormoni sessuali (SHBG), una proteina che lega il T,
riducendo la sua attività biologica anche a livello
cutaneo [2]. Alcuni EP contenenti, oltre al
componente estrogeno (etinilestradiolo, EE), un
progestinico dotato di proprietà antiandrogene,
sono più efficaci in condizioni più iperandrogeniche.
Gli EP orali contenenti EE 30 µ­g + drospirenone
(DRSP) 3 mg hanno dimostrato, in studi eseguiti in
passato, importanti azioni anti-androgene [5–7],
paragonabili a quelle di EP contenenti EE 35 µg +
ciproterone acetato (CPA) 2 mg [8]. Anche EP
contenenti EE 30 µg + clormadinone acetato
(CMA) 2 mg hanno dimostrato effetti antiandrogeni [9–11]. Lo scopo di questo studio era
quello di confrontare gli effetti di EE/DRSP e di
EE/CMA su donne iperandrogeniche da un punto
di vista ormonale e dermatologico.
Materiali­e­metodi
Sono state arruolate nello studio 55 donne che
presentavano manifestazioni iperandrogeniche
(seborrea, acne, crescita dei peli) e caratteristiche
www.sicontraccezione.it
plasmatiche ormonali iperandrogeniche. Trenta
pazienti (età media: 24,5 anni; range: 18–30) sono
state assegnate a caso (per randomizzazione) al
trattamento con un EP contenente EE 30 µg +
DRSP 3 mg per 21 giorni al mese per 6 mesi e 25
pazienti hanno ricevuto un trattamento con un EP
contenente EE 30 µg + CMA 2 mg (età media: 24,1
anni; range: 18–28) con lo stesso regime di
somministrazione.
L’acne è stata valutata utilizzando un punteggio di
Ferriman-Gallwey modificato [12], in cui il tipo di
pelo in ciascuna delle 11 aree sensibili agli
androgeni è classificato da 0 (nessuno) a 4
(virilizzazione franca). In questa classificazione i
punteggi superiori a 8 identificano condizioni di
irsutismo di diversa gravità.
Per quanto riguarda il pattern ormonale, i seguenti
ormoni sono stati valutati nella fase follicolare
iniziale (3° giorno del ciclo mestruale): ormone
follicolo-stimolante (FSH), ormone luteinizzante
(LH), prolattina (PRL), delta-4 androstenedione (A),
testosterone totale (T), deidroepiandrosterone
solfato (DHEAS), globulina legante gli ormoni
sessuali (SHBG), 17-idrossiprogesterone (17OHP).
In fase luteinica (21° giorno del ciclo mestruale),
sono stati valutati i livelli plasmatici di progesterone
(P). È stato calcolato il “free androgen index”
(indice androgeno libero) (T6100/SHBG) come
marker dell’androgenizzazione. Per tutte le
determinazioni ormonali, sono stati usati kit RIA.
L’ecografia transvaginale è stata eseguita in tutte le
pazienti per studiare la morfologia ovarica.
Le caratteristiche della pelle valutate durante lo
studio sono state misurate con il Cutometer MPA
5801 (Courage-Khazaka Electronic GmbH,
Colonia, Germania), un apparecchio che può
valutare i seguenti parametri cutanei in maniera
non-invasiva:
l’idratazione
della
pelle
(Corneometer®, misura l’idratazione della pelle
9
S.I.C. DONNA News
Effetto di due estroprogestinici contenenti etinilestradiolo 30 µg e drospirenone 3 mg ed etinilestradiolo
30 µg e clormadinone 2 mg sulle manifestazioni iperandrogeniche cutanee ed ormonali
con metodo capacitivo); la perdita d’acqua transepidermica (Tewameter®, TEWL, espressa come
g/h/m2), il sebo (Sebumeter®, metodo fotometrico,
espresso come mg di sebo/cm2). I parametri della
qualità come il volume (relativo alla profondità in
microrilievo, espresso in unità arbitrarie), l’energia
(relativa all’omogeneità della pelle, espressa in unità
arbitrarie) e la superficie (relativa alla pelle liscia,
espressa in unità arbitrarie) sono stati valutati
mediante il Visioscan® VC 98 (Courage-Khazaka
Electronic GmbH, Colonia, Germania); lo
sperimentatore era lo stesso per tutta la durata
dello studio ed era sempre all’oscuro del
trattamento effettuato.
Risultati
I due gruppi di trattamento erano paragonabili per
età, altezza, peso e Indice di Massa Corporea (Body
Mass Index) (BMI).
La seborrea (Figura 1) è diminuita significativamente
rispetto al basale a 3 e 6 mesi sia per EE/DRSP che per
EE/CMA (P<0,01 per tutti rispetto al basale),
ma questo effetto era maggiore nel gruppo trattato
con EE/DRSP in confronto a EE/CMA durante
l’osservazione (P<0,05 fra gruppi).
La corneometria (parametro relativo all’idratazione
della pelle) ha mostrato un significativo aumento nel
gruppo trattato con EE/DRSP a 6 mesi rispetto al
basale (P <0,01); l’effetto di EE/DRSP era
significativamente superiore a quello di EE/CMA (P
<0,05 fra gruppi) a 6 mesi.
Il valore di TEWL (evaporazione cutanea
dell’acqua) è diminuito durante lo studio in
entrambi i gruppi trattati a 3 e 6 mesi, ma era
significativo a 3 mesi solo per EE/DRSP (P <0,05) e
per entrambi i trattamenti a 6 mesi (P <0,05
rispetto al basale). L’effetto di EE/DRSP era
maggiore di quello di EE/CMA a 3 mesi (P<0,05 per
il confronto fra gruppi).
Il volume (parametro relativo alla profondità del
microrilievo) era diminuito durante il trattamento.
Per EE/DRSP, vi era una tendenza significativa alla
diminuzione a 3 mesi (P <0,01 rispetto al basale), ma
non per EE/CMA; i risultati del trattamento erano
paragonabili a 6 mesi ed entrambi erano
significativamente diversi rispetto al basale (P <0,01).
Il parametro energia (relativo all’omogeneità della
pelle, è aumentato significativamente solo per
EE/DRSP a 6 mesi (P<0,05), con una tendenza
all’aumento solo per EE/CMA. Il parametro
superficie (relativo alla pelle liscia) è diminuito
significativamente (P<0,05) in entrambi i gruppi a 6
mesi rispetto al basale.
Per quanto riguarda l’acne, il punteggio ha mostrato
una significativa diminuzione (Figura 2, ) sia per
EE/DRSP che per EE/CMA a 3 e 6 mesi (P <0,01
rispetto al basale). Inoltre, a 3 mesi EE/DRSP era
significativamente più efficace e più rapido di EE/CMA
Le spirali con la tecnologia
a più alto livello al costo più basso
Multi-Safe®
CU 375
Neo-Safe® T
CU 380
Multi-Safe® CU 375 short
Per informazioni
e/o acquisto diretto:
[email protected]
www.mktpharma.it
tel 06 39746189
10
www.sicontraccezione.it
S.I.C. DONNA News
Effetto di due estroprogestinici contenenti etinilestradiolo 30 µg e drospirenone 3 mg ed etinilestradiolo
30 µg e clormadinone 2 mg sulle manifestazioni iperandrogeniche cutanee ed ormonali
Discussione
Il trattamento di donne iperandrogeniche con due
EP contenenti EE 30 µg + DRSP 3 mg e EE 30 µg +
CMA 2 mg per 6 mesi ha migliorato i segni e
sintomi clinici dell’aumentata azione androgena, dal
punto di vista sia cutaneo che ormonale.
La seborrea, l’acne e la crescita dei peli hanno
www.sicontraccezione.it
2
SEBORREA
diskin)
pelle)
SEBORRHEA(mcg/cm
(mcg/cm2 of
EE
mcg/DRSP 3 3mg
mg
EE 30
30mcg/DRSP
30 mcg/CMA 22mg
mg
EE 30mcg/CMA
EE
8000
6000
4000
2000
0
3
months
6
mesi
*p<0.01 vs baseline
^p<0.05
*p<0,01 vs.
basalefor EE/DRSP vs EE/CMA
*p<0,05 per EE/DRSP vs. EE/CMA
Values are expressed as mean and confidence interval 95%
i valori sono espressi come media ed intervallo di confidenza al 95%
Figure
1. Seborrheadurante
during the lo
study
Figura 1.
Seborrea
studio
EE
mcg/DRSP 33mg
mg
EE 30
30mcg/DRSP
punteggio
dell’ACNE
2 of skin)
SEBORRHEA
(mcg/cm
nel ridurre il punteggio dell’acne (P<0,05), anche se è
stato poi raggiunto un valore simile a 6 mesi.
Il punteggio di Ferriman-Gallwey è diminuito
durante lo studio (Figura 3), con una tendenza a 3
mesi ed una significativa riduzione a 6 mesi (P <0,01
rispetto al basale per entrambi i gruppi). A 6 mesi,
vi era una significativa differenza fra EE/DRSP e
EE/CMA ed il primo prodotto mostrava una
diminuzione più importante del punteggio (P<0,05
per EE/DRSP rispetto a EE/CMA).
L’androstenedione (A) ha mostrato una significativa
riduzione con l’andar del tempo (P <0,01 rispetto
al basale) per entrambi i gruppi, anche se si è avuto
un maggior effetto con EE/ DRSP che con EE/CMA
(P<0,05) a 3 e 6 mesi.
Anche il DHEAS è diminuito con l’andar del tempo,
ma la significatività statistica per entrambi i gruppi
rispetto al basale veniva raggiunta a 6 mesi di
trattamento; P <0,01 per entrambi i gruppi rispetto
al basale).
Il testosterone totale (T) era ridotto durante il
trattamento ormonale con entrambi i composti (P
<0,01 rispetto al basale a 3 e 6 mesi). A 3 mesi di
trattamento si è avuto un effetto significativamente
maggiore nella diminuzione dei livelli di T con
EE/DRSP (P <0,01 per EE/DRSP rispetto a
EE/CMA); questa differenza era invariata a 6 mesi di
osservazione (P <0,01 fra trattamenti) (Figura 4).
La SHBG è aumentata con entrambi i trattamenti
EP durante l’osservazione; P <0,01 rispetto al
basale a 3 e 6 mesi per entrambi gli EP); in
particolare, a 3 mesi si è avuta una tendenza
maggiore (ma non significativa) all’aumento di
SHBG con l’EE/DRSP rispetto all’EE/CMA.
Il “free androgen index” (indice androgeno libero)
era significativamente diminuito durante il
trattamento a 3 e 6 mesi rispetto al basale (P
<0,01) con entrambi i trattamenti. A 3 mesi,
EE/DRSP ha ridotto il FAI più di EE/CMA rispetto
al basale (P <0,05 fra trattamenti), senza differenze
significative fra i due gruppi a 6 mesi.
EE 30mcg/CMA
30 mcg/CMA 2mg
2 mg
EE
8000
6000
4000
2000
0
3
months
mesi
6
*p<0.01 vs baseline
*p<0,01 vs. basale
^p<0.05 for EE/DRSP vs EE/CMA
*p<0,05 per
EE/DRSP vs. EE/CMA
arecome
expressed
ased
mean
and confidence
interval
i valori sono Values
espressi
media
intervallo
di confidenza
al 95%
95%
Figura 2.
Punteggio
durante lo
Figure
1. Seborrhea dell’acne
during the study
studio.
11
S.I.C. DONNA News
Effetto di due estroprogestinici contenenti etinilestradiolo 30 µg e drospirenone 3 mg ed etinilestradiolo
30 µg e clormadinone 2 mg sulle manifestazioni iperandrogeniche cutanee ed ormonali
18
EE
mcg/DRSP 33mg
mg
30mcg/DRSP
EE 30
EE30mcg/CMA
30 mcg/CMA 2mg
2 mg
EE
FG score
Punteggio FG
16
14
12
10
8
0
3
months
mesi
6
*p<0.01 vs baseline
*p<0,01 vs. basale
^p<0.05 for EE/DRSP vs EE/CMA
*p<0,05 per EE/DRSP vs. EE/CMA
Values
are expressed
as mean
and confidence
intervalal95%
i valori sono
espressi
come media
ed intervallo
di confidenza
95%
Figure 3. Ferryman-Gallwey during the study
Figura 3. Punteggio di Ferryman-Gallwey
durante lo studio.
18
EE
mcg/DRSP 33mg
mg
EE 30
30mcg/DRSP
EE30mcg/CMA
30 mcg/CMA 2mg
2 mg
EE
T score
(nmoli/L)
FG
16
14
12
10
8
0
3
months
mesi
6
*p<0.01 vs baseline
*p<0,01 vs.^p<0.05
basale for EE/DRSP vs EE/CMA
*p<0,05 per EE/DRSP vs. EE/CMA
Values
are expressed
as mean
confidence
interval 95%
i valori sono
espressi
come media
ed and
intervallo
di confidenza
al 95%
Figure 3. Ferryman-Gallwey during the study
12
Figura 4. Livelli di T durante lo studio.
mostrato un significativo miglioramento con
l’andar del tempo con entrambi i trattamenti, ma
EE/DRSP era più potente dell’EE/CMA nel
migliorare questi parametri. La diminuzione più
importante della seborrea con EE/DRSP può
spiegare in parte il migliore effetto sull’acne.
Inoltre, l’acne era diminuita in misura maggiore
dall’EE/DRSP in confronto all’EE/CMA, come si è
verificato per il T e per il FAI, che è un marker di
androgenizzazione [1]. La diminuzione del sebo
cutaneo, come la riduzione del punteggio dell’acne
e del punteggio di Ferriman-Gallwey sono dovute
alla diminuzione dei livelli di androgeni e dell’azione
sulla pelle, come risultato della diminuita
produzione di androgeni, da un lato, e
dell’aumentata produzione di SHBG dall’altro lato.
Sotto questo aspetto, è importante ricordare
l’effetto sinergico fra componente estrogena e
progestinica dell’EP nel trattare le manifestazioni
iperandrogeniche. A tale scopo, l’azione antiandrogena di un progestinico può essere molto
importante da un punto di vista clinico. Il DRSP è
un progestinico derivato dallo spironolattone, con
importanti proprietà anti-mineralocorticoidi e
anti-androgene [13]; la potenza anti-androgena del
DRSP è circa un terzo di quella del ciproterone
acetato [14,15] ed è maggiore di quella dello
spironolattone [15]. Anche il CMA ha un effetto
antiandrogeno, come riferito in diversi lavori
[9–11].
Un
effetto
simile
sulle
manifestazioni
iperandrogeniche è stato segnalato in uno studio
comparativo con EP orali contenenti EE 30 µg +
DRSP 3 mg e EE 35 µg + CPA 2 mg [8]. Inoltre, un
altro studio ha segnalato che l’EE/DRSP era efficace
almeno come l’EE/CPA nel trattare l’irsutismo [16].
Questo è un punto di interesse molto importante
nella pratica clinica e nella farmacologia clinica,
perché questi studi hanno dimostrato una
sovrapposizione nell’attività antiandrogena fra
questi EP contenenti o DRSP o ciproterone
acetato, quest’ultimo è il progestinico
antiandrogeno più potente [10,17]. Inoltre, è stato
segnalato in passato che il DRSP ha un effetto
antiandrogeno maggiore del CMA [18]. Questi dati
potrebbero spiegare i risultati di questo studio, in
cui il composto contenente EE/DRSP era più
efficace dell’EE/CMA nel migliorare le
manifestazioni androgene cutanee e nel ridurre i
www.sicontraccezione.it
S.I.C. DONNA News
Effetto di due estroprogestinici contenenti etinilestradiolo 30 µg e drospirenone 3 mg ed etinilestradiolo
30 µg e clormadinone 2 mg sulle manifestazioni iperandrogeniche cutanee ed ormonali
livelli (A, T) e l’attività degli androgeni (espressi
come FAI).
Come per altri parametri cutanei valutati in questo
studio, l’aumento del parametro corneometria
(reperto che indica un miglioramento della salute
della pelle), relativo all’idratazione della pelle,
suggerisce che la stimolazione estrogena
dell’organismo con gli EP, in maggior misura se
associati ad una riduzione della concentrazione e/o
della funzione degli androgeni, possa migliorare il
grado di idratazione cutanea. Questo effetto è
probabilmente dovuto ad un’azione estrogena sui
glicosaminoglicani (e sui mucopolisaccaridi acidi) e,
particolarmente, sulla sintesi dell’acido ialuronico
nella pelle; questi composti sono in grado di
aumentare il contenuto cutaneo d’acqua sotto
stimolazione estrogena [19–21]. Anche dallo stesso
punto di vista potrebbe essere considerata la
riduzione della TEWL (relativa all’evaporazione),
perché una riduzione della TEWL dimostra una
migliore condizione della pelle.
L’aumento del parametro energia (relativo
all’omogeneità della superficie cutanea), associato
alla diminuzione del volume (relativo alla
profondità del microrilievo della pelle, una
diminuzione che indica un miglioramento delle
condizioni della pelle), dimostra ulteriormente
come il trattamento con EP possa migliorare, oltre
al pattern ormonale e alle classiche manifestazioni
associate ad uno squilibrio iperandrogenico
(seborrea, acne, ecc.), anche l’aspetto complessivo
e la qualità della pelle, aumentando l’idratazione e
migliorando le caratteristiche della superficie della
pelle. Sembra importante ricordare che le
manifestazioni cliniche dell’iperandrogenismo, oltre
ad essere un marker dello squilibrio ormonale,
costituiscono la base di un profondo malessere
psicologico per i soggetti interessati [2,3].
Il trattamento con EP, e particolarmente con EP
contenenti progestinici con azione antiandrogena,
ci consente di migliorare l’aspetto della pelle
cambiando l’equilibrio ormonale verso una
condizione più estrogena (come è dimostrato dalla
diminuzione dei livelli di FAI), con importanti effetti
benefici sulla qualità della vita di pazienti affette da
iperandrogenismo. Sotto questo aspetto, i
composti contenenti EE/DRSP sembrano
clinicamente più adatti dell’EE/CMA.
Bibliografia
Bibliografia
1.
10. Raudrant D, Rabe T. Progestogens with antiandrogenic properties. Drugs
2003;63:463-492.Bibliografia
11. Zahradnik HP. Belara a reliable oral contraceptive with additional benefits for
health and efficacy in dysmenorrhea. Eur J Contracept Reprod Health Care
2005;1:12-18.
12. Ferriman D, GallweyJD. Clinical assessment of body hair growth in women. J Clin
Endocrinol Metab 1961 ;2l :1440-1447,
13. Oelkers WH. Drospirenone in combination with estrogens: for contraception and
hormone replacement therapy. Climacteric 2005;3:15-27.
14. Rowlands S. Newer progestogens, J Fam Plann Reprod Health Care 2003;29:13 16.
15. Elger W, Beier S, Pollow K, Garfield R, Shi SQ, Hillisch A. Conception and
pharmacodynamic profile of drospirenone. Steroids 2003;68:891-905.
16. Batukan C, Muderris H, Ozcelik B, Ozturk B, Ozturk A. Comparison of two oral
contraceptives containing either drospirenone or cyproterone acetate in the
treatment of hirsutism, Gynecol Endocrinol 2007;23:38-44,
17. Kuhl H. Pharmacology of estrogens and progestogen a: influence of different routes
of administration. Climacteric 2005; 8 (suppl 1): 3 63.
18. Schneider HP. Androgens and antiandrogens. Ann NY Acad Sci 2003;997:292 306.
19. Grosman N, Hvidberg E, Schou J. The effect of oestrogenic treatment on the acid
mucopolysaccaride pattern in skin of mice. Acta Pharmacol Toxicol 1971;30:458 464.
20. Uzuka M, Nakajima K, Ohta S, Mori Y. The mechanism of estrogen-induced increase
in hyaluronic acid biosynthesis, with special reference to estrogen receptor in the
mouse skin. Biochim Biophys Acta 1980;627:199-206.
21. Pierard-Franchimond C, Letane C, Goffin V, Pierard GE. Skin water-holding capacity
and transdermal estrogen therapy for menopause: a pilot study. Maturitas 1995;22:
151-154.
2.
3.
4.
5.
6.
7.
8.
9.
Hatch R, Rosenfield RL, Kim MH, Tredway D. Hirsutism: implications, etiology, and
management. Am J Obstet Gynecol 1981;140:815-830.
Elsenbruch S, Hahn S, Kowalsky D, Offner AH, Schedlowski M, Mann K, Jannsen OE.
Quality of life, psychosocial well-being, and sexual satisfaction in women with
polycistic ovary syndrome, J Clin Endocrinol Metab 2003;88:5801 5807,
Hahn S, Janssen OE, Tan S, Pleger K, Mann K, Schedlowski M, Kimmig R, Benson S,
Balamitsa E, Elsenbruch S, Clinical and psychological correlates of quality-of-life in
polycystic ovary syndrome, Eur J Endocrinol 2005;153:853 860,
Lee AT, Zane LT, Dermatologic manifestations of polycystic ovary syndrome. Am J
Clin Dermatol 2007;8:201-219.
Guido M, Romualdi D, Giuliani M, Suriano R, Selvaggi L, Apa R, Lanzone A.
Drospirenone for the treatment of hirsute women with polycystic ovary
syndrome: a clinical, endocrino¬logical, metabolic pilot study. J Clin Endocrinol
Metab 2004;89:2817-2823.
Muhn P, Fuhrmann U, Fritzemeier KH, Krattenmacher R, Schillinger E.
Drospirenone: a novel progestogen with antimineralocorticoid and antiandrogenic
activity. Ann NY Acad Sci 1995;761:311 335.
Muhn P, Krattenmacher R, Beier S, Elger W, Schillinger E. Drospirenone: a novel
progestogen with antimineralocorticoid and antiandrogenic activity.
Pharmacological characterization in animal models. Contraception 1995;51:99-110.
van Vloten WA, van Haselen CW, van Zuuren EJ, Gerlinger C, Heithecker R. The
effect of 2 combined oral contraceptives containing either drospirenone or
cyproterone acetate on acne and seborrhea. Cutis 2002;69:2-15.
Schramm G, Steffens D. A 12-month evaluation of the CMA-containing oral
contraceptive Belara: efficacy, tolarebility and antiandrogenic properties.
Contraception 2003;67:305 312.
www.sicontraccezione.it
13
S.I.C. DONNA News
articoli s cientifici
Da: “Effect of an oral contraceptive with
Chlormadinone acetate on depressive mood”
(1)
Johannes C . Huber (1), Marie- Luise S. Heskamp (2) and Georg A.K. Schramm (2)
Department of Gynaecology and Obstetrics, Division of Gynaecological Endocrinology and Reproductive
Medicine, University of Vienna, Austria
(2)
Medical Department, Grunenthal GmbH, Aachen, Germany
M
olte donne in età riproduttiva sono
soggette a frequenti ed importanti disturbi
dell’umore, (irritabilità e nervosismo,
eccitabilità ed ansia), soprattutto in particolari
momenti della loro vita, quali il periodo
premestruale, il puerperio e la perimenopausa.
Accanto a disturbi psichiatrici più rilevanti, un
elevato, benché sottostimato, numero di donne
soffre periodicamente di variazioni emozionali
come labilità affettiva (improvvisi sbalzi di umore),
pessimismo, insoddisfazione, voglia di piangere,
difficoltà a concentrarsi, disturbi del sonno,
tensione, rabbia e sensazioni di oppressione e di
essere fuori controllo. Sebbene non definita da una
precisa patologia, tale sintomatologia, più
generalmente definita come “disturbi dell’umore”,
è spesso associata ad una considerevole riduzione
della qualità di vita.
La ricerca nel campo della farmacologia molecolare
ha dimostrato che gli steroidi ovarici possono
interagire con il Sistema Nervoso Centrale (SNC):
in generale, l’estradiolo è associato ad un effetto
stimolatorio ed il progesterone ad un effetto
inibitorio sulle attività neuronali. In particolare, il
progesterone ha mostrato esercitare effetti
stabilizzanti l’umore, effetti ansiolitici, anestetici ed
antiepilettici.
Tali effetti positivi sull’umore sono mediati
in gran parte dai suoi metaboliti neuroattivi
3-α-ridotti (allopregnanolone ed epipregnanolone),
attraverso la modulazione del recettore
dell’acido γ-ammino-butirrico (GABAA), uno dei
principali recettori inibenti del SNC (ovvero
l’attivazione del recettore GABAA risulterebbe in
effetti ansiolitici, antiepilettici, sedativi e bilancianti
l’umore).
È noto come il periodo terminale della fase
luteale di un ciclo ovulatorio (periodo
premestruale), proprio quando i disturbi
dell’umore si fanno spesso più severi, sia
caratterizzato dall’abbassamento dei livelli di
progesterone. Studi in donne affette da sindrome
premestruale e da destabilizzazione dell’umore
14
hanno rilevato bassi livelli di allopregnanolone: è
stato dunque ipotizzato che la brusca caduta dei
livelli di progesterone immediatamente prima della
mestruazione possa essere associata alla riduzione
dell’effetto ansiolitico e bilanciante l’umore del
recettore GABAA.
Ad oggi, solo pochi studi hanno indagato gli effetti
del trattamento con contraccettivi orali (CO), ed
in particolare della componente progestinica, sulle
funzioni psico-fisiologiche. Da un lato, alcuni
contraccettivi orali combinati (COC) monofasici
sono stati associati a labilità affettiva, ansietà e ad
altri sintomi depressivi. Dall’altro, gli steroidi ovarici
sono stati valutati come trattamenti efficaci in caso
di umore depresso.
I progestinici utilizzati nei COC comprendono
molecole diverse: sia molecole di sintesi derivate
dal 17α-idrossi-progesterone (clormadinone
acetato [CMA], ciproterone acetato e medrossiprogesterone acetato), sia i derivati del 19nortestosterone (levonorgestrel, desogestrel,
norgestimate e gestodene) sia i derivati dello
spirolattone (drospirenone).
Alcuni Autori sottolineano come gli effetti avversi
sull’umore esercitati dai COC in alcune donne
possano essere associati all’uso di progestinici
derivati dal testosterone. Le varie molecole
progestiniche differiscono molto fra loro in termini
di effetti biologici, e di questo andrebbe tenuto
conto quando si prescrive la terapia con COC.
In particolare, i diversi progestinici possono
esercitare effetti molto variabili sul SNC. Vi è ad
esempio una forte evidenza clinica dell’effetto
sull’umore indotto dalla somministrazione di CMA.
In particolare, sono stati analizzati 4 studi
osservazionali, non-interventistici, prospettici che
hanno coinvolto circa 50.000 donne, trattate con il
COC a base di 30 mcg di EE e 2 mg di CMA
(Belara®) assunto sia in regime tradizionale di 28
giorni, che in regime continuato, per 4, 6 o 12 cicli.
I dati clinici ottenuti, confermano l’effetto positivo
dell’assunzione di questa pillola sul benessere
emotivo e sui cambiamenti d’umore.
www.sicontraccezione.it
S.I.C. DONNA News
Da: ”Effect of an oral contraceptive with Chlormadinone acetate on depressive mood”
Il miglioramento dell’umore depresso è stato infatti
documentato sia dopo 4, che dopo 6 e 12 cicli di
trattamento con tale associazione contraccettiva.
Gli Autori ipotizzano differenti meccanismi
d’azione con i quali CMA possa esplicare i suoi
effetti sui disturbi dell’umore.
In particolare vi sono evidenze che suggeriscono
una interazione di CMA con il sistema nervoso
centrale attraverso metaboliti neuroattivi, quali
l’allopregnanolone e l’epipregnanolone. Un recente
studio condotto su ratti fertili e ovarectomizzati,
ha mostrato come la somministrazione di CMA sia
in grado di determinare un significativo aumento
dei livelli di allopregnanolone nell’area
dell’ippocampo e al contempo di favorire la
benefica azione dell’estrogeno a livello di
ippocampo, ipotalamo e ghiandola pituitaria
anteriore.
Questo ed altri modelli teorici sono effettivamente
supportati da una consistente evidenza clinica.
È chiaro come sia necessario investigare
ulteriormente tali ipotesi, così come valutare altri
possibili meccanismi. Studi preclinici sono
attualmente in corso, e tale tipo di ricerca si rende
necessaria per raggiungere nuove prospettive nella
comprensione dei trattamenti farmacologici dei
disturbi dell’umore, un problema diffuso ed ancora
tanto sottostimato nelle donne in età riproduttiva.
Bibliografia
R
•
•
•
•
•
Huber JC, Heskamp MLS, Schramm G. Effect of an oral contraceptive with
chlormadinone acetate on depressive mood. Clin Drug Invest 2008; 28 (12):
783-91.
Schramm G, Heckes B. Switching hormonal contraceptives to a chlormadinone
acetate-containing oral contraceptive. The Contraceptive Switch Study.
Contraception 2007; 76 (2): 84-90.
Schramm G, Steffens D. Contraceptive efficacy and tolerability of chlormadinone
acetate 2mg/ethinylestradiol 0.03mg (Belara®). Clin Drug Invest 2002; 22 (4): 221-31.
www.sicontraccezione.it
•
Bock K, Heskamp ML, Schramm G. Influence of chlormadinone acetate on
dysmenorrhoea and other cycle-related complaints [in German]. Gyne 2008; 8: 219-25.
Schramm G, Steffens D. A 12-month evaluation of the CMA-containing oral
contraceptive Belara®: efficacy, tolerability and anti-androgenic properties.
Contraception 2003 Apr; 67 (4): 305-12.
Lenzi E, Begliuomini S, Pluchino M, et al. Effect of chlormadinone acetate
administration on central and peripheral allopregnanolone in OVX rats. Gynecol
Endocrinol 2008; 24 Suppl. 1: OP227.
15
Si consiglia l’uso di
1 capsula 2 volte al giorno
(pari a 200 mg di Lattoferrina)
preferibilmente lontano dai pasti
INDICAZIONI:
La Lattoferrina è una glicoproteina in grado di legare
e trasportare il ferro. L’assunzione di Lattoferrina può
essere utile per il fisiologico miglioramento del
metabolismo del ferro specie nei casi di carenze
riconducibili a cattiva alimentazione o situazioni di
aumentato fabbisogno di ferro
S.I.C. DONNA News
articoli s cientifici
Dispositivi contraccettivi intrauterini:
un aggiornamento
Demetrio Costantino (1), Claudia Guaraldi (2)
(1)
Azienda USL Ferrara, (2) Ospedale di Valdagno (VI)
I
dispositivi contraccettivi intrauterini (IUD)
hanno un’origine molto lontana nel tempo:
derivano da osservazioni in campo veterinario
in cui si era notato che introducendo corpi
estranei nell’utero di animali si determinava una
sterilità temporanea. Solo però dal 1920 inizia una
sua storia documentabile in campo umano che lo
renderanno sempre più piccolo confortevole ed
efficace.
Tipi­di­IUD­e­meccanismo­d’azione
Le prime spirali erano non medicate ed erano
costituite esclusivamente da quel supporto plastico
che oggi è solo una parte dello IUD; queste spirali
sono state poi soppiantate dalle spirali attuali,
infatti esistono fondamentalmente due tipi di IUD:
la IUD al rame e la IUD medicata al progesterone.
Sono metodi contraccettivi validi ed efficaci,
prontamente reversibili, e hanno come grande
vantaggio la lunga durata d’azione (anni), la non
influenza sul rapporto sessuale, il fatto che la donna
non deve ricordarsi di assumere giornalmente
medicinali e la assenza di utilizzo di sostanze
ormonali nel caso della spirale al rame.
Da non dimenticare che, a parte il costo iniziale
che può essere anche abbastanza alto nel caso di
spirali medicate, il lungo periodo di utilizzo
comunque lo rende un metodo economico e a
basso costo per il controllo delle nascite.
Per quanto riguarda l’efficacia l’OMS la classifica
come metodo molto efficace quando impiegato
correttamente e regolarmente, con un numero di
gravidanze di 0,6/100 donne nei primi dodici mesi
di impiego.
Lo IUD al rame è costituito da un supporto
plastico attorno a cui è avvolto un filo di rame ed
ha di solito una forma a T o con 2 braccia che
consentono al dispositivo di rimanere ben
posizionato all’interno dell’utero.
Spesso è presente un core di argento che permette
un maggior rilascio di rame all’interno dell’utero.
Hanno una durata che va dai 3 ai 10 anni a seconda
del tipo di spirale.
www.sicontraccezione.it
L’effetto contraccettivo della spirale al rame è
legato al fatto che la sua presenza all’interno
dell’utero crea uno stato di flogosi sterile che
riduce la mobilità degli spermatozoi ed ha un
effetto spermicida, aumentato dagli ioni rame che
vengono rilasciati all’interno dell’utero e inoltre
viene così creato un ambiente intrauterino ostile
all’impianto. L’efficacia contraccettiva sembra legata
alla superficie di rame presente, che deve essere
> 250mm2.
La IUD medicata al progesterone invece, è
costituito da una struttura in polietilene a forma di
T impregnata con bario solfato.
È un sistema contraccettivo ormonale locale: l’asta
verticale è circondata da un cilindro contenente
una miscela di poliidrossimetilsilossano e
levonorgestrel (LNG).
Il cilindro è ricoperto da una membrana
semipermeabile di polidimetilsilossano,che regola il
rilascio di LNG nella cavità uterina (20 mcg/die).
Il suo effetto contraccettivo è mediato perciò
anche dal rilascio di progestinico in sede
intrauterina: oltre ad inibire la motilità e
funzionalità degli spermatozoi, ne impedisce il
passaggio rendendo più viscoso e impenetrabile il
muco cervicale, crea atrofia endometriale, inibisce
l’ovulazione nel 5-15% dei casi. Riduce la finestra di
fertilizzazione attivando la glicodelina A.
La sicurezza contraccettiva sembra superiore alla
IUD al rame (0,14/100 donne/anno come tasso di
errore con un tasso a 5 anni di 0.7/100 donne).
Il ritorno alla fertilità con gli IUD medicati al
progesterone è sovrapponibile a quello per gli IUD
al rame senza alcuna differenza anche se
confrontati con i tassi di fertilità di chi non ha
utilizzato nessun metodo contraccettivo o i
contraccettivi orali.
In Gran Bretagna esiste poi un tipo di spirale al
rame costituito da un filo di sutura non
biodegradabile 00 in polipropilene sul quale sono
infilati sei piccoli cilindri di rame, per una lunghezza
totale di 3 cm, che procurano una superficie totale
di 330mm2 , il cilindro superiore ed inferiore sono
fissati sul filo in modo da trattenere anche i quattro
17
S.I.C. DONNA News
Dispositivi contraccettivi intrauterini: un aggiornamento
cilindri restanti, e la struttura in assenza del
supporto plastico sembra permettere un’ampia
mobilità in tutte le direzioni. Il fissaggio avviene
posizionando il nodo del filo di sutura che
costituisce la spirale nel contesto del miometrio
fundico con un apposito strumento ad uncino.
Queste caratteristiche di ancoraggio e l’assenza del
supporto plastico permetterebbero di diminuire il
tasso di espulsioni spontanee e gli effetti collaterali
della stessa, con un tasso di gravidanza annuo
intorno allo 0,2%. In realtà in letteratura esistono
dati che dimostrano che la difficoltà di inserimento
di questo tipo di spirale produce tassi di espulsione
paragonabili ad altri dispositivi, e un non sostanziale
miglioramento del sanguinamento uterino (che è
legato al rame) e del dolore pelvico.
Controindicazioni,­ effetti­ collaterali­ dello
IUD,­ e­ benefici­ non­ contraccettivi­ dello
iud­medicato­al­progesterone
Le controindicazioni assolute all’inserimento dello
IUD sono diverse: gravidanza in atto, anomalie
morfologiche dell’utero che deformino la cavità
compresi i fibromi uterini, una allergia al rame o la
malattia di Wilson per le spirali al rame, sospetta
neoplasia uterina o sanguinamenti uterini anomali
non indagati. L’anemia grave, la metrorragia e le
menometrorragie
risultano
essere
controindicazioni all’inserimento dello IUD al rame
perché quest’ultimo può avere come effetto
collaterale un aumento del flusso mestruale e
quindi aumentare il problema. Discorso diverso va
invece fatto per lo IUD medicato al progesterone
che è invece indicato per la riduzione e la cura di
queste problematiche. Infatti la forte azione
antiestrogenica del levonorgestrel all’interno
dell’utero impedisce l’azione degli estrogeni
producendo una forte azione antiproliferativa ed
una soppressione endometriale tanto da portare a
soppressione del bleeding, ipomenorrea fino
all’amenorrea nel 20% dei casi. In questo senso
quindi la spirale al progesterone presenta un
importante indicazione terapeutica per il
trattamento medico delle meno-metrorraggie.
Stesso dicasi per l’endometriosi e la dismenorrea
ad essa collegata nonché per l’adenomiosi ed il
sanguinamento ad essa correlato: mentre per la
spirale al rame questi sintomi potrebbero essere
esacerbati, con la spirale medicata al progesterone,
questo problema non esiste, anzi può essere
18
considerata una sua indicazione terapeutica.
Un altro capitolo molto importante che riguarda la
IUD è quello relativo a IUD e PID. Sicuramente una
controindicazione assoluta all’inserimento dello
IUD è una PID in atto o recente (negli ultimi 3
mesi) una endometrite post partum ed un aborto
settico, poiché la presenza dello IUD può aggravare
lo stato con il perpetuarsi dell’infezione ed una sua
recidiva; inoltre poiché non è la spirale per la
presenza dei fili ma il suo inserimento a portare
l’infezione nelle salpingi, controindicazione assoluta
sono anche le infezioni sessualmente trasmesse
(IST) non trattate (chlamydia, neissera trichomonas,
lue), che potrebbero portare ad una PID, la TBC
genito-urinaria e l’immunosoppressione cronica
anche da HIV per il rischio maggiore di infezioni.
D’altro canto però non è raccomandato l’esame
batteriologico di routine prima dell’inserimento
dello IUD né la profilassi antibiotica se non in
gruppi particolarmente a rischio per IST (OMS).
Una recente Cochrane review del 2008 ha
dimostrato che la profilassi con antibiotico
(doxiciclina o azitromicina) non dava un
significativo beneficio, ed inoltre, dato a nostro
avviso molto più importante per sfatare questo
mito, è che il rischio di infezioni in generale
associate allo IUD era veramente basso
indipendentemente dalla profilassi antibiotica.
Se si verificano episodi infettivi dopo l’inserimento
dello IUD, questi si verificano nel primo mese e
quindi particolare attenzione deve fare la donna ai
sintomi dolorosi associati a malessere e febbre
dopo l’inserimento del dispositivo contraccettivo
intrauterino.
Considerato, quindi, il basso rischio di incidenza di
PID, non è più controindicato l’inserimento dello
IUD nelle nullipare, questo può essere solo un
poco più difficoltoso dato le caratteristiche del
collo uterino delle nullipare.
Va ricordato inoltre che lo IUD al progesterone
oltre agli effetti terapeutici legati allo ormone in
esso contenuto, ha minore incidenza di PID e di
GEU dello IUD al rame.
Un corretto training dell’operatore ed una
corretta scelta del momento per l’inserimento
(fine del ciclo mestruale, dopo un aborto del 1°
trimestre, dopo almeno 6 settimane dal parto)
possono ridurre al minimo fino ad eliminarli, i rischi
di lesione legati alla procedura, il disconfort della
paziente, i rischi di reazione vagale.
Non è raccomandata né anestesia né altra
www.sicontraccezione.it
S.I.C. DONNA News
Dispositivi contraccettivi intrauterini: un aggiornamento
premedicazione per l’inserimento dello IUD, tranne
la profilassi antibiotica in caso di valvulopatia cardiaca
per la profilassi dell’endocardite.
Lo IUD al rame rimane un metodo contraccettivo
importante nelle donne che presentano rischi
cardiovascolari, tromboembolici, nelle obese,
fumatrici, dislipidemiche
o con patologie
endocrine quali il diabete o patologie correlate agli
ormoni femminili (es Ca mammario) pur
emergendo ormai che il levonorgestrel rilasciato
all’interno dell’utero ha un minimo impatto
metabolico sistemico: comunque per la maggior
parte di queste donne se la spirale con rame ricade
nella categoria 1 dell’OMS (senza limitazione
d’uso), lo IUD al progesterone per la maggior parte
ricade nella categoria 2 (i benefici della
contraccezione sono superiori al rischio teorico o
dimostrato).
D’altronde lo IUD è un metodo molto importante
durante l’allattamento, e anche lo IUD al
progesterone può essere utilizzato attendendo
però 6 settimane dopo il parto.
Conclusioni
Ancora ulteriori studi dovranno chiarire il ruolo
che lo IUD al progesterone ricoprirà soprattutto
nel campo della terapia medica dei disturbi
ginecologici, e altri dovranno chiarire come si
potranno ridurre gli effetti collaterali delle IUD al
rame per aiutarne la compliance, peraltro alta,
magari modificandone la forma e i supporti.
A tutt’oggi lo IUD è un ottimo metodo
contraccettivo reversibile, di lunga durata, di costo
contenuto e dagli effetti collaterali sicuramente
molto limitati, i quali si sono dimostrati molto
meno frequenti e importanti di quanto sostenuto
in passato.
Una corretta anamnesi e selezione delle pazienti,
un corretto training nell’inserimento e una
adeguata aderenza ai controlli, riduce al minimo i
rischi di insuccesso della metodica, gli effetti
indesiderati e gli abbandoni dovuti agli effetti
collaterali dei dispositivi contraccettivi intrauterini.
Metodi contraccettivi
DISPOSITIVI INTRAUTERINI
Nome­Commerciale
Nova T 380
Mirena
Multiload CU 375
Ginefix
No Gravid
Gravigard
Mini Gravigard
Anticon 400
Anticon 300
Mini Anticon
Anticon Gold
Multi-Safe CU 375
Multi-Safe CU 375 short
Neo-Safe TCU 380
Durata­di­azione­in­anni
Azienda­Farmaceutica
Bayer Schering Pharma 5
Bayer Schering Pharma 5
5
Schering Plough
5
Rottapharm
3
Irmed
3
Spa
2
Spa
2
Uniderm
2
Uniderm
2
Uniderm
10
Uniderm
5
Eurim Pharm
5
Eurim Pharm
5
Eurim Pharm
Medicazione
Rame
LNG 750 mcg
Rame
Rame
Rame
Rame
Rame
Rame
Rame
Rame
Oro
Rame
Rame
Rame
Bibliografia
Bi
•
•
•
•
•
•
Criteri medici di eleggibilità per l’impiego di metodi contraccettivi; OMS, 2000, Ginevra.
Guida all’uso dei farmaci, AIFA, 2005.
H.Van Kets et al.; The GyneFix implant systems for interval, postabortal and
postpartum contraception: a significant advance in long term reversibile
contraception international study group on intrauterine drug delivery.The European
Journal of Contraception and reproductive Health Care; Vol.2, N°1, march 1997.
www.sicontraccezione.it
D.A. Grimes et al., Antibiotic prophylaxis for intrauterine contraceptive device
insertion (Review), The Cochrane Library, 2008, Issue 4.
D.A.Grimes et al. Cochrane Systematic reviews of IUD trials: lesson learned.
Contraception, 75 (2007) S55-S59
Kulier et al., Copper containing intra-uterine devices for contraception (Review);
The Cochrane Library, 2008,Iissue 4.
19
UNIVERSITÀ DEGLI STUDI DI MODENA
Dipartimento Clinico di Ginecologia e Ostetricia
in collaborazione con:
UNIVERSITÀ DEGLI STUDI DI NAPOLI FEDERICO II
Dipartimento di Scienze Ostetrico Ginecologiche,
Urologiche e Medicina della Riproduzione
Corso teorico-pratico
di isteroscopia operativa
Trattamento
isteroscopico
delle patologie
endouterine:
resettoscopia
o “office”?
Direttori del Corso:
C. Nappi, A. Volpe
15-16
ottobre
2009
modena
Policlinico di Modena
Istituto di Ginecologia Ostetricia
Aula 6° piano
Via del pozzo, 71
RICHIESTI I CREDITI ECM
Segreteria Organizzativa
U MKT Consulting
Via Cassia, 1110 – 00189 Roma
Tel. 0639746189 - Fax. 0645438292
[email protected]
www.mkt-consulting.it
◆ CORSI SIEOG 4/5 MAGGIO:
CORSO DI ECOGRAFIA PER OSTETRICHE
ROMA • 4 Maggio
CORSO DI NEUOROSONOLOGIA FETALE
ROMA • 4/5 Maggio
◆ SCUOLA PERMANENTE DI FORMAZIONE SU:
TERAPIE ORMONALI IN GINECOLOGIA ED
OSTETRICIA
direttori del Corso: V. de Leo, F. Petraglia
SiENA • 4/7 Ottobre
◆ 3° CONGRESSO NAZIONALE DELLA S.I.C.
(SOCIETÀ ITALIANA DELLA CONTRACCEZIONE)
Presidenti: A.Volpe, G.B. Melis, C. Nappi, G. Scarselli
1° CONGRESSO NAZIONALE DELLA S.M.I.C.
(SOCIETÀ MEDICA ITALIANA PER LA
CONTRACCEZIONE)
Presidenti: E. Arisi, R. Michieli, M. Orlandella
MOdENA • 7/9 Maggio
◆ CORSO TEORICO PRATICO DI ISTEROSCOPIA
OPERATIVA:
TRATTAMENTO ISTEROSCOPICO DELLE
PATOLOGIE ENDOUTERINE: RESETTOSCOPIA
O “OFFICE”?
direttori del Corso: C.Nappi, A. Volpe
MOdENA • 15/16 Ottobre
◆ CONGRESSO NAZIONALE DELLA FISS
(FEDERAZIONE ITALIANA DI SESSUOLOGIA
SCIENTIFICA)
Presidente: S.Caruso
TAORMiNA • 27/30 Maggio
◆ XIII WEEK-END CLINICO NAZIONALE SIdR
(SOCIETÀ ITALIANA DELLA RIPRODUZIONE)
Segreteria Scientifica: A. Cagnacci
CASTROCARO • 6/7 Novembre
◆ IV CORSO NAZIONALE DI FORMAZIONE
PERMANENTE SU:
TERAPIE ORMONALI IN GINECOLOGIA
direttori del Corso: A.Cianci, S. Caruso
CATANiA • 4/6 Giugno
◆ I° WORKSHOP SIFIOG
(SOCIETÀ ITALIANA DI FITOTERAPIA
ED INTEGRATORI IN OSTETRICIA
E GINECOLOGIA)
Presidente: F. Vicariotto
MiLANO • 27 Novembre
◆ 2° WORKSHOP NAZIONALE PER OSTETRICHE:
L’OSTETRICA NELLA GESTIONE
DELL’AMBULATORIO DELLA
GRAVIDANZA A BASSO RISCHIO
Presidente: E. Colosi
GROSSETO • 26 Giugno
◆ XII CONGRESSO NAZIONALE DELLA S.I.M.
(SOCIETÀ ITALIANA DELLA MENOPAUSA)
Presidente: C. Nappi
NAPOLi • 10/12 dicembre
◆ LE GRAVIDANZE MULTIPLE
Presidente: E. Colosi
GROSSETO • 25 Settembre
◆ VI CORSO DI COLPOSCOPIA E PREVENZIONE
GINECOLOGICA
Presidenti: M. Moscarini, A. Vecchione
ROMA • 18/19 dicembre
Per­informazioni­
MKT­Consulting • Phone: +39 06 39746189
e.mail: [email protected] • www.mkt-consulting.it