METABOLISMO
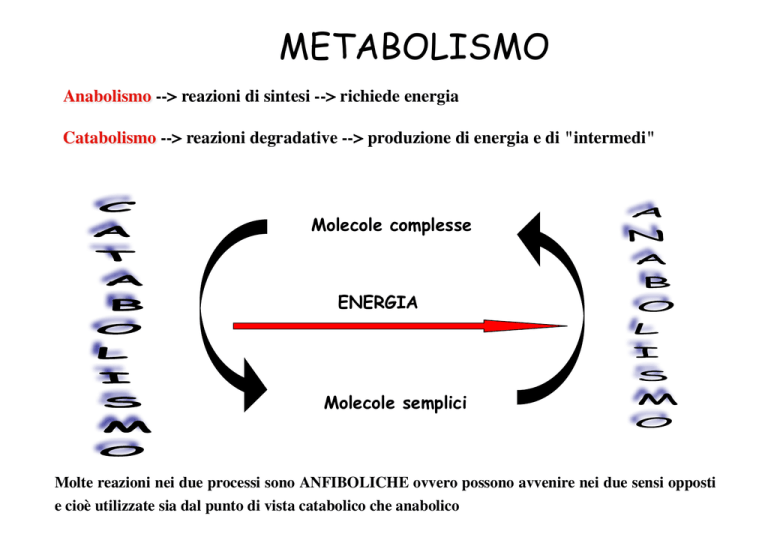
Anabolismo --> reazioni di sintesi --> richiede energia
Catabolismo --> reazioni degradative --> produzione di energia e di "intermedi"
Molecole complesse
ENERGIA
Molecole semplici
Molte reazioni nei due processi sono ANFIBOLICHE ovvero possono avvenire nei due sensi opposti
e cioè utilizzate sia dal punto di vista catabolico che anabolico
L’ENERGIA
L ’ energia è la capacità di compiere un lavoro, di effettuare delle trasformazioni
chimiche e tutto ciò che si “costruisce” in natura richiede energia
che lavori può compiere una cellula?
•lavoro chimico
•lavoro di trasporto
•lavoro meccanico
La fonte primaria di energia è la luce, che viene utilizzata dai fototrofi per produrre
materia organica che viene a sua volta utilizzata dai chemiotrofi.
I
chemiotrofi
ossidano
i
composti organici liberando CO2
utilizzata poi dai fototrofi
PRINCIPALI MODALITÀ DI METABOLISMO
MICROBICO
In natura non esiste alcuna molecola organica che non possa essere
degradata dai microrganismi (inclusi sughero, paraffina, gomma,
carburanti etc.)
H2,
NO2-,
NH4+,
S°,
H2S,
Fe2+
PRINCIPALI TIPI NUTRIZIONALI
FOTOAUTOTROFI:
LUCE COME SORGENTE DI ENERGIA
ANIDRIDE CARBONICA COME SORGENTE DI CARBONIO
FOTORGANOTROFI:
LUCE COME SORGENTE DI ENERGIA
COMPOSTI ORGANICI COME SORGENTE DI CARBONIO
CHEMIOLITOTROFI:
OSSIDAZIONE DI COMPOSTI INORGANICI RIDOTTI COME SORGENTE DI
ENERGIA
ANIDRIDE CARBONICA COME SORGENTE DI CARBONIO
CHEMIORGANOTROFI:
ENERGIA E CARBONIO DA FONTI ORGANICHE
Velocità delle reazioni di sintesi nei batteri può essere molto elevata
(Escherichia coli per esempio è in grado di compiere una generazione ogni 20-30 minuti)
Microrganismi e gli organismi superiori --> differenze a livello di catabolismo
Le reazioni cataboliche producono composti contenenti legami ad alto valore energetico
La molecola chiave nel trasporto dell'energia: adenosina trifosfato (ATP)
Altri composti ad alta energia:
ATP
Anabolismo
Catabolismo
Enolpiruvati, Aminoaciladenilati
Lavoro Meccanico
Trasporto Attivo
ADP + Pi
nucleosidi 5'-trifosfati: UTP, GTP, CTP
Acetil-Coenzima A
ATP --> ADP + Pi + 7.3 Kcal.
ATP + X --> ADP + X-P
L’ATP si forma dall’energia rilasciata/prodotta durante processi come la respirazione
aerobica, la respirazione anaerobica, la fermentazione, la fotosintesi la
fototrasduzione. La sua idrolisi ad ADP e fosfato rende possibile il lavoro chimico, di
trasporto e meccanico
ATP
L’ATP (Adenosina-5’-trifosfato) è una molecola fondamentale nei processi metabolici e
rappresenta un sito di accumulo di energia facilmente spendibile
L’idrolisi di questa molecola, con la liberazione di un gruppo P, libera energia che si rende
disponibile per compiere lavoro
Gran parte delle reazioni chimiche sono caratterizzate da un equilibrio tra
reagenti e prodotti tale equilibrio può essere spostato verso i reagenti o
verso i prodotti a seconda della variazione dell ’ energia libera (DG)
associata alla reazione
Molte
delle
reazioni
svolte
nelle
cellule
sono
endoergoniche
e
non
arriverebbero a termine senza un intervento energetico esterno
L’idrolisi dell’ATP è un processo fortemente esoergonico che può quindi
spingere a termine una reazione endoergonica che avviene simultaneamente
Equilibrio
spostato a
sinistra
Equilibrio
spostato a
destra
Ecco definito il ruolo di “moneta di scambio
energetico” svolto dall’ATP
Si forma in seguito a processi che fissano e
liberano
energia
(Fotosintesi,
Fermentazione, Respirazione) e la sua
idrolisi (esoergonica) viene utilizzata per
portare a termine reazioni endoergoniche
fondamentali per la cellula
Sintesi dell’ATP
Le variazioni di energia sono anche associate a reazioni di OSSIDORIDUZIONE e al movimento (flusso) di elettroni
Nelle red-ox gli elettroni si spostano da un donatore (agente riducente) ad un
accettore (agente ossidante)
La costante di equilibrio delle reazioni red-ox è il potenziale di riduzione (E0)
…minore è il valore di E0 (<0) per una reazione di riduzione e maggiore sarà
l’attitudine del riducente e trasferire elettroni
Il trasferimento di elettroni secondo gradiente di E0 porta alla produzione
di energia
il trasportatore più comune di elettroni è il NAD (nicotinammide adenina
dinucleotide)
la coppia NAD+/NADH ha un E0= -0.32 volt (molto negativo)
Le ossidazioni biologiche
Molte delle reazioni biochimiche sono delle reazioni di ossido-riduzione
Ossidazione --> perdita di e- o di H --> Energia
Riduzione --> acquisizione di e- o di H
+ 2H
Acido piruvico
Acido lattico
- 2H
Nel metabolismo cellulare il trasferimento di H da una molecola all'altra viene operata da coenzimi
che vengono ciclicamente ossidati e ridotti:
pirimidinici: nicotinamide-adenina-dinucleotide (NAD+)
nicotinamide-adenina-dinucleotide-fosfato (NADP+)
flavinici: flavin-adenina-dinucleotide (FAD)
flavin mononucleotide (FMN)
Ubichinone (coenzima)
Citocromi (proteine con anelli porfirinici che trasportano e- attraverso red-ox del Fe)
Il NAD dunque funge da
intermedio
per
trasferire
elettroni e ricopre un ruolo molto
importante nelle reazioni che
coinvolgono formazione di energia
dinucleotide
l ’ O2 da solo non potrebbe mai
ridursi ad acqua perché l’E0 della
reazione è molto alto, viceversa
gli elettroni possono essere
trasferiti all’ossigeno attraverso
il
NAD
in
una
reazione
energicamente più vantaggiosa
NADH + H+ + 1/2 O2 = H2O + NAD+
Quando gli elettroni si muovono da NADH a O2 nella respirazione aerobia si
libera una notevole quantità di energia che viene utilizzata per sintetizzare ATP
Viceversa, quando si devono trasferire elettroni contro gradiente red-ox c’è
bisogno di energia che nel caso della fotosintesi deriva dalla luce
Eo = -0,32
Eo = + 0,82
GLI ENZIMI
Gli ENZIMI possono essere definiti come proteine catalitiche che presentano
una elevata specificità per la reazione catalizzata e per le molecole su cui
agiscono
Un catalizzatore è una molecola che accelera l’avvenimento di una reazione
chimica senza risultare alterato alla fine della reazione
Gli enzimi accelerano le reazioni cellulari agendo sui substrati e convertendoli
in prodotti
Attenzione!!! L’equilibrio energetico NON si sposta verso i prodotti ma l’azione
dell’enzima provoca un aumento della velocità della reazione…possono aumentare
la velocità da 108 a 1020 volte rispetto a quella spontanea!!
Esempio di funzionamento di un enzima: l’ALDOLASI
Fruttosio difosfato aldolasi
La parte dell ’ enzima dove avviene la reazione si
chiama sito attivo che è specifico per il substrato
Importanti attivatori non proteici degli enzimi sono i
cofattori che generalmente sono ioni
In molti casi però i cofattori non sono ioni e si
modificano durante la reazione e si comportano quasi
come un substrato vengono chiamati coenzimi
Esempio di funzionamento di un coenzima: IL NAD
Ac. 1-3-difosfoglicerico
Gliceraldeide-3-P
acetaldeide
etanolo
Tipi di metabolismo energetico
Metabolismo
Donatore di eFermentazione
ATP per fosforilazione a Composto organico:
livello di substrato zuccheri, aminoacidi, acidi
organici
Respirazione aerobica
ATP per fosforilazione Composto organico
ossidativa e a livello di
substrato Composto inorganico
H2, H2S, S, NH3, Fe3+
Respirazione anaerobica
ATP per fosforilazione Composto organico
ossidativa Composto organico (C2-C4)
o inorganico (H2, H2S)
Composto inorganico (H2)
o organico (C1-C2)
Fotosintesi
ATP per fotofosforilazione H2S e S
Composto organico
Accettore di e-
Microrganismi
Composto
organico
Chemiorganotrofi
anaerobi o anaerobi facolt.
O2
O2
Chemiorganotrofi
aerobi o anerobi facolt.
Chemioautotrofi aerobi
NO3SO4--
Denitrificanti anaer. facolt.
Desulforicanti anaerobi
CO2
Metanogeni anaerobi
---
Fotoautotrofi obbligati
anaerobi
Fotoautotrofi facoltativi
anaerobi facoltativi
METABOLISMO MICROBICO DEI CHEMIOETEROTROFI O CHEMIORGANOTROFI
SORGENTE
DI ENERGIA
UTILIZZATA
TIPO
NUTRIZIONALE
SORGENTE
DI CARBONIO
ASSIMILATA
TIPO
NUTRIZIONALE
GRUPPI
FISIOLOGICI
GENERAZIONE DI ATP E NADH
PROCESSO
DONATORE DI e-
ACCETTORE e-
-eDONATORE OX.
C. ORGANICO
+eACCETTORE RID.
C. ORGANICO
Molti batteri anerobi
obbligati e facoltativi;
alcuni funghi e lieviti
FERMENTAZIONE
C. ORGANICO OX.
[O CO2]
OSSIDAZIONE
C. CHIMICI
C. ORGANICI
[ORG. E INORG.]
C. ORGANICO RID.
[O H2]
O2
RESPIRAZIONE
Molti batteri aerobi
obbligati e facoltativi;
molti funghi e protozoi
H2 O
CHEMIOTROFI
NO3-
CHEMIORGANOTROFI
NITRATO RIDUTTORI
C. ORGANICI
NO2NO3-
RESPIRAZIONE
ANAEROBICA
DENITRIFICANTI
CO2
NO2-N2
SO4-SOLFATO RIDUTTORI
H2 S
METABOLISMO MICROBICO DEI CHEMIOAUTOTROFI O CHEMIOLITOTROFI
SORGENTE
DI ENERGIA
UTILIZZATA
TIPO
NUTRIZIONALE
SORGENTE
DI CARBONIO
ASSIMILATA
TIPO
NUTRIZIONALE
GRUPPI
FISIOLOGICI
GENERAZIONE DI ATP E NADH
PROCESSO
DONATORE DI e-eDONATORE OX.
ACCETTORE e+eACCETTORE RID.
H2
IDROGENOBATTERI
H2 O
NH3
OSSIDAZIONE
C. INORGANICI
RIDOTTI
O2
AMMONIO OSSIDANTI
[NITROSANTI]
CO2
RESPIRAZIONE
NO2-
H2O
NO2CHEMIOTROFI
NITRITO OSSIDANTI
[NITRICANTI]
CHEMIOLITOTROFI
NO3H2 S S
SOLFURO OSSIDANTI
[SOLFOSSIDANTI]
S
SO4-H2
CO2
RESPIRAZIONE
ANAEROBICA
BATTERI
METANOGENI
H2 O
CH4
METABOLISMO MICROBICO DEI FOTOTROFI
SORGENTE
DI ENERGIA
UTILIZZATA
TIPO
NUTRIZIONALE
SORGENTE
DI CARBONIO
ASSIMILATA
TIPO
NUTRIZIONALE
GRUPPI
FISIOLOGICI
GENERAZIONE DI ATP E NADH
PROCESSO
DONATORE DI e-eDONATORE OX.
ACCETTORE e+eACCETTORE RID.
BACTERIORODOPSINA
HALOBACTERIUM
FOTOTRADUZIONE
C. ORGANICO
COMPOSTI ORGANICI
LUCE
RADIANTE
BATTERI PORPORA
NON SULFUREI
C. ORGANICO OX.
FOTORGANOTROFI
NADP
H2 S
S
FOTOSINTESI
FOTOTROFI
CO2
FOTOLITOTROFI
BATTERI VERDI E
PORPORA SULFUREI
SO4--
S
H2 O
O2
NADPH
CYANOBATTERI
(ALGHE BLU VERDI)
ALGHE EUCARIOT.
ALCUNI PROTOZOI
Ciclo Biogeochimico
Descrive le trasformazioni di
elementi fondamentali per gli
organismi viventi causate sia
da da processi biologici che
chimici.
I Chemio-organotrofi possono utilizzare a scopo energetico tutte le sostanze organiche
naturali, nonché quelle di sintesi ad esse strutturalmente rapportabili
I Glucidi sono diffusissimi nella biosfera, disponibili in forme semplici e
complesse, omo-polimeri o etero-polimeri di zuccheri semplici
Dall'attacco delle forme più complesse derivano molecole progressivamente più
piccole
Ogni tipo di struttura molecolare glucidica può essere degradata, in adatte
condizioni, grazie all'attività di enzimi specifici.
Gli enzimi che agiscono sulle strutture glucidiche sono diversamente diffusi nel
mondo microbico:
- alcuni, come per esempio le amilasi, ricorrono in microrganismi appartenenti a
numerosi gruppi sistematici;
- altri, come per esempio gli enzimi cellulosolitici, sono prodotti soltanto da pochi e
peculiari gruppi microbici.
Col catabolismo dei Monosi, disponibili come tali o derivanti dall'attacco dei
Poliosi, i diversi gruppi microbici danno origine a diversi prodotti finali
attraverso processi di RESPIRAZIONE o di FERMENTAZIONE. Questo
aspetto del metabolismo può essere riferito al Glucosio quale monoso
decisamente rappresentativo
Con le figure successive si ricorda che questi processi hanno un intermedio
comune: l’Acido Piruvico
A questo "hub" i microrganismi possono giungere attraverso tre diverse vie
metaboliche
Catabolismo dei carboidrati
Avviene tramite un intermedio comune, il glucosio 6-fosfato
Glicogeno e Amido
Glucosio
ATP
ATP
Galattosio
Mannosio
ADP
ADP
Glucosio 1-fosfato
Glucosio 6-fosfato
Pentosi
Vie cataboliche
1) Glicolisi o via di Embeden-Meyerhof
2) Via dei Pentoso Fosfati
3) Via di Warburg e Dickens o shunt dell'esoso monofosfato
4) Via di Entner-Doudoroff
5) Via dei Bifidobatteri o shunt dell'esosofosfato
Produzione di
piruvato
Catabolismo del Glucosio
(1)
Via della glicolisi o
di Embeden Meyerhof-Parnas
ossidazione
E’ il percorso più comune della
degradazione del glucosio ad acido
piruvico e avviene sia in presenza
che in assenza di O2
Sono così chiamate perché la
fosforilazione dell’ADP è accoppiata
con la rottura esoergonica di un
substrato ad alta energia
Glucosio + 2ADP + 3PO4 + 2 NAD+
2 acido piruvico + 2ATP +2NADH + 2H+
Catabolismo del Glucosio
(2)
Via dei Pentoso Fosfati
•Può
decorrere
anche
contemporaneamente
alla
glicolisi e alla via di ED
•Avviene sia in aerobiosi
che in anaerobiosi
•E’ importante sia come via
catabolica che anabolica
Transchetolasi
Transaldolasi
Acido piruvico
Bilancio della via dei pentoso-fosfati
3 Glucosio 6-P + 6NADP+ + 3H2O
2 fruttosio 6-P + gliceraldeide 3-P + 3 CO2 + 6NADPH + 6H+
Il
fruttosio
6-P
può
essere
riconvertito
a
glucosio
6-P
mentre
la
fosfogliceraldeide va ad acido piruvico attraverso gli enzimi glicolitici
La fosfogliceraldeide può anche rientrare nella via dei pentosofosfati
formando fruttosio 6-P e da questo glucosio 6-P con la completa
degradazione del glucosio a CO2 e produzione di una grande quantità di
NADPH :
Glucosio6-P + 12NADP+ + 7H2O
6CO2 + 12NADPH + 12H+ + P
Funzioni della via dei pentoso-fosfati
1) produzione di ATP quando:
• la fosfogliceraldeide viene convertita ad ac. Piruvico tramite la
seconda parte della glicolisi e porta alla produzione di ATP
• la fosfogliceraldeide entra nel ciclo di Krebs
• NADPH può essere convertito a NADH con la formazione di ATP
nella catena di trasporto degli elettroni
2) Il NADPH può essere usato come donatore di elettroni per
l’energia richiesta nelle biosintesi
3) I pentosi intermedi della via dei pentoso-fosfati sono utili per
diverse biosintesi:
eritrosio
amminoacidi aromatici
ribosio
acidi nucleici
glucosio
peptidoglicano
Catabolismo del Glucosio
(3)
Via di Entner-Doudoroff
La glicolisi è la via più comune per la
produzione di acido piruvico. Tuttavia
molti Gram- (Pseudomonas, Rhizobium,
Azotobacter, Agrobacterium) e rari
Gram+ (Enterococcus faecalis) possono
presentare questa via alternativa in cui
da 1 molecola di glucosio si ottengono 2
di acido piruvico, 1 ATP, 1 NADPH, 1
NADH.
Il ciclo di Krebs
o ciclo degli acidi tricarbossilici
Il ciclo degli acidi tricarbossilici libera energia per la conversione di ciò che
rimane dello zucchero semplice (piruvato) a CO2
L’acetil-CoA
•è una molecola ricca di energia costituita dal coenzima A e dall’acido acetico
legati attraverso un legame tioestere ad alta energia
•è prodotto anche dal catabolismo dei lipidi e degli amminoacidi ed è
degradato nel ciclo di Krebs
Il ciclo è funzionale in molti batteri aerobi, protozoi e molte alghe e funghi
A parte la funzione di produzione di energia, lo scopo di questo ciclo è anche di
produrre scheletri di atomi di carbonio da utilizzare nelle biosintesi
Ac piruvico
CoA
NAD+
Il ciclo di Krebs
NADH + H+
CO2
condensazione
2 atomi
di C
4 atomi
di C
6 atomi
di C
5 atomi
di C
Fosforilazione a livello del substrato
Per ogni molecola di Acetil-CoA
ossidata si generano:
2CO2 + 3NADH + 1FADH2 + 1GTP
Le reazioni fin qui analizzate portano ad una quantità significativa di riducenti
come NADH e NADPH e FADH2 tuttavia la resa in ATP è piuttosto bassa…
Respirazione aerobia
La sintesi di quantità sostanziali di ATP avviene attraverso l’utilizzo di O2 come ultimo
accettore di elettroni nella catena di trasporto degli elettroni e l ’ ATP viene
sintetizzata attraverso la fosforilazione ossidativa
La catena di trasporto degli elettroni è costituita da una serie di trasportatori
di e- situato a livello della membrana citoplasmatica (o nei mitocondri) che favoriscono il
trasferimento di e- da donatori (NADH, FADH2) ad accettori, come l’O2
gli e- vengono trasferiti da trasportatori con potenziale - verso altri con potenziale
+, per combinarsi alla fine con H2 e O2 e formare H2O
Durante questo trasporto di elettroni si rende disponibile energia per la sintesi di ATP
a partire da ADP, tale sintesi associata a fenomeni red-ox prende il nome di
fosforilazione ossidativa
Si possono ricavare, dunque, 3 ATP per ogni NADH e 2 ATP per ogni FADH2 che
entrano nella catena di trasporto
Dalla via glicolitica si ricavano in
tutto
8ATP.
Ma
se
i
microrganismi non “ respirano ”
ovvero in assenza di O2 ovvero in
condizioni anaerobie il NADH
formatosi durante la glicolisi non
porta a produzione di ATP per
fosforilazione ossidativa e la
resa è di sole 2ATP!!
Con la respirazione aerobia invece, attraverso la catena di trasporto degli elettroni, si
converte il glucosio in 6CO2 con una resa energetica di 38ATP
La respirazione è quindi energicamente molto più vantaggiosa
Nei batteri non sono presenti tutti i citocromi dei mitocondri quindi il rapporto P/H
non è esattamente lo stesso e la resa può portare ad un numero di molecole di ATP
< 38
Il meccanismo di sintesi dell ’ ATP non è ancora del tutto chiaro anche se esistono
diverse ipotesi
sicuramente avviene a mezzo del complesso proteico ATPasi o ATP sintasi localizzato
nella superficie interna della membrana citoplasmatica
Generazione di ATP per fosforilazione ossidativa
Teoria chemiosmotica di Mitchell
Espulsione di H+ dalla cellula (pompa protonica)
Teoria della variazione conformazionale
Energia derivante dalla catena di trasporto degli elettroni genera una variazione
nell’ATPasi
La fermentazione
Ma cosa avviene in assenza di O2?
Il NADH prodotto durante la glicolisi non può essere utilizzato per donare
elettroni
Nel caso della fermentazione l’ultimo accettore di elettroni diventa una
molecola organica
I processi in cui le molecole organiche fungono sia da donatori che da
accettori di e- si chiamano FERMENTAZIONI
La molecola che funge da ultimo accettore è UN COMPOSTO ORGANICO:
l’acido piruvico (ferm. lattica); acetaldeide (ferm. alcolica); ecc
Schema riassuntivo delle fermentazioni a partire dall’acido piruvico
Alcolica
Omolattica
Acido piruvico
Acido lattico
CO2 + Etanolo
CO2
H2
Acido formico
Acido acetico
Acido lattico
Acido succinico
Etanolo
2,3-butilenglicol
CO2
Piruvato
Piruvico
decarbossilasi
CO2
Acido propionico
Acido acetico
CO2 + H2
Acido acetico
Acetone
Alcool isopropilico
Acido butirrico
NADH + H+ à NAD+
Acetaldeide + CO2
Etanolo
Alcool deidrogenasi
NADH + H+ à NAD+
Piruvato
Acido lattico
Fermentazione Lattica:
ac piruvico (lattico deidrogenasi + NADH)
acido lattico
questa è operata da molti batteri
prende il nome di omolattica quando tutto il piruvato viene trasformato
in lattato
prende il nome di eterolattica quando parte del piruvato va a formare
anche etanolo e CO2
Fermentazione alcolica:
operata da lieviti, funghi e alcuni batteri, porta alla produzione di
etanolo e CO2 a partire da piruvato.
Omolattica
Alcolica
Eterolattica
L’Effetto Pasteur
E’ il diverso responso di crescita dato dai microrganismi nel caso in cui vivano in presenza o
assenza di O2
Si ha una resa in biomassa maggiore in presenza di ossigeno (respirazione = maggiore crescita)
si ha fermentazione in assenza di ossigeno e minore crescita
La respirazione anaerobia
E ’ operata dai microrganismi che utilizzano sostanze inorganiche diverse
dall’O2 come ultimi accettori di eAlcune specie dei generi Bacillus e Pseudomonas (anaerobi facoltativi) possono
utilizzare i nitrati come ultimi accettori di elettroni.
I nitrati vengono ridotti a nitriti
poiché i nitriti sono tossici questi vengono ulteriormente ridotti ad N2 tramite
un processo detto DENITRIFICAZIONE (batteri denitrificanti)
I METANOGENI usano la CO2 o i carbonati come accettori di elettroni e li
riducono a metano
In Desulfovibrio i solfati fungono da accettori di elettroni e vengono ridotti a
solfuro
La respirazione anaerobia porta ad una produzione di ATP inferiore a
quella ottenibile attraverso la respirazione aerobia…
…questo succede perché gli accettori di elettroni di questa catena di
trasporto hanno un potenziale più basso rispetto all’O2
Nella catena di trasporto degli elettroni
NADH (-0,32 Volt) -------------->
O2
(> di + 0,82 volt)
Visto che la resa energetica è direttamente proporzionale alla
differenza di potenziale, l ’ energia che si rende disponibile per la
fosforilazione ossidativa in questo caso è minore
Respirazione anaerobica
Metabolismo respiratorio che avviene in assenza di O2
Accettore terminale di elettroni: composti inorganici ossidati (NO3-, SO42-, CO2, CO32-)
A) Denitrificazione
chemioeterotrofi anaerobi facoltativi: Bacillus e Pseudomonas
chemioautotrofi anaerobi facoltativi: Thiobacillus
Nitrato riduttasi: da nitrato a nitrito (NO3- --> NO2-)
2 HNO3 + 10 H+ + 10 e- --> N2 + 6H2O
suolo e acque --> ciclo dell'N
nitrati nelle acque: tossicità ed eutrofizzazione
B) Desulforicazione
SO42- e SO3- come accettori di eanaerobi obbligati: Desulfovibrio, Desulfomonas e Clostridium
10H+ + 8 e- + SO42- --> H2S + 4H2O
sedimenti profondi e terreni acquitrinosi
raramente rumine ed intestino
C) Metanogenesi
CO2 o CO3 2- accetori di e- ---> CH4
Archebatteri anaerobi non aerotolleranti
Methanobacterium, Methanococcus, Methanosarcina, ecc.
CO2: carbossil. ridutt. dell'Acetil-CoA --> piruvato
rumine, sedimenti, acquitrini
Catabolismo proteico
Le proteine vengono attaccate da proteasi liberando amminoacidi
gli amminoacidi vengono trasportati nelle cellule e vanno incontro a reazioni
di
deamminazione
(con
liberazione
di
un
gruppo
amminico)
e
transamminazione (con formazione di un altro amminoacido)
Lo scheletro carbonioso può essere convertito in CoA ed entrare nel ciclo
di Krebs oppure costituire una base per le biosintesi
la parte azotata viene liberata sotto forma di ammoniaca o ammonio
(alcalinizza il mezzo)
Ciclo dell’azoto
Racchiude
gli
importanti
passaggi
di
nitrificazione,
denitrificazione
e
azotofissazione
La nitrificazione è un processo aerobio di ossidazione dello ione ammonio (NH4+)
a nitrito (nitrosazione, Nitrosomonas e Nitrosococcus) e poi a nitrato
(nitricazione)
La denitrificazione prevede condizioni ambientali diverse: il nitrato è utilizzato
come ultimo accettore di elettroni nella respirazione anaerobica (Pseudomonas
denitrificans)
Il nitrato può andare ad N2 gassoso, NO, oppure può essere convertito in NH3
attraverso una riduzione dissimilativa (organicazione, Geobacter, Desulfovibrio,
Clostridium).
Ciclo dell’azoto
L’ azotofissazione può essere operata sia da batteri aerobi che anaerobi.
In aerobiosi molti asimbionti possono azotofissare (Azotobacter, Azospirillium),
in anaerobiosi gli unici azotofissatori asimbionti appartengono al genere
Clostridium.
Gli azotofissatori simbionti stabiliscono dei rapporti di simbiosi con alcune
piante, ad esempio le leguminose (Rhizobium, Bradyrhizobium).
Nei simbionti l’azotofissazione avviene in condizioni strettamente anaerobie, è
un processo che richiede energia e avviene grazie al funzionamento del
complesso enzimatico della nitrogenasi.
Natmosferico: utilizzabile solo da alcuni microrganismi (Azotofissatori)
NH3 e NO3-: forme di Nutilizzabili
Fissazione non biologica dell'N2 atmosferica:
scariche elettriche e reazioni fotochimiche
Fissazione biologica dell'N2 atmosferica:
8H+ + N2 --> 2NH3 + H2
Nitrogenasi: Fe, S, Mo proteina sensibile all'O2
Fe-S --> nitrogenasi riduttasi
Fe-Mo --> nitrogenasi
Elettroni --> NADH --> Ferridossina --> N2-Nitrogenasi --> NH3
Energia fornita da 16 mol. di ATP
Saggio dell'attività nitrogenasica: riduzione dell'acetilene a eticlene
CH CH + 2e- + 2H+ --> CH2=CH2
Microrganismi Azotofissatori
Simbionti (di piante: leguminose) --> Rhizobium
Liberi: aerobi eterotrofi: Azospirillum, Azotobacter, Bejerinkia
aerobi fotoautotrofi: Cianobatteri
anaerobi eterotrofi: Clostridium
anaerobi facoltativi: Klebsiella, Enterobacter
anaerobi fotoautotrofi: Chromatium, Rhodospirillum
Assimilazione dell'NO3Dissimilazione Riduttiva --> Denitrificazione
Assimilazione Riduttiva: avviene in 2 stadi
NO3- --> NADPH+ Nitrato reduttasi (flavoprot.-Mo) --> NO2NO2- --> NH2OH (idrossilamina) --> NH3
Assimilazione dell'NH3
Può avvenire in 3 modi:
ac. a-chetoglut. + NH3 + Glutam. Deidrig. +NADPH --> ac. glutammico
ac. glutammico + NH3 + ATP + Glutam. Sintetasi --> Glutammina
ac. aspartico + NH3 + ATP + Asparag. Sintetasi --> Asparagina
Acido glutammico e gutammina sono donatori di gruppi aminici e amidici per la sintesi di altri
aminoacidi e nucleosidi: Reazioni di transaminazione catalizzate da transaminasi
Catabolismo dei Lipidi
I Lipidi (trigliceridi) non possono essere trasportati attraverso la membrana.
Essi vengono attaccati da Lipasi extracellulari, con liberazione di glicerolo e di
acidi grassi.
Glicerolo, acidi grassi e gruppi idrofilici sono liberati anche dall'azione di
quattro diverse Fosfolipasi sulle strutture fosfolipidiche.
esterasi
Acido oleico
C18
b-OSSIDAZIONE
Ciclo di
Krebs
Sintesi
Lipidiche
Gli acidi grassi vanno incontro a b-ossidazione con
Catena di
trasporto
degli
elettroni
produzione di FADH e NADH (che entrano nella catena di trasporto di e-) +
produzione di Acetil-CoA che entra nelle vie anaboliche (sintesi di lipidi…) oppure
nel ciclo di Krebs
Idrocarburi
Gli Idrocarburi possono costituire altra eccellente fonte energetica per
i microrganismi.
Le diverse classi di questi composti possono subire vari tipi di attacchi
da parte di specie microbiche
Metabolismo degli idrocarburi
Tali composti, essendo generalmente poveri di O2 , devono essere
ossigenati per diventare biologicamente attivi e più solubili in H2O
Processi di ossigenazione catalizzati da ossigenasi
Mono-ossigenasi
butano + O2 +NADH2 --> butanolo + H2O + NAD+
Diossigenasi
benzene + O2 --> cis-diolo --> CO2 + Piruvato + Acetaldeide
Ciclo del carbonio nell’ambiente
Anaerobiosi
Aerobiosi
Fissazione del carbonio
Fissazione del carbonio
Materia organica
CO2
Fermentazione
CO2
Respirazione
Ossidazione del
monossido di
carbonio
Metanogenesi
H2
CO
CH4
Assimilazione dell'SO42I solfati rappresentano la fonte di S per la maggior parte dei microrganismi
Assimilazione riduttiva:
SO42- ---> H2S ---> composti organici
Serina + H2S ---> Cisteina