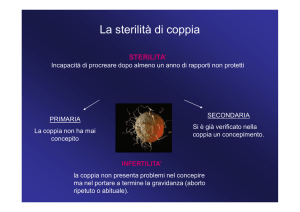
La sterilità di coppia
La sterilità femminile
Stefano Venturoli
Clinica Ginecologica e Fisiopatologia della Riproduzione Umana
Università di Bologna
Alma Mater Studiorum
Definizione - Epidemiologia
INFERTILITA’ Incapacità di portare a
termine una gravidanza sino alla nascita di
un individuo
STERILITA’ Mancanza di concepimento dopo
12-18 mesi di rapporti regolari e non protetti
(10-15%)
Fattori che influenzano la fertilità
CONSIDERA !! Mediamente il primo parto, nella donna italiana avviene al 32°anno di
età : la ricerca della gravidanza è quindi spostata avanti nel tempo per motivi sociali
ETA’ DELLA DONNA: Dopo i 35 aa le probabilità di
concepire diventano inversamente proporzionali
all’età. L’incidenza della sterilità tende ad aumentare
con l’età femminile.
25-29 aa: 5.6%
30-34 aa: 11.7%
35-39 aa: 13.7%
40-44 aa: 14.7%
dopo i 35 anni la fertilità della
coppia è gia diminuita del 50%
Fattori che influenzano la fertilità
FREQUENZA
DEI
RAPPORTI
SESSUALI:
Direttamente correlata alle possibilità di una
gravidanza. La frequenza coitale ottimale nella coppia è in
relazione all’insieme dei parametri della fertilità
TEMPO RICERCA FIGLI: Entro un anno di rapporti
sessuali frequenti e non protetti, l’86% delle coppie
ottiene una gravidanza.
Le possibilità di un concepimento si riducono in
modo proporzionale con il trascorrere del tempo
Sterilità femminile: fattori di rischio
• Età > 35 anni *
• Anamnesi familiare di POF *
• Agenti iatrogeni (pregressa chirurgia pelvica,
chemioterapia) *
( * qualità e numero oociti)
•Obesità (BMI>30 kg/m2) e magrezza #
(# anovulatorietà)
• Endometriosi °
•PID (Pelvic Infiammatory Disease) °
•Utilizzo di IUD °
(° danni all’apparato riproduttivo)
Fisiologia della Riproduzione
Da cosa è definita la salute riproduttiva e come si compie?
Cioè, attraverso quali tappe essa si realizza ?
- la capacità di far maturare mensilmente, un ovulo sano
e fecondabile
- la capacità di produrre liquido seminale fertile
- la capacità della vagina, della cervice e della cavità uterina
di veicolare il liquido seminale “capacitato” e fertile
- la competenza delle salpingi nel captare l’ovulo,
nel veicolare gli spermatozoi, nel consentire
la fecondazione, lo sviluppo embrionale e nel trasportare
in modo retrogrado l’embrione fino alla cavità uterina;
- la capacità dell’utero di sostenere l’impianto embrionale
e portare a termine la gravidanza.
- la capacità dell’embrione di svilupparsi fino a termine
di gravidanza
Sterilità femminile: Cause
Fattore Cervicale (5-10%)
• Anatomiche: conizzazione, sinechie cervicali
• Funzionali: alterazioni del muco cervicale
• Infiammatorie: endocerviciti
Fattore Uterino (5-10%)
• Sinechie intrauterine, Sd di Asherman
• Malformazioni uterine o anomalie acquisite
• Patologie endocavitarie (miomi, polipi, endometriti)
Sterilità femminile: Cause
Fattore Tubarico (35%)
• Alterazioni funzionali
• Alterazioni anatomiche congenite (agenesia/atresia)
• Obliterazioni parziali e totali del lume, alterazioni
della parete e
• Danni fimbriali da cause * flogistiche, * endometriosiche,
* chirurgiche
e * post-chirurgiche
descrizione dell’ovulazione
e della captazione ovocitaria in-vivo
… Le fimbrie di entrambe le tube appaiono distese nella
fossetta ovarica e posizionate al di sotto del polo
posteriore delle ovaia. Dal lato dell’ovulazione le
fimbrie sono rigide e turgide e mostrano una
pulsatilità sincrona con quella cardiaca. Le estremità
si proiettano sul punto di rottura del follicolo mentre
la matrice del cumulo ooforo viene rilasciata
lentamente dall’ovaio…
(Grodts S. 1998)
Importanza della relazione tra ovaio e fimbrie
Sterilità femminile: Patologia tubarica
Sterilità femminile: Patologia tubarica
Sterilità femminile: Patologia uterina
Sterilità femminile: Endometriosi
Sterilità femminile: Cause
Fattore Pelvico (15-25%) (anche extragenitale)
- Aderenze e lesioni endometriosiche
- Aderenze e lesioni flogistiche (TBC, Clamidia)
- Alterazioni della anatomia topografica addominale
Fattori Idiopatici (20-35%)
- Tutte quelle condizioni per le quali la * diagnosi di certezza non può
ancora essere posta, per * oggettiva carenza di mezzi diagnostici (su
ovaia-spermatozoi, funzionalità ), per * con-causalità più o meno
manifesta o documentabile, maschile e femminile, o per * fattori di cui si
ipotizza la potenzialità ma di cui non esiste certezza documentale , quali
le cause immunologiche, o la così detta “incompatibilità di coppia” .
Sterilità femminile: Cause
Fattore Endocrino (30-40%)
• Mancanza di ovulazione o rarità ovulatoria (da cause
interne all’asse riproduttivo:ipotalamiche, ipofisarie,
ovariche)
• Alterata funzione del corpo luteo
• Secrezione ormonale patologica (iperprolattinemia,
eccesso di androgeni extra ovarici, anomalie tiroidee e
surrenaliche)
Sterilità maschile: fattori di rischio
• Criptorchidismo
• Varicocele
• Traumi testicolari
• Infezioni del tratto riproduttivo (epididimiti,
prostatiti)
• Cause iatrogene (pregressa chirurgia pelvica,
chemioterapia)
• Malattie sistemiche ed endocrine
• Torsione del funicolo spermatico
• Esposizione a fattori ambientali e occupazionali
(fumo, alcol, droghe)
Sterilità maschile: Cause
Sterilità Secretoria (30-40%) (assenza o danno al
tessuto produttore degli spermatozoi nel testicolo)
• Congenita (su base endocrina e talora su base
cromosomica)
• Acquisita
varicocele,
criptorchidismo,
orchite parotitica,
alcool, droghe,
ipogonadismo ipogonadotropo,
uso di Ciclofosfamide (antineoplastico/immunosoppressore),
Sulfasalazina, (utilizzata nel trattamento di malattie infiammatorie
dell'intestino) Ketoconazolo (un antimicotico), Spironolattone (un
diuretico e antiandrogeno)
Sterilità maschile: Cause
Sterilità Escretoria (10-15%)
(assenza della possibilità
eiaculatoria)
• Congenita (agenesia del deferente o dell’epididimo,
obliterazione dotti eiaculatori, alterazione rete testis)
• Acquisite (traumi, infezioni, interventi chirurgici)
DIAGNOSI DELLA STERILITA’
Sterilità Femminile
Sterilità Maschile
Sterilità di Coppia
Diagnosi - DONNA
Valutazione Ovulazione
• Anamnesi + Esame obbiettivo + Ecografia pelvica TV
• Monitoraggio temperatura basale o indicatori periodo fertile
• Dosaggi ormonali (FSH, LH, E, P, T, PRL)
Valutazione degli stati di flogosi genitale
• Esame colturale del secreto vaginale (batteri e miceti,
Chlamydia, Micoplasma, Ureaplasma, Gardnerella,
Trichomonas, Herpes vaginalis)
Valutazione Pervietà tubarica e Morfologia uterina
• Sonoisterosalpingografia (o similari di 1° livello)
• Laparoscopia e isteroscopia diagnostica
Esami Genetici
• Mappa cromosomica
Esami diagnostici strumentali a nostra
disposizione
• Isterosalpingografia (HSG)
• Ecografia TA/TV/2D/2D
• Sonoisterografia (SIS)
• Sono-istero-salpingografia (HyCoSy)
• Isteroscopia e Laparoscopia
• (Fertiloscopia, Salpingoscopia,
Falloppioscopia )
Quali caratteristiche dovrebbe
possedere l’esame diagnostico ideale?
• ACCURATEZZA
Sensibilità
Specificità
•RAPIDITÀ
• RIDOTTA INVASIVITÀ
•COST- EFFECTIVENESS
• INFORMAZIONI UTILI SUL TIPO DI
TRATTAMENTO, nel contesto clinico
(durata della infertilità, età della donna ….)
Sensibilità
La sensibilità è la capacità di identificare
correttamente gli individui ammalati.
In termini di probabilità, la sensibilità è la
probabilità che un individuo ammalato risulti
positivo al test
si può anche dire che essa è la proporzione
degli individui ammalati che risultano positivi
al test.
Specificità
La specificità è la capacità di identificare
correttamente gli individui sani
In termini di probabilità, la specificità è la
probabilità che un individuo sano risulti
negativo al test
si può anche dire che essa è la proporzione
degli individui sani che risultano negativi al
test
Isterosalpingografia (HSG)
Tecnica radiografica con uso di m.d.c.
Consente di valutare :
• CAVITA’ UTERINA
• PERVIETA’ TUBARICA
[Kupesic,Ultras Obstet Gynecol, 2001]
HSG:quadri patologici visualizzabili
•anomalie uterine congenite o acquisite
- polipi endometriali
- miomi sottomucosi
- sinechie
• quadri ostruttivi tubarici
- salpingite istmica nodosa
- fimosi fimbriale
• sindromi aderenziali che ostacolano il
deflusso del mdc in addome
[ Kupesic 2001, ASRM 2006]
Ultrasonografia
patologia uterina
L’ecografia trans-vaginale si è dimostrata una valida
alternativa alla HSG nella diagnosi delle malformazioni
uterine
[ Braun et al 2005, Perquin et al 2007]
Nonostante la patologia tubarica
sia la principale causa di
sterilità, alterazioni a carico
della conformazione e della
superficie endocavitaria uterina
rivestono una importanza clinica
non trascurabile
[Homer et al 2000]
Sonoisterografia (S.I.S.):tecnica
1. esecuzione di ecografia TV per valutare assetto uterino
2. introduzione di un piccolo catetere endocervicale
3. iniezione di soluzione salina sterile
Mioma sottomucoso
Sinechie
Sonoisterografia (S.I.S.)
Per ottenere una ottima visualizzazione dell’endometrio
e del miometrio è necessario distendere la cavità
uterina mediante l’introduzione di un m.d.c. anecogeno
[ Kupesic 2001]
Sonoisterosalpingografia (HyCoSy)
La pervietà tubarica viene accertata mediante
introduzione di un m.d.c. ecografico positivo
• piccole immagini puntiformi
ecogene in movimento nella
soluzione fisiologica introdotta
• le bolle d’aria si dispongono in
fila nel lume tubarico
• al passaggio in addome
visualizzazione di una sottile
striscia iperecogena ai lati
dell’utero
Ecografia 3- D e patologia uterina
contemporanea analisi dei tre piani
ortogonali e della superficie uterina
valutazione di:
• CAVITA’ UTERINA
• FONDO UTERO
• SPESSORE
PARIETALE
(Kupesic & Plavsic 2007)
Diagnosi - DONNA
Laparoscopia diagnostica
Utero setto
Utero bicorne
Utero regolare
Diagnosi - DONNA
Laparoscopia diagnostica
Cisti
endometriosica
Cisti
dermoide
Ovaia regolari
LAPAROSCOPIA PERMETTE LA VALUTAZIONE DI
1. Pervietà/Impervietà tubarica
2. Presenza di aderenze, la natura
e la loro esatta posizione
3. Morfologia fimbriale e tubarica
4. Superficie peritoneale e
presenza di endometriosi
Quale capacità prognostica per la fertilità?
PERVIETA’ TUBARICA
Capacità prognostica
La pervietà tubarica è necessaria ma non sufficiente a
garantire la fertilità
(Mol et al., 1999; Papaioannou et al., 2007)
ADERENZE PERITUBARICHE
Significato prognostico
Prognosis is described in terms of adjusted Fecundity Rate
Ratios (FRR)
FRR (adjustet Fecundity Rate Ratio):
Aderenze moderate: 0,72
Aderenze severe: 1,2
Assenza di significato prognostico
(Mol et al., 1999; Papaioannou et al., 2007)
•Caratteristiche delle fimbrie
Fimbrie corte ma libere
Fimbrie
libere
Fimbrie conglutinate
Diagnosi - UOMO
Valutazione Funzionalità Spermatica
• Anamnesi + esame obbiettivo
• Spermiogramma, spermiocoltura
• Dosaggi ormonali
• Eco Doppler testicolare
Esami Genetici
• Mappa cromosomica
Diagnosi - UOMO
Esame del liquido seminale (Who 2001)
• Volume seminale
• pH
• Concentrazione spermatozoi
• Motilità (%)
• Morfologia (%)
• Leucociti
> 2 ml
> 7.2
> 20x106/ml
> 50% con
motilità
progressiva /o
> 25% con
motilità
rapidamente
progressiva
> 15-30%
< 1x106/ml
Non si può prescindere da un preciso e codificato
comportamento clinico, quando si affronta la sterilità
Algoritmo diagnostico /terapeutico - DONNA
Algoritmo diagnostico /terapeutico - UOMO
Terapia della Sterilita’
DEFINIZIONE
Procedimenti che comportano la rimozione della causa di
sterilità, agendo direttamente sul soggetto (maschiofemmina) affetto da patologia, mediante un atto
terapeutico
Cause Principali
- Flogosi del tratto genitale, maschile (M) e femminile (F)
- Anomalie anatomiche congenite o acquisite M. e F.
- Anovulatorietà
- Oligoastenoteratospermia flogistica, meccanica e/o
endocrina
Procreazione Medicalmente Assistita
DEFINIZIONE
Procedimenti che comportano il “diretto trattamento“ di
oociti umani, spermatozoi o embrioni, nell’ambito di un
progetto finalizzato a realizzare una gravidanza
Identificabili come procedimenti:
a) di I° e II livello, oppure
b) intracorporei o extracorporei
LEGGE 40/2004 PMA - IMPLICAZIONI
(Emendamenti)
1. E’ vietata la produzione, la sperimentazione e il
congelamento di embrioni umani a fini di ricerca
2. E’ consentito l’accesso alla procreazione
medicalmente assistita solo per coppie sterili
3. E’ consentita la fecondazione di un numero
massimo di tre ovuli alla volta
4. Non è permessa l’analisi pre impianto
5. E’ vietata la fecondazione eterologa, cioè la
possibilità di ricorrere alla donazione di gameti
esterni alla coppia
Procreazione medicalmente assistita
I LIVELLO
• Inseminazione intrauterina su ciclo naturale
• Inseminazione intrauterina previa induzione multipla
dell’ovulazione (IUI)
II LIVELLO
• Fecondazione in vitro e trasferimento dell’embrione
(FIVET)
• Iniezione intracitoplasmatica dello spermatozoo (ICSI) e
trasferimento dell’embrione
• Prelievo testicolare di gameti (prelievo percutaneo o
biopsia testicolare)
• Trasferimento intratubarico di gameti maschili e femminili
(GIFT), zigoti (ZIFT), o embrioni (TET) per via transaddominale
Procreazione medicalmente assistita
INTRACORPOREA
• Inseminazione intrauterina su ciclo naturale
• Inseminazione intrauterina previa induzione multipla
dell’ovulazione (IUI)
•Trasferimento intratubarico di gameti maschili e femminili
(GIFT),
EXTRACORPOREA
• Fecondazione in vitro e trasferimento dell’embrione
(FIVET)
• Iniezione intracitoplasmatica dello spermatozoo (ICSI)
• Trasferimento intratubarico (GIFT) di , zigoti (ZIFT), o
embrioni (TET) per via transaddominale
Procreazione medicalmente assistita
Tecniche per il prelievo in caso di azoospermia
• Aspirazione percutanea di spermatozoi per via testicolare
(TESA)
• Estrazione di spermatozoi per via testicolare (TESE)
• Aspirazione microchirurgica di spermatozoi dall’epididimo
(MESA)
• Aspirazione percutanea di spermatozoi dall’epididimo
(PESA)
Procreazione medicalmente assistita
I LIVELLO - INDICAZIONI • Sterilità inspiegata
• Infertilità maschile di grado lieve moderato
• Endometriosi I-II stadio e casi selezionati di III-IV stadio,
in particolare dopo intervento chirurgico
• Ripetuti insuccessi di induzione della gravidanza con
stimolazione dell’ovulazione e rapporti mirati
• Patologie sessuali e coitali
• Fattore cervicale
Procreazione medicalmente assistita
II LIVELLO (FIVET) - INDICAZIONI • Patologia tubarica acquisita o congenita
• Infertilità maschile di grado moderato quando i
trattamenti di I livello non hanno dato risultati
• Endometriosi III-IV stadio
• Infertilità inspiegata se il trattamento precedente non ha
dato risultati
• Seme crioconservato in relazione alla qualità seminale
successiva alla scongelamento
• Fallimento dell’iter terapeutico a basa tecnologia
Procreazione medicalmente assistita
II LIVELLO (ICSI) - INDICAZIONI • Infertilità maschile di grado severo
• Azoospermia ostruttiva e secretiva (spermatozoi
testicolari o epididimari)
• Mancata o ridotta fertilizzazione in precedenti cicli di
fertilizzazione in vitro
• Ovociti scongelati
• Ridotto numero di ovociti
• Seme crioconservato in relazione alla qualità seminale
successiva alla scongelamento
FASI OPERATIVE DELLE TECNICHE DI PMA
Fasi Comuni
• induzione della ovulazione controllata o della
superovulazione
• preparazione del seme
Fasi Specifiche
• (IUI) introduzione del seme nella cavità uterina
• (FIVET/ICSI) prelievo degli ovociti
• fecondazione degli ovociti e creazione dell’embrione
• transfer embrionale intra cavitario
TECNICHE DI PROCREAZIONE MEDICALMENTE ASSISTITA
INDUZIONE DELLA SUPEROVULAZIONE
Fase che accomuna tutte la tecniche di fecondazione assistita.
L’obiettivo della superovulazione è quello di produrre un numero
controllato/elevato
di
ovociti
fertilizzabili,
superando
farmacologicamente il controllo endogeno della funzione riproduttiva.
1. SOMMINISTRAZIONE DELL’ANALOGO DEL GnRH
Dopo 14 giorni ecografia pelvica di controllo desensibilizzazione ipofisaria
2. SOMMINISTRAZIONE DELLE GONADOTROPINE
Dal 1 al 7 gg: terapia domiciliare
Dall’ 8 giorno di stimolazione: monitoraggio ecografico ed ormonale
3. SOMMINISTRAZIONE DELL’ HCG
MONITORAGGIO DELL’INDUZIONE DELLA
SUPEROVULAZIONE
LIVELLI PLASMATICI DI E2
ASPETTO ECOGRAFICO
MONITORAGGIO DELL’INDUZIONE DELLA
SUPEROVULAZIONE
ASPETTO ECOGRAFICO
INSEMINAZIONE INTRAUTERINA
COSA COMPORTA
1) INDUZIONE DELLA SUPEROVULAZIONE
SOMMINISTRAZIONE DELLE GONADOTROPINE
Dal 1 al 5 gg: terapia domiciliare
Dall’ 6 giorno di stimolazione: monitoraggio ecografico ed ormonale
2) INDUZIONE DELLA OVULAZIONE
SOMMINISTRAZIONE DELL’ HCG
3) DEPOSIZIONE DEL SEME NELL’UTERO
1. Un campione di seme del partner verrà prodotto lo stesso giorno
in cui si è programmata l’IUI.
1. Il campione di seme verrà processato in laboratorio allo scopo di
capacitare, selezionare e concentrare gli spermatozoi mobili in un
piccolo volume di terreno di coltura specifico.
1. Il seme verrà deposto dal ginecologo nell’utero utilizzando un
catetere sottile e morbido.
FIVET
FERTILIZZAZIONE IN VITRO E TRASFERIMENTO DI EMBRIONI IN CAVITA’ UTERINA
COSA COMPORTA
- il prelievo ecoguidato degli ovociti dalle
ovaie della donna
- la fertilizzazione in laboratorio con gli
spermatozoi del partner e la coltura per lo
sviluppo embrionale
- il trasferimento nell’utero degli embrioni
sviluppati in laboratorio.
FOLLICOLI MATURI
OVOCITA FERTILIZZATO
EMBRIONE A 8 CELLULE
I.V.F.
ICSI
Iniezione intracitoplasmatica dello spermatozoo
Come si esegue l’ICSI?
1. Un ovocita maturo viene tenuto da un lato con
una particolare micropipetta
Un microago dalla punta sottile ed affilata viene
utilizzato per fermare lo spermatozoo, indicato
dalla freccia nella figura, ed aspirarlo al suo
interno. (a destra nella figura)
2. Questo microago viene quindi inserito
lentamente all’interno del citoplasma dell’ovocita.
(Fig. 2 lo spermatozoo è indicato dalla freccia)
3.
Lo spermatozoo viene iniettato e depositato
all’interno dell’ovocita (Fig. 3)
GIFT
Trasferimeto intratubarico dei gameti
PREVEDE
- IL PRELIEVO ECOGUIDATO DEGLI OVOCITI
- IL TRASFERIMENTO DI GAMETI (OVOCITI E SPERMATOZOI) DIRETTAMENTE NELLA
TUBA DI FALLOPPIO PER VIA LAPAROSCOPICA NELLA STESSA SEDUTA
OPERATORIA.
MESA-TESE-PESA
Sono tecniche di fecondazione assistita che prevedono il prelievo
degli spermatozoi, direttamente :
a livello dell’epipidimo
- con tecnica microchirurgica (MESA)
- tramite agoaspirazione percutanea (PESA)
a livello del testicolo
- con tecnica microchirurgica (TESE).
Gli spermatozoi cosi’ ottenuti vengono poi utilizzati
per fertilizzare gli ovociti mediante tecnica ICSI.
GRAVIDANZE PER CICLO E TRANSFER
2004-2007
35%
33%
31%
30%
25%
25%
26%
23%
22%
20%
15%
19%
16%
10%
5%
0%
2004
2005
2006
2007
GRAVIDANZE/CICLO
16%
19%
26%
23%
GRAVIDANZE/TRANSFER
22%
25%
31%
33%
GRAVIDANZE/TRANSFER PER FASCIA DI ETÀ
2005-2007
50%
40%
30%
46%
44%
43%
40%
32%
30%
32%
32%
26%
20%
20%
17%
12%
10%
5%
0%
6%
4%
2005
2006
2007
< 29 Anni
32%
40%
44%
30-34 Anni
30%
43%
46%
35--39 Anni
26%
32%
32%
40-42 Anni
12%
17%
20%
>43 Anni
5%
4%
6%
ABORTI PER FASCIA DI ETÀ
2007
47%
48%
42%
36%
30%
24%
20%
18%
17%
18%
12%
6%
0%
2007
< 29 Anni
18%
30-34 Anni
20%
35--39 Anni
17%
>40 Anni
47%
GRAVIDANZE MULTIPLE
2005-2007
92%
90%
85%
79%
75%
60%
45%
30%
15%
0%
18%
7%
1%1%
2% 1%
12%
1% 2%
2005
2006
2007
SINGOLE
92%
79%
85%
BIGEMINE
7%
18%
12%
TRIGEMINE
1%
2%
1%
ECTOPICHE
1%
1%
2%