RINOTRACHEITE
INFETTIVA
(IBR)
Prof.ssa Annamaria Pratelli
Principali Herpesvirus animali
Famiglia Herpesviridae
Subfamily Alphaherpesvirinae
Varicellovirus
Subfamily Betaherpesvirinae
BoHV-1
Citomegalovirus
Simplexvirus
BoHV-5
HHV-5
BoHV-2
CaHV
Roseolovirus
HHV-1
HHV-6 e HHV-7
CpHV-1
HHV-2
CvHV-1
Subfamily Gammaherpesvirinae
CvHV-2
Lymphocryptovirus
EHV-1
HHV-4
EHV-4
Macavirus
OvHV-2
FeHV-1
BoHV-6
HHV-3
AlHV-1
SuHV-1
Herpesvirus bovini
Virus species
Subfamily
Disease following infection
α
Infectious bovine rhinotracheitis
Cattle as natural host
Bovine herpesvirus 1 (BoHV-1)
Bovine herpesvirus 2 (BoHV-2)
Bovine herpesvirus 4 (BoHV-4)
Bovine herpesvirus 5 (BoHV-5)
Bovine lymphotrophic herpesvirus
(BLHV)
α
γ
α
Bovine mammillitis-pseudo lumpy skin disease
Not determined
Bovine herpesvirus encephalitis
γ
Not determined
Alcelaphine herpesvirus 1 (AlHV-1)
γ
Malignant catarrhal fever
Ovine herpesvirus 2 (OvHV-2)
γ
Malignant catarrhal fever
Suid herpesvirus 1 (SuHV-1)
α
Aujeszky’s disease
Cattle as foreign host
Stipiti di Bovine Herpesvirus 1
Sottotipi
(analisi con endonucleasi di restrizione)
• BoHV.1.1
associato a IBR e aborto
BHV-1.2a infezione feto e aborto
• BoHV.1.2
associato a IPV-IBP
• BoHV.1.3
associato ad encefalite
BHV-1.2b non associato a aborto
Bovine Herpesvirus 1 BoHV.1
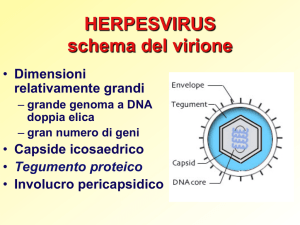
-HERPESVIRUS
ds-DNA
Envelope con glicoproteine
Capside icosaedrico
Replicazione intranucleare
Caratteristiche delle infezioni da BoHV.1
Infezione nasale o genitale
Moltiplicazione del virus a livello mucosale
Lesioni : vescicole, ulcere e necrosi
Reazione generale: febbre, abbattimento anoressia,
caduta produzione lattea
Immunodepressione
• Sinergia con altre infezioni
LATENZA
FENOMENO IN VIVO
TRASMISSIONE BoHV.1
ceppo virale
Due forme cliniche principali
via di infezione
RESPIRATORIA
GENITALE
IBR
IPV
IBV
VIE di TRASMISSIONE
Mucose alte vie respiratorie e congiuntivali
Mucose genitali
Principale fonte di disseminazione BoHV.1 sono animali
infetti con sintomi
TRASMISSIONE BoHV.1
Diretta
Aerosol
Monta
Contatto delle mucose
Contatto con placente o feti abortiti
•
Indiretta
Embryotransfer
Materiale seminale
N.B.
BoHV.1 persiste nel seme per lungo tempo:
escreto in modo intermittente
• BoHV.1 resiste al congelamento
Escrezione BoHV.1 da vitelli con IBR e IPV: 1-2 settimane
Escrezione BoHV.1 da vitelli con IBP: 2-3 settimane
Aborto: si ha una notevole diffusione BoHV.1 tramite cotiledoni
ESCREZIONE VIRUS e TITOLO/gr MUCO
IBR
10-16 gg
108-1010TCID50
IPV
8-14 gg
1011TCID50
IBP
14-22 gg
1011TCID50
Aborto
nei cotiledoni: 106-106.5TCID50
Escrezione dopo infezione primaria
log UFP/100mg
7
6
5
4
3
2
1
0
0
1
2
3
4
5
6
7
Giorni
8 10 12 14 16
IBR
Replicazione primaria
Tratto respiratorio
superiore
Escrezione virale, lesioni necrotiche mucose
Viremia linfocito-associata. Localizzazioni secondarie:
-Ovaio, placenta aborto
-Intestino Enteriti letali Vitelli
-Meningoencefaliti Vitelli
Febbre
Congiuntivite
Iperemia mucosa nasale
Calo produzione latte
Scolo nasale/oculare
Laringotracheite
Aborto Encefaliti Enteriti
IPV
seme infetto
monta naturale o F.A.
Replicazione locale
Vulvovaginite
Balanopostite
Mucosa respiratoria
o genitale
Terminazioni
nervose periferiche
RIESCREZIONE
Mucosa respiratoria
o genitale
FATTORI
STRESSANTI
Terminazioni
nervose periferiche
Gangli trigemino (IBR)
e sacrali (IPV)
RIATTIVAZIONE
LATENZA
Equilibrio ospite/virus
Cervello
Cervelletto
Ganglio
trigemino
Nervo
mascellare
BoHV.1
Trasporto assonale retrogrado
INFEZIONE PRIMARIA
MOLTIPLICAZIONE VIRALE
ALTRI
ANIMALI
ESCREZIONE
NASALE
RISPOSTA IMMUNE PRIMARIA
ARRESTO DELL’ESCREZIONE
Trasporto per via assonale retrogrado
localizzazione nel ganglio nervoso
regionale
PERSISTENZA VIRALE
PORTATORE
LATENTE
LATENZA
LATENZA
INFEZIONE PRIMARIA
GUARIGIONE CLINICA
INFEZIONE LATENTE
STIPITI VACCINALI INDUCONO LATENZA
LATENZA
IBR
IPV/IBP
GANGLI DEL TRIGEMINO, TORACICI, etc.
GANGLI SACRALI
Infezione persistente di cellula e organismo
Presenza del genoma virale non integrato
Assenza di moltiplicazione virale
Livelli di trascrizione e traduzione ridotti
Assenza di virioni di nuova generazione
Assenza di lesioni cellulari
Assenza di stimolazione immunitaria
Nel neurone sensitivo con infezione latente:
BoHV.1: LRT (latency-related transcript)
LATENZA
Si prestano meglio a nascondere il virus:
-gene TK (enzima importante x sintesi DNA) poco presente
-lento metabolismo
-MHC1* poco esposti
PORTATORE LATENTE
Contagiante solo in fase di
SLATENTIZZAZIONE
LATENZA
FARMACI
RIATTIVAZIONE
IMMUNODEPRESSIONE
STRESS
•VACCINAZIONE
•MALATTIE INTERCORRENTI (BVD, PI-3)
•SOMMINISTRAZIONE FARMACI
•TRASPORTO
•PARTO
RIATTIVAZIONE con ELIMINAZIONE
VIRUS e/o SINTOMI
RIATTIVAZIONE LATENZA
Ganglio
trigemino
Trasporto assonale
anterogrado
Moltiplicazione virale in
periferia
RI-ESCREZIONE
RIESCREZIONE DOPO RIATTIVAZIONE
log UFP/100mg
7
6
5
4
3
2
1
0
0
1
2
3
4
5
6
7
Giorni
8
9 10 11 12 13 14
LATENZA
IMPLICAZIONI
VACCINAZIONE CON STIPITE ATTENUATO
NON PREVIENE LATENZA VIRUS SELVAGGIO
Vaccini prevengono segni clinici, ma non infezione e quindi latenza
Vaccini marker attenuato: protezione da infezione migliore
rispetto allo spento
•
•
Vaccini marker inattivati: riduzione escrezione migliore
dopo riattivazione rispetto attenuato
Protocollo ottimale: vivo e poi spento
INFEZIONE ASINTOMATICA
BoHV.1 viene escreto anche da animali con infezione asintomatica
Sviluppo infezione asintomatica:
-stipiti a bassa virulenza
-reinfezione (conseguente alla diminuzione dell’immunità)
-riattivazione infezione latente
FATTORI DI RISCHIO
TRA ALLEVAMENTI
- (re)introduzione animali
• infezione primaria
• riescrezione da latenza
– trasmissione attraverso l’aria (4 m)
NELL’AMBITO DELL’ALLEVAMENTO
Riescrezione da latenza
• R0 = 7 per un periodo di 4 settimane
• lenta diffusione
Quadri clinici dell’infezione da BoHV.1
Rinotracheite infettiva bovina
Vulvovaginite infettiva pustolosa
Balanopostite pustolosa
Meningoencefalite
Aborto
Forma neonatale sistemica mortale
CARATTERI DELLA MALATTIA
FORMA RESPIRATORIA
ENTITÀ VARIABILE
• ETÀ ANIMALI COLPITI
• AFFOLLAMENTO
• STIPITE VIRALE
FORMA RESPIRATORIA
CARATTERI DELLA MALATTIA
MORBILITÀ ELEVATA
MORTALITÀ BASSA
Incubazione: 2-5 gg
Fase acuta: 5-10 gg
•FEBBRE (42°C) e TACHIPNEA
•IPEREMIA MUCOSA NASALE
•SCOLO NASALE/OCULARE
•CONGIUNTIVITE
•TOSSE
•INAPPETENZA
•CALO PRODUZIONE LATTE
•Possibili polmoniti batteriche
CARATTERI DELLA MALATTIA
FORMA GENITALE IPV
TALVOLTA INAPPARENTE
Incubazione: 1-3 gg dopo accoppiamento
• EDEMA VULVARE E PERINEALE
• ESSUDAZIONE MUCOPURULENTA
• DOLORABILITÀ LOCALE
(difficoltà accoppiamento)
• PLACCHE NECROTICHE
Su vulva e regione caudale vagina presenza di pustole di 2-3mm
che tendono a confluire, per poi ulcerare e guarire in 10-15
• IPOFERTILITÀ/ABORTO
CARATTERI DELLA MALATTIA
ABORTO
3-6 settimane dopo focolaio IBR
•Prevalente fra 5-8 mese di gravidanza
•Feto espulso dopo 2-3 settimane dalla morte
•Piccoli focolai necrotici, fegato, reni, surreni, timo
•Dopo aborto si può avere metrite
CARATTERI DELLA MALATTIA
FORMA GENITALE IPB
TALVOLTA INAPPARENTE
Incubazione: 1-3 gg dopo accoppiamento
• BALANOPOSTITE ESSUDATIVA
• VIRUS TRASMISSIBILE CON SPERMA
FECONDAZIONE NATURALE/ARTIFICIALE
CARATTERI DELLA MALATTIA
FORMA NEUROLOGICA
ENCEFALITE NON PURULENTA
•INCOORDINAZIONE MOTORIA
•MOVIMENTI IN CIRCOLO
•DECUBITO PERMANENTE
•MORTE dopo 3 gg
CARATTERI DELLA MALATTIA
FORMA NEONATALE SISTEMICA
Infezione si instaura in ultimi giorni di
gravidanza, o nei primissimi giorni di vita
•Sintomi respiratori e gastroenterici
•Mortalità elevata
LESIONI ANATOMOPATOLOGICHE
FORMA RESPIRATORIA
–Rinite sierosa/mucopurulenta-necrotica con interessamento turbinati e
trachea
–Forme iperacute (raramente): bronchite e bronchiolite necrotizzante,
ispessimento setti interlobulari, aumento di volume dei lobi anteriori
–Frequentemente: broncopolmonite batterica di modesta entità
(Mannheimia, Haemophylus)
FORMA GENITALE
Iperemia mucosa vulvare, vaginale, di glande, prepuzio con emorragie
dei follicoli linfoidi
ABORTO
Feto edematoso, autolitico (no isolamento), lesioni necrotiche al fegato
FORMA ENCEFALICA
Iperemia e petecchie cerebrali, CSF intorbidito per presenza di cellule
DIAGNOSI
VIROLOGICA
•secreto nasale e congiuntivale
•essudato vaginale o prepuziale
•sperma
•feti abortiti
•cotiledoni
Isolamento virus
PCR
SIEROLOGICA
•sieroneutralizzazione
•ELISA
•stato d’infezione
•doppio campione
PROFILASSI IBR
NECESSITÀ!!!!
Impatto negativo dell’infezione
•ECONOMICO
• SANITARIO
PROFILASSI
NON
FARE NIENTE
VACCINARE
CONTROLLARE ED ERADICARE
•CON VACCINAZIONE
•SENZA VACCINAZIONE
NORMATIVA
La normativa nazionale e comunitaria richiede la
negatività sierologica dei tori destinati alla produzione di
materiale seminale e alle bovine produttrici di embrioni
Orientamento UE: inserire IBR nella lista delle malattie oggetto
di Piani di Eradicazione con partecipazione finanziaria della
Comunità
Al momento l’adesione ai piani di controllo è facoltativa ed è
applicata in diverse regioni in Italia
Eradicazione conclusa in:
Danimarca, Finlandia, Norvegia, Svezia, Svizzera, Austria,
alcune aree della Baviera (VIETATI VACCINI)
Attualmente hanno in corso piani obbligatori di eradicazione:
Olanda e Belgio Germania, Francia
Italia (piani volontari applicati in alcune regioni)
FREE
FREE
FREE ?
FREE ?
FREE
FREE
FREE
FREE
FREE
OIE
HANDISTATUS II
BOLZANO
INDENNE
PIANI ERADICAZIONE VOLONTARIA APA
•PUGLIA
•CALABRIA
•BASILICATA
•CAMPANIA
PIANI ERADICAZIONE:
•PIEMONTE
•VENETO
•LOMBARDIA
•FRIULI V. GIULIA
•PROVINCIA TRENTO
PROFILASSI DIRETTA E INDIRETTA
In allevamenti soggetti a programmi di controllo/eradicazione IBR si
adottano misure di profilassi diretta e, se necessario, indiretta, al
fine di evitare introduzione BoHV.1 in azienda e la sua trasmissione
DIFFICOLTA’
INDIVIDUAZIONE BOVINI CON INFEZIONE LATENTE
ALTA INCIDENZA INFEZIONI ASINTOMATICHE (adulti)
PROFILASSI DIRETTA
Interventi di lotta per impedire:
introduzione BoHV.1, eliminarlo da ambiente e prevenirne la circolazione
• Quarantena ed accertamenti diagnostici per i capi di nuova introduzione;
• Accertamenti in caso di contatti esterni a rischio (fiere, mercati, pascoli ecc.);
• Misure per evitare contatti con altri allevamenti tramite persone, mezzi e
strumenti
• Controllo periodico dei sieronegativi
• Eventuale vaccinazione dei soggetti positivi
L’eliminazione dei capi positivi è la misura più efficace ma non sempre praticabile,
spt in fasi iniziali del piano di eradicazione.
Si devono adottare pertanto misure alternative, integrate con interventi di
profilassi indiretta
• Esclusione o effettuazione sotto stretto controllo, di interventi farmacologici
che favoriscono la riattivazione
Misure generali di biosicurezza
Misure generali di biosicurezza
QUARANTENA PER ANIMALI NUOVA INTRODUZIONE
EVITARE MONTA NATURALE FINO ALL’ERADICAZIONE
EVITARE CONTATTI CON OVI-CAPRINI (ruolo modesto ma non sottovalutabile)
GESTIONE ANIMALI PER CATEGORIA DI ETA’
GARANTIRE BENESSERE ANIMALE (DGR 876 DEL 18/12/2006)
•MIGLIORAMENTO VENTILAZIONE
•RIDUZIONE CARICO ANIMALI
•RIDUZIONE EVENTI STRESSANTI
VACCINO SPENTO
CARATTERISTICHE
È INNOCUO
PUÒ ESSERE SOMMINISTRATO IN GRAVIDANZA
NON DETERMINA ELEVATO STRESS
DETERMINA RIDUZIONE ESCREZIONE VIRALE
TITOLO E GIORNI (10-100 volte)
RICHIAMI!!
VACCINO VIVO ATTENUATO
CARATTERISTICHE
DETERMINA RIDUZIONE DI RIESCREZIONE GIORNI E
TITOLO (2-3 gg/ 1000 volte)
STIMOLAZIONE COMPLETA IMMUNITA’
PROTEGGE DA FORME CLINICHE
NON PUÒ ESSERE SOMMINISTRATO IN GRAVIDANZA
(ABORTO)
DETERMINA LATENZA E PUÒ RIATTIVARSI
RIATTIVAZIONE VIRUS ATTENUATO PUÒ COMPORTARE
ABORTO E PRESENZA VIRUS IN SPERMA
VACCINO TERMOSENSIBILE
CARATTERISTICHE
SOMMINISTRATO PER VIA INALATORIA
PUÒ ESSERE SOMMINISTRATO IN GRAVIDANZA
STIMOLA IMMUNITÀ MUCOSALE
IMPEDISCE INFEZIONE VIRUS SELVAGGIO
POCO PRATICO
VACCINO A SUB-UNITÀ
CARATTERISTICHE
COSTITUITI DA SINGOLE GLICOPROTEINE
RESPONSABILI DI IMMUNITÀ PROTETTIVA
ANCORA ALLO STUDIO
INSIEME AI VACCINI A DNA
gD
VACCINO A MARKER
IMMUNOLOGICO NEGATIVO
Vaccino marcato (BoHV-1, PRV): deleto del gene gE
DIFFERENZIARE ANIMALE VACCINATO INFETTO
La scelta della delezione può ricadere su un qualsiasi Ag, se:
in virus selvaggio sia sempre espresso e in grado di indurre
produzione di Ac specifici
non deve però essere Ag essenziale per replicazione virale, e per
induzione dell'immunità
Delezione non può riguardare
• Ag indispensabili per replicazione
• Ag immunogeni più importanti
VACCINO A MARKER
IMMUNOLOGICO NEGATIVO
IR
UL
UL53
gK
UL27
UL44
gC
gB
UL22
gH
UL10
gM
US TR
delezione in ceppo vaccinale
UL1
gL
US4 US6 US7 US8
gG gD gI gE
VACCINO A MARKER
IMMUNOLOGICO NEGATIVO: VANTAGGI
• Vaccinazione non preclude identificazione sierologica di infetti
• Situazione siero-epidemiologica può essere valutata in
popolazioni vaccinate
• Efficacia può essere facilmente valutata in trials di campo
• Possono essere implementati programmi di
vaccinazione/eradicazione
INTERPRETAZIONE di SIEROLOGIA
INFEZIONE
VACCINAZIONE
ANTICORPI
ANTI BoHV-1
+
+
ANTICORPI
ANTI gE
+
-
Necessità di utilizzare il companion test kit ELISA
Costi elevati
INFETTO o VACCINATO??
Virus vaccinale NON ha gE
Virus di campo ha gE
L’animale ha Ac anti gE?
NO
sieropositività dovuta a
vaccino (deleto)
SI
sieropositività dovuta a infezione o
a vaccinazione con vaccino tradizionale
E se dopo 4,6, 8 mesi incontra virus selvaggio?
Si infetta e produce anticorpi anti gE
VACCINI DELETI: POSSIBILI RISCHI
Ricombinazione in vivo con ceppi virulenti selvaggi
:
• Riacquisizione della struttura virale iniziale e della patogenicità
• Comparsa di marker immunologico negativo nel ceppo selvaggio
IMPROBABILE:
•
Necessita presenza contemporanea in animale di virus deleto e virus selvaggio
•
Animali vaccinati acquisiscono, in alcune settimane, protezione totale
• Una stessa cellula dovrebbe venire infettata, nello stesso momento, da dosi
to, elevate di entrambi i virus (titolo di virus selvaggio in ambiente è molto più
bassa rispetto a quella del virus vaccinale).
PROFILASSI
centri fecondazione
allevamenti riproduttori
allevamenti fornitori embrioni
INDENNI da IBR
• DM 28/6/91 n. 323
• Dir 88/407/CEE
• Dir 97/12/CE
Il piano di eradicazione e profilassi dell’IBR è riservato agli
allevamenti bovini ufficialmente indenni per tubercolosi, brucellosi
e leucosi bovina enzootica
ORGANIZZAZIONE
PIANI DI CONTROLLO
•CONOSCERE PREVALENZA INFEZIONE
•LIVELLI DI INFEZIONE
PIANI DI ERADICAZIONE
•COSTI
•TEMPI DI ATTUAZIONE
QUALIFICA DI INDENNITÀ OIE
Territorio indenne (codice OIE 2001)
Le province in cui sono presenti il 99,8% di allevamenti indenni/ufficialmente
indenni da BoHV.1 ed in cui non si sono verificati casi clinici o sospetti di
malattia (da 3 anni) possono acquisire la qualifica di “provincia indenne da IBR”.
Il territorio mantiene la qualifica di indenne se, in seguito a controlli annuali su tutti
gli allevamenti presenti, non viene superato lo 0,2% di prevalenza
Nessun animale è stato vaccinato per IBR/IPV negli ultimi 3 anni
Bovini introdotti nel territorio devono provenire da allevamenti
indenni/ufficialmente indenni oppure devono sottostare a 30 gg di isolamento in
stazione di quarantena ed essere sottoposti a due controlli sierologici, a distanza di
21 gg, con esito favorevole.
Mantenimento della qualifica:
-Per inseminazione artificiale, solo seme raccolto da tori sieronegativi per BoHV-1.
-Solo embrioni ottenuti da donatrici di allevamenti indenni/ufficialmente indenni da
BoHV-1 oppure trattati con chimotripsina
Come si raggiunge l’obiettivo?
Allevamento indenne
Tutti i capi sottoposti a controllo sono risultati:
negativi al test per la ricerca di Ac totali verso BoHV-1
negativi al test per la ricerca degli Ac verso E2, qualora
vengano praticati i trattamenti vaccinali per BoHV-1
A 2 controlli ufficiali eseguiti a distanza di almeno 2 mesi e non
oltre 12 mesi
Allevamento ufficialmente indenne
Tutti i capi sottoposti a controllo non sono stati vaccinati e sono risultati:
negativi a 2 test per la ricerca di Ac totali verso BoHV-1,
eseguiti ad intervallo da 2 a 12 mesi.
Le attuali norme non contemplano la qualifica di ufficialmente indenne per gli
allevamenti che abbiano vaccinato, ma nei quali le vaccinazioni siano state
sospese da tempo
MANTENIMENTO DELLA QUALIFICA
•Effettuato annualmente controllo con esito favorevole su tutti gli animali > 12 mesi;
•In allevamenti ufficialmente indenni non è praticata la vaccinazione per BoHV-1;
•Animali introdotti provengono da allevamenti con medesima qualifica, attestata dal
certificato sanitario di scorta;
•Se animali introdotti provengano da allevamenti non indenni/ufficialmente
indenni da BoHV-1 è necessario che siano stati sottoposti nell’allevamento di origine
a test sierologico con esito favorevole nei 30 gg precedenti l’introduzione.
E’ inoltre necessario che siano isolati dal resto dell’allevamento di destinazione per almeno
30 gg, durante i quali devono essere eseguite 2 prove sierologiche con esito
favorevole distanziate di 21 gg;
•Per inseminazione utilizzato seme raccolto da tori negativi alla ricerca di
Ac totali per BoHV-1 (requisito già obbligatorio ai sensi del DM 30/04/1996);
•Utilizzati embrioni ottenuti da donatrici appartenenti ad allevamenti
indenni/ufficialmente indenni da BoHV-1 oppure trattati con chimotripsina;
•Isolati per trenta giorni dal resto dell’allevamento e sottoposti a controllo
sierologico (due prove a distanza di 21 gg) tutti gli animali che in occasione
di fiere, mercati, trasferimenti in altre strutture, siano venuti in contatto con animali
di allevamenti non indenni/ufficialmente indenni da BoHV-1.
REVOCA e RIACQUISIZIONE DELLA QUALIFICA
In caso di riscontro di positività ai controlli ufficiali, la qualifica è
revocata e può essere riacquisita:
• dopo aver eliminato i capi infetti;
• dopo avere eseguito una scrupolosa indagine epidemiologica volta
ad accertare le cause dell’introduzione del contagio;
• dopo avere modificato il piano aziendale per adeguare le misure
preventive;
• successivamente a due controlli sierologici negativi effettuati a
distanza di almeno 2 mesi
METODI di PROFILASSI
ELEVATA PREVALENZA
50%
Fase transitoria
Vaccinare (diverse poss)
Vaccini deleti
Tempi ridotti
ERADICAZIONE
Bassa
prevalenza
<3%
Eliminare i
sieropositivi
Vaccino inattivato
VACCINARE SOLO GLI ANIMALI SIEROPOSITIVI
METODI di PROFILASSI
STALLE NEGATIVE IBR
Non vaccinare! Solo profilassi diretta
N.B. Alto rischio introduzione BoHV.1
STALLE con POSITIVITA’ < 10%
1.Eliminare sieropositivi
Profilassi diretta
2.Vaccinare sieropositivi
Limitare rischi riattivazione dei positivi
STALLE con POSITIVITA’ solo di ADULTI Profilassi diretta
Vaccinare sieropositivi con vaccino tradizionale o deleto,
e giovani sieronegativi con deleto
Limitare rischi riattivazione dei positivi
N.B.
Importante vaccinare negativi: potrebbero essere falsi negativi (no Ac, BoHV.1 latente)
STALLE con POSITIVITA’ DIFFUSA
Vaccinare
LATENZA e ANTICORPI SPECIFICI
Sono due conseguenze differenti di
infezione primaria con BoHV.1
Si può teoreticamente presumere che
un portatore latente di BoHV.1
possa essere sieronegativo
COMPLICAZIONI NEI PROGRAMMI DI CONTROLLO
GRAZIE PER L’ATTENZIONE