Patologia (Generale) e Terminologia Medica
Corso di Laurea in Chimica
e Tecnologia Farmaceutiche
Marco Cei & Alberto Genovesi Ebert
Spedali Riuniti, Livorno
1
Danno Cellulare
2
Modalità di adattamento:
•Ipertrofia:
•Iperplasia:
•Atrofia:
•Metaplasia:
3
Modalità di adattamento:
Ipertrofia: ingrandimento delle cellule e delle
dimensioni di organo
➢Risposta a sovraccarico di lavoro o ormoni
➢Mediata da fattori di crescita prodotti in
risposta a stress meccanici o altri stimoli
Si verifica in tessuti incapaci di divisione
cellulare
4
5
IPERTROFIA
L’organo ipertrofico non ha cellule nuove ma solo cellule piu’ grandi, per la sintesi di
maggiori quantità di proteine e altri componenti strutturali.
Aumento del volume nucleare, dei polisomi, dei mitocondri, del volume delle creste
mitocondriali
Ipertrofia della muscolatura liscia: negli organi cavi (stomaco, cuore, intestino, vasi,
ecc) a monte di una stenosi (riduzione dell'orifizio) sopravvenuta per deformazione,
cicatrizzazione della parete dell’organo. La difficoltà di passaggio del contenuto provoca
una distensione a monte del restringimento e quindi ipertrofia del segmento muscolare
corrispondente.
Esempio di ipertrofia: utero
Normale
Gravidico
Normale
Gravidico
7
Esempio di ipertrofia: miocardio
Sovraccarico di lavoro:
Ipertrofia:
Richieste metab.
Probabilità ischemia/IMA
8
Modalità di adattamento:
Iperplasia: aumento del numero delle cellule.
➢Risposta a stimolazione ormonale o fattori di
crescita
Si verifica in tessuti le cui cellule sono capaci
di replicarsi
9
La capacità iperplasica, per un tessuto, dipende dalla capacità
delle cellule di dividersi, permettendo così la classificazione dei
tessuti ad elementi labili, stabili e perenni.
LABILI: alta capacità mitotica (epiteli di rivestimento
– tessuto emopoietico)
STABILI: capacità mitotica limitata (fegato
– tubuli renali)
PERENNI: non hanno capacità mitotica (sistema nervoso
centrale – cuore)
10
L’iperplasia puo’ quindi avvenire solo nei tessuti che contengono cellule
capaci di dividersi.
Iperplasia tiroidea: la tiroide si accresce a seguito della
stimolazione delle cellule tioidee da parte del TSH
Ciclo mestruale: le ghiandole dell’endometrio aumentano per effetto della
proliferazione indotta da stimolazione endocrina ovarica
normale
iperplasia
11
Modalità di adattamento:
Atrofia/ipoplasia: riduzione delle dimensioni e/o
numero delle cellule e delle dimensioni di organo
➢Risultato di ridotto apporto nutrizionale o
stimolazione/ormonale/nervosa o disuso
Riduzione di sintesi dei costituenti cellulari e
aumento dell distruzione degli organuli cellulari
12
Esempio di atrofia:atrofia muscolare
•Decreased workload (atrophy of disuse).
•Loss of innervation (denervation atrophy).
•Diminished blood supply.
•Inadequate nutrition
13
Esempio di atrofia: cervello senile
36 anni
82 anni
14
Metaplasia
Modificazione reversibile in cui un tipo cellulare
differenziato viene sostituito da un altro tipo
differenziato.
➢ Adattamento a stimoli irritativi ripetuti
15
Esempio di metaplasia: polmone
Nei fumatori cronici l’
epitelio cilindrico
ciliato muciparo è
sostituito da cellule
stratificate di tipo
pavimentoso ricco di
cheratina.
Modificazione talora
precancerosa
16
Esempio di metaplasia: esofago
Esofago di Barrett: Reflusso gastroesofageo> Metaplasia
“intestinale”: sostituzione di epitelio squamoso
stratificato, con epitelio colonnare e cellule mucipare
fattore di rischio importante per l'adenocarcinoma esofageo
17
Modalità di adattamento:
•Ipertrofia:
• Aumento del volume di organo, senza apprezzabili
variazione del numero di cellule.
•Iperplasia:
• Aumento di numero e volume delle cellule.
•Atrofia:
• Riduzione del volume di organo/cellule
•Metaplasia:
• La sostituzione di un tipo cellulare con un altro.
18
Danno Cellulare
19
Cause di danno cellulare
•Difetto di ossigeno o ipossia.
•Agenti chimici
•Agenti biologici (batteri, virus
•Reazioni immunitarie
•Difetti genetici
•Anomalie nutrizionali
•Agenti fisici
•Invecchiamento
etc)
20
Danno Cellulare
21
Danno Cellulare da Agenti Chimici
Lista infinita…..
• …Glucosio
• …Soluzioni
• …O2
ipertoniche
ad alta concentrazione
• Veleni
Arsenico, Cianuri, Mercurio
• Tossici
ambientali e Inquinamento
• Insetticidi,
• Prodotti
diserbanti
di lavorazioni industriali, CO,
• Farmaci
22
Meccanismi Biochimici e Sedi di
Danno Cellulare
23
Nella cellula si producono prevalentemente attraverso 5 processi
Che producono specie reattive dell’ossigeno (Reactive Oxigen Species, ROS)
24
25
26
Cause di ipossia tissutale
•Riduzione della Hb: Anemia
•Riduzione saturazione della Hb (pAO2, pO2
ambiente, polmoni)
•Ridotto apporto ematico regionale: ischemia
Aterosclerosi (stenosi vascolare)
Trombosi
Embolia
Compressione
•Alterata respirazione cellulare (anossia istotossica
KCN, CO)
27
“Dizionario”
• Anemia:
riduzione del Q di GR
• Ischemia:
apporto ematico insufficiente alle necessità
metaboliche
• Trombosi:
• Embolia:
formazione di un aggregato di PLT…
materiale che parte da una sede e giunge ad
“occludere/ostruire” distalmente
28
Insulto ischemico reversibile
•
•
•
•
•
•
•
•
•
tensione di O2
produzione di ATP,
glicolisi anaerobica
pH: denatura le proteine,
proteasi e fosfatasi
attiva
trasporto attivo di ioni trasmembrana
gradiente osmotico trasmembrama
Rigonfiamento cellulare
Danno delle membrane reticulo endoplasmatico, riduz.
sintesi proteica, danno ultra structure citoscheletro
•Il nucleo può rimanere inatto e la cellula può ritornare
integra
29
Cellule Tubulari Renali Normali
• Cellule epiteliali
citoplasma eosinofilo
(rosa) nuclei (porpora)
basofili , acidi nucleici
confinati nei nuclei
• Presenza di “Ciglia” sulla
superficie apicale
• Interstitio non infiltrato
nè congesto
30
Rigonfiamento delle Cellule Tubulari
Renali
• Aumento della colorazione
eosinofilia
• Riduzione della
colorazione basofilia
• Membrane arrotondate
perdita delle connessioni
intercellulari e delle ciglia
• Danno dei tubuli con
membrane basali intatte
• Nuclei per lo più intatti,
un pò avvicinati
31
Perdita dell’Omeostasi del Calcio
Il Ca2+ intracellulare è mantenuto ad una concentrazione molto bassa rispetto ai
livelli extracellulari, e la maggior parte del Ca2+ è sequestrato nei mitocondri e nel
reticolo endoplasmatico. L’aumento del Ca2+ intracellulare, causato da un danno
come l’ischemia, porta all’attivazione di enzimi ATPasi ( che degradano ATP),
fosfolipasi (che promuovono il danno di membrana), endonucleasi (frammentano il
DNA)
32
Danno (ischemico) irreversibile:
•[Ca++] citoplasma normale < 1000–10000 volte
[Ca++] extracell., mitocondr, e ER
•Inibiz. Pompa Ca++ ATP-dependente > aumento
influsso da mitochondri, ER, fluidi extracellulari
•La cellula rigonfia ha citosol con pH più basso,>
[Ca++], [Na+]
•Aumento acidità & conc. ionica: denaturazione delle
proteina
•Ca++ activa enzimi litici
•Fosfolipasi A, ribonucleasi, proteasi degradano
membrane, ribosomi, proteine strutturali
•Necrosi
Infarto (infarcire), area localizzata di necrosi di un
tessuto, secondaria ad ischemia o altro insulto.
33
Cellule Tubulari Renali Necrotiche
•Frammentazione
cellulare
•Perdita/rottura
dei nuclei Cariolisi
•Rottura
delle
membrane
•Perdita
della
arrchiettura
tissutale
34
La Cascata Ischemica
35
Il danno ischemico, come quello ipossico induce:
difetto nella regolazione del volume cellulare causato dal blocco della pompa
sodio-potassio ATP dipendente (con aumento dell’entrata di acqua e perdita di
potassio),
accumulo di acido lattico (ed altri metaboliti) con conseguente aumento del
carico osmotico intracellulare
aumento del calcio intracellulare dovuto al rilascio dello stesso dal reticolo
endoplasmatico e dall’ingresso di calcio extracellulare.
Intervento terapeutico: ripristino del flusso sanguigno
Entità e durata dell’insulto ischemico: morte di una parte delle cellule del
tessuto ischemico.
Infarto Miocardico
37
Infarto Miocardico:
Perdita/riduzione della funzione
38
Danno Cellulare
Liberazione del contenuto
cellulare >interstizio>circolo:
Dosaggio di marcatori specifici
di tessuto (es. enzimi):
orientamento diagnostico
39
La necrosi: morfologia del tessuto
Una volta che le singole cellule sono andate incontro alle alterazioni
suddette, l’insieme delle cellule necrotiche può assumere diversi
aspetti morfologici:
✓
✓
✓
Necrosi coagulativa ( il tessuto appare compatto, come cotto)
✓
Prevale la denaturazione delle proteine;
✓
Preservazione dei contorni cellulari per giorni;
✓
Caratteristica della morte ipossica (miocardio);
Necrosi colliquativa (il tessuto appare semifluido)
✓
Predomina la digestione enzimatica;
✓
Perdita dei contorni cellulari;
✓
Caratteristica del cervello.
Necrosi caseosa (il tessuto ha una consistenza soffice, che
ricorda il formaggio)
✓
Tipica del tubercolo
40
41
42
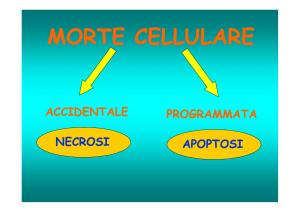
Morte Cellulare
43
Morte Cellulare: Apoptosi
Morte cellulare “programmata”
L‘equilibrio è mantenuto
quando la consistenza delle
(1972 JF Kerr, AH Wyllie, AR
mitosi (proliferazione
Currie dal greco “caduta delle cellulare) in un tessuto è
foglie e dei petali dei fiori”)
bilanciata dalla morte di
un numero equivalente di
cellule
44
Relazione tra Apoptosi e Mitosi e Massa Tissutale
45
Equlibrio
46
Esempi di Apoptosi
✓
Membrane interdigitali
del feto;
✓
Ricambio cellulare dei
villi intestinali;
✓
Rimozione cellule
ematopoietiche vecchie
✓
Delezione linfociti T
autoreattivi nel timo
✓
Sviluppo connessioni
neuronali;
47
Necrosi
Apoptosi
•Gruppo di cellule
•Da agenti/eventi dannosi
•La reversibilità precede
•Poche o singole cellule
•Morte programmata
•Se iniziata irreversibile
•Utilizza energia
•Collasso cellulare e
la irreversibilità
•Deprivazione di energia
•Rigonfiamento cellulare
per entrata di acqua
disassemblaggio del
citoscheletro
•Casuale distruzione di
•Impacchettaggio del
organelli e materiale
nucleare da liberazione
lisosomiale
•Il materiale distrutto
stimola l’ infiammazione
materiale distrutto in
organelli
•Le molecole nuove che si
formano stimolano la
fagocitosi non l’
48
ischemi
a
traumi
fisici
o
chimici
cellula
normale
segnal
iscatenan
ti
specifi
ci
NECROS
I
la cellula si
rigonfia
i suoi organelli
sono
danneggiati
APOPTOS
I
la cellula si
raggrinza
organell indenn
i
i
cromatina
addensata
il nucleo collass
a
e si
frammenta
la
forma membrana
protuberanze
la cellula si
lisa
si
distruggono
organelli e
cromatin
a
si
corpi formano
apoptoti
ci
fagocit
a
il
contenuto
cellular
e
viene
rilasciato
infiammazione
nessuna infiammazione
fagociti
localii
inglobano
residui
Enzimi Protagonisti dell’Apoptosi
Caspasi=C.ASPasi
Proteasi a cisteina presenti nelle cellule come
proenzimi
Attivazione a cascata
Taglio del substrato dopo residui di aspartato
distinte in: c. iniziatrici (cas –8, -9, -10)
c. esecutrici (cas –3,-7)
Agiscono su:
• endonucleasi (CAD)*
• proteine citoscheletriche
• proteine della matrice nucleare
* caspase-activated deoxyribonuclease
50
Due vie di attivazione
•Estrinseca,
mediata da “death receptors”
•Intrinseca,
mediata dai mitocondri
51
La via estrinseca
I Recettori di Morte
52
La via intrinseca:
Mitocondrio Protagonista
• La diminuzione del potenziale di membrana, l’
eccessiva produzione di radicali, la presenza
di ioni Ca++ ed altri stimoli, possono
determinare l'apertura di pori della membrana
mitocondriale
detti
megachannels
o
mitochondrial pores, con conseguente
alterazione della sua permeabilità. Ciò
provoca la fuoriuscita di fattori normalmente
sequestrati, quali il citocromo ccitocromo c o
l'AIFAIF (apoptosis inducing factor) che sono
in grado di innescare l'apoptosi se a contatto
con cofattori citoplasmatici
53
Apoptosi, Necrosi & ATP
• L’apoptosi
richiede ATP per permettere fenomeni
attivi quali l'idrolisi enzimatica delle macromolecole,
la condensazione nucleare e la formazione di blebs,
fenomeni che non avvengono invece in corso di necrosi
• La
disponibilità di ATP determina la strada che la
cellula sceglierà per morire:
• quando
l'ATP scende sotto una certa concentrazionesoglia, la cellula muore per apoptosi
• quando
il calo è massiccio e rapido, la cellula va
incontro a necrosi
54
Regolazione dell’apoptosi
•Anti-apoptotici
– Bcl-2, Bcl-XL
– IAPs
– HSP27, HSP72,
HSP90
•Pro-apoptotici
– Bax, Bad, Bid
– P53
– HSP10, HSP60
55
56
57